अल्फ्रेड वर्नर: Difference between revisions
No edit summary |
No edit summary |
||
| Line 34: | Line 34: | ||
1893 में, वर्नर जटिल आयनों वाले समन्वय यौगिकों के लिए सही संरचनाओं का प्रस्ताव करने वाले पहले व्यक्ति थे, जिसमें एक केंद्रीय संक्रमण धातु परमाणु तटस्थ या आयनिक लिगेंड से घिरा होता है। | 1893 में, वर्नर जटिल आयनों वाले समन्वय यौगिकों के लिए सही संरचनाओं का प्रस्ताव करने वाले पहले व्यक्ति थे, जिसमें एक केंद्रीय संक्रमण धातु परमाणु तटस्थ या आयनिक लिगेंड से घिरा होता है। | ||
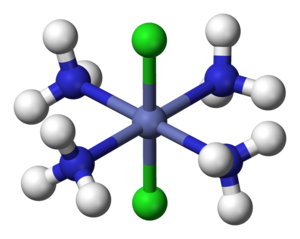
उदाहरण के लिए, यह ज्ञात था कि कोबाल्ट सूत्र CoCl3•6NH3 के साथ एक "जटिल" हेक्सामिनकोबाल्ट (III) क्लोराइड बनाता है, | उदाहरण के लिए, यह ज्ञात था कि कोबाल्ट सूत्र CoCl3•6NH3 के साथ एक "जटिल" हेक्सामिनकोबाल्ट (III) क्लोराइड बनाता है, लेकिन बिंदु द्वारा इंगित संघ की प्रकृति रहस्यमय थी।वर्नर ने [Co(NH3)6]Cl3 की संरचना प्रस्तावित की, जिसमें Co3 आयन एक अष्टफलक के शीर्ष पर छह NH3 से घिरा हुआ है। तीन Cl− मुक्त आयनों के रूप में अलग हो जाते हैं, जिसे वर्नर ने जलीय घोल में यौगिक की चालकता को मापकर और सिल्वर नाइट्रेट के साथ वर्षा का उपयोग करके क्लोराइड आयन के विश्लेषण द्वारा भी पुष्टि की। बाद में, CoCl3•6NH3 की रासायनिक प्रकृति के लिए वर्नर के प्रस्ताव की पुष्टि करने के लिए चुंबकीय संवेदनशीलता विश्लेषण का भी उपयोग किया गया था। | ||
[[Image:Cis-dichlorotetraamminecobalt(III).png|thumb|सिस-[Co(NH<sub>3</sub>)<sub>4</sub> Cl<sub>2</sub>]<sup>+</sup>]] | [[Image:Cis-dichlorotetraamminecobalt(III).png|thumb|सिस-[Co(NH<sub>3</sub>)<sub>4</sub> Cl<sub>2</sub>]<sup>+</sup>]] | ||
[[Image:Trans-dichlorotetraamminecobalt(III).png|thumb|ट्रांस-[Co(NH<sub>3</sub>)<sub>4</sub> Cl<sub>2</sub>]<sup>+</sup> ]]एक से अधिक प्रकार के लिगैंड वाले परिसरों के लिए, वर्नर प्रेक्षित समावयवियों की संख्या की व्याख्या करने में सफल रहे। उदाहरण के लिए, उन्होंने दो टेट्रामाइन समावयव "Co(NH3)4Cl3", एक हरे और एक बैंगनी रंग के अस्तित्व की व्याख्या की। वर्नर ने प्रस्तावित किया कि ये सूत्र [Co(NH3)4Cl2]Cl के दो ज्यामितीय समावयव हैं, जिसमें एक | [[Image:Trans-dichlorotetraamminecobalt(III).png|thumb|ट्रांस-[Co(NH<sub>3</sub>)<sub>4</sub> Cl<sub>2</sub>]<sup>+</sup> ]]एक से अधिक प्रकार के लिगैंड वाले परिसरों के लिए, वर्नर प्रेक्षित समावयवियों की संख्या की व्याख्या करने में सफल रहे। उदाहरण के लिए, उन्होंने दो टेट्रामाइन समावयव "Co(NH3)4Cl3", एक हरे और एक बैंगनी रंग के अस्तित्व की व्याख्या की। वर्नर ने प्रस्तावित किया कि ये सूत्र [Co(NH3)4Cl2]Cl के दो ज्यामितीय समावयव हैं, जिसमें एक Cl<sup>−</sup> आयन पृथक है जैसा कि चालकता मापन द्वारा पुष्टि की गई है। Co परमाणु एक अष्टफलक के शीर्ष पर चार NH3 और दो Cl लिगेंड से घिरा हुआ है। हरा समावयव "ट्रांस" है। | ||
वर्नर ने प्रकाशिक समावयवी के साथ परिसर भी तैयार किए, और 1914 में उन्होंने कार्बन की कमी वाले पहले कृत्रिम कायरल यौगिक की सूचना दी, जिसे सूत्र [Co(Co(NH3)4(OH)2)3]Br6) के साथ हेक्सोल के रूप में जाना जाता है | वर्नर ने प्रकाशिक समावयवी के साथ परिसर भी तैयार किए, और 1914 में उन्होंने कार्बन की कमी वाले पहले कृत्रिम कायरल यौगिक की सूचना दी, जिसे सूत्र [Co(Co(NH3)4(OH)2)3]Br6) के साथ हेक्सोल के रूप में जाना जाता है | ||
=== संयोजकता की प्रकृति === | === संयोजकता की प्रकृति === | ||
वर्नर से पहले, रसायनज्ञों ने विभिन्न प्रकार के बंधनों को अलग किए बिना एक तत्व की संयोजन क्षमता को उसके बँधो की संख्या के रूप में परिभाषित किया। यद्यपि ,उदाहरण के लिए [Co(NH3)6]Cl3 जैसे परिसरों में वर्नर ने माना कि Co-Cl बंध दूरी पर | वर्नर से पहले, रसायनज्ञों ने विभिन्न प्रकार के बंधनों को अलग किए बिना एक तत्व की संयोजन क्षमता को उसके बँधो की संख्या के रूप में परिभाषित किया। यद्यपि ,उदाहरण के लिए [Co(NH3)6]Cl3 जैसे परिसरों में वर्नर ने माना कि Co-Cl बंध दूरी 3 पर "प्राथमिक" संयोजन क्षमता के अनुरूप हैं, जबकि Co-NH3 बंध जो "द्वितीयक" के अनुरूप हैं "या 6 की दुर्बल संयोजन क्षमता से कम दूरी पर है। 6 की द्वितीयक संयोजकता को उन्होंने समन्वय संख्या के रूप में संदर्भित किया जिसे उन्होंने केंद्रीय धातु परमाणु से जुड़े अणुओं की संख्या (यहाँ NH3 की) के रूप में परिभाषित किया। अन्य परिसरों में उन्होंने 4 या 8 की समन्वय संख्याएँ प्राप्त की । | ||
इन विचारों और इसी तरह के अन्य विचारों पर, 1904 में रिचर्ड अबेग ने सूत्रित किया जिसे अब एबेग के नियम के रूप में जाना जाता है, जिसमें कहा गया है कि किसी तत्व की अधिकतम सकारात्मक और नकारात्मक संयोजन क्षमता के बीच का अंतर प्रायः आठ होता है। इस नियम का उपयोग बाद में 1916 में किया गया था जब गिल्बर्ट एन. लुईस ने अपने घनीय परमाणु सिद्धांत में " अष्टक नियम" तैयार किया था।। | इन विचारों और इसी तरह के अन्य विचारों पर, 1904 में रिचर्ड अबेग ने सूत्रित किया जिसे अब एबेग के नियम के रूप में जाना जाता है, जिसमें कहा गया है कि किसी तत्व की अधिकतम सकारात्मक और नकारात्मक संयोजन क्षमता के बीच का अंतर प्रायः आठ होता है। इस नियम का उपयोग बाद में 1916 में किया गया था जब गिल्बर्ट एन. लुईस ने अपने घनीय परमाणु सिद्धांत में " अष्टक नियम" तैयार किया था।। | ||
Revision as of 09:32, 5 March 2023
Alfred Werner | |
|---|---|
 Werner circa 1915 | |
| जन्म | 12 December 1866 |
| मर गया | 15 November 1919 (aged 52) Zurich, Switzerland |
| राष्ट्रीयता | Swiss |
| अल्मा मेटर | University of Zurich ETH Zurich |
| के लिए जाना जाता है | Configuration of transition metal complexes |
| Spouse | Emma Werner[1] |
| पुरस्कार | Nobel Prize for Chemistry (1913) |
| Scientific career | |
| खेत | Inorganic chemistry |
| संस्थानों | University of Zurich |
| Doctoral advisor | Arthur Rudolf Hantzsch, Marcellin Berthelot[citation needed] |
अल्फ्रेड वर्नर (12 दिसंबर 1866 - 15 नवंबर 1919) एक स्विस रसायनज्ञ थे जो ई टी एच ज्यूरिख के छात्र थे और ज्यूरिख विश्वविद्यालय में प्रोफेसर थे। उन्होंने 1913 में संक्रमण धातु परिसरों के अष्टफलकीय विन्यास के प्रस्ताव के लिए रसायन विज्ञान में नोबेल पुरस्कार जीता। वर्नर ने आधुनिक समन्वय रसायन शास्त्र के लिए आधार विकसित किया। वह नोबेल पुरस्कार जीतने वाले पहले अकार्बनिक रसायनज्ञ थे, और 1973 से पहले एकमात्र सहायक मठाधिकारी थे।[2]
जीवनी
वर्नर का जन्म 1866 में मुलहाउस, अल्सेस (जो उस समय फ्रांस का हिस्सा था, लेकिन जिसे 1871 में जर्मनी द्वारा कब्जा कर लिया गया था) में हुआ था। उनका पालन-पोषण रोमन कैथोलिक के रूप में हुआ।[3] वह जीन-एडम वर्नर, एक संधानी कार्यकर्ता, और उनकी दूसरी पत्नी, सलोमी जीनत वर्नर, जो एक धनी परिवार से जुडी हुई थी, की चौथी और अंतिम संतान थे।[3] वे ज्यूरिख में स्विस फेडरल संस्थान (पॉलिटेक्निकम) में रसायन विज्ञान का अध्ययन करने के लिए स्विट्जरलैंड गए, चूंकि इस संस्थान को 1909 तक डॉक्टरेट की उपाधि प्रदान करने का अधिकार नहीं था, इसलिए वर्नर ने 1890 में ज्यूरिख विश्वविद्यालय से औपचारिक रूप से डॉक्टरेट की उपाधि प्राप्त की।[3] पेरिस में पोस्टडॉक्टरल अध्ययन के बाद, वह पढ़ाने के लिए स्विस फेडरल संस्थान (1892) में लौट आए। 1893 में वे ज्यूरिख विश्वविद्यालय चले गए, जहां वे 1895 में प्रोफेसर बने। 1894 में वे स्विस नागरिक बन गए।[3]
अपने अंतिम वर्ष में, वह एक सामान्य, प्रगतिशील, अपक्षयी धमनीकाठिन्य से पीड़ित थे जो विशेष रूप से मस्तिष्क और वर्षों से अत्यधिक शराब पीने और अधिक काम करने से बढ़ गया था। ज्यूरिख के एक मनोरोग अस्पताल में उनकी मृत्यु हो गई।[3]
15 नवंबर 1919 को 52 साल की उम्र में ज़्यूरिख में धमनीकाठिन्य के कारण वर्नर की मृत्यु हो गई।
अनुसंधान
समन्वय रसायन
1893 में, वर्नर जटिल आयनों वाले समन्वय यौगिकों के लिए सही संरचनाओं का प्रस्ताव करने वाले पहले व्यक्ति थे, जिसमें एक केंद्रीय संक्रमण धातु परमाणु तटस्थ या आयनिक लिगेंड से घिरा होता है।
उदाहरण के लिए, यह ज्ञात था कि कोबाल्ट सूत्र CoCl3•6NH3 के साथ एक "जटिल" हेक्सामिनकोबाल्ट (III) क्लोराइड बनाता है, लेकिन बिंदु द्वारा इंगित संघ की प्रकृति रहस्यमय थी।वर्नर ने [Co(NH3)6]Cl3 की संरचना प्रस्तावित की, जिसमें Co3 आयन एक अष्टफलक के शीर्ष पर छह NH3 से घिरा हुआ है। तीन Cl− मुक्त आयनों के रूप में अलग हो जाते हैं, जिसे वर्नर ने जलीय घोल में यौगिक की चालकता को मापकर और सिल्वर नाइट्रेट के साथ वर्षा का उपयोग करके क्लोराइड आयन के विश्लेषण द्वारा भी पुष्टि की। बाद में, CoCl3•6NH3 की रासायनिक प्रकृति के लिए वर्नर के प्रस्ताव की पुष्टि करने के लिए चुंबकीय संवेदनशीलता विश्लेषण का भी उपयोग किया गया था।
एक से अधिक प्रकार के लिगैंड वाले परिसरों के लिए, वर्नर प्रेक्षित समावयवियों की संख्या की व्याख्या करने में सफल रहे। उदाहरण के लिए, उन्होंने दो टेट्रामाइन समावयव "Co(NH3)4Cl3", एक हरे और एक बैंगनी रंग के अस्तित्व की व्याख्या की। वर्नर ने प्रस्तावित किया कि ये सूत्र [Co(NH3)4Cl2]Cl के दो ज्यामितीय समावयव हैं, जिसमें एक Cl− आयन पृथक है जैसा कि चालकता मापन द्वारा पुष्टि की गई है। Co परमाणु एक अष्टफलक के शीर्ष पर चार NH3 और दो Cl लिगेंड से घिरा हुआ है। हरा समावयव "ट्रांस" है।
वर्नर ने प्रकाशिक समावयवी के साथ परिसर भी तैयार किए, और 1914 में उन्होंने कार्बन की कमी वाले पहले कृत्रिम कायरल यौगिक की सूचना दी, जिसे सूत्र [Co(Co(NH3)4(OH)2)3]Br6) के साथ हेक्सोल के रूप में जाना जाता है
संयोजकता की प्रकृति
वर्नर से पहले, रसायनज्ञों ने विभिन्न प्रकार के बंधनों को अलग किए बिना एक तत्व की संयोजन क्षमता को उसके बँधो की संख्या के रूप में परिभाषित किया। यद्यपि ,उदाहरण के लिए [Co(NH3)6]Cl3 जैसे परिसरों में वर्नर ने माना कि Co-Cl बंध दूरी 3 पर "प्राथमिक" संयोजन क्षमता के अनुरूप हैं, जबकि Co-NH3 बंध जो "द्वितीयक" के अनुरूप हैं "या 6 की दुर्बल संयोजन क्षमता से कम दूरी पर है। 6 की द्वितीयक संयोजकता को उन्होंने समन्वय संख्या के रूप में संदर्भित किया जिसे उन्होंने केंद्रीय धातु परमाणु से जुड़े अणुओं की संख्या (यहाँ NH3 की) के रूप में परिभाषित किया। अन्य परिसरों में उन्होंने 4 या 8 की समन्वय संख्याएँ प्राप्त की ।
इन विचारों और इसी तरह के अन्य विचारों पर, 1904 में रिचर्ड अबेग ने सूत्रित किया जिसे अब एबेग के नियम के रूप में जाना जाता है, जिसमें कहा गया है कि किसी तत्व की अधिकतम सकारात्मक और नकारात्मक संयोजन क्षमता के बीच का अंतर प्रायः आठ होता है। इस नियम का उपयोग बाद में 1916 में किया गया था जब गिल्बर्ट एन. लुईस ने अपने घनीय परमाणु सिद्धांत में " अष्टक नियम" तैयार किया था।।
आधुनिक शब्दावली में वर्नर की प्राथमिक संयोजकता ऑक्सीकरण अवस्था से मेल खाती है, और उसकी द्वितीयक संयोजकता को समन्वय संख्या कहा जाता है। Co-Cl बंध (उपरोक्त उदाहरण में) को आयनिक के रूप में वर्गीकृत किया गया है, और प्रत्येक Co-N बंध लुईस अम्ल Co3+ और लुईस क्षार NH3 के बीच एक समन्वयित सहसंयोजक बंधन है।
निर्माण
- लेहरबच डेर स्टीरियो रसायन पाठ्य पुस्तक है। फिशर, जेना 1904 अंकीय संस्करण जो विश्वविद्यालय और राज्य पुस्तकालय डसेलडोर्फ से सम्बंधित है।
संदर्भ
- W. Gregory Jackson; Josephine A. McKeon; Silvia Cortez (2004). "Alfred Werner's Inorganic Counterparts of Racemic and Mesomeric Tartaric Acid: A Milestone Revisited". Inorg. Chem. 43 (20): 6249–6254. doi:10.1021/ic040042e. PMID 15446870.
- Kristin Bowman-James (2005). "Alfred Werner Revisited: The Coordination Chemistry of Anions". Acc. Chem. Res. 38 (8): 671–678. doi:10.1021/ar040071t. PMID 16104690.
- ↑ "Alfred Werner - Nobel Prize for Chemistry 1913" (PDF). University of Zurich. Retrieved 9 December 2022.
He moved there with his wife, Emma Wilhelmine, née Giesker, whom he had married on 1 October 1894.
- ↑ https://www.nobelprize.org/nobel_prizes/chemistry/laureates/1913/werner-bio.html Nobel Prize Retrieved 1 December 2012
- ↑ 3.0 3.1 3.2 3.3 3.4 "Alfred Werner - Swiss chemist". britannica.com. Retrieved 14 April 2018.
बाहरी संबंध
- {{Nobelprize}} template missing ID and not present in Wikidata. including the Nobel Lecture, 11 December 1913 On the Constitution and Configuration of Higher-Order Compounds
- The Nobel Prize in Chemistry 1913 - short article about his work on the linkage of atoms in molecules by which he has thrown new light on earlier investigations and opened up new fields of research especially in inorganic chemistry.