हेक्सोल: Difference between revisions
mNo edit summary |
No edit summary |
||
| Line 29: | Line 29: | ||
| AutoignitionPt = }} | | AutoignitionPt = }} | ||
}} | }} | ||
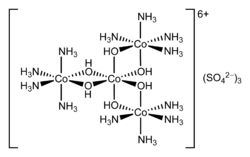
[[रसायन विज्ञान]] में, हेक्सोल | [[रसायन विज्ञान]] में, हेक्सोल एक धनायन है, जिसका सूत्र {[Co(NH<sub>3</sub>)<sub>4</sub>(OH)<sub>2</sub>]<sub>3</sub>Co}<sup>6+</sup> है यह एक समन्वय परिसर है जिसकी [[ऑक्सीकरण अवस्था]] +3 है। समन्वय परिसर में चार [[कोबाल्ट]] धनायन, बारह [[अमोनिया]] {{chem|NH|3}}अणु, और छह [[हाइड्रॉकसिल]] {{chem|HO|-}}आयन, होते हैं जिसकी ऑक्सीकरण संख्या +6 होती है। हाइड्रॉक्सी समूह केंद्रीय कोबाल्ट परमाणु और अन्य तीन के बीच पुलों के रूप में कार्य करते हैं, जो अमोनिया लिगैंड्स को ले जाते हैं। | ||
हेक्सोल के लवण, जैसे सल्फेट {[ | हेक्सोल के लवण, जैसे सल्फेट {[Co(NH<sub>3</sub>)<sub>4</sub>(OH)<sub>2</sub>]<sub>3</sub>Co}(SO<sub>4</sub>)<sub>3</sub>(H<sub>2</sub>O)<sub>x</sub>, पहले कृत्रिम गैर-कार्बन युक्त काइरल यौगिकों के रूप में ऐतिहासिक महत्व के हैं।<ref>Miessler, G. L. and Tarr, D. A. ''Inorganic Chemistry'', 3rd ed., Pearson/Prentice Hall publisher, {{ISBN|0-13-035471-6}}.</ref> <ref>{{cite journal |doi=10.1002/chir.20912|title=Optical Activity and Alfred Werner's Coordination Chemistry|year=2011|last1=Ernst|first1=Karl-Heinz|last2=Berke|first2=Heinz|journal=Chirality|volume=23|issue=3|pages=187–189|pmid=20928897}}</ref> | ||
== तैयारी == | == तैयारी == | ||
हेक्सोल के लवणों को सर्वप्रथम जोर्जेंसन द्वारा वर्णित किया गया था।<ref>{{cite journal|author=Jørgensen, S. M. |title=Zur Konstitution der Kobalt-, Chrom- und Rhodiumbasen|journal= Zeitschrift für Anorganische Chemie |year=1898|volume =16| pages =184–197|doi=10.1002/zaac.18980160116|url=https://zenodo.org/record/1428082}}</ref> हालाँकि यह वर्नर था जिसने इसकी संरचना को पहचाना।<ref name="hexol resolution"/> | हेक्सोल के लवणों को सर्वप्रथम जोर्जेंसन द्वारा वर्णित किया गया था।<ref>{{cite journal|author=Jørgensen, S. M. |title=Zur Konstitution der Kobalt-, Chrom- und Rhodiumbasen|journal= Zeitschrift für Anorganische Chemie |year=1898|volume =16| pages =184–197|doi=10.1002/zaac.18980160116|url=https://zenodo.org/record/1428082}}</ref> हालाँकि यह वर्नर था जिसने इसकी संरचना को पहचाना।<ref name="hexol resolution"/> सिस डाइकोटेट्रामाइनकोबाल्ट(III) धनायन [Co(NH<sub>3</sub>)<sub>4</sub>(H<sub>2</sub>O)<sub>2</sub>]<sup>3+</sup> युक्त तनु क्षार वाले विलयन को गर्म करके धनायन तैयार किया जाता है|<ref name="InorgSyn"/> | ||
[Co(NH<sub>3</sub>)<sub>4</sub>(H<sub>2</sub>O)<sub>2</sub>]<sup>3+</sup> + 2 HO<sup>−</sup> → {[Co(NH<sub>3</sub>)<sub>4</sub>(OH)<sub>2</sub>]<sub>3</sub>Co}<sup>6+</sup> + 4 NH<sub>4</sub><sup>+</sup> + 4 H<sub>2</sub>O | |||
=== हेक्सोल सल्फेट === | === हेक्सोल सल्फेट === | ||
सल्फेट के साथ शुरू करना और | सल्फेट के साथ शुरू करना और क्षार के रूप में [[अमोनियम हाइड्रॉक्साइड]] का उपयोग करना, शर्तों के क्षार पर, 9-हाइड्रेट, 6-हाइड्रेट, या हेक्सोल सल्फेट के 4-हाइड्रेट प्राप्त करता है। ये लवण पानी में कम घुलनशीलता के साथ गहरे भूरे-बैंगनी या काले सारणीबद्ध क्रिस्टल बनाते हैं। जब केंद्रित [[हाइड्रोक्लोरिक एसिड|हाइड्रोक्लोरिक अम्ल]] के साथ इलाज किया जाता है, तो हेक्सोल सल्फेट सीआईएस-डाइकोटेट्रामाइनकोबाल्ट (III) सल्फेट में परिवर्तित हो जाता है। [[सल्फ्यूरिक एसिड|सल्फ्यूरिक अम्ल]] को उबालने में, हेक्सोल सल्फेट ऑक्सीजन और नाइट्रोजन के विकास के साथ और भी कम हो जाता है।<ref name="InorgSyn">{{cite book|author1=Kauffman, George B. |author2=Pinnell, Robert P. |title=Tris[Tetrammine-μ-Dihydroxo-Cobalt(III)] Cobalt(III) Sulfate 4-Hydrate|chapter=Tris[tetrammine-μ-dihydroxo-cobalt(III)]cobalt(III) Sulfate 4-Hydrate |series= Inorganic Syntheses|year= 1960 |volume =6|pages=176–179|doi=10.1002/9780470132371.ch56|isbn=9780470132371 }}</ref> | ||
== ऑप्टिकल गुण == | == ऑप्टिकल गुण == | ||
हेक्सोल केशन दो चिरायता के रूप में मौजूद है जो केंद्रीय कोबाल्ट परमाणु और तीन बिडेंटेट परिधीय इकाइयों [सीओ(एनएच<sub>3</sub>)<sub>4</sub>(ओएच)<sub>2</sub>] के बीच बॉन्ड की व्यवस्था के | हेक्सोल केशन दो चिरायता के रूप में मौजूद है जो केंद्रीय कोबाल्ट परमाणु और तीन बिडेंटेट परिधीय इकाइयों [सीओ(एनएच<sub>3</sub>)<sub>4</sub>(ओएच)<sub>2</sub>] के बीच बॉन्ड की व्यवस्था के क्षार पर एक दूसरे की दर्पण छवियां हैं। यह डी{{sub|3}}([[तीन आयामों में बिंदु समूह|तीन आयामों) में बिंदु समूह के अंतर्गत आता है]]। चिरायता की प्रकृति की तुलना [[फेरिओक्सालेट]] {{chem|[Fe(C|2|O|4|)|3|]|3-}} आयनों से की जा सकती है . | ||
प्रयोगों के एक ऐतिहासिक सेट में, वैकल्पिक रूप से सक्रिय आयनों के साथ हेक्सोल का नमक - विशेष रूप से, इसका डी-(+)- ब्रोमोकेम्फोरसल्फोनेट - [[भिन्नात्मक क्रिस्टलीकरण (रसायन विज्ञान)|भिन्नात्मक क्रिस्टलीकरण]] द्वारा दो | प्रयोगों के एक ऐतिहासिक सेट में, वैकल्पिक रूप से सक्रिय आयनों के साथ हेक्सोल का नमक - विशेष रूप से, इसका डी-(+)- ब्रोमोकेम्फोरसल्फोनेट - [[भिन्नात्मक क्रिस्टलीकरण (रसायन विज्ञान)|भिन्नात्मक क्रिस्टलीकरण]] द्वारा दो धनायन आइसोमर्स के अलग-अलग लवणों में हल किया गया था।<ref name="hexol resolution">{{cite journal | title=Über mehrkernige Metallammoniake | language=de |trans-title=Poly-nucleated Metal-amines | author=Werner, A. | journal=Ber. Dtsch. Chem. Ges. | year=1907 | volume=40 | issue=2 | pages=2103–2125 | doi=10.1002/cber.190704002126| url=https://zenodo.org/record/1426223 }}</ref> एक अधिक कुशल संकल्प में बीआईएस (टारट्रेटो) डायंटिमोनेट (III) आयन शामिल है। हेक्सोल हेक्साकेशन में 2640 ° का उच्च विशिष्ट घुमाव है।<ref>{{cite book|author1=Yasui, Takaji |author2=Ama, Tomoharu |author3=Kauffman, George B. |title=Inorganic Syntheses |chapter=Resolution of the Dodecaamminehexa-μ-Hydroxo-Tetracobalt(III) Ion|series= Inorganic Syntheses |year=1992|volume=29|pages=169–174|doi=10.1002/9780470132609.ch41|isbn=9780470132609 }}</ref> | ||
== दूसरा हेक्सोल == | == दूसरा हेक्सोल == | ||
वर्नर ने एक दूसरे | वर्नर ने एक दूसरे अकाइरल हेक्सोल (फ्रेमी के नमक के उत्पादन से एक मामूली उपोत्पाद) का भी वर्णन किया जिसे उन्होंने गलत तरीके से एक रैखिक टेट्रामर के रूप में पहचाना। दूसरा हेक्सोल हेक्सान्यूक्लियर है (प्रत्येक आयन में छह कोबाल्ट केंद्र होते हैं), टेट्रान्यूक्लियर नहीं।<ref>{{cite journal|title=The rediscovery of Alfred Werner's second hexol|journal=[[Chemical Communications]]|issue=20|year= 2004|pages=2322–2323|doi=10.1039/B408277J|last1=Jackson|first1=W. Gregory|last2=McKeon|first2=Josephine A.|last3=Zehnder|first3=Margareta|last4=Neuberger|first4=Markus|last5=Fallab|first5=Silvio|pmid=15490001}}</ref> इसका बिन्दु समूह सी<sub>2</sub>एच है, और इसका सूत्र {{chem|[Co|6|(NH|3|)|14|(OH)|8|O|2|]|6+}} है, जबकि हेक्सोल का है {{chem|[Co|4|(NH|3|)|12|(OH)|6||]|6+}}. | ||
:[[File:Werner's-second-hexol-2004-2D-wedged.png|350px|वर्नर की दूसरी हेक्सोल 2004 व्याख्या]] | :[[File:Werner's-second-hexol-2004-2D-wedged.png|350px|वर्नर की दूसरी हेक्सोल 2004 व्याख्या]] | ||
Revision as of 20:27, 23 February 2023
| |

| |
| Names | |
|---|---|
| IUPAC name
Tris[tetrammine-μ-dihydroxocobalt(III)]cobalt (III) ion
| |
| Identifiers | |
3D model (JSmol)
|
|
| |
| |
| Properties | |
| Co4H42N12O18S3 | |
| Molar mass | 830.31 g·mol−1 |
| Sparingly soluble in water [1] | |
Except where otherwise noted, data are given for materials in their standard state (at 25 °C [77 °F], 100 kPa).
| |
रसायन विज्ञान में, हेक्सोल एक धनायन है, जिसका सूत्र {[Co(NH3)4(OH)2]3Co}6+ है यह एक समन्वय परिसर है जिसकी ऑक्सीकरण अवस्था +3 है। समन्वय परिसर में चार कोबाल्ट धनायन, बारह अमोनिया NH
3अणु, और छह हाइड्रॉकसिल HO−
आयन, होते हैं जिसकी ऑक्सीकरण संख्या +6 होती है। हाइड्रॉक्सी समूह केंद्रीय कोबाल्ट परमाणु और अन्य तीन के बीच पुलों के रूप में कार्य करते हैं, जो अमोनिया लिगैंड्स को ले जाते हैं।
हेक्सोल के लवण, जैसे सल्फेट {[Co(NH3)4(OH)2]3Co}(SO4)3(H2O)x, पहले कृत्रिम गैर-कार्बन युक्त काइरल यौगिकों के रूप में ऐतिहासिक महत्व के हैं।[2] [3]
तैयारी
हेक्सोल के लवणों को सर्वप्रथम जोर्जेंसन द्वारा वर्णित किया गया था।[4] हालाँकि यह वर्नर था जिसने इसकी संरचना को पहचाना।[5] सिस डाइकोटेट्रामाइनकोबाल्ट(III) धनायन [Co(NH3)4(H2O)2]3+ युक्त तनु क्षार वाले विलयन को गर्म करके धनायन तैयार किया जाता है|[1]
[Co(NH3)4(H2O)2]3+ + 2 HO− → {[Co(NH3)4(OH)2]3Co}6+ + 4 NH4+ + 4 H2O
हेक्सोल सल्फेट
सल्फेट के साथ शुरू करना और क्षार के रूप में अमोनियम हाइड्रॉक्साइड का उपयोग करना, शर्तों के क्षार पर, 9-हाइड्रेट, 6-हाइड्रेट, या हेक्सोल सल्फेट के 4-हाइड्रेट प्राप्त करता है। ये लवण पानी में कम घुलनशीलता के साथ गहरे भूरे-बैंगनी या काले सारणीबद्ध क्रिस्टल बनाते हैं। जब केंद्रित हाइड्रोक्लोरिक अम्ल के साथ इलाज किया जाता है, तो हेक्सोल सल्फेट सीआईएस-डाइकोटेट्रामाइनकोबाल्ट (III) सल्फेट में परिवर्तित हो जाता है। सल्फ्यूरिक अम्ल को उबालने में, हेक्सोल सल्फेट ऑक्सीजन और नाइट्रोजन के विकास के साथ और भी कम हो जाता है।[1]
ऑप्टिकल गुण
हेक्सोल केशन दो चिरायता के रूप में मौजूद है जो केंद्रीय कोबाल्ट परमाणु और तीन बिडेंटेट परिधीय इकाइयों [सीओ(एनएच3)4(ओएच)2] के बीच बॉन्ड की व्यवस्था के क्षार पर एक दूसरे की दर्पण छवियां हैं। यह डी3(तीन आयामों) में बिंदु समूह के अंतर्गत आता है। चिरायता की प्रकृति की तुलना फेरिओक्सालेट [Fe(C
2O
4)
3]3−
आयनों से की जा सकती है .
प्रयोगों के एक ऐतिहासिक सेट में, वैकल्पिक रूप से सक्रिय आयनों के साथ हेक्सोल का नमक - विशेष रूप से, इसका डी-(+)- ब्रोमोकेम्फोरसल्फोनेट - भिन्नात्मक क्रिस्टलीकरण द्वारा दो धनायन आइसोमर्स के अलग-अलग लवणों में हल किया गया था।[5] एक अधिक कुशल संकल्प में बीआईएस (टारट्रेटो) डायंटिमोनेट (III) आयन शामिल है। हेक्सोल हेक्साकेशन में 2640 ° का उच्च विशिष्ट घुमाव है।[6]
दूसरा हेक्सोल
वर्नर ने एक दूसरे अकाइरल हेक्सोल (फ्रेमी के नमक के उत्पादन से एक मामूली उपोत्पाद) का भी वर्णन किया जिसे उन्होंने गलत तरीके से एक रैखिक टेट्रामर के रूप में पहचाना। दूसरा हेक्सोल हेक्सान्यूक्लियर है (प्रत्येक आयन में छह कोबाल्ट केंद्र होते हैं), टेट्रान्यूक्लियर नहीं।[7] इसका बिन्दु समूह सी2एच है, और इसका सूत्र [Co
6(NH
3)
14(OH)
8O
2]6+
है, जबकि हेक्सोल का है [Co
4(NH
3)
12(OH)
6]6+
.
संदर्भ
- ↑ 1.0 1.1 1.2 Kauffman, George B.; Pinnell, Robert P. (1960). "Tris[tetrammine-μ-dihydroxo-cobalt(III)]cobalt(III) Sulfate 4-Hydrate". Tris[Tetrammine-μ-Dihydroxo-Cobalt(III)] Cobalt(III) Sulfate 4-Hydrate. Inorganic Syntheses. Vol. 6. pp. 176–179. doi:10.1002/9780470132371.ch56. ISBN 9780470132371.
- ↑ Miessler, G. L. and Tarr, D. A. Inorganic Chemistry, 3rd ed., Pearson/Prentice Hall publisher, ISBN 0-13-035471-6.
- ↑ Ernst, Karl-Heinz; Berke, Heinz (2011). "Optical Activity and Alfred Werner's Coordination Chemistry". Chirality. 23 (3): 187–189. doi:10.1002/chir.20912. PMID 20928897.
- ↑ Jørgensen, S. M. (1898). "Zur Konstitution der Kobalt-, Chrom- und Rhodiumbasen". Zeitschrift für Anorganische Chemie. 16: 184–197. doi:10.1002/zaac.18980160116.
- ↑ 5.0 5.1 Werner, A. (1907). "Über mehrkernige Metallammoniake" [Poly-nucleated Metal-amines]. Ber. Dtsch. Chem. Ges. (in Deutsch). 40 (2): 2103–2125. doi:10.1002/cber.190704002126.
- ↑ Yasui, Takaji; Ama, Tomoharu; Kauffman, George B. (1992). "Resolution of the Dodecaamminehexa-μ-Hydroxo-Tetracobalt(III) Ion". Inorganic Syntheses. Inorganic Syntheses. Vol. 29. pp. 169–174. doi:10.1002/9780470132609.ch41. ISBN 9780470132609.
- ↑ Jackson, W. Gregory; McKeon, Josephine A.; Zehnder, Margareta; Neuberger, Markus; Fallab, Silvio (2004). "The rediscovery of Alfred Werner's second hexol". Chemical Communications (20): 2322–2323. doi:10.1039/B408277J. PMID 15490001.
बाहरी संबंध
- Hexol Molecule of the Month September 1997 Website
- National Pollutant Inventory – सीओbalt fact sheet
