संचय विन्यास रसायन: Difference between revisions
m (11 revisions imported from alpha:संचय_विन्यास_रसायन) |
No edit summary |
||
| Line 143: | Line 143: | ||
{{Branches of chemistry}} | {{Branches of chemistry}} | ||
{{DEFAULTSORT:Combinatorial Chemistry}} | {{DEFAULTSORT:Combinatorial Chemistry}} | ||
[[Category:All articles with unsourced statements|Combinatorial Chemistry]] | |||
[[Category:Articles with hatnote templates targeting a nonexistent page|Combinatorial Chemistry]] | |||
[[Category: | [[Category:Articles with unsourced statements from November 2012|Combinatorial Chemistry]] | ||
[[Category:Created On 06/05/2023]] | [[Category:CS1 English-language sources (en)]] | ||
[[Category:Vigyan Ready]] | [[Category:Collapse templates|Combinatorial Chemistry]] | ||
[[Category:Created On 06/05/2023|Combinatorial Chemistry]] | |||
[[Category:Machine Translated Page|Combinatorial Chemistry]] | |||
[[Category:Navigational boxes| ]] | |||
[[Category:Navigational boxes without horizontal lists|Combinatorial Chemistry]] | |||
[[Category:Pages with script errors|Combinatorial Chemistry]] | |||
[[Category:Sidebars with styles needing conversion|Combinatorial Chemistry]] | |||
[[Category:Template documentation pages|Documentation/doc]] | |||
[[Category:Templates Vigyan Ready|Combinatorial Chemistry]] | |||
[[Category:Templates generating microformats|Combinatorial Chemistry]] | |||
[[Category:Templates that are not mobile friendly|Combinatorial Chemistry]] | |||
[[Category:Templates using TemplateData|Combinatorial Chemistry]] | |||
[[Category:Wikipedia metatemplates|Combinatorial Chemistry]] | |||
[[Category:कॉम्बिनेटरिक्स|रसायन विज्ञान]] | |||
[[Category:कॉम्बिनेटरियल केमिस्ट्री| कॉम्बिनेटरियल केमिस्ट्री ]] | |||
[[Category:दवाओं की खोज|Combinatorial Chemistry]] | |||
[[Category:पदार्थ विज्ञान|Combinatorial Chemistry]] | |||
[[Category:रसायन विज्ञान|Combinatorial Chemistry]] | |||
Latest revision as of 16:56, 17 May 2023
संचयविन्यास रसायन में रासायनिक संश्लिष्ट विधियाँ सम्मिलित होती हैं जो समान प्रक्रिया में बड़ी संख्या में (दसियों से हज़ारों या यहाँ तक कि लाखों) यौगिकों को तैयार करना संभव बनाती हैं। इन यौगिक लाइब्रेरी को मिश्रण, व्यक्तिगत यौगिकों के समूह या कंप्यूटर सॉफ्टवेयर द्वारा उत्पन्न रासायनिक संरचनाओं के रूप में बनाया जा सकता है।[1] संचयविन्यास रसायन का उपयोग छोटे अणुओं के संश्लेषण और पेप्टाइड्स के लिए किया जा सकता है।
रणनीतियाँ जो लाइब्रेरी के उपयोगी घटकों की पहचान करने की स्वीकृति देती हैं, वे भी संयोजी रसायन विज्ञान का भाग हैं। संचयविन्यास रसायन में उपयोग की जाने वाली विधियों को रसायन के बाहर भी प्रयुक्त किया जाता है।
इतिहास
संचयविन्यास रसायन का आविष्कार फुरका ए (ईटोवोस लोरैंड विश्वविद्यालय बुडापेस्ट हंगरी) द्वारा किया गया था, जिन्होंने 1982 में अप्रचलित किए गए एक दस्तावेज में इसके सिद्धांत, संयोजन संश्लेषण और एक विसंवलन प्रक्रिया का वर्णन किया था।[2] संयोजन विधि का सिद्धांत है : एकल चरणबद्ध प्रक्रिया में एक बहु-घटक यौगिक मिश्रण (संयोजन समूह) को संश्लेषित करें और समान प्रक्रिया में औषधि पदाभिलाषी या अन्य प्रकार के उपयोगी यौगिकों को खोजने के लिए इसे जांच करें। संयोजन विधि का सबसे महत्वपूर्ण नवाचार संश्लेषण में मिश्रण का उपयोग करना है और अनुवीक्षण जो प्रक्रिया की उच्च उत्पादकता सुनिश्चित करती है। आविष्कार के लिए प्रेरित करने वाली प्रेरणाएँ 2002 में प्रकाशित हुई थीं।[3]
परिचय
संयोजी विधि में अणुओं का संश्लेषण तेजी से बड़ी संख्या में अणुओं को उत्पन्न कर सकता है। उदाहरण के लिए, विविधता के तीन बिंदुओं (R1, R2, और R3) के साथ एक अणु संभव उत्पन्न कर सकता है। संरचनाएं, जहां , , और उपयोग किए गए विभिन्न प्रतिस्थापियों की संख्या हैं।[2]
संयोजन रसायन का मूल सिद्धांत बहुत बड़ी संख्या में यौगिकों के लाइब्रेरी को तैयार करना है और फिर लाइब्रेरी के उपयोगी घटकों की पहचान करना है।
हालांकि 1990 के दशक के बाद से उद्योग द्वारा संयुक्त रसायन विज्ञान को वास्तव में स्वीकृत किया गया है,[4] इसके कारण 1960 के दशक में देखी जा सकती हैं जब रॉकफेलर विश्वविद्यालय के एक शोधकर्ता ब्रूस मेरिफिल्ड ने पेप्टाइड्स के ठोस-अवस्था संश्लेषण की जांच प्रारंभ की थी।
अपने आधुनिक रूप में, संचयविन्यास रसायन शास्त्र का संभवतः औषधि उद्योग में इसका सबसे बड़ा प्रभाव पड़ा है।[5] एक यौगिक की गतिविधि प्रोफ़ाइल को अनुकूलित करने का प्रयास करने वाले शोधकर्ता कई अलग-अलग लेकिन संबंधित यौगिकों का 'रासायनिक लाइब्रेरी' बनाते हैं।[6][7] रोबोटिक्स में हुई वृद्धि ने संयोजी संश्लेषण के लिए एक औद्योगिक दृष्टिकोण का नेतृत्व किया है, जिससे कंपनियां नियमित रूप से प्रति वर्ष 100,000 से अधिक नए और अद्वितीय यौगिकों का उत्पादन कर पाती हैं।[8]
बड़ी संख्या में संरचनात्मक संभावनाओं को नियंत्रण करने के लिए, शोधकर्ता प्रायः एक ' आभासी लाइब्रेरी' बनाते हैं, सभी उपलब्ध अभिकारक के साथ दिए गए फार्माकोफोर (भेषजगुण) की सभी संभावित संरचनाओं की एक संगणनात्मक गणना है।[9] इस तरह के लाइब्रेरी में हजारों से लाखों 'आभासी' यौगिक सम्मिलित हो सकते हैं। शोधकर्ता विभिन्न गणनाओं और मानदंडों के आधार पर वास्तविक संश्लेषण के लिए 'आभासी लाइब्रेरी' के (एडीएमई, संगणनात्मक रसायन विज्ञान और परिमाणात्मक संरचना-गतिविधि संबंध देखें) एक उपसमुच्चय का चयन करेगा।
बहुलक (पेप्टाइड्स और ऑलिगोन्यूक्लियोटाइड्स)
संयोजी विभाजित-मिश्रण (विभंजन और संचय) संश्लेषण
संयोजी विभंजन-मिश्रण (विभंजन और संचय) संश्लेषण [10][11] रॉबर्ट ब्रूस मेरिफिल्ड द्वारा विकसित ठोस-प्रावस्था संश्लेषण पर आधारित है।[12] यदि 20 एमिनो अम्ल (या अन्य प्रकार के मूलभूत अंग) का उपयोग करके एक संयोजी पेप्टाइड समूह को संश्लेषित किया जाता है, तो बिंदु के रूप ठोस सहायक को 20 बराबर भागों में विभाजित किया जाता है। इसके बाद प्रत्येक भाग में एक अलग अमीनो अम्ल का युग्मन होता है। तीसरा प्रावस्था सभी भागों का मिश्रण है। इन तीन चरणों में एक चक्र सम्मिलित है। चक्र के चरणों को दोहराकर पेप्टाइड श्रृंखलाओं को बढ़ाया जा सकता है।
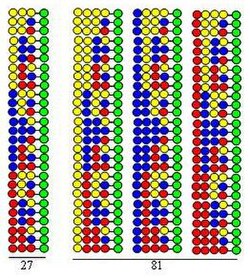
प्रक्रिया को दोनों चक्रों में निर्माण खंड के रूप में समान तीन अमीनो अम्ल का उपयोग करके डाइपेप्टाइड समूह के संश्लेषण द्वारा चित्रित किया गया है। इस समूह के प्रत्येक घटक में अलग-अलग क्रम में व्यवस्थित दो अमीनो अम्ल होते हैं। युग्मन में उपयोग किए जाने वाले अमीनो अम्ल को आकृति में पीले, नीले और लाल गोले द्वारा दर्शाया गया है। विभिन्न तीर ठोस संबल रेजिन (हरे गोले) को समान भागों में विभाजित करते हुए दिखाते हैं, ऊर्ध्वाधर तीरों का अर्थ है युग्मन और अभिसरण तीर संबल के भागों को मिलाने और समरूप बनाने का प्रतिनिधित्व करते हैं।
चित्र से पता चलता है कि दो संश्लिष्ट चक्रों में 9 डाईपेप्टाइड बनते हैं। तीसरे और चौथे चक्र में क्रमशः 27 ट्राइपेप्टाइड और 81 टेट्रापेप्टाइड बनेंगे।
"विभाजित-मिश्रण संश्लेषण" में कई उत्कृष्ट विशेषताएं हैं:
- यह अत्यधिक दक्ष है। जैसा कि चित्र प्रदर्शित करता है कि संश्लेषित प्रक्रिया (3, 9, 27, 81) में बनने वाले पेप्टाइड्स की संख्या निष्पादित चक्रों की संख्या के साथ तेजी से बढ़ती है। प्रत्येक संश्लेषित चक्र में 20 अमीनो अम्ल का उपयोग करके गठित पेप्टाइड्स की संख्या क्रमशः 400, 8,000, 160,000 और 3,200,000 है। इसका तात्पर्य यह है कि निष्पादित चक्रों की संख्या के साथ पेप्टाइड्स की संख्या तेजी से बढ़ती है।
- सभी पेप्टाइड अनुक्रम इस प्रक्रिया में बनते हैं जो चक्रों में प्रयुक्त अमीनो अम्ल के संयोजन से निकाले जा सकते हैं।
- संबल को समान नमूनों में विभाजित करना संग्रह के घटकों को लगभग समान मोलीय मात्रा में निर्माण सुनिश्चित होता है।
- संबल के प्रत्येक बिंदु पर केवल समान पेप्टाइड बनता है। यह युग्मन चरणों में केवल एक अमीनो अम्ल का उपयोग करने का परिणाम है। हालांकि, यह पूरी तरह से अज्ञात है कि पेप्टाइड कौन सा है जो एक चयनित बिंदु पर प्रग्रहण कर लेता है।
- विभाजित-मिश्रण पद्धति का उपयोग कार्बनिक या किसी अन्य प्रकार के समूह के संश्लेषण के लिए किया जा सकता है जिसे चरणबद्ध प्रक्रिया में इसके निर्माण खंड से तैयार किया जा सकता है।
1990 में तीन समूहों ने जैविक विधियों द्वारा और एक साल बाद फोडोर एट अल द्वारा पेप्टाइड [13][14][15] लाइब्रेरी को तैयार करने के तरीकों का वर्णन किया। छोटे कांच की स्लाइड्स पर पेप्टाइड सरणियों के संश्लेषण के लिए एक उल्लेखनीय विधि प्रकाशित की।[16] पेप्टाइड सरणियों की तैयारी के लिए मारियो गेसेन और उनके सहयोगियों द्वारा एक समानांतर संश्लेषण विधि विकसित की गई थी।[17] उन्होंने ठोस संबल के साथ अपने सिरों पर लेपित प्लास्टिक की छड़ (पिन) पर 96 पेप्टाइड्स को संश्लेषित किया। पिनों को एक सूक्ष्मदर्शी प्लेट मे अच्छी तरह रखे अभिकर्मकों के विलयन में निमज्जित किया गया। विधि विशेष रूप से स्वचालित समांतर संश्लेषक का उपयोग करके व्यापक रूप से प्रयुक्त होती है। यद्यपि समानांतर विधि वास्तविक दहनशील विधि की तुलना में बहुत मंद है, इसका लाभ यह है कि यह सही से ज्ञात है कि प्रत्येक पिन पर कौन सा पेप्टाइड या अन्य यौगिक बनता है।
विभाजित-मिश्रण और समान संश्लेषण दोनों के लाभों को मिलाने के लिए आगे की प्रक्रियाएँ विकसित की गईं। दो समूहों द्वारा वर्णित विधि में[18][19] ठोस संबल को पारगम्य प्लास्टिक झिल्ली में एक रेडियो-आवृत्ति टैग के साथ संलग्न किया गया था जो झिल्ली में बनने वाले यौगिक के कोड को ले गया था। प्रक्रिया विभाजित-मिश्रण विधि के समान की गई थी। विभाजित प्रावस्था में, हालांकि, झिल्ली के रेडियो-आवृत्ति टैग से पढ़े गए कोड के अनुसार प्रतिक्रिया वाहिकाओं के बीच झिल्ली वितरित किए गए थे।
फुरका एट अल द्वारा इसी उद्देश्य के लिए एक अलग विधि विकसित की गई थी।[20] स्ट्रिंग संश्लेषण कहा जाता है। इस पद्धति में, झिल्ली में कोई कोड नहीं होता है। वे एक हार में बिंदुओ की तरह पिरोए जाते हैं और दृढ़ रूप में प्रतिक्रिया वाहिकाओं में रखे जाते हैं। झिल्ली की पहचान, साथ ही साथ उनके पदार्थ, स्ट्रिंग्स पर व्याप्त उनकी स्थिति द्वारा संग्रहीत की जाती है। युग्मन के प्रत्येक प्रावस्था के बाद, निश्चित नियमों के अनुसार नए तारों के बीच झिल्ली का पुनर्वितरण किया जाता है।
छोटे अणु
औषधि खोज प्रक्रिया में भाग के छोटे अणुओं का संश्लेषण और जैविक मूल्यांकन सामान्य रूप से एक लंबी और कठिन प्रक्रिया रही है। संचयविन्यास रसायन विज्ञान हाल के दशकों में बड़ी संख्या में संभावित छोटे छोटे अणु औषधि पदाभिलाषी को शीघ्र और कुशलता से संश्लेषित करने के दृष्टिकोण के रूप में प्रदर्शित है। विशिष्ट संश्लेषण में, एक संश्लेषित योजना के अंत में केवल एक लक्ष्य अणु का उत्पादन होता है, संश्लेषण में प्रत्येक प्रावस्था में केवल समान उत्पाद का उत्पादन होता है। संयोजी संश्लेषण में, केवल एक प्रारंभिक पदार्थ का उपयोग करते समय, समान प्रतिक्रिया स्थितियों का उपयोग करके अणुओं के एक बड़ी लाइब्रेरी को संश्लेषित करना संभव है, जिसे तब उनकी जैविक गतिविधि के लिए जांचा जा सकता है। उत्पादों के इस निकाय को फिर तीन समान भागों में विभाजित किया जाता है जिसमें तीन उत्पादों में से प्रत्येक होता है, और फिर तीन अलग-अलग निकायों में से प्रत्येक को अभिकर्मक B, C, या D की एक अन्य इकाई के साथ प्रतिक्रिया दी जाती है, जो पूर्व 3 से 9 अद्वितीय यौगिकों का उत्पादन करती है। इस प्रक्रिया को तब तक दोहराया जाता है जब तक कि मूलभूत अंग की वांछित संख्या नहीं जुड़ जाती है, जिससे कई यौगिक बनते हैं। एक बहु-प्रावस्था संश्लेषण द्वारा यौगिकों के एक लाइब्रेरी को संश्लेषित करते समय, कुशल प्रतिक्रिया विधियों को नियोजित किया जाना चाहिए, और यदि प्रत्येक प्रतिक्रिया प्रावस्था के बाद पारंपरिक निर्मलीकरण विधियों का उपयोग किया जाता है, तो उत्पादन और दक्षता प्रभावित होगी।
ठोस-प्रावस्था संश्लेषण विशिष्ट शमन और निर्मलीकरण चरणों की आवश्यकता को कम करने के लिए संभावित समाधान प्रदान करता है जो प्रायः संश्लेषित रसायन विज्ञान में उपयोग किया जाता है। सामान्य रूप से, प्रारंभिक अणु एक ठोस सहायक (सामान्य रूप से एक अघुलनशील बहुलक) का अनुसरण करता है, फिर अतिरिक्त प्रतिक्रियाएं की जाती हैं, और अंतिम उत्पाद को शुद्ध किया जाता है और फिर पिंड सहायक से स्पष्ट किया जाता है। चूंकि लक्ष्य के अणु एक पिंड संबल से जुड़े होते हैं, इसलिए प्रत्येक प्रतिक्रिया के बाद निर्मलीकरण को कम करना संभव होता है, जिससे स्थायी तरल-तरल निष्कर्षण और विलायक वाष्पीकरण चरणों की आवश्यकता समाप्त हो जाती है, जिसमें अधिकांश संश्लेषित रसायन सम्मिलित होते हैं। इसके अतिरिक्त, विषम अभिकारकों का उपयोग करके, अतिक्रमण अभिकर्मकों का उपयोग मंद प्रतिक्रियाओं को पूरा करने के लिए किया जा सकता है, जिससे उत्पादन में और संशोधन हो सकता है। क्रोमैटोग्राफी (वर्णलेखिकी) जैसे अतिरिक्त निर्मलीकरण चरणों की आवश्यकता के बिना अतिक्रमण अभिकर्मकों को आसानी से प्रक्षालित किया जा सकता है।
इन वर्षों में, संयोजी रसायन विज्ञान में ठोस-प्रावस्था कार्बनिक संश्लेषण के उपयोग को परिष्कृत करने के लिए विभिन्न प्रकार के तरीकों का विकास किया गया है, जिसमें संश्लेषण और निर्मलीकरण की आसानी बढ़ाने के प्रयासों के साथ-साथ मध्यवर्ती उत्पादों को चिह्नित करने के लिए गैर-पारंपरिक तरीके भी सम्मिलित हैं। यद्यपि यहाँ वर्णित अधिकांश उदाहरण प्रत्येक प्रतिक्रिया प्रावस्था में विषम प्रतिक्रिया माध्यम को नियोजित करेंगे, बूथ और हॉजेस केवल पारंपरिक समाधान-प्रावस्था संश्लेषण के निर्मलीकरण प्रावस्था के समय ठोस-समर्थित अभिकर्मकों का उपयोग करने का एक प्रारंभिक उदाहरण प्रदान करते हैं।[21] उनके विचार में, समाधान-प्रावस्था रसायन विज्ञान, रेजिन के अणुओं को स्थिरक और हटाने के साथ-साथ स्थापित समाधान-प्रावस्था प्रतिक्रियाओं के ठोस-प्रावस्था एनालॉग्स को पुनः बनाने की आवश्यकता को समाप्त करने के लिए आवश्यक संबंध और विदलन प्रतिक्रियाओं से संरक्षण करने के लाभ प्रदान करता है।
संश्लेषण के अंत में एकल निर्मलीकरण चरण एक या अधिक अशुद्धियों को हटाने की स्वीकृति देता है, यह मानते हुए कि आपत्तिजनक अशुद्धता की रासायनिक संरचना ज्ञात है। जबकि ठोस-समर्थित अभिकर्मकों का उपयोग यौगिकों के संश्लेषण को बहुत सरल करता है, कई दहनशील संश्लेषणों को कई चरणों की आवश्यकता होती है, जिनमें से प्रत्येक को अभी भी निर्मलीकरण के कुछ रूपों की आवश्यकता होती है। आर्मस्ट्रांग एट अल बहु-घटक संघनन (एमसीसी ) कहे जाने वाले संयोजी समूहों को उत्पन्न करने के लिए एक-पात्र पद्धति का वर्णन करें।[22] इस योजना में, तीन या अधिक अभिकर्मक इस तरह से प्रतिक्रिया करते हैं कि प्रत्येक अभिकर्मक को समान प्रावस्था में अंतिम उत्पाद में सम्मिलित किया जाता है, जिससे बहु-प्रावस्था संश्लेषण की आवश्यकता समाप्त हो जाती है जिसमें कई निर्मलीकरण प्रावस्था सम्मिलित होते हैं। बहु-घटक संघनन में, यह निर्धारित करने के लिए कोई विसंक्रमण आवश्यक नहीं है कि कौन से यौगिक जैविक रूप से सक्रिय हैं क्योंकि सरणी में प्रत्येक संश्लेषण में केवल समान उत्पाद होता है, इस प्रकार यौगिक की पहचान स्पष्ट रूप से ज्ञात होनी चाहिए।
अन्य सरणी संश्लेषण, फिर भी विभाजित संश्लेषण द्वारा ओलिगोपेप्टाइड का एक बड़ी लाइब्रेरी उत्पन्न हुई।[23] हजारों यौगिकों को बनाने का दोष यह है कि निर्मित यौगिकों की संरचना का निर्धारण करना कठिन होता है। उनका समाधान आणविक टैग का उपयोग करना है, जहां एक डाई की एक छोटी राशि (1 pmol/bead) बिंदु से जुड़ी होती है, और एक निश्चित बिंदु की पहचान यह विश्लेषण करके निर्धारित की जा सकती है कि बिंदु पर कौन से टैग सम्मिलित हैं। टैग संलग्न करने से ग्राही की पहचान कितनी आसान हो जाती है, इसके बाद भी प्रत्येक सम्मिश्रण को उसकी ग्राही बंधन क्षमता के लिए व्यक्तिगत रूप से जांच करना अपेक्षाकृत अधिक असंभव होगा, इसलिए प्रत्येक ग्राही से एक डाई जुड़ी हुई थी, जैसे कि केवल वे ग्राही जो अपने कार्यद्रव से आबद्ध होते हैं, जो एक रंग परिवर्तन उत्पन्न करते हैं।
जब कई प्रतिक्रियाओं को एक सरणी में चलाने की आवश्यकता होती है (जैसे आर्मस्ट्रांग के एमसीसी सरणियों में से एक में वर्णित 96 प्रतिक्रियाएं), संश्लेषण के कुछ अधिक स्थायी स्वरूपों को दक्षता में सुधार के लिए स्वचालित किया जा सकता है। डेविट और जार्निक ने "डाइवोमेर विधि" नामक एक विधि का विस्तार किया है, जिसमें रासायनिक प्रतिक्रियाओं के कई लघु संस्करण सभी एक साथ संरचित किए जाते हैं।[24] यह विधि एक ऐसे उपकरण का उपयोग करती है जो रेजिन भार और प्रक्षालन चक्रों के साथ-साथ प्रतिक्रिया चक्र की सुरक्षा और निर्मलीकरण को स्वचालित करती है, और विभिन्न प्रकार के अणु वर्गों, हाइडेंटोइन्स और बेंजोडायजेपाइन को संश्लेषित करने के लिए इसका उपयोग करके उनकी विधि और उपकरण की व्यवहार्यता प्रदर्शित करती है। अधिकतम स्थितियों में 40 अलग-अलग प्रतिक्रियाएं चल रही हैं।
प्रायः, कीमती उपकरण और श्वाबैकर एट अल का उपयोग करना संभव नहीं होता है। लाइब्रेरी सदस्यों के समांतर संश्लेषण और यौगिकों के पूरे लाइब्रेरी के मूल्यांकन के संयोजन की एक सरल विधि का वर्णन करें।[25] उनकी पद्धति में, एक तन्तु जिसे अलग-अलग क्षेत्रों में विभाजित किया जाता है, एक वेलन के चारों ओर विलोपित किया जाता है, जहां एक अलग अभिकर्मक को प्रत्येक क्षेत्र में जोड़ा जाता है जो केवल समान प्रजाति को धारण करता है। तन्तु को पुनः विभाजित किया जाता है और एक अलग आकार के सिलेंडर के चारों ओर विलोपित किया जाता है, और फिर इस प्रक्रिया को पुनरावृत किया जाता है। इस पद्धति की सौम्यता यह है कि प्रत्येक उत्पाद की पहचान केवल तन्तु के साथ उसके स्थान से जानी जा सकती है, और संबंधित जैविक गतिविधि की पहचान प्रतिदीप्ति संकेतों के फूरियर रूपांतरण द्वारा की जाती है।
यहां वर्णित अधिकांश संश्लेषणों में, प्रारंभिक अभिकर्मक को ठोस संबल को/से जोड़ना और निकालना आवश्यक है। यह एक हाइड्रॉक्सिल समूह की उत्पादन को उत्पन्न कर दे सकता है, जो लक्ष्य सम्मिश्रण की जैविक गतिविधि को संभावित रूप से प्रभावित कर सकता है। एल्मैन 192 व्यक्तिगत 1,4-बेंजोडायजेपाइन यौगिक प्राप्त करने के लिए एक बहु-प्रावस्था संश्लेषण योजना में ठोस प्रावस्था का उपयोग करता है, जो प्रसिद्ध चिकित्सीय कारक हैं।[26] संभावित हाइड्रॉक्सिल समूह के अन्तः क्षेप की संभावना को नष्ट करने के लिए, अणुओं को पिंड संबल से जोड़ने के लिए सिलिल-एरिल रसायन शास्त्र का उपयोग करने वाली एक नवीन विधि का उपयोग किया जाता है जो संबल से अलग हो जाता है और शृंखलन का कोई चिन्ह नहीं छोड़ता है।
अणु को एक ठोस संबल के लिए स्थिरण करते समय, मध्यवर्ती को रेजिन से अणु को अलग किए बिना एक दूसरे से अलग नहीं किया जा सकता है। चूँकि प्रतिक्रिया की वृद्धि को जांच करने और उत्पाद संरचना की पुष्टि करने के लिए उपयोग की जाने वाली कई पारंपरिक लक्षण वर्णन तकनीकें समाधान-आधारित हैं, इसलिए विभिन्न तकनीकों का उपयोग किया जाना चाहिए। जेल-प्रावस्था 13 सी एनएमआर स्पेक्ट्रमदर्शी, एमएएलडीआई द्रव्यमान स्पेक्ट्रममिति, और आईआर स्पेक्ट्रमदर्शी का उपयोग संरचना की पुष्टि करने और ठोस-प्रावस्था प्रतिक्रियाओं की वृद्धि की सुरक्षा के लिए किया गया है।[27] गॉर्डन एट अल, कई स्थितियों का अध्ययन का वर्णन करते हैं जो छोटे अणुओं के दहनशील लाइब्रेरी को उत्पन्न करने के लिए इमाइन और पेप्टिडिल फॉस्फोनेट्स का उपयोग करते हैं।[27] इमाइन संग्रह उत्पन्न करने के लिए, एक रेजिन से जुड़े एक एमिनो अम्ल को एल्डिहाइड की उपस्थिति में प्रतिक्रिया दी जाती है। लेखकों ने प्रतिक्रियाओं की वृद्धि की सुरक्षा के लिए तेजी से 13 सी जेल प्रावस्था एनएमआर स्पेक्ट्रमदर्शी और स्थायित्व कोण प्रचक्रण 1 एच एनएमआर स्पेक्ट्रमदर्शी का उपयोग प्रदर्शित किया और दिखाया कि जब ट्राइमिथाइल ऑर्थोफोर्मेट को विलायक के रूप में उपयोग किया जाता है, तो कमरे के तापमान पर 10 मिनट से भी कम समय में अधिकांश इमाइन बन सकते हैं। निर्मित इमाइन को तब 4-थियाजोलिडिनोन्स, B-लैक्टम्स और पायरोलिडाइन्स उत्पन्न करने के लिए व्युत्पन्न किया गया था।
ठोस-प्रावस्था संबल का उपयोग यौगिकों के बड़े संयोजी लाइब्रेरी के संश्लेषण को बहुत सरल करता है। यह एक प्रारंभिक पदार्थ को एक ठोस संबल के लिए स्थिरण करके किया जाता है और फिर पर्याप्त रूप से बड़े लाइब्रेरी के निर्माण तक बाद की प्रतिक्रियाओं को संचरित करता है, जिसके बाद उत्पादों को अवलंब से अलग किया जाता है। मानक द्रव-तरल निष्कर्षण शोधन तकनीकों के संयोजन में समाधान-प्रावस्था संश्लेषण योजनाओं में उपयोग के लिए ठोस-प्रावस्था शुद्धि का उपयोग भी प्रदर्शित किया गया है।
विसंवलन और अनुवीक्षण
संयोजी लाइब्रेरी
संयोजी लाइब्रेरी छोटे-अणु रासायनिक यौगिकों के विशेष बहु-घटक मिश्रण हैं जो एकल चरणबद्ध प्रक्रिया में संश्लेषित होते हैं। वे व्यक्तिगत यौगिकों के संग्रह के साथ-साथ समानांतर संश्लेषण द्वारा तैयार यौगिकों की श्रृंखला से भिन्न होते हैं। यह एक महत्वपूर्ण विशेषता है कि उनके संश्लेषण में मिश्रण का उपयोग किया जाता है। मिश्रण का उपयोग प्रक्रिया की उच्च दक्षता सुनिश्चित करता है। दोनों अभिकारक मिश्रण हो सकते हैं और इस स्थिति में प्रक्रिया और भी अधिक दक्ष होगी। हालांकि व्यावहारिक कारणों से, विपाटित-मिश्रण विधि का उपयोग करने की परामर्श दी जाती है जिसमें दो मिश्रणों में से एक को एकल निर्माण खंड (बीबीएस) से बदल दिया जाता है। मिश्रण इतने महत्वपूर्ण हैं कि संश्लेषण में मिश्रण का उपयोग किए बिना कोई संयोजन लाइब्रेरी नहीं हैं, और यदि प्रक्रिया में मिश्रण का उपयोग अनिवार्य रूप से संयोजी लाइब्रेरी के रूप में किया जाता है। विभाजित-मिश्रण संश्लेषण सामान्य रूप से ठोस आलंबन का उपयोग करके स्पष्ट किया जाता है लेकिन इसे समाधान में भी प्रयुक्त करना संभव है। चूंकि वह संरचना करता है इसलिए घटक अज्ञात हैं, अनुवीक्षण करने में विसंवलन विधियों का उपयोग करने की आवश्यकता है। संयोजी लाइब्रेरी की सबसे महत्वपूर्ण विशेषताओं में से एक यह है कि पूरे मिश्रण को समान प्रक्रिया में प्रदर्शित किया जा सकता है। यह इन लाइब्रेरी को औषधीय अनुसंधान में बहुत उपयोगी बनाता है। पूर्ण संयोजी लाइब्रेरी के आंशिक लाइब्रेरी को भी संश्लेषित किया जा सकता है। उनमें से कुछ का उपयोग विसंवलन में किया जा सकता है[28]
ठोस संबल से विखंडित लाइब्रेरी का विघटन
यदि संयोजी लाइब्रेरी के संश्लेषित अणुओं को ठोस आधार से अलग किया जाता है तो एक घुलनशील मिश्रण बनता है। इस तरह के समाधान में लाखों अलग-अलग यौगिक मिल सकते हैं। जब यह संश्लेषित विधि विकसित की गई थी, तो पहली बार अणुओं की पहचान करना और उपयोगी गुणों वाले अणुओं को खोजना असंभव लग रहा था। हालाँकि, समस्या को हल करने के लिए उपयोगी घटकों की पहचान के लिए रणनीतियाँ विकसित की गई थीं। ये सभी रणनीतियाँ आंशिक मिश्रण के संश्लेषण और परीक्षण पर आधारित हैं। 1982 में नोटरीकृत फुरका के उपर्युक्त आलवख में शीघ्र से शीघ्र पुनरावृत्त रणनीति का वर्णन किया गया है।[2] विधि को बाद में एर्ब एट अल पुनरावर्ती विसंवलन के नाम से द्वारा स्वतंत्र रूप से प्रकाशित किया गया था।[29]
पुनरावर्ती विसंवलन
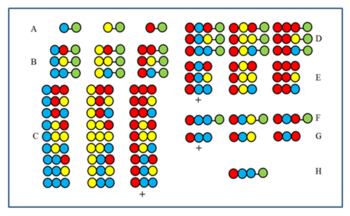
विधि को चित्र द्वारा समझा जा सकता है। 27 सदस्यीय पेप्टाइड लाइब्रेरी को तीन अमीनो अम्ल से संश्लेषित किया जाता है। पहले (A) और दूसरे (B) चक्रों के बाद उन्हें मिलाने से पहले नमूने अलग रखे गए थे। तीसरे चक्र (C) के उत्पादों को मिलाने से पहले विभाजित किया जाता है फिर गतिविधि के लिए परीक्षण किया जाता है। मान लीजिए कि + चिन्ह द्वारा लेबल किया गया समूह सक्रिय है। अंतिम युग्मन स्थिति (CP) पर सभी सदस्यों के पास लाल अमीनो अम्ल होता है। परिणामस्वरूप, सक्रिय सदस्य के पास अंतिम CP में लाल अमीनो अम्ल भी होता है। फिर लाल अमीनो अम्ल को नमूने D प्राप्त करने के लिए दूसरे चक्र (B) के बाद अलग रखे गए तीन नमूनों से जोड़ा जाता है। विभंजन के बाद, तीन E नमूने बनते हैं। यदि परीक्षण के बाद + द्वारा चिह्नित नमूना सक्रिय है तो यह दर्शाता है कि नीला अमीनो अम्ल सक्रिय घटक में दूसरे CP पर प्रग्रहण कर लेता है। फिर तीन A नमूनों में पहले नीला फिर लाल अमीनो अम्ल युग्मित (F) होता है, फिर विदलन (G) के बाद पुनः परीक्षण किया जाता है। यदि + घटक सक्रिय प्रमाणित होता है, तो सक्रिय घटक का क्रम निर्धारित किया जाता है और H में दिखाया जाता है।
स्थितीय अवलोकन
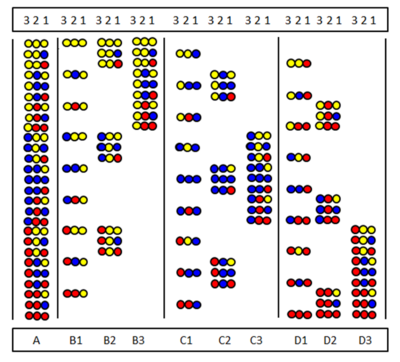
फुरका एट अल [30] और पिनिला एट अल द्वारा स्वतंत्र रूप से स्थितीय अवलोकन प्रारंभ की गई थी।[31] विधि मिश्रणों की श्रृंखला के संश्लेषण और परीक्षण पर आधारित है। जिसमें समान अमीनो अम्ल एक निश्चित अनुक्रम स्थिति पर प्रग्रहण कर लेता है। यह चित्र तीन अमीनो अम्ल से बने पूर्ण पेप्टाइड त्रितयणु लाइब्रेरी (A) के नौ उप-लाइब्रेरी (B1-D3) को दर्शाता है। उप-लाइब्रेरी में एक स्थिति होती है जो सभी घटकों में समान अमीनो अम्ल द्वारा प्रग्रहण कर ली जाती है। एक लाइब्रेरी के संश्लेषण में संबल विभाजित नहीं होता है और पूरे नमूने में केवल एक एमिनो अम्ल जोड़ा जाता है। परिणामस्वरूप, एक स्थिति वास्तव में सभी घटकों में समान अमीनो अम्ल द्वारा प्रग्रहण कर ली जाती है। उदाहरण के लिए, B2 उप-लाइब्रेरी स्थिति 2 में सभी नौ घटकों में पीले अमीनो अम्ल का प्रग्रहण है। यदि अनुवीक्षण परीक्षण में यह उप-लाइब्रेरी धनात्मक प्रतिक्रिया देती है तो इसका तात्पर्य है कि सक्रिय पेप्टाइड में स्थिति 2 भी पीले अमीनो अम्ल द्वारा प्रग्रहण कर लिया गया है। सभी नौ (या कभी-कभी कम) उप-लाइब्रेरी का परीक्षण करके अमीनो अम्ल अनुक्रम निर्धारित किया जा सकता है।
लोप (ओमिशन) लाइब्रेरी
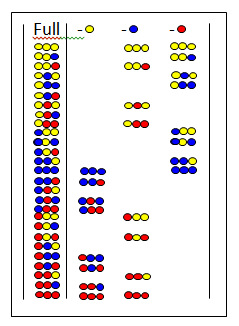
लोप लाइब्रेरी में[32][33] मिश्रण के सभी पेप्टाइड्स से एक निश्चित अमीनो अम्ल नष्ट है। यह चित्र पूर्ण लाइब्रेरी और तीन लोप लाइब्रेरी को दर्शाता है। शीर्ष पर छोड़े गए अमीनो अम्ल दिखाए जाते हैं। यदि लोप लाइब्रेरी एक ऋणात्मक परीक्षण देता है तो सक्रिय घटक में छोड़ा गया अमीनो अम्ल सम्मिलित होता है।
बंधे हुए संयोजी लाइब्रेरी का विखंडन
यदि पेप्टाइड्स को ठोस संबल से अलग नहीं किया जाता है तो हम बिंदुओ के मेल को संयोजित करते है, प्रत्येक बिंदु में एक पेप्टाइड होता है। स्मिथ और उनके सहयोगी[34] ने पहले दिखाया था कि पेप्टाइड्स का परीक्षण शृंखला के रूप में भी किया जा सकता है। इस दृष्टिकोण का उपयोग पेप्टाइड लाइब्रेरी की अनुवीक्षण में भी किया गया था। शृंखला पेप्टाइड लाइब्रेरी को प्रतिबंध करने लक्ष्य प्रोटीन के साथ परीक्षण किया गया था। जिन बिंदुओ से प्रोटीन जुड़ा हुआ था, उन्हें निकाल लिया गया, बिन्दु से प्रोटीन को हटा दिया गया, फिर अनुक्रमण द्वारा शृंखला पेप्टाइड की पहचान की गई। टेलर और मोर्केन ने कुछ अलग दृष्टिकोण स्वीकृत किया।[35] उन्होंने गैर-पेप्टाइड शृंखला लाइब्रेरी में उत्प्रेरक की पहचान करने के लिए अवरक्त ऊष्मालेखन का उपयोग किया। विधि उस ऊष्मा पर आधारित होती है जो बिंदुओ में विकसित होती है जिसमें उत्प्रेरक होता है जब शृंखला लाइब्रेरी को कार्यद्रव के समाधान में निमज्जित किया जाता है। जब एक अवरक्त सूक्ष्मदर्शी के माध्यम से बिंदुओ की जांच की जाती है तो बिंदु युक्त उत्प्रेरक प्रदीप्ति बिन्दुओ के रूप में दिखाई देते हैं और उन्हें बाहर निकाला जा सकता है।
एन्कोडेड संयोजी लाइब्रेरी
यदि हम एक गैर-पेप्टाइड कार्बनिक लाइब्रेरिज लाइब्रेरी के साथ व्यवहार करते हैं, तो बिंदु की पदार्थ की पहचान निर्धारित करना उतना आसान नहीं है जितना कि पेप्टाइड के स्थिति में होता है। इस कठिनाई को कम करने के लिए, लाइब्रेरी के संश्लेषण के साथ-साथ बिंदुओ को संलग्न करने के तरीकों को विकसित किया गया था, अणु जो बिंदु में बने यौगिक की संरचना को कूटबद्ध करते हैं।ओह्लमेयर और उनके सहयोगियों ने एक बाइनरी एन्कोडिंग विधि प्रकाशित की[36] उन्होंने 18 टैगिंग अणुओं के मिश्रण का उपयोग किया, जो उन्हें बिंदुओ से अलग करने के बाद इलेक्ट्रॉन प्रग्रहण गैस क्रोमैटोग्राफी द्वारा पहचाना जा सकता था। सरकार एट अल वर्णित पेंटेनोइक एमाइड्स (COPAs) के चिरल ओलिगोमर्स जिनका उपयोग बड़े पैमाने पर एन्कोडेड ओबीओसी लाइब्रेरी के निर्माण के लिए किया जा सकता है।[37] केर एट अल एक नवीन एन्कोडिंग विधि प्रस्तुत की[38] बिंदुओ से एक लंबकोणीय रूप से संरक्षित हटाने योग्य द्विकार्यात्मक शृंखलन को बिन्दुओ से जोड़ा गया था। शृंखलन के एक सिरे का उपयोग लाइब्रेरी के गैर-प्राकृतिक ब्लॉकों को संलग्न करने के लिए किया गया था, जबकि दूसरे सिरे पर अमीनो अम्ल त्रिक को एन्कोडिंग से जोड़ा गया था। ब्लॉक गैर-प्राकृतिक अमीनो अम्ल थे और उनके एन्कोडिंग अमीनो अम्ल त्रिक की श्रृंखला को एडमैन निम्नीकरण द्वारा निर्धारित किया जा सकता था। इस तरह के एन्कोडिंग का महत्वपूर्ण स्वरूप लाइब्रेरी के सदस्यों को उनके संलग्न एन्कोडिंग टैग के साथ मिलकर एक घुलनशील लाइब्रेरी बनाने की संभावना थी। निकोलाजेव एट अल द्वारा समान दृष्टिकोण का उपयोग किया गया था। पेप्टाइड्स के साथ एन्कोडिंग के लिए[39] 1992 में ब्रेनर और लर्नर ने ठोस संबल के बिंदुओ को एनकोड करने के लिए डीएनए अनुक्रम प्रस्तुत किया जो सबसे सफल एन्कोडिंग विधि प्रमाणित हुई।[40] नील्सन, ब्रेनर और जैंडा ने डीएनए एन्कोडिंग को प्रयुक्त करने के लिए केर दृष्टिकोण का भी उपयोग किया[41] समय की नवीनतम अवधि में डीएनए अनुक्रमण में महत्वपूर्ण वृद्धि हुई है। अगली पीढ़ी की तकनीक समानांतर में बड़ी संख्या में नमूनों को अनुक्रमित करना संभव बनाती है जो डीएनए एन्कोडेड लाइब्रेरी की अनुवीक्षण में बहुत महत्वपूर्ण है। एक अन्य नवप्रवर्तन था जिसने डीएनए एन्कोडिंग की सफलता में योगदान दिया। 2000 में हैल्पिन और हारबरी ने डीएनए एन्कोडेड संयोजी लाइब्रेरी के विपाटित-मिश्रण संश्लेषण में ठोस संबल को छोड़ दिया और इसे एन्कोडिंग डीएनए ओलिगोमर्स द्वारा बदल दिया। ठोस प्रावस्था विभाजन और संचय संश्लेषण में लाइब्रेरी के घटकों की संख्या संबल के बिंदुओ की संख्या से अधिक नहीं हो सकती है। लेखकों के नवीन दृष्टिकोण से, इस नियंत्रण को समाप्त कर दिया गया और व्यावहारिक रूप से असीमित संख्या में नए यौगिक तैयार करना संभव हो गया।[42] उदाहरण के लिए डेनिश कंपनी नवविकास ने 40 ट्रिलियन युक्त डीएनए एन्कोडेड लाइब्रेरी को संश्लेषित किया! अवयव[43] डीएनए एन्कोडेड लाइब्रेरी घुलनशील हैं जो अनुवीक्षण में कुशल आत्मीयता बंधन को प्रयुक्त करना संभव बनाता है। कुछ लेखक डीएनए एन्कोडेड संयोजी लाइब्रेरी के एक्रोमिम के लिए डीईएल प्रयुक्त करते हैं, अन्य डीईसीएल का उपयोग कर रहे हैं। बाद मे अपेक्षाकृत अधिक अच्छा प्रतीत होता है क्योंकि इस नाम में इन लाइब्रेरी की संयुक्त प्रकृति स्पष्ट रूप से व्यक्त की गई है। वर्तमान सहस्राब्दी के पहले दशक में कई प्रकार के डीएनए एन्कोडेड संयोजी लाइब्रेरी को प्रस्तुत किया गया था और उनका वर्णन किया गया था। इन लाइब्रेरी को औषधि अनुसंधान में बहुत सफलतापूर्वक प्रयुक्त किया जाता है।
- गार्टनर एट अल द्वारा 2001 में वर्णित संयोजन लाइब्रेरी के डीएनए टेम्पलेटेड संश्लेषण।[44]
- 2004 में म्लेको एट अल द्वारा आविष्कार की गई दोहरी फ़ार्माकोफ़ोर डीएनए एन्कोडेड संयोजी लाइब्रेरी।[45]
- 2004 में हार्बरी हैल्पिन और हारबरी द्वारा प्रकाशित अनुक्रम एन्कोडेड रूटिंग।[46]
- एकल फ़ार्माकोफ़ोर डीएनए एन्कोडेड संयोजी लाइब्रेरी को 2008 में मनोकी एट अल द्वारा प्रस्तुत किया गया।[47]
- 2009 में हैनसेन एट अल द्वारा प्रकाशित योक्टोलीटर-पैमाना अभिक्रियक का उपयोग करके निर्मित डीएनए एन्कोडेड संयोजी लाइब्रेरी।[48]
पृष्ठ डीएनए-एन्कोडेड रासायनिक लाइब्रेरी में उनके संश्लेषण और अनुप्रयोग के बारे में विवरण पाए जाते हैं। डीएनए एन्कोडेड घुलनशील संयोजी लाइब्रेरी में कमियां भी हैं। सबसे पहले, ठोस संबल के उपयोग से मिलने वाला लाभ पूरी तरह से नष्ट हो जाता है। इसके अतिरिक्त, डीएनए एन्कोडिंग श्रृंखलाओं का बहुआयनिक वर्ण संश्लेषण में गैर-जलीय विलायक की उपयोगिता को सीमित करता है। इस कारण से कई प्रयोगशालाएं डीईसीएल के संश्लेषण में उपयोग के लिए डीएनए संगत प्रतिक्रियाओं को विकसित करना चयन करती हैं। और उपलब्ध में से कुछ का पहले ही वर्णन किया जा चुका है[49][50][51]
पदार्थ विज्ञान
पदार्थ विज्ञान ने नए पदार्थों की खोज के लिए संचयविन्यास रसायन विज्ञान की तकनीकों को प्रयुक्त किया है। नब्बे के दशक के मध्य [52] सिलिकॉन कार्यद्रव पर तत्वों के सह-निक्षेपण द्वारा प्राप्त संदीप्तिशील पदार्थ के संदर्भ में इस कार्य का नेतृत्व पीजी शुल्त्स एट अल ने किया था। उनका कार्य 1970 में जे. जे. हनक द्वारा किया गया था[53] लेकिन उस समय विधि के प्रसार के लिए कंप्यूटर और रोबोटिक्स उपकरण उपलब्ध नहीं थे। कई शैक्षणिक समूहों[54][55][56][57] के साथ-साथ बड़े अनुसंधान और विकास कार्यक्रमों वाली कंपनियों (सिमाइक्स तकनीक, जीई, डॉव रसायन आदि) द्वारा कार्य जारी रखा गया है। उत्प्रेरण,[58] विलेपन,[59] इलेक्ट्रॉनिक्स,[60] और कई अन्य क्षेत्र के लिए तकनीक का बड़े पैमाने पर उपयोग किया गया है।[61] उत्पादित डेटा की विशाल मात्रा को नियंत्रित करने, प्रशासित करने और संग्रहीत करने के लिए उपयुक्त सूचना विज्ञान उपकरणों का अनुप्रयोग महत्वपूर्ण है।[62] बड़े प्रयोगात्मक स्थानों को कुशलतापूर्वक संबोधित करने के लिए प्रयोग विधियों के नए प्रकार के डिजाइन भी विकसित किए गए हैं जिन्हें संयोजन विधियों का उपयोग करके संशोधित किया जा सकता है।[63]
विविधता उन्मुख लाइब्रेरी
तथापि दो दशकों से भी अधिक समय से संयोजी रसायन प्रारंभिक औषधि की खोज का एक अनिवार्य भाग रहा है, लेकिन अब तक एफडीए द्वारा नैदानिक उपयोग के लिए केवल एक डे नोवो संयोजन रसायन-संश्लेषित रसायन (सोराफनीब, उन्नत गुर्दे के कैंसर के लिए संकेतित एक मल्टीकाइनेज अवरोधक) को स्वीकृति दी गई है।[64] संयोजी रसायन विज्ञान के उत्पादों द्वारा समावेश किए गए बल्कि सीमित रासायनिक स्थान से जुड़ने के लिए दृष्टिकोण की विकृत सफलता दर के विश्लेषण का सुझाव दिया गया है।[65] संयोजी रसायन लाइब्रेरी में यौगिकों के गुणों की तुलना स्वीकृत दवाओं और प्राकृतिक उत्पादों से तुलना करते समय, फ़ेहर और श्मिट[65] द्वारा ध्यान दिया गया कि संचयविन्यास रसायन शास्त्र लाइब्रेरी विशेष रूप से चिरायता (रसायन विज्ञान) की कमी के साथ-साथ संरचना की कठोरता से निहित हैं, दोनों को व्यापक रूप से औषधि-जैसी गुणों के रूप में माना जाता है। तथापि हाल के दिनों में प्राकृतिक उत्पाद औषधि की खोज संभव्यता औषधीय उद्योग में सबसे आधुनिक प्रणाली के अनुकूल प्रवृत्ति नहीं रही है,[citation needed] नई रासायनिक संस्थाओं का एक बड़ा भाग अभी भी प्रकृति-व्युत्पन्न यौगिक हैं,[66][67][68][69][70][71] और इस प्रकार, यह सुझाव दिया गया है कि अनुवीक्षण लाइब्रेरी की रासायनिक विविधता को बढ़ाकर संचयविन्यास रसायन विज्ञान की प्रभावशीलता में संशोधन किया जा सकता है।[72] चिरायता और कठोरता के रूप में दो सबसे महत्वपूर्ण विशेषताएं हैं जो अनुमोदित दवाओं और प्राकृतिक उत्पादों को संचयविन्यास रसायन विज्ञान लाइब्रेरी में यौगिकों से अलग करती हैं ये दो समस्याएं हैं जो तथाकथित विविधता उन्मुख लाइब्रेरी में जोर देते हैं, अर्थात यौगिक संग्रह जो केवल बड़ी संख्या में यौगिकों के अतिरिक्त रासायनिक स्थान को विस्तृत करने का लक्ष्य रखते हैं।।[73][74][75][76][77][78]
पेटेंट वर्गीकरण उपवर्ग
अंतर्राष्ट्रीय पेटेंट वर्गीकरण (आईपीसी) के 8वें संस्करण में, जो 1 जनवरी, 2006 को प्रयुक्त हुआ, संयुक्त रसायन विज्ञान "C40B" के क्षेत्र में आविष्कारों से संबंधित पेटेंट अनुप्रयोगों और पेटेंट के लिए एक विशेष उपवर्ग बनाया गया है।
यह भी देखें
- संयोजन
- रासायनिक सूचना विज्ञान
- संयुक्त जीव विज्ञान
- औषधि का अन्वेषण
- गतिशील संयोजन रसायन
- उच्च परिणाम अनुवीक्षण
- गणितीय रसायन
- आणविक मॉडलिंग
संदर्भ
- ↑ Pottel, J.; Moitessier, N. (2017). "सिंथेटिक रूप से सुलभ, स्थानीय रासायनिक उप-स्थानों का अनुकूलन योग्य उत्पादन". J. Chem. Inf. Model. 57 (3): 454–467. doi:10.1021/acs.jcim.6b00648. PMID 28234470.
- ↑ 2.0 2.1 2.2 फुरका ए. Tanulmány, gyógyászatilag hasznosítható पेप्टाइडक szisztematikus felkutatásának lehetőségéről (और औषधीय रूप से उपयोगी पेप्टाइड्स के लिए व्यवस्थित खोज की संभावना पर अध्ययन https://mersz.hu/mod/object.php?objazonosito=matud202006_f42772_i2
- ↑ https://en.wikipedia.org/wiki/Combinatorial_chemistry#cite_note-3
- ↑ "COMBINATORIAL CHEMISTRY: A REVIEW". International Journal of Pharmaceutical Sciences and Research. 4 (7). July 2013. doi:10.13040/IJPSR.0975-8232.4(7).2502-16. Retrieved June 21, 2020.
- ↑ Lesney, Mark S. (2002). "Concocting combinatorials: Chemistry in drug development". Retrieved October 19, 2018.
- ↑ Dolle, Roland (2011). रासायनिक पुस्तकालय डिजाइन का ऐतिहासिक अवलोकन. in Zhou, J.Z. (ed.), Chemical Library Design, Methods in Molecular Biology, Springer, 2011, Chapter 1, pp. 3-25.
- ↑ Podlewska, S.; Czarnecki, W.M.; Kafel, R.; Bojarski, A.J. (2017). "Creating the New from the Old: Combinatorial Libraries Generation with Machine-Learning-Based Compound Structure Optimization". J. Chem. Inf. Modeling. 57 (2): 133–147. doi:10.1021/acs.jcim.6b00426. PMID 28158942.
- ↑ Jeffrey W. Noonan et al. "Advancing Parallel Solution Phase Library Synthesis through Efficient Purification, Quantitation, and Characterization Techniques" Journal of Laboratory Automation, 48 (1992) 3789.
- ↑ E. V.Gordeeva et al. "COMPASS program - an original semi-empirical approach to computer-assisted synthesis" Tetrahedron, 48 (1992) 3789.
- ↑ Furka Á, Sebestyén F, Asgedom M, Dibó G. Cornucopia of peptides by synthesis. In Highlights of Modern Biochemistry, Proceedings of the 14th International Congress of Biochemistry. VSP.Utrecht.1988; 5; p. 47.
- ↑ Á. Furka, F. Sebestyen, M. Asgedom, G. Dibo, General method for rapid synthesis of multicomponent peptide mixtures. Int. J. Peptide Protein Res., 1991, 37, 487-493.
- ↑ Merrifield RB, 1963 J. Am. Chem. Soc. 85, 2149.
- ↑ Scott, J.; Smith, G. (1990-07-27). "एक एपिटोप लाइब्रेरी के साथ पेप्टाइड लिगेंड की खोज". Science. American Association for the Advancement of Science (AAAS). 249 (4967): 386–390. Bibcode:1990Sci...249..386S. doi:10.1126/science.1696028. ISSN 0036-8075. PMID 1696028.
- ↑ Cwirla, S. E.; Peters, E. A.; Barrett, R. W.; Dower, W. J. (1990-08-01). "Peptides on phage: a vast library of peptides for identifying ligands". Proceedings of the National Academy of Sciences. 87 (16): 6378–6382. Bibcode:1990PNAS...87.6378C. doi:10.1073/pnas.87.16.6378. ISSN 0027-8424. PMC 54537. PMID 2201029.
- ↑ J. J. Devlin, L. C. Panganiban and P. E. Devlin Science 1990, 249, 404.
- ↑ Fodor SP, Read JL, Pirrung MC, Stryer L, Lu AT, Solas D, 1991. Light-directed, spatially addressable parallel chemical synthesis. Science 251, 767-73.
- ↑ H. M. Geysen, R. H. Meloen, S. J. Barteling Proc. Natl. Acad. Sci. USA 1984, 81, 3998.
- ↑ E. J. Moran, S. Sarshar, J. F. Cargill, M. Shahbaz, A Lio, A. M. M. Mjalli, R. W. Armstrong J. Am. Chem. Soc. 1995, 117, 10787.
- ↑ K. C. Nicolaou, X –Y. Xiao, Z. Parandoosh, A. Senyei, M. P. Nova Angew. Chem. Int. Ed. Engl. 1995, 36, 2289.
- ↑ Á. Furka, J. W. Christensen, E. Healy, H. R. Tanner, H. Saneii J. Comb. Chem. 2000, 2, 220.
- ↑ Booth, R. John; Hodges, John C. (1999–2001). "मिश्रित संश्लेषण उत्पादों के तेजी से शुद्धिकरण के लिए ठोस-समर्थित अभिकर्मक रणनीतियाँ". Accounts of Chemical Research (in English). 32 (1): 18–26. doi:10.1021/ar970311n. ISSN 0001-4842.
- ↑ Armstrong, Robert W.; Combs, Andrew P.; Tempest, Paul A.; Brown, S. David; Keating, Thomas A. (1996–2001). "कॉम्बिनेटरियल लाइब्रेरी सिंथेसिस के लिए मल्टीपल-कंपोनेंट कंडेनसेशन स्ट्रैटेजीज". Accounts of Chemical Research (in English). 29 (3): 123–131. doi:10.1021/ar9502083. ISSN 0001-4842. S2CID 95815562.
- ↑ Still, W. Clark (1996–2001). "एन्कोडेड कॉम्बिनेटरियल लाइब्रेरी का उपयोग करके सिंथेटिक रिसेप्टर्स द्वारा अनुक्रम-चयनात्मक पेप्टाइड बाइंडिंग की खोज". Accounts of Chemical Research (in English). 29 (3): 155–163. doi:10.1021/ar950166i. ISSN 0001-4842.
- ↑ DeWitt, Sheila Hobbs; Czarnik, Anthony W. (1996–2001). "पार्के-डेविस के डायवर्सोमर विधि का उपयोग करके संयुक्त कार्बनिक संश्लेषण". Accounts of Chemical Research (in English). 29 (3): 114–122. doi:10.1021/ar950209v. ISSN 0001-4842.
- ↑ Schwabacher, Alan W.; Shen, Yixing; Johnson, Christopher W. (1999–2009). "फूरियर ट्रांसफॉर्म कॉम्बिनेटरियल केमिस्ट्री". Journal of the American Chemical Society (in English). 121 (37): 8669–8670. doi:10.1021/ja991452i. ISSN 0002-7863.
- ↑ Ellman, Jonathan A. (1996–2001). "लघु-अणु पुस्तकालयों का डिजाइन, संश्लेषण और मूल्यांकन". Accounts of Chemical Research (in English). 29 (3): 132–143. doi:10.1021/ar950190w. ISSN 0001-4842.
- ↑ 27.0 27.1 Gordon, E. M.; Gallop, M. A.; Patel, D. V. (1996–2001). "कॉम्बिनेटरियल ऑर्गेनिक सिंथेसिस में रणनीति और रणनीति। ड्रग डिस्कवरी के लिए आवेदन". Accounts of Chemical Research (in English). 29 (3): 144–154. doi:10.1021/ar950170u. ISSN 0001-4842.
- ↑ A. Furka Sub-Library Composition of Peptide Libraries. Potential Application in Screening. Drug Development Research 33, 90-97 (1994).
- ↑ Erb E, Janda KD, Brenner S (1994) Recursive deconvolution of combinatorial chemical libraries Proc. Natl Acad Sci.USA 91; 11422-11426.
- ↑ Furka Á, Sebestyén F, WC 93/24517, 1993.
- ↑ Pinilla C, Appel JR, Blanc P, Houghten RA (1993) Rapid identification of high affinity peptide ligands using positional scanning synthetic peptide combinatorial libraries. BioTechniques 13(6); 901-5.
- ↑ Carell TE, Winter A, Rebek J Jr. (1994) A Novel Procedure for the Synthesis of Libraries Containing Small Organic Molecules, Angew Chem Int Ed Engl 33; 2059-2061.
- ↑ Câmpian E, Peterson M, Saneii HH, Furka Á, (1998) Deconvolution by omission libraries, Bioorg &[ Med Chem Letters 8; 2357-2362.
- ↑ J. A. Smith J. G. R. Hurrel, S. J. Leach A novel method for delineating antigenic determinants: peptide synthesis and radioimmunoassay using the same solid support. Immunochemistry 1977, 14, 565.
- ↑ S. J. Taylor, J. P. Morken Thermographic Selection of Effective Catalysts from an Encoded Polymer-Bound Library Science 1998, 280, 267.
- ↑ Ohlmeyer MHJ, Swanson RN, Dillard LW, Reader JC, Asouline G, Kobayashi R, Wigler M, Still WC (1993) Complex synthetic chemical libraries indexed with molecular tags, Proc Natl Acad Sci USA 90; 10922-10926.
- ↑ Sarkar M, Pascal BD, Steckler C, Aquino C., Micalizio GC, Kodadek T, Chalmers MJ (1993) Decoding Split and Pool Combinatorial Libraries with Electron Transfer Dissociation Tandem Mass Spectrometry, J Am Soc Mass Spectrom 24(7): 1026-36.
- ↑ Kerr JM, Banville SC, Zuckermann RN (1993) Encoded Combinatorial Peptide Libraries Containing Non-Natural Amino Acids, J Am Chem. Soc 115; 2529-2531.
- ↑ Nikolaiev V, Stierandová A, Krchnák V, Seligmann B, Lam KS, Salmon SE, Lebl M, (1993) Peptide-encoding for structure determination of nonsequenceable polymers within libraries synthesized and tested on solid-phase supports, Pept Res. 6(3):161-70.
- ↑ Brenner S, Lerner RA. (1992) Encoded combinatorial chemistry. Proc Natl Acad Sci USA 89; 5381–5383.
- ↑ Nielsen J, Brenner S, Janda KD. (1993) Synthetic methods for the implementation of encoded combinatorial chemistry. Journal of the American Chemical Society, 115 (21); 9812–9813.
- ↑ Harbury DR, Halpin DR (2000) WO 00/23458.
- ↑ B. Halford How DNA-encoded libraries are revolutionizing drug discovery. C&EN 2017, 95, Issue 25.
- ↑ Gartner ZJ, Tse BN, Grubina RB, Doyon JB, Snyder TM, Liu DR (2004) DNA-Templated Organic Synthesis and Selection of a Library of Macrocycles, Science 305; 1601-1605.
- ↑ Melkko S, Scheuermann J, Dumelin CE, Neri D (2004) Encoded self-assembling chemical libraries Nat Biotechnol 22; 568-574.
- ↑ Halpin DR, Harbury PB (2004) DNA Display I. Sequence-Encoded Routing of DNA Populations, PLoS Biology 2; 1015-102.
- ↑ Mannocci L, Zhang Y, Scheuermann J, Leimbacher M, De Bellis G, Rizzi E, Dumelin C, Melkko S, and Neri N (2008) High-throughput sequencing allows the identification of binding molecules isolated from DNA-encoded chemical libraries, Proc Natl Acad Sci USA 105;17670–17675.
- ↑ Hansen MH, Blakskjær P, Petersen LK, Hansen TH, Højfeldt JW, Gothelf KV, HansenNJV (2009) A Yoctoliter-Scale DNA Reactor for Small-Molecule Evolution (2009) J Am Chem Soc 131; 1322-1327.
- ↑ Luk KC, Satz AL (2014) DNA‐Compatible Chemistry in: Goodnow Jr. RA Editor A Handbook for DNA‐Encoded Chemistry: Theory and Applications for Exploring Chemical Space and Drug Discovery, Wiley, pp 67-98.
- ↑ Satz AL, Cai J, Chen Y,§, Goodnow R, Felix Gruber F, Kowalczyk A, Petersen A, Naderi-Oboodi G, Orzechowski L, Strebel Q (2015) DNA Compatible Multistep Synthesis and Applications to DNA Encoded Libraries Bioconjugate Chem 26; 1623−1632.
- ↑ Li Y, Gabriele E, Samain F, Favalli N, Sladojevich F, Scheuermann J, Neri D (2016) Optimized reaction conditions for amide bond formation in DNA-encoded combinatorial libraries, ACS Comb Sci 18(8); 438–443.
- ↑ X. -D. Xiang et al. "A Combinatorial Approach to Materials Discovery" Science 268 (1995) 1738
- ↑ J.J. Hanak, J. Mater. Sci, 1970, 5, 964-971
- ↑ Combinatorial methods for development of sensing materials, Springer, 2009. ISBN 978-0-387-73712-6
- ↑ V. M. Mirsky, V. Kulikov, Q. Hao, O. S. Wolfbeis. Multiparameter High Throughput Characterization of Combinatorial Chemical Microarrays of Chemosensitive Polymers. Macromolec. Rap. Comm., 2004, 25, 253-258
- ↑ H. Koinuma et al. "Combinatorial solid state materials science and technology" Sci. Technol. Adv. Mater. 1 (2000) 1 free download
- ↑ Andrei Ionut Mardare et al. "Combinatorial solid state materials science and technology" Sci. Technol. Adv. Mater. 9 (2008) 035009 free download
- ↑ Applied Catalysis A, Volume 254, Issue 1, Pages 1-170 (10 November 2003)
- ↑ J. N. Cawse et al., Progress in Organic Coatings, Volume 47, Issue 2, August 2003, Pages 128-135
- ↑ Combinatorial Methods for High-Throughput Materials Science, MRS Proceedings Volume 1024E, Fall 2007
- ↑ Combinatorial and Artificial Intelligence Methods in Materials Science II, MRS Proceedings Volume 804, Fall 2004
- ↑ QSAR and Combinatorial Science, 24, Number 1 (February 2005)
- ↑ J. N. Cawse, Ed., Experimental Design for Combinatorial and High Throughput Materials Development, John Wiley and Sons, 2002.
- ↑ D. Newman and G. Cragg "Natural Products as Sources of New Drugs over the Last 25 Years" J Nat Prod 70 (2007) 461
- ↑ 65.0 65.1 M. Feher and J. M. Schmidt "Property Distributions: Differences between Drugs, Natural Products, and Molecules from Combinatorial Chemistry" J. Chem. Inf. Comput. Sci., 43 (2003) 218
- ↑ Cordier, C.; Morton, D.; Murrison, S.; Nelson, A.; O'Leary-Steele, C. (2008). "बायोएक्टिव कंपाउंड लाइब्रेरी के विविधता-उन्मुख संश्लेषण में एक प्रेरणा के रूप में प्राकृतिक उत्पाद". Nat. Prod. Rep. 25 (4): 719–737. doi:10.1039/B706296F. PMC 2496956. PMID 18663392. S2CID 15697405.
- ↑ de Sousa Luis, J.A.; Costa Barros, R.P.; de Sousa, N.F.; Muratov, E.; Scotti, L.; Scotti, M.T. (2021). "प्राकृतिक उत्पादों के डेटाबेस की वर्चुअल स्क्रीनिंग". Mini-Rev. Med. Chem. 21 (18): 2657–2730. doi:10.2174/1389557520666200730161549. PMID 32744975. S2CID 220965407.
- ↑ Harvey, A.L. (2008). "दवा की खोज में प्राकृतिक उत्पाद". Drug Discov. Today. 13 (19–20): 894–901. doi:10.1016/j.drudis.2008.07.004. PMID 18691670.
- ↑ Kohli, S. (2018). मॉलिक्यूलर इनसाइट ऑफ़ ड्रग डिज़ाइन, एड में न्यू ड्रग लेड के स्रोत के रूप में प्रकृति के लिए एकीकृत दृष्टिकोण। आदित्य, ए. (PDF). IntechOpen. pp. 29–44. doi:10.5772/intechopen.74961. S2CID 64364163. Archived (PDF) from the original on 2022-05-27.
- ↑ Kaiser, M.; Wetzel, S.; Kumar, K.; Waldmann, H. (2008). "यौगिक पुस्तकालयों का जीव विज्ञान-प्रेरित संश्लेषण". Cell. Mol. Life Sci. 65 (7–8): 1186–1201. doi:10.1007/s00018-007-7492-1. PMID 18193390. S2CID 22601514.
- ↑ Teague, S.J.; Davis, A.M.; Leeson, P.D.; Oprea, T. (1999). "सीसे के समान संयोजी पुस्तकालयों का डिजाइन". Angew. Chem. Int. Ed. 38 (24): 3743–3748. doi:10.1002/(SICI)1521-3773(19991216)38:24<3743::AID-ANIE3743>3.0.CO;2-U. PMID 10649345.
- ↑ Su QB, Beeler AB, Lobkovsky E, Porco JA, Panek JS "Stereochemical diversity through cyclodimerization: Synthesis of polyketide-like macrodiolides." Org Lett 2003, 5:2149-2152.
- ↑ Medina-Franco, J.L.; Martínez-Mayorga, K.; Giulianotti, M.A.; Houghten, R.A.; Pinilla, C. (2008). "दवा की खोज में रासायनिक स्थान का दृश्य". Curr Comput-Aided Drug Des. 4 (4): 322–333. doi:10.2174/157340908786786010.
- ↑ Rosén, J.; Gottfries, J.; Muresan, S.; Backlund, A.; Oprea, T.I. (2009). "प्राकृतिक उत्पादों के माध्यम से उपन्यास रासायनिक अंतरिक्ष अन्वेषण". J. Med. Chem. 52 (7): 1953–1962. doi:10.1021/jm801514w. PMC 2696019. PMID 19265440.
- ↑ Lachance, H.; Wetzel, S.; Kumar, K.; Waldmann, H. (2012). "ड्रग डिस्कवरी के लिए प्राकृतिक उत्पाद रासायनिक स्थान को चार्ट करना, नेविगेट करना और पॉप्युलेट करना". J. Med. Chem. 55 (13): 5989–6001. doi:10.1021/jm300288g. PMID 22537178.
- ↑ Reymond, J.-L.; Awale, M. (2012). "केमिकल यूनिवर्स डेटाबेस का उपयोग करके ड्रग डिस्कवरी के लिए केमिकल स्पेस की खोज करना". ACS Chem. Neurosci. 3 (9): 649–657. doi:10.1021/cn3000422. PMC 3447393. PMID 23019491.
- ↑ Medina-Franco, J.L. (2013). Chemoinformatic characterization of the chemical space and molecular diversity of compound libraries, in Diversity-Oriented Synthesis: Basics and Applications in Organic Synthesis, Drug Discovery, and Chemical Biology, Trabocchi, A.; Ed., Chapter 10, 2013, 325-352. John Wiley & Sons, Inc.
- ↑ Klein, R.; Lindell, S.D. (2014). Combinatorial Chemistry Library Design, in, Plant Chemical Biology, Audenaert, D.; Overvoorde, P.; Eds. New Jersey: John Wiley & Sons, Inc. pp. 40–63.
बाहरी संबंध
- English version of the 1982 document
- "The concealed side of the history of combinatorial chemistry"
- IUPAC's "Glossary of Terms Used in Combinatorial Chemistry"
- ACS Combinatorial Science (formerly Journal of Combinatorial Chemistry)
- Combinatorial Chemistry Review
- Molecular Diversity
- Combinatorial Chemistry and High Throughput Screening
- Combinatorial Chemistry: an Online Journal
- SmiLib - A free open-source software for combinatorial library enumeration
- GLARE - A free open-source software for combinatorial library design