हाइड्रोज़ोइक एसिड: Difference between revisions
(Created page with "{{Short description|Unstable and toxic chemical compound}} {{Chembox | verifiedrevid = 443860054 | Name = Hydrazoic acid | ImageFile = Hydrogen-azide-2D-dimensions.png | Image...") |
No edit summary |
||
| Line 70: | Line 70: | ||
}} | }} | ||
'''हाइड्रेजोइक अम्ल''', जिसे '''हाइड्रोजन एजाइड''' या '''ऐजोइमाइड''' के रूप में भी जाना जाता है,<ref name="EB1911">{{Cite EB1911 |wstitle=Azoimide |volume=3 |pages=82–83}} This also contains a detailed description of the contemporaneous production process.</ref> जो रासायनिक सूत्र {{chem2|HN3}} वाला यौगिक है|<ref>{{cite book | title = अकार्बनिक और Organometallic यौगिकों का शब्दकोश| publisher = Chapman & Hall }}</ref> यह कमरे के तापमान और दबाव में एक रंगहीन, अस्थिर और विस्फोटक तरल है। यह [[नाइट्रोजन]] और [[हाइड्रोजन]] का एक यौगिक है, और इसलिए एक [[निक्टोजन हाइड्राइड]] है। इसे पहली बार 1890 में [[ थिओडोर कर्टियस ]] द्वारा अलग किया गया था।<ref>{{Cite journal | last = Curtius | first = Theodor | author-link = Theodor Curtius | title = Ueber Stickstoffwasserstoffsäure (Azoimid) N<sub>3</sub>H |trans-title=On hydrazoic acid (azoimide) N<sub>3</sub>H | journal = Berichte der Deutschen Chemischen Gesellschaft | year = 1890 | volume = 23 | issue = 2 | pages = 3023–3033 | url = http://babel.hathitrust.org/cgi/pt?id=umn.319510006827352;view=1up;seq=919 | doi=10.1002/cber.189002302232}}</ref> अम्ल के कुछ अनुप्रयोग हैं, लेकिन इसका [[संयुग्मी क्षार]], एजाइड आयन, विशेष प्रक्रियाओं में उपयोगी है। | |||
हाइड्रेजोइक अम्ल, अपने साथी [[खनिज अम्ल]] की तरह, जल में घुलनशील है। विशुद्ध (अनडाइल्यूटेड) हाइड्रेजोइक अम्ल खतरनाक रूप से विस्फोटक होता है<ref>{{Cite journal|last1=Furman|first1=David|last2=Dubnikova|first2=Faina|last3=van Duin|first3=Adri C. T.|last4=Zeiri|first4=Yehuda|last5=Kosloff|first5=Ronnie|date=2016-03-10|title=विस्फोट रसायन विज्ञान के अनुप्रयोगों के साथ तरल हाइड्रोजोइक एसिड के लिए प्रतिक्रियाशील बल क्षेत्र|journal=The Journal of Physical Chemistry C|volume=120|issue=9|pages=4744–4752|doi=10.1021/acs.jpcc.5b10812|bibcode=2016APS..MARH20013F|s2cid=102029987 |issn=1932-7447}}</ref> जिसमें [[निर्माण की एक मानक एन्थैल्पी]] Δ<sub>f</sub>H<sup>o</sup> (l, 298K) = +264 kJ/mol होती है।<ref name="InorgChem" />तनु होने पर, गैस और जलीय विलयन (<10%) सुरक्षित रूप से तैयार किए जा सकते हैं लेकिन तुरंत उपयोग किए जाने चाहिए; इसके कम क्वथनांक के कारण, हाइड्रेजोइक अम्ल वाष्पीकरण और संघनन पर समृद्ध होता है जैसे कि विस्फोट के लिए अक्षम तनु विलयन पात्र या रिएक्टर के हेडस्पेस में ड्रॉपलेट का निर्माण कर सकता है जो विस्फोट करने में सक्षम हैं।<ref>Gonzalez-Bobes, F. et al Org. Process Res. Dev. 2012, 16, 2051-2057.</ref><ref>Treitler, D. S. et al Org. Process Res. Dev. 2017, 21, 460-467.</ref> | |||
== उत्पादन == | == उत्पादन == | ||
अम्लआमतौर पर [[ सोडियम एज़ाइड ]] जैसे एजाइड नमक के अम्लीकरण से बनता है। आम तौर पर जलमें सोडियम एजाइड के समाधान में एज़ाइड नमक के साथ संतुलन में हाइड्रेजोइक अम्लकी ट्रेस मात्रा होती है, लेकिन एक मजबूत अम्लकी शुरूआत प्राथमिक प्रजातियों को हाइड्रेजोइक अम्लके समाधान में परिवर्तित कर सकती है। बाद में शुद्ध अम्ल भिन्नात्मक आसवन द्वारा एक अत्यधिक विस्फोटक रंगहीन तरल के रूप में एक अप्रिय गंध के साथ प्राप्त किया जा सकता है।<ref name="EB1911"/> | |||
:{{chem2|NaN3 + HCl → HN3 + NaCl}} | :{{chem2|NaN3 + HCl → HN3 + NaCl}} | ||
अघुलनशील [[ बेरियम सल्फ़ेट ]] को छानकर तनु [[सल्फ्यूरिक एसिड]] | अघुलनशील [[ बेरियम सल्फ़ेट ]] को छानकर तनु [[सल्फ्यूरिक एसिड|सल्फ्यूरिक]] अम्लके साथ [[बेरियम एजाइड]] घोल का उपचार करके इसका जलीय विलयन भी तैयार किया जा सकता है।<ref>L . F. Audrieth, C. F. Gibbs Hydrogen Azide in Aqueous and Ethereal Solution" Inorganic Syntheses 1939, vol. 1, pp. 71-79.</ref> | ||
यह मूल रूप से [[ नाइट्रस तेजाब ]] के साथ जलीय [[हाइड्राज़ीन]] की प्रतिक्रिया से तैयार किया गया था: | यह मूल रूप से [[ नाइट्रस तेजाब ]] के साथ जलीय [[हाइड्राज़ीन]] की प्रतिक्रिया से तैयार किया गया था: | ||
| Line 89: | Line 89: | ||
:{{chem2|[N2H5]+ + HNO2 → HN3 + H2O + [H3O]+}} | :{{chem2|[N2H5]+ + HNO2 → HN3 + H2O + [H3O]+}} | ||
[[हाइड्रोजन पेरोक्साइड]], [[नाइट्रोसिल क्लोराइड]], [[ ट्राइक्लोरैमाइन ]] या [[नाइट्रिक एसिड]] | [[हाइड्रोजन पेरोक्साइड]], [[नाइट्रोसिल क्लोराइड]], [[ ट्राइक्लोरैमाइन ]] या [[नाइट्रिक एसिड|नाइट्रिक]] अम्लजैसे अन्य ऑक्सीडाइजिंग एजेंटों का भी हाइड्राज़ीन से हाइड्रेजोइक अम्लका उत्पादन करने के लिए उपयोग किया जा सकता है।<ref>{{Greenwood&Earnshaw2nd|page=432}}</ref> | ||
== निपटान से पहले विनाश == | == निपटान से पहले विनाश == | ||
हाइड्रोजोइक | हाइड्रोजोइक अम्लनाइट्रस अम्लके साथ प्रतिक्रिया करता है: | ||
:{{chem2|HN3 + HNO2 → N2O + N2 + H2O}} | :{{chem2|HN3 + HNO2 → N2O + N2 + H2O}} | ||
| Line 102: | Line 102: | ||
== प्रतिक्रियाएं == | == प्रतिक्रियाएं == | ||
इसके गुणों में | इसके गुणों में हाइड्रेजोइक अम्लहलोजन अम्लके लिए कुछ सादृश्य दिखाता है, क्योंकि यह खराब घुलनशील (जलमें) सीसा, चांदी और पारा (I) लवण बनाता है। धात्विक लवण सभी निर्जल रूप में क्रिस्टलीकृत होते हैं और गर्म करने पर विघटित हो जाते हैं, जिससे शुद्ध धातु का अवशेष निकल जाता है।<ref name="EB1911"/>यह एक दुर्बल अम्ल (pK<sub>a</sub> = 4.75.<ref name="InorgChem">{{cite book | ||
| title = Inorganic Chemistry, 3rd Edition | | title = Inorganic Chemistry, 3rd Edition | ||
| chapter = Chapter 15: The group 15 elements | | chapter = Chapter 15: The group 15 elements | ||
| Line 111: | Line 111: | ||
| isbn = 978-0-13-175553-6 | | isbn = 978-0-13-175553-6 | ||
| page = 449 | | page = 449 | ||
}}</ref>) इसके भारी धातु के लवण विस्फोटक होते हैं और आसानी से [[अल्काइल आयोडाइड]] के साथ परस्पर क्रिया करते हैं। भारी क्षार धातुओं ([[लिथियम]] को छोड़कर) या क्षारीय पृथ्वी धातुओं के एज़ाइड्स विस्फोटक नहीं होते हैं, लेकिन गर्म करने पर अधिक नियंत्रित तरीके से विघटित होते हैं, स्पेक्ट्रोस्कोपिक रूप से शुद्ध होते हैं {{chem2|N2}} गैस।<ref name="wiberg"/>हाइड्रोजन की मुक्ति और लवण के निर्माण के साथ | }}</ref>) इसके भारी धातु के लवण विस्फोटक होते हैं और आसानी से [[अल्काइल आयोडाइड]] के साथ परस्पर क्रिया करते हैं। भारी क्षार धातुओं ([[लिथियम]] को छोड़कर) या क्षारीय पृथ्वी धातुओं के एज़ाइड्स विस्फोटक नहीं होते हैं, लेकिन गर्म करने पर अधिक नियंत्रित तरीके से विघटित होते हैं, स्पेक्ट्रोस्कोपिक रूप से शुद्ध होते हैं {{chem2|N2}} गैस।<ref name="wiberg"/>हाइड्रोजन की मुक्ति और लवण के निर्माण के साथ हाइड्रेजोइक अम्लके समाधान कई धातुओं (जैसे [[जस्ता]], [[लोहा]]) को घोलते हैं, जिन्हें एज़ाइड्स (पूर्व में एज़ोइमाइड्स या हाइड्राज़ोएट्स भी कहा जाता है) कहा जाता है। | ||
नाइट्रोजन के निष्कासन के साथ, | नाइट्रोजन के निष्कासन के साथ, हाइड्रेजोइक अम्लएल्डिहाइड, केटोन्स और कार्बोक्जिलिक अम्लसहित कार्बोनिल डेरिवेटिव के साथ प्रतिक्रिया कर सकता है, एक अमाइन या एमाइड देने के लिए। इसे [[श्मिट प्रतिक्रिया]] या श्मिट पुनर्व्यवस्था कहा जाता है। | ||
[[File:Schmidt_Reaktion_Übersicht_Carbonsäuren1.svg|alt=|center|frameकम|350x350पीएक्स]] | [[File:Schmidt_Reaktion_Übersicht_Carbonsäuren1.svg|alt=|center|frameकम|350x350पीएक्स]] | ||
[[File:Schmidt Reaktion Übersicht Ketone1.svg|alt=|center|frameकम|400x400पीएक्स]]सबसे मजबूत अम्लों में घुलने से अमीनोडायज़ोनियम आयन युक्त विस्फोटक लवण उत्पन्न होते हैं {{chem2|[H2N\dN\dN]+ ⇌ [H2N\sN\tN]+}}, उदाहरण के लिए:<ref name="wiberg">{{cite book | [[File:Schmidt Reaktion Übersicht Ketone1.svg|alt=|center|frameकम|400x400पीएक्स]]सबसे मजबूत अम्लों में घुलने से अमीनोडायज़ोनियम आयन युक्त विस्फोटक लवण उत्पन्न होते हैं {{chem2|[H2N\dN\dN]+ ⇌ [H2N\sN\tN]+}}, उदाहरण के लिए:<ref name="wiberg">{{cite book | ||
| Line 129: | Line 129: | ||
आयन {{chem2|[H2N\dN\dN]+}} [[डायज़ोमेथेन]] के लिए [[isoelectronic]] है {{chem2|H2C\dN+\dN-}}. | आयन {{chem2|[H2N\dN\dN]+}} [[डायज़ोमेथेन]] के लिए [[isoelectronic]] है {{chem2|H2C\dN+\dN-}}. | ||
झटके, घर्षण, चिंगारी आदि से उत्पन्न | झटके, घर्षण, चिंगारी आदि से उत्पन्न हाइड्रेजोइक अम्लका अपघटन नाइट्रोजन और हाइड्रोजन का उत्पादन करता है: | ||
:{{chem2|2 HN3 → H2 + 3 N2}} | :{{chem2|2 HN3 → H2 + 3 N2}} | ||
हाइड्रेजोइक अम्लपर्याप्त ऊर्जा पर अनिमोलेक्युलर अपघटन से गुजरता है: | |||
:{{chem2|HN3 → NH + N2}} | :{{chem2|HN3 → NH + N2}} | ||
| Line 141: | Line 141: | ||
== विषाक्तता == | == विषाक्तता == | ||
हाइड्रेजोइक अम्लअस्थिर और अत्यधिक विषैला होता है। इसमें तीखी गंध होती है और इसके वाष्प से तेज सिरदर्द हो सकता है। यौगिक गैर-संचयी जहर के रूप में कार्य करता है। | |||
== अनुप्रयोग == | == अनुप्रयोग == | ||
[[2-फ्यूरोनिट्राइल]], एक फार्मास्युटिकल इंटरमीडिएट और संभावित कृत्रिम मिठास एजेंट को हाइड्रोजोइक | [[2-फ्यूरोनिट्राइल]], एक फार्मास्युटिकल इंटरमीडिएट और संभावित कृत्रिम मिठास एजेंट को हाइड्रोजोइक अम्लके मिश्रण के साथ फरफुरल का इलाज करके अच्छी उपज में तैयार किया गया है ({{chem2|HN3}}) और [[परक्लोरिक तेजाब]] ({{chem2|HClO4}}) 35 डिग्री सेल्सियस पर [[बेंजीन]] समाधान में मैग्नीशियम पर्क्लोरेट की उपस्थिति में।<ref>{{cite journal | author = P. A. Pavlov | title = Synthesis of 5-substituted furannitriles and their reaction with hydrazine | journal = Khimiya Geterotsiklicheskikh Soedinenii | volume = 2 | pages = 181–186 | year = 1986 |last2 = Kul'nevich | first2 = V. G.}}</ref><ref>{{cite journal | author = B. Bandgar | title = पानी में जैविक प्रतिक्रियाएँ। हल्के परिस्थितियों में एनबीएस का उपयोग करके एल्डिहाइड का नाइट्राइल में परिवर्तन| journal = Synthetic Communications | volume = 36 | pages = 1347–1352 | year = 2006 |last2 = Makone | first2 = S. | issue = 10 | doi=10.1080/00397910500522009| s2cid = 98593006 }}</ref> | ||
[[सभी गैस-चरण [[आयोडीन]] लेजर]] (एजीआईएल) उत्तेजित [[नाइट्रोजन क्लोराइड]] का उत्पादन करने के लिए [[क्लोरीन]] के साथ गैसीय | [[सभी गैस-चरण [[आयोडीन]] लेजर]] (एजीआईएल) उत्तेजित [[नाइट्रोजन क्लोराइड]] का उत्पादन करने के लिए [[क्लोरीन]] के साथ गैसीय हाइड्रेजोइक अम्लको मिलाता है, जो तब आयोडीन को लेस करने के लिए उपयोग किया जाता है; यह COIL लेज़रों की तरल रसायन संबंधी आवश्यकताओं से बचा जाता है। | ||
==संदर्भ== | ==संदर्भ== | ||
Revision as of 18:32, 27 May 2023
| |

| |

| |
| Names | |
|---|---|
| IUPAC name
Hydrogen azide
| |
| Other names
Hydrogen azide
Azoimide | |
| Identifiers | |
3D model (JSmol)
|
|
| ChEBI | |
| ChEMBL | |
| ChemSpider | |
| EC Number |
|
| 773 | |
PubChem CID
|
|
| UNII | |
| |
| |
| Properties | |
| HN3 | |
| Molar mass | 43.029 g·mol−1 |
| Appearance | colorless, highly volatile liquid |
| Density | 1.09 g/cm3 |
| Melting point | −80 °C (−112 °F; 193 K) |
| Boiling point | 37 °C (99 °F; 310 K) |
| highly soluble | |
| Solubility | soluble in alkali, alcohol, ether |
| Acidity (pKa) | 4.6 [1] |
| Conjugate base | Azide |
| Structure | |
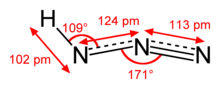
| approximately linear | |
| Hazards | |
| Occupational safety and health (OHS/OSH): | |
Main hazards
|
Highly toxic, explosive, reactive |
| GHS labelling: | |
  
| |
| Danger | |
| H200, H319, H335, H370 | |
| P201, P202, P260, P261, P264, P270, P271, P280, P281, P304+P340, P305+P351+P338, P307+P311, P312, P321, P337+P313, P372, P373, P380, P401, P403+P233, P405, P501 | |
| NFPA 704 (fire diamond) | |
| Related compounds | |
Other cations
|
Sodium azide |
| Ammonia Hydrazine | |
Except where otherwise noted, data are given for materials in their standard state (at 25 °C [77 °F], 100 kPa).
| |
हाइड्रेजोइक अम्ल, जिसे हाइड्रोजन एजाइड या ऐजोइमाइड के रूप में भी जाना जाता है,[2] जो रासायनिक सूत्र HN3 वाला यौगिक है|[3] यह कमरे के तापमान और दबाव में एक रंगहीन, अस्थिर और विस्फोटक तरल है। यह नाइट्रोजन और हाइड्रोजन का एक यौगिक है, और इसलिए एक निक्टोजन हाइड्राइड है। इसे पहली बार 1890 में थिओडोर कर्टियस द्वारा अलग किया गया था।[4] अम्ल के कुछ अनुप्रयोग हैं, लेकिन इसका संयुग्मी क्षार, एजाइड आयन, विशेष प्रक्रियाओं में उपयोगी है।
हाइड्रेजोइक अम्ल, अपने साथी खनिज अम्ल की तरह, जल में घुलनशील है। विशुद्ध (अनडाइल्यूटेड) हाइड्रेजोइक अम्ल खतरनाक रूप से विस्फोटक होता है[5] जिसमें निर्माण की एक मानक एन्थैल्पी ΔfHo (l, 298K) = +264 kJ/mol होती है।[6]तनु होने पर, गैस और जलीय विलयन (<10%) सुरक्षित रूप से तैयार किए जा सकते हैं लेकिन तुरंत उपयोग किए जाने चाहिए; इसके कम क्वथनांक के कारण, हाइड्रेजोइक अम्ल वाष्पीकरण और संघनन पर समृद्ध होता है जैसे कि विस्फोट के लिए अक्षम तनु विलयन पात्र या रिएक्टर के हेडस्पेस में ड्रॉपलेट का निर्माण कर सकता है जो विस्फोट करने में सक्षम हैं।[7][8]
उत्पादन
अम्लआमतौर पर सोडियम एज़ाइड जैसे एजाइड नमक के अम्लीकरण से बनता है। आम तौर पर जलमें सोडियम एजाइड के समाधान में एज़ाइड नमक के साथ संतुलन में हाइड्रेजोइक अम्लकी ट्रेस मात्रा होती है, लेकिन एक मजबूत अम्लकी शुरूआत प्राथमिक प्रजातियों को हाइड्रेजोइक अम्लके समाधान में परिवर्तित कर सकती है। बाद में शुद्ध अम्ल भिन्नात्मक आसवन द्वारा एक अत्यधिक विस्फोटक रंगहीन तरल के रूप में एक अप्रिय गंध के साथ प्राप्त किया जा सकता है।[2]
- NaN3 + HCl → HN3 + NaCl
अघुलनशील बेरियम सल्फ़ेट को छानकर तनु सल्फ्यूरिक अम्लके साथ बेरियम एजाइड घोल का उपचार करके इसका जलीय विलयन भी तैयार किया जा सकता है।[9] यह मूल रूप से नाइट्रस तेजाब के साथ जलीय हाइड्राज़ीन की प्रतिक्रिया से तैयार किया गया था:
- N2H4 + HNO2 → HN3 + 2 H2O
हाइड्राज़ीन केशन के साथ [N2H5]+ यह प्रतिक्रिया इस प्रकार लिखी जाती है:
- [N2H5]+ + HNO2 → HN3 + H2O + [H3O]+
हाइड्रोजन पेरोक्साइड, नाइट्रोसिल क्लोराइड, ट्राइक्लोरैमाइन या नाइट्रिक अम्लजैसे अन्य ऑक्सीडाइजिंग एजेंटों का भी हाइड्राज़ीन से हाइड्रेजोइक अम्लका उत्पादन करने के लिए उपयोग किया जा सकता है।[10]
निपटान से पहले विनाश
हाइड्रोजोइक अम्लनाइट्रस अम्लके साथ प्रतिक्रिया करता है:
- HN3 + HNO2 → N2O + N2 + H2O
यह प्रतिक्रिया असामान्य है क्योंकि इसमें चार अलग-अलग ऑक्सीकरण राज्यों में नाइट्रोजन वाले यौगिक शामिल हैं।[11]
प्रतिक्रियाएं
इसके गुणों में हाइड्रेजोइक अम्लहलोजन अम्लके लिए कुछ सादृश्य दिखाता है, क्योंकि यह खराब घुलनशील (जलमें) सीसा, चांदी और पारा (I) लवण बनाता है। धात्विक लवण सभी निर्जल रूप में क्रिस्टलीकृत होते हैं और गर्म करने पर विघटित हो जाते हैं, जिससे शुद्ध धातु का अवशेष निकल जाता है।[2]यह एक दुर्बल अम्ल (pKa = 4.75.[6]) इसके भारी धातु के लवण विस्फोटक होते हैं और आसानी से अल्काइल आयोडाइड के साथ परस्पर क्रिया करते हैं। भारी क्षार धातुओं (लिथियम को छोड़कर) या क्षारीय पृथ्वी धातुओं के एज़ाइड्स विस्फोटक नहीं होते हैं, लेकिन गर्म करने पर अधिक नियंत्रित तरीके से विघटित होते हैं, स्पेक्ट्रोस्कोपिक रूप से शुद्ध होते हैं N2 गैस।[12]हाइड्रोजन की मुक्ति और लवण के निर्माण के साथ हाइड्रेजोइक अम्लके समाधान कई धातुओं (जैसे जस्ता, लोहा) को घोलते हैं, जिन्हें एज़ाइड्स (पूर्व में एज़ोइमाइड्स या हाइड्राज़ोएट्स भी कहा जाता है) कहा जाता है।
नाइट्रोजन के निष्कासन के साथ, हाइड्रेजोइक अम्लएल्डिहाइड, केटोन्स और कार्बोक्जिलिक अम्लसहित कार्बोनिल डेरिवेटिव के साथ प्रतिक्रिया कर सकता है, एक अमाइन या एमाइड देने के लिए। इसे श्मिट प्रतिक्रिया या श्मिट पुनर्व्यवस्था कहा जाता है।
सबसे मजबूत अम्लों में घुलने से अमीनोडायज़ोनियम आयन युक्त विस्फोटक लवण उत्पन्न होते हैं [H2N=N=N]+ ⇌ [H2N−N≡N]+, उदाहरण के लिए:[12]
- HN=N=N + H[SbCl6] → [H2N=N=N]+[SbCl6]−
आयन [H2N=N=N]+ डायज़ोमेथेन के लिए isoelectronic है H2C=N+=N−.
झटके, घर्षण, चिंगारी आदि से उत्पन्न हाइड्रेजोइक अम्लका अपघटन नाइट्रोजन और हाइड्रोजन का उत्पादन करता है:
- 2 HN3 → H2 + 3 N2
हाइड्रेजोइक अम्लपर्याप्त ऊर्जा पर अनिमोलेक्युलर अपघटन से गुजरता है:
- HN3 → NH + N2
निम्नतम ऊर्जा मार्ग NH को त्रिक अवस्था में उत्पन्न करता है, जिससे यह स्पिन-निषिद्ध प्रतिक्रिया बन जाती है। यह उन कुछ प्रतिक्रियाओं में से एक है, जिनकी दर जमीनी इलेक्ट्रॉनिक स्थिति में विशिष्ट मात्रा में कंपन ऊर्जा के लिए निर्धारित की गई है, लेजर फोटोडिसोसिएशन अध्ययन द्वारा।[13] इसके अलावा, इन असमान आणविक दरों का सैद्धांतिक रूप से विश्लेषण किया गया है, और प्रयोगात्मक और गणना की गई दरें उचित समझौते में हैं।[14]
विषाक्तता
हाइड्रेजोइक अम्लअस्थिर और अत्यधिक विषैला होता है। इसमें तीखी गंध होती है और इसके वाष्प से तेज सिरदर्द हो सकता है। यौगिक गैर-संचयी जहर के रूप में कार्य करता है।
अनुप्रयोग
2-फ्यूरोनिट्राइल, एक फार्मास्युटिकल इंटरमीडिएट और संभावित कृत्रिम मिठास एजेंट को हाइड्रोजोइक अम्लके मिश्रण के साथ फरफुरल का इलाज करके अच्छी उपज में तैयार किया गया है (HN3) और परक्लोरिक तेजाब (HClO4) 35 डिग्री सेल्सियस पर बेंजीन समाधान में मैग्नीशियम पर्क्लोरेट की उपस्थिति में।[15][16] [[सभी गैस-चरण आयोडीन लेजर]] (एजीआईएल) उत्तेजित नाइट्रोजन क्लोराइड का उत्पादन करने के लिए क्लोरीन के साथ गैसीय हाइड्रेजोइक अम्लको मिलाता है, जो तब आयोडीन को लेस करने के लिए उपयोग किया जाता है; यह COIL लेज़रों की तरल रसायन संबंधी आवश्यकताओं से बचा जाता है।
संदर्भ
- ↑ Pradyot Patnaik. Handbook of Inorganic Chemicals. McGraw-Hill, 2002, ISBN 0-07-049439-8
- ↑ 2.0 2.1 2.2 Chisholm, Hugh, ed. (1911). . Encyclopædia Britannica (in English). Vol. 3 (11th ed.). Cambridge University Press. pp. 82–83. This also contains a detailed description of the contemporaneous production process.
- ↑ अकार्बनिक और Organometallic यौगिकों का शब्दकोश. Chapman & Hall.
- ↑ Curtius, Theodor (1890). "Ueber Stickstoffwasserstoffsäure (Azoimid) N3H" [On hydrazoic acid (azoimide) N3H]. Berichte der Deutschen Chemischen Gesellschaft. 23 (2): 3023–3033. doi:10.1002/cber.189002302232.
- ↑ Furman, David; Dubnikova, Faina; van Duin, Adri C. T.; Zeiri, Yehuda; Kosloff, Ronnie (2016-03-10). "विस्फोट रसायन विज्ञान के अनुप्रयोगों के साथ तरल हाइड्रोजोइक एसिड के लिए प्रतिक्रियाशील बल क्षेत्र". The Journal of Physical Chemistry C. 120 (9): 4744–4752. Bibcode:2016APS..MARH20013F. doi:10.1021/acs.jpcc.5b10812. ISSN 1932-7447. S2CID 102029987.
- ↑ 6.0 6.1 Catherine E. Housecroft; Alan G. Sharpe (2008). "Chapter 15: The group 15 elements". Inorganic Chemistry, 3rd Edition. Pearson. p. 449. ISBN 978-0-13-175553-6.
- ↑ Gonzalez-Bobes, F. et al Org. Process Res. Dev. 2012, 16, 2051-2057.
- ↑ Treitler, D. S. et al Org. Process Res. Dev. 2017, 21, 460-467.
- ↑ L . F. Audrieth, C. F. Gibbs Hydrogen Azide in Aqueous and Ethereal Solution" Inorganic Syntheses 1939, vol. 1, pp. 71-79.
- ↑ Greenwood, Norman N.; Earnshaw, Alan (1997). Chemistry of the Elements (2nd ed.). Butterworth-Heinemann. p. 432. ISBN 978-0-08-037941-8.
- ↑ Greenwood, pp. 461–464.
- ↑ 12.0 12.1 Egon Wiberg; Nils Wiberg; Arnold Frederick Holleman (2001). "The Nitrogen Group". Inorganic chemistry. Academic Press. p. 625. ISBN 978-0-12-352651-9.
- ↑ Foy, B.R.; Casassa, M.P.; Stephenson, J.C.; King, D.S. (1990). "Overtone-excited HN
3 (X1A') - Anharmonic resonance, homogeneous linewidths, and dissociation rates". Journal of Chemical Physics. 92: 2782–2789. doi:10.1063/1.457924. - ↑ Besora, M.; Harvey, J.N. (2008). "Understanding the rate of spin-forbidden thermolysis of HN
3 and CH
3N
3". Journal of Chemical Physics. 129 (4): 044303. doi:10.1063/1.2953697. PMID 18681642. - ↑ P. A. Pavlov; Kul'nevich, V. G. (1986). "Synthesis of 5-substituted furannitriles and their reaction with hydrazine". Khimiya Geterotsiklicheskikh Soedinenii. 2: 181–186.
- ↑ B. Bandgar; Makone, S. (2006). "पानी में जैविक प्रतिक्रियाएँ। हल्के परिस्थितियों में एनबीएस का उपयोग करके एल्डिहाइड का नाइट्राइल में परिवर्तन". Synthetic Communications. 36 (10): 1347–1352. doi:10.1080/00397910500522009. S2CID 98593006.
बाहरी संबंध
 Media related to हाइड्रोज़ोइक एसिड at Wikimedia Commons
Media related to हाइड्रोज़ोइक एसिड at Wikimedia Commons- OSHA: Hydrazoic Acid Archived 2008-04-04 at the Wayback Machine


