सोडियम ट्राइफॉस्फेट: Difference between revisions
(Created page with "{{Distinguish|Trisodium phosphate}} {{chembox | Verifiedfields = changed | Watchedfields = changed | verifiedrevid = 450509626 | ImageFile = Sodium tripolyphosphate.svg | Imag...") |
No edit summary |
||
| Line 1: | Line 1: | ||
{{Distinguish| | {{Distinguish|ट्राइसोडियम फॉस्फेट}} | ||
{{chembox | {{chembox | ||
| Verifiedfields = changed | | Verifiedfields = changed | ||
| Line 41: | Line 41: | ||
}} | }} | ||
सोडियम ट्राइफॉस्फेट (एसटीपी), सोडियम | '''सोडियम ट्राइफॉस्फेट''' (एसटीपी), '''सोडियम ट्राइपोलीफॉस्फेट''' (एसटीपीपी), या '''ट्राइपोलीफॉस्फेट''' (टीपीपी),<ref name="Danish EPA 615 2001">[http://www2.mst.dk/udgiv/publications/2001/87-7944-596-9/html/kap07_eng.htm#7.1.1 Complexing agents], [http://www2.mst.dk/udgiv/publications/2001/87-7944-596-9/html/default_eng.htm Environmental and Health Assessment of Substances in Household Detergents and Cosmetic Detergent Products], [http://www.mst.dk/English/ Danish Environmental Protection Agency], Accessed 2008-07-15</ref> सूत्र Na<sub>5</sub>P<sub>3</sub>O<sub>10</sub> के साथ एक [[अकार्बनिक यौगिक]] है। यह पॉलीफोस्फेट पेंटा-आयन का [[सोडियम]] नमक है, जो [[ ट्राइफॉस्फोरिक एसिड |ट्राइफॉस्फोरिक एसिड]] का संयुग्म आधार है। यह कई घरेलू और औद्योगिक उत्पादों, विशेष रूप से डिटर्जेंट के घटक के रूप में बड़े पैमाने पर उत्पादित होता है। यूट्रोफिकेशन से जुड़ी पर्यावरणीय समस्याओं का श्रेय इसके व्यापक उपयोग को जाता है।<ref name=GE/> | ||
== तैयारी और गुण == | == तैयारी और गुण == | ||
सोडियम ट्राइपोलीफॉस्फेट [[डिसोडियम फॉस्फेट]], | सोडियम ट्राइपोलीफॉस्फेट [[डिसोडियम फॉस्फेट]], Na<sub>2</sub>HPO<sub>4</sub>, और [[मोनोसोडियम फॉस्फेट]], NaH<sub>2</sub>PO<sub>4</sub> के स्टोइकियोमेट्रिक मिश्रण को सावधानीपूर्वक नियंत्रित परिस्थितियों में गर्म करके बनाया जाता है।<ref name=GE>{{Greenwood&Earnshaw}}</ref> | ||
: 2 | : 2 Na<sub>2</sub>HPO<sub>4</sub> + NaH<sub>2</sub>PO<sub>4</sub> → Na<sub>5</sub>P<sub>3</sub>O<sub>10</sub> + 2 H<sub>2</sub>O | ||
इस तरह सालाना लगभग 2 मिलियन टन का उत्पादन होता है।<ref name=Ullmann/> | इस तरह सालाना लगभग 2 मिलियन टन का उत्पादन होता है।<ref name=Ullmann/> | ||
एसटीपीपी एक रंगहीन नमक है, जो [[निर्जल]] रूप में और हेक्साहाइड्रेट दोनों के रूप में मौजूद है। ऋणायन को पेंटानिओनिक श्रृंखला[O<sub>3</sub>POP(O)<sub>2</sub>OPO<sub>3</sub>]<sup>5−</sup><ref>{{cite journal |last1=Corbridge |first1=D. E. C. |title=The crystal structure of sodium triphosphate, Na<sub>5</sub>P<sub>3</sub>O<sub>10</sub>, phase I |journal=Acta Crystallographica |date=1 March 1960 |volume=13 |issue=3 |pages=263–269 |doi=10.1107/S0365110X60000583 }}</ref><ref>{{cite journal |last1=Davies |first1=D. R. |last2=Corbridge |first2=D. E. C. |title=The crystal structure of sodium triphosphate, Na<sub>5</sub>P<sub>3</sub>O<sub>10</sub>, phase II |journal=Acta Crystallographica |date=1 May 1958 |volume=11 |issue=5 |pages=315–319 |doi=10.1107/S0365110X58000876 }}</ref> के रूप में वर्णित किया जा सकता है। कई संबंधित di-, tri- और पॉलीफोस्फेट चक्रीय ट्राइफॉस्फेट (जैसे [[सोडियम ट्राइमेटाफॉस्फेट]]) सहित जाने जाते हैं। यह दृढ़ता से धातु के पिंजरों को एक बिडेंटेट और ट्राइडेंटेट चेलेटिंग एजेंट के रूप में बांधता है। | |||
[[Image:Triphosphate chelation.svg|thumb|180px|left|ट्राइफॉस्फेट द्वारा धातु धनायन का केलेशन।]] | [[Image:Triphosphate chelation.svg|thumb|180px|left|ट्राइफॉस्फेट द्वारा धातु धनायन का केलेशन।]] | ||
Revision as of 17:22, 25 May 2023
| |
| Names | |
|---|---|
| IUPAC name
Pentasodium triphosphate
| |
| Other names
sodium tripolyphosphate, polygon, STPP
| |
| Identifiers | |
PubChem CID
|
|
| RTECS number |
|
| UNII | |
| Properties | |
| Na5P3O10 | |
| Molar mass | 367.864 g/mol |
| Appearance | white powder |
| Density | 2.52 g/cm3 |
| Melting point | 622 °C (1,152 °F; 895 K) |
| 14.5 g/100 mL (25 °C) | |
| Hazards | |
| NFPA 704 (fire diamond) | |
| Flash point | Non-flammable |
| Safety data sheet (SDS) | ICSC 1469 |
| Related compounds | |
Other anions
|
Trisodium phosphate Tetrasodium pyrophosphate Sodium hexametaphosphate |
Other cations
|
Pentapotassium triphosphate |
Except where otherwise noted, data are given for materials in their standard state (at 25 °C [77 °F], 100 kPa).
| |
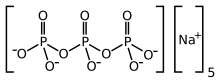
सोडियम ट्राइफॉस्फेट (एसटीपी), सोडियम ट्राइपोलीफॉस्फेट (एसटीपीपी), या ट्राइपोलीफॉस्फेट (टीपीपी),[1] सूत्र Na5P3O10 के साथ एक अकार्बनिक यौगिक है। यह पॉलीफोस्फेट पेंटा-आयन का सोडियम नमक है, जो ट्राइफॉस्फोरिक एसिड का संयुग्म आधार है। यह कई घरेलू और औद्योगिक उत्पादों, विशेष रूप से डिटर्जेंट के घटक के रूप में बड़े पैमाने पर उत्पादित होता है। यूट्रोफिकेशन से जुड़ी पर्यावरणीय समस्याओं का श्रेय इसके व्यापक उपयोग को जाता है।[2]
तैयारी और गुण
सोडियम ट्राइपोलीफॉस्फेट डिसोडियम फॉस्फेट, Na2HPO4, और मोनोसोडियम फॉस्फेट, NaH2PO4 के स्टोइकियोमेट्रिक मिश्रण को सावधानीपूर्वक नियंत्रित परिस्थितियों में गर्म करके बनाया जाता है।[2]
- 2 Na2HPO4 + NaH2PO4 → Na5P3O10 + 2 H2O
इस तरह सालाना लगभग 2 मिलियन टन का उत्पादन होता है।[3]
एसटीपीपी एक रंगहीन नमक है, जो निर्जल रूप में और हेक्साहाइड्रेट दोनों के रूप में मौजूद है। ऋणायन को पेंटानिओनिक श्रृंखला[O3POP(O)2OPO3]5−[4][5] के रूप में वर्णित किया जा सकता है। कई संबंधित di-, tri- और पॉलीफोस्फेट चक्रीय ट्राइफॉस्फेट (जैसे सोडियम ट्राइमेटाफॉस्फेट) सहित जाने जाते हैं। यह दृढ़ता से धातु के पिंजरों को एक बिडेंटेट और ट्राइडेंटेट चेलेटिंग एजेंट के रूप में बांधता है।
उपयोग करता है
डिटर्जेंट
अधिकांश एसटीपीपी वाणिज्यिक डिटर्जेंट के एक घटक के रूप में खपत होती है। यह एक पानी सॉफ़्नर के लिए एक बिल्डर, औद्योगिक शब्दजाल के रूप में कार्य करता है। कठोर जल में (पानी जिसमें Mg की उच्च सांद्रता होती है2+ और सीए2+), डिटर्जेंट निष्क्रिय कर दिए जाते हैं। अत्यधिक आवेशित चेलेटिंग एजेंट होने के नाते, TPP5− संकेतों को मजबूती से बांधता है और उन्हें सल्फोनेट डिटर्जेंट में दखल देने से रोकता है।[3]
खाना
STPP सीफूड, मीट, पोल्ट्री और संयोजित आहार के लिए एक परिरक्षक है।[3]यह खाद्य उत्पादन में ई संख्या E451 के रूप में आम है। खाद्य पदार्थों में, STPP का उपयोग पायसीकारी के रूप में और नमी बनाए रखने के लिए किया जाता है। कई सरकारें खाद्य पदार्थों में अनुमत मात्राओं को नियंत्रित करती हैं, क्योंकि यह विशेष रूप से समुद्री भोजन के बिक्री भार को काफी हद तक बढ़ा सकती है। यूनाइटेड स्टेट्स खाद्य एवं औषधि प्रशासन एसटीपीपी को आम तौर पर सुरक्षित के रूप में सूचीबद्ध करता है।[6]
अन्य
अन्य उपयोगों (सैकड़ों हजारों टन/वर्ष) में सिरेमिक इंजीनियरिंग (एक निश्चित सीमा तक ग्लेज़ की चिपचिपाहट कम करना), चमड़े चमड़ा कमाना (मास्किंग एजेंट और सिंथेटिक टैनिंग एजेंट के रूप में - SYNTAN), पिण्डन निरोधक कारक , सेटिंग रिटार्डर, ज्वाला मंदक , शामिल हैं। कागज, जंग रोधी यौगिक पिगमेंट, कपड़ा, रबड़ निर्माण, किण्वन (जैव रसायन), एंटीफ्ऱीज़र[3]टीपीपी का उपयोग पॉलीसेकेराइड आधारित दवा वितरण में पॉलीअनियन क्रॉसलिंकर के रूप में किया जाता है।[7] टूथपेस्ट में सोडियम ट्राइफॉस्फेट हो सकता है।[8][9][10][11][12][13][14]
स्वास्थ्य प्रभाव
उच्च सीरम फॉस्फेट एकाग्रता को हृदय संबंधी घटनाओं और मृत्यु दर के भविष्यवक्ता के रूप में पहचाना गया है। जबकि फॉस्फेट शरीर और भोजन में कार्बनिक रूपों में मौजूद होता है, सोडियम ट्राइफॉस्फेट जैसे फॉस्फेट के अकार्बनिक रूपों को आसानी से सोख लिया जाता है और इसके परिणामस्वरूप सीरम में फॉस्फेट का स्तर बढ़ सकता है।[15] पॉलीफॉस्फेट आयनों के लवण त्वचा और श्लेष्मा झिल्ली को मध्यम रूप से परेशान करते हैं क्योंकि वे हल्के क्षारीय होते हैं।[1]
पर्यावरणीय प्रभाव
क्योंकि यह बहुत घुलनशील है | पानी में घुलनशील है, अपशिष्ट जल उपचार द्वारा एसटीपीपी को महत्वपूर्ण रूप से हटाया नहीं जाता है। एसटीपीपी orthophosphate को हाइड्रोलाइज करता है, जिसे प्राकृतिक फास्फोरस चक्र में आत्मसात कर लिया जाता है। फास्फोरस युक्त डिटर्जेंट कई ताजे पानी के यूट्रोफिकेशन में योगदान करते हैं।[1]

यह भी देखें
- सोडियम ट्राइमेटाफ़ॉस्फेट, एक चक्रीय ट्राइफ़ॉस्फेट
संदर्भ
- ↑ 1.0 1.1 1.2 Complexing agents, Environmental and Health Assessment of Substances in Household Detergents and Cosmetic Detergent Products, Danish Environmental Protection Agency, Accessed 2008-07-15
- ↑ 2.0 2.1 Greenwood, Norman N.; Earnshaw, Alan (1997). Chemistry of the Elements (2nd ed.). Butterworth-Heinemann. ISBN 978-0-08-037941-8.
- ↑ 3.0 3.1 3.2 3.3 Schrödter, Klaus; Bettermann, Gerhard; Staffel, Thomas; Wahl, Friedrich; Klein, Thomas; Hofmann, Thomas (2008). "Phosphoric Acid and Phosphates". उलमन्स एनसाइक्लोपीडिया ऑफ इंडस्ट्रियल केमिस्ट्री. doi:10.1002/14356007.a19_465.pub3. ISBN 978-3527306732. S2CID 94458523.
- ↑ Corbridge, D. E. C. (1 March 1960). "The crystal structure of sodium triphosphate, Na5P3O10, phase I". Acta Crystallographica. 13 (3): 263–269. doi:10.1107/S0365110X60000583.
- ↑ Davies, D. R.; Corbridge, D. E. C. (1 May 1958). "The crystal structure of sodium triphosphate, Na5P3O10, phase II". Acta Crystallographica. 11 (5): 315–319. doi:10.1107/S0365110X58000876.
- ↑ "Substances Added to Food (Formerly EAFUS)".
- ↑ Calvo, P.; Remuñán‐López, C.; Vila-Jato, J. L.; Alonso, M. J. (3 January 1997). "प्रोटीन वाहक के रूप में उपन्यास हाइड्रोफिलिक चिटोसन-पॉलीइथाइलीन ऑक्साइड नैनोपार्टिकल्स". Journal of Applied Polymer Science. 63 (1): 125–132. doi:10.1002/(SICI)1097-4628(19970103)63:1<125::AID-APP13>3.0.CO;2-4.
- ↑ Saxton, C. A.; Ouderaa, F. J. G. (January 1989). "मसूड़े की सूजन के विकास पर जिंक साइट्रेट और ट्राईक्लोसन युक्त दंत चिकित्सा का प्रभाव". Journal of Periodontal Research. 24 (1): 75–80. doi:10.1111/j.1600-0765.1989.tb00860.x. PMID 2524573.
- ↑ Lobene, RR; Weatherford, T; Ross, NM; Lamm, RA; Menaker, L (1986). "क्लिनिकल परीक्षणों में उपयोग के लिए एक संशोधित मसूड़ा सूचकांक।". Clinical Preventive Dentistry. 8 (1): 3–6. PMID 3485495.
- ↑ Lobene, RR; Soparkar, PM; Newman, MB (1982). "डेंटल फ्लॉस का उपयोग। पट्टिका और मसूड़े की सूजन पर प्रभाव।". Clinical Preventive Dentistry. 4 (1): 5–8. PMID 6980082.
- ↑ Mankodi, Suru; Bartizek, Robert D.; Leslie Winston, J.; Biesbrock, Aaron R.; McClanahan, Stephen F.; He, Tao (January 2005). "Anti-gingivitis efficacy of a stabilized 0.454% stannous fluoride/sodium hexametaphosphate dentifrice. A controlled 6-month clinical trial". Journal of Clinical Periodontology. 32 (1): 75–80. doi:10.1111/j.1600-051X.2004.00639.x. PMID 15642062.
- ↑ Mankodi, S; Petrone, DM; Battista, G; Petrone, ME; Chaknis, P; DeVizio, W; Volpe, AR; Proskin, HM (1997). "Clinical efficacy of an optimized stannous fluoride dentifrice, Part 2: A 6-month plaque/gingivitis clinical study, northeast USA". Compendium of Continuing Education in Dentistry. 18 Spec No: 10–5. PMID 12206029.
- ↑ Mallatt, Mark; Mankodi, Suru; Bauroth, Karen; Bsoul, Samer A.; Bartizek, Robert D.; He, Tao (September 2007). "A controlled 6-month clinical trial to study the effects of a stannous fluoride dentifrice on gingivitis". Journal of Clinical Periodontology. 34 (9): 762–767. doi:10.1111/j.1600-051X.2007.01109.x. PMID 17645550.
- ↑ Lang, Niklaus P. (1990). "पेरियोडोंटल बीमारी की महामारी विज्ञान". Archives of Oral Biology. 35: S9–S14. doi:10.1016/0003-9969(90)90125-t. PMID 2088238.
- ↑ Ritz, Eberhard; Hahn, Kai; Ketteler, Markus; Kuhlmann, Martin K; Mann, Johannes (2012). "Phosphate Additives in Food—a Health Risk". Deutsches Ärzteblatt International. 109 (4): 49–55. doi:10.3238/arztebl.2012.0049. PMC 3278747. PMID 22334826.

