रेन्टजेनियम: Difference between revisions
m (added Category:Vigyan Ready using HotCat) |
No edit summary |
||
| (One intermediate revision by one other user not shown) | |||
| Line 138: | Line 138: | ||
[[Category:CS1 errors]] | [[Category:CS1 errors]] | ||
[[Category:Collapse templates]] | [[Category:Collapse templates]] | ||
[[Category:Commons category link from Wikidata]] | |||
[[Category:Commons category link is the pagename]] | [[Category:Commons category link is the pagename]] | ||
[[Category:Created On 18/05/2023]] | [[Category:Created On 18/05/2023]] | ||
[[Category:Good articles]] | [[Category:Good articles]] | ||
[[Category:Lua-based templates]] | |||
[[Category:Machine Translated Page]] | [[Category:Machine Translated Page]] | ||
[[Category:Navigational boxes| ]] | [[Category:Navigational boxes| ]] | ||
[[Category:Vigyan Ready]] | [[Category:Navigational boxes without horizontal lists]] | ||
[[Category:Pages including recorded pronunciations]] | |||
[[Category:Pages using infobox element with unknown parameters|Z]] | |||
[[Category:Pages with reference errors]] | |||
[[Category:Pages with script errors]] | |||
[[Category:Sidebars with styles needing conversion]] | |||
[[Category:Template documentation pages|Documentation/doc]] | |||
[[Category:Templates Vigyan Ready]] | |||
[[Category:Templates generating microformats]] | |||
[[Category:Templates that add a tracking category]] | |||
[[Category:Templates that are not mobile friendly]] | |||
[[Category:Templates that generate short descriptions]] | |||
[[Category:Templates using TemplateData]] | |||
[[Category:Use mdy dates from March 2018]] | |||
[[Category:Wikipedia metatemplates]] | |||
Latest revision as of 14:03, 15 June 2023
| Roentgenium | ||||||
|---|---|---|---|---|---|---|
| उच्चारण | ||||||
| जन अंक | [282] (unconfirmed: 286) | |||||
| Roentgenium in the periodic table | ||||||
| ||||||
| Atomic number (Z) | 111 | |||||
| समूह | group 11 | |||||
| अवधि | period 7 | |||||
| ब्लॉक | d-block | |||||
| ऋणावेशित सूक्ष्म अणु का विन्यास | [Rn] 5f14 6d9 7s2 (predicted)[1][2] | |||||
| प्रति शेल इलेक्ट्रॉन | 2, 8, 18, 32, 32, 17, 2 (predicted) | |||||
| भौतिक गुण | ||||||
| Phase at STP | solid (predicted)[3] | |||||
| Density (near r.t.) | 22–24 g/cm3 (predicted)[4][5] | |||||
| परमाणु गुण | ||||||
| ऑक्सीकरण राज्य | (−1), (+1), (+3), (+5), (+7) (predicted)[2][6][7] | |||||
| Ionization energies | ||||||
| परमाणु का आधा घेरा | empirical: 138 pm (predicted)[2][6] | |||||
| सहसंयोजक त्रिज्या | 121 pm (estimated)[8] | |||||
| अन्य गुण | ||||||
| प्राकृतिक घटना | synthetic | |||||
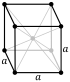
| क्रिस्टल की संरचना | body-centered cubic (bcc) (predicted)[3] | |||||
| CAS नंबर | 54386-24-2 | |||||
| History | ||||||
| नामी | after Wilhelm Röntgen | |||||
| खोज] | Gesellschaft für Schwerionenforschung (1994) | |||||
| ||||||
रेन्टजेनियम एक रासायनिक तत्व है जिसका प्रतीक Rg और परमाणु संख्या 111 है। यह एक अत्यंत रेडियोधर्मी कृत्रिम तत्व है जिसे प्रयोगशाला में बनाया जा सकता है लेकिन यह प्रकृति में नहीं पाया जाता है। सबसे स्थिर ज्ञात समस्थानिक, रेंटजेनियम -282, का आधा जीवन 100 सेकंड है, हालांकि अपुष्ट रेंटजेनियम -286 का आधा जीवन लगभग 10.7 मिनट हो सकता है। रेन्टजेनियम को पहली बार 1994 में डार्मस्टाट, जर्मनी के निकट भारी आयन अनुसंधान के लिए जीएसआई हेल्महोल्ट्ज द्वारा बनाया गया था। इसका नाम भौतिक विज्ञानी विल्हेम रॉन्टगन (जिसे रॉन्टजेन भी कहा जाता है) के नाम पर रखा गया है, जिन्होंने एक्स-रे की खोज की थी। केवल कुछ ही रेंटजेनियम परमाणुओं को कभी संश्लेषित किया गया है, और वैज्ञानिक अध्ययन से परे उनका कोई वर्तमान व्यावहारिक अनुप्रयोग नहीं है।
आवर्त सारणी में, यह एक डी-ब्लॉक ट्रांसएक्टिनाइड तत्व है। यह 7वीं आवर्त का सदस्य है और समूह 11 तत्वों में रखा गया है, हालांकि यह पुष्टि करने के लिए कोई रासायनिक प्रयोग नहीं किया गया है कि यह संक्रमण धातुओं की 6डी श्रृंखला के नौवें सदस्य के रूप में समूह 11 में सोने के लिए भारी समरूपता के रूप में व्यवहार करता है। रोएंटजेनियम की गणना इसके हल्के होमोलॉग्स, ताँबा, चाँदी और सोना के समान गुणों के लिए की जाती है, हालांकि यह उनसे कुछ अंतर दिखा सकता है। रेन्टजेनियम को कमरे के तापमान पर ठोस माना जाता है और इसकी नियमित अवस्था में धातु की उपस्थिति होती है।
परिचय
सबसे भारी परमाणु नाभिक परमाणु प्रतिक्रियाओं में बनाए जाते हैं जो असमान आकार के दो अन्य नाभिक को एक में मिलाते हैं; लगभग, द्रव्यमान के संदर्भ में दो नाभिक जितने अधिक असमान होते हैं, दोनों के प्रतिक्रिया करने की संभावना उतनी ही अधिक होती है। भारी नाभिकों से बनी सामग्री को एक लक्ष्य बनाया जाता है, जिस पर हल्के नाभिकों के बीम द्वारा बमबारी की जाती है। दो नाभिक एक में विलय तभी कर सकते हैं जब वे एक-दूसरे के काफी निकट हों; प्रायः, नाभिक (सभी धनात्मक रूप से आवेशित) इलेक्ट्रोस्टैटिक प्रतिकर्षण के कारण एक दूसरे को पीछे हटाते हैं। मजबूत अंतःक्रिया इस प्रतिकर्षण को दूर कर सकती है लेकिन केवल एक नाभिक से बहुत कम दूरी के भीतर; बीम नाभिक के वेग की तुलना में इस तरह के प्रतिकर्षण को नगण्य बनाने के लिए बीम नाभिक को बहुत तेज किया जाता है। दो नाभिकों के फ्यूज होने के लिए अकेले पास आना पर्याप्त नहीं है: जब दो नाभिक एक-दूसरे के पास आते हैं, तो वे प्रायः लगभग 10-20 सेकंड के लिए एक साथ रहते हैं और एक एकल बनाने के बदले नाभिक (जरूरी नहीं कि उसी संरचना में प्रतिक्रिया से पहले) फिर अलग हो जाते हैं। यदि संलयन होता है, तो अस्थायी विलय - जिसे यौगिक नाभिक कहा जाता है - एक उत्तेजित अवस्था है। अपनी उत्तेजना ऊर्जा को खोने और अधिक स्थिर स्थिति तक पहुंचने के लिए, एक यौगिक नाभिक या तो विखंडन करता है या एक या कई न्यूट्रॉन को बाहर निकालता है, जो ऊर्जा को दूर ले जाते हैं। प्रारंभिक टक्कर के बाद यह लगभग 10−16 सेकंड में होता है।
बीम लक्ष्य के माध्यम से गुजरता है और अगले कक्ष, विभाजक तक पहुंचता है; यदि एक नया नाभिक उत्पन्न होता है, तो इसे इस बीम के साथ ले जाया जाता है। विभाजक में, नए उत्पादित नाभिक को अन्य न्यूक्लाइड्स (जो कि मूल बीम और किसी भी अन्य प्रतिक्रिया उत्पादों) से अलग किया जाता है और एक सतह-बाधा संसूचक में स्थानांतरित किया जाता है, जो नाभिक को रोकता है।
संसूचक पर आगामी प्रभाव का सटीक स्थान चिह्नित है; इसकी ऊर्जा और आगमन के समय को भी चिन्हित किया गया है। स्थानांतरण में लगभग 10−6 सेकंड लगते हैं; पता लगाने के लिए, नाभिक को इतने लंबे समय तक जीवित रहना चाहिए। एक बार इसका क्षय पंजीकृत होने के बाद नाभिक को फिर से रिकॉर्ड किया जाता है, और क्षय का स्थान, ऊर्जा और समय मापा जाता है। एक नाभिक की स्थिरता मजबूत अंतःक्रिया द्वारा प्रदान की जाती है। हालाँकि, इसकी सीमा बहुत कम है; जैसे-जैसे नाभिक बड़े होते जाते हैं, सबसे बाहरी नाभिकों (प्रोटॉन और न्यूट्रॉन) पर उनका प्रभाव कमजोर होता जाता है। उसी समय, प्रोटॉन के बीच इलेक्ट्रोस्टैटिक प्रतिकर्षण द्वारा नाभिक फट जाता है, क्योंकि इसकी असीमित सीमा होती है। इस प्रकार सबसे भारी तत्वों के नाभिकों की सैद्धांतिक रूप से भविष्यवाणी की जाती है और अब तक देखा गया है मुख्य रूप से क्षय मोड के माध्यम से क्षय होता है जो इस तरह के प्रतिकर्षण के कारण होता है: अल्फा क्षय और सहज विखंडन; ये मोड अत्यधिक भारी तत्वों के नाभिक के लिए प्रमुख हैं। अल्फा क्षय उत्सर्जित अल्फा कणों द्वारा पंजीकृत होते हैं, और वास्तविक क्षय से पहले क्षय उत्पादों को निर्धारित करना आसान होता है; यदि इस तरह के क्षय या लगातार क्षय की एक श्रृंखला ज्ञात नाभिक उत्पन्न करती है, तो प्रतिक्रिया का मूल उत्पाद अंकगणितीय रूप से निर्धारित किया जा सकता है। सहज विखंडन, हालांकि, विभिन्न नाभिकों को उत्पादों के रूप में उत्पन्न करता है, इसलिए मूल न्यूक्लाइड को अपनी संतति से निर्धारित नहीं किया जा सकता है।
सबसे भारी तत्वों में से एक को संश्लेषित करने के उद्देश्य से भौतिकविदों के लिए उपलब्ध जानकारी इस प्रकार संसूचकों पर एकत्र की गई जानकारी है: जिसमें संसूचक के लिए एक कण के आगमन का स्थान, ऊर्जा और समय, और इसके क्षय हैं। भौतिक विज्ञानी इन आंकड़ों का विश्लेषण करते हैं और यह निष्कर्ष निकालना चाहते हैं कि यह वास्तव में एक नए तत्व के कारण हुआ था और दावा किए गए से भिन्न न्यूक्लाइड के कारण नहीं हो सकता था। प्रायः, प्रदान किये गए आँकड़े इस निष्कर्ष के लिए अपर्याप्त है कि एक नया तत्व निश्चित रूप से बनाया गया था और देखे गए प्रभावों के लिए कोई अन्य स्पष्टीकरण नहीं है; डेटा की व्याख्या करने में त्रुटियां की गई हैं।
इतिहास
आधिकारिक खोज
रेन्टजेनियम 8 दिसंबर, 1994 को जर्मनी के डार्मस्टैड में गेसेलस्कॉफ्ट फर स्च्वेरीवेनफोरस्चयंग (जीएसआई) में सिगर्ड हॉफमैन के नेतृत्व वाली एक अंतरराष्ट्रीय टीम द्वारा रासायनिक तत्वों की खोज की गई थी।[9] टीम नेनिकल -64 के त्वरित नाभिकों के साथ बिस्मथ-209 के लक्ष्य पर बमबारी की और समस्थानिक रेंटजेनियम-272 के तीन नाभिकों का पता लगाया:
यह प्रतिक्रिया पहले 1986 में डबना (तब सोवियत संघ में) में संयुक्त परमाणु अनुसंधान संस्थान में आयोजित की गई थी, लेकिन तब 272Rg का कोई परमाणु नहीं देखा गया था।[10] 2001 में, आई यु पी ए सी/आई यु पी ए पी संयुक्त कार्य दल (जे डब्ल्यू पी) ने निष्कर्ष निकाला कि उस समय खोज के लिए अपर्याप्त प्रमाण थे।[11] जीएसआई टीम ने 2002 में अपना प्रयोग दोहराया और तीन और परमाणुओं का पता लगाया।[12][13] अपनी 2003 की रिपोर्ट में, जेडब्ल्यूपी ने फैसला किया कि इस तत्व की खोज के लिए जीएसआई टीम को स्वीकार किया जाना चाहिए।[14]
नामकरण
अनाम और अनदेखे तत्वों के लिए मेंडेलीव के नामकरण का उपयोग करते हुए, रेंटजेनियम को ईका-गोल्ड के रूप में जाना जाना चाहिए। 1979 में, आई यु पी ए सी ने अनुशंसा प्रकाशित कीं, जिसके अनुसार तत्व को यूनुनियम कहा जाना था (यूयूयू के संबंधित प्रतीक के साथ),[15] एक स्थानधारक के रूप में एक व्यवस्थित तत्व नाम, जब तक कि तत्व की खोज नहीं की गई (और खोज की पुष्टि की गई) और एक स्थायी नाम तय किया गया था। यद्यपि रासायनिक समुदाय में सभी स्तरों पर व्यापक रूप से उपयोग किया जाता है, रसायन विज्ञान कक्षाओं से लेकर उन्नत पाठ्यपुस्तकों तक, अनुसंशाओं को ज्यादातर क्षेत्र में वैज्ञानिकों के बीच अनदेखा किया जाता है, जिन्होंने इसे E111, (111) या यहां तक कि केवल 111 के प्रतीक के साथ तत्व 111 कहा।[2]
एक्स-रे के खोजकर्ता जर्मन भौतिक विज्ञानी विल्हेम कॉनराड रॉन्टगन को सम्मानित करने के लिए 2004 में जीएसआई टीम द्वारा रेन्टजेनियम (Rg) नाम का सुझाव दिया गया था।[16] [16] यह नाम आई यु पी ए सी द्वारा 1 नवंबर, 2004 को स्वीकार किया गया था।[16]
समस्थानिक
| Isotope | Half-life[lower-alpha 1] | Decay mode |
Discovery year |
Discovery reaction | |
|---|---|---|---|---|---|
| Value | ref | ||||
| 272Rg | 4.5 ms | [17] | α | 1994 | 209Bi(64Ni,n) |
| 274Rg | 29 ms | [17] | α | 2004 | 278Nh(—,α) |
| 278Rg | 4.6 ms | [18] | α | 2006 | 282Nh(—,α) |
| 279Rg | 90 ms | [18] | α, SF | 2003 | 287Mc(—,2α) |
| 280Rg | 3.9 s | [18] | α, EC | 2003 | 288Mc(—,2α) |
| 281Rg | 11 s | [18] | SF, α | 2010 | 293Ts(—,3α) |
| 282Rg | 1.7 min | [19] | α | 2010 | 294Ts(—,3α) |
| 283Rg[lower-alpha 2] | 5.1 min | SF | 1999 | 283Cn(e−,νe) | |
| 286Rg[lower-alpha 2] | 10.7 min | [20] | α | 1998 | 290Fl(e−,νeα) |
रेन्टजेनियम में कोई स्थिर या प्राकृतिक रूप से पाए जाने वाले समस्थानिक नहीं होते हैं। कई रेडियोधर्मी समस्थानिकों को प्रयोगशाला में संश्लेषित किया गया है, या तो हल्के तत्वों के नाभिकों के संलयन द्वारा या भारी तत्वों के मध्यवर्ती क्षय उत्पादों के रूप में। 272, 274, 278-283, और 286 (283 और 286 अपुष्ट) परमाणु भार के साथ रेंटजेनियम के नौ अलग-अलग समस्थानिकों की सूचना दी गई है, जिनमें से दो, रेंटजेनियम-272 और रेंटजेनियम-274 ज्ञात लेकिन अपुष्ट मितस्थायी स्थिति हैं। ये सभी अल्फा क्षय या सहज विखंडन के माध्यम से क्षय होते हैं,[21] यद्यपि 280Rg में एक इलेक्ट्रॉन कैप्चर शाखा भी हो सकती है।[22]
स्थिरता और आधा जीवन
सभी रेन्टजेनियम समस्थानिक बेहद अस्थिर और रेडियोधर्मी हैं; सामान्यतः, भारी समस्थानिक हल्के की तुलना में अधिक स्थिर होते हैं। सबसे स्थिर ज्ञात रेंटजेनियम समस्थानिक, 282Rg, सबसे भारी ज्ञात रॉन्टजेनियम समस्थानिक भी है; इसका 100 सेकंड का आधा जीवन है। अपुष्ट 286Rg और भी भारी है और लगभग 10.7 मिनट का एक और भी लंबा आधा जीवन प्रतीत होता है, जो इसे सबसे लंबे समय तक रहने वाले अतिभारी न्यूक्लाइड्स में से एक बना देगा; इसी तरह, अपुष्ट 28ɜRg का लगभग 5.1 मिनट का लंबा आधा जीवन प्रतीत होता है। समस्थानिकों 280Rg और 281Rg के बारे में यह भी बताया गया है कि वे एक सेकंड में आधे जीवन जीते हैं। शेष समस्थानिकों का आधा जीवन मिलीसेकेंड श्रेणी में होता है।[21]
अनुमानित गुण
परमाणु गुणों के अलावा, रोएंटजेनियम या इसके यौगिकों के किसी भी गुण को मापा नहीं गया है; यह इसके बेहद सीमित और महंगे उत्पादन [23]और तथ्य यह है कि रेंटजेनियम (और इसके माता-पिता) बहुत जल्दी क्षय हो जाते हैं। रेंटजेनियम धातु के गुण अज्ञात रहते हैं और केवल पूर्वाकलन उपलब्ध हैं।
रासायनिक
रेन्टजेनियम संक्रमण धातुओं की 6डी श्रृंखला का नौवां सदस्य है।[24] इसकी आयनीकरण क्षमता और परमाणु त्रिज्या और आयनिक त्रिज्या की गणना इसके हल्के होमोलॉग गोल्ड के समान है, इस प्रकार इसका अर्थ है कि रेंटजेनियम के मूल गुण अन्य समूह 11 तत्वों, तांबा, चांदी और सोने के समान होंगे; हालाँकि, यह भी अनुमान लगाया गया है कि इसके हल्के समरूपों से कई अंतर दिखाई देंगे।[2]
रेन्टजेनियम को एक महान धातु होने की भविष्यवाणी की गई है। Rg3+/Rg युगल के लिए 1.9 V की मानक इलेक्ट्रोड क्षमता Au3+/Au युगल के लिए 1.5 V की तुलना में अधिक है। रोएंटजेनियम की भविष्यवाणी की गई 1020 kJ/mol की प्रथम आयनन ऊर्जा की 1037 kJ/mo पर नोबल गैस रेडॉन से लगभग मेल खाती है।[2] लाइटर समूह 11 तत्वों के सबसे स्थिर ऑक्सीकरण अवस्थाओं के आधार पर, कम स्थिर +1 अवस्था के साथ, रेंटजेनियम को स्थिर +5 और +3 ऑक्सीकरण अवस्थाओं को दिखाने की भविष्यवाणी की जाती है। +3 स्थिति के सबसे स्थिर होने की भविष्यवाणी की गई है। रोएंटजेनियम (III) की सोने (III) के साथ तुलनीय प्रतिक्रियाशीलता होने की उम्मीद है, लेकिन यह अधिक स्थिर होना चाहिए और बड़ी मात्रा में यौगिकों का निर्माण करना चाहिए। सापेक्षतावादी प्रभावों के कारण सोना भी कुछ हद तक स्थिर -1 अवस्था बनाता है, और यह सुझाव दिया गया है कि रेंटजेनियम भी ऐसा कर सकता है:[2]फिर भी, रेन्टजेनियम की इलेक्ट्रॉन बंधुता लगभग 1.6 eV (37 kcal/mol) होने की उम्मीद है, सोने के 2.3 eV (53 kcal/mol) मूल्य से काफी कम है, इसलिए रोएंटगेनीड्स स्थिर या संभव भी नहीं हो सकता है।[6] 6d कक्षक चौथे संक्रमण धातु श्रृंखला के अंत में आपेक्षिक प्रभावों और स्पिन-ऑर्बिट अंतःक्रियाओं द्वारा अस्थिर हो जाते हैं, इस प्रकार उच्च ऑक्सीकरण अवस्था रोएंटजेनियम (V) को इसके हल्के होमोलॉग गोल्ड (V) (केवल गोल्ड पेंटाफ्लोराइड में जाना जाता है) की तुलना में अधिक स्थिर बनाते हैं (पेंटाफ्लोराइड, Au2F10) क्योंकि 6d इलेक्ट्रॉन अधिक सीमा तक बंधन में भाग लेते हैं। स्पिन-ऑर्बिट इंटरैक्शन अधिक बंधन वाले 6d इलेक्ट्रॉनों के साथ आणविक रेंटजेनियम यौगिकों को स्थिर करता है; उदाहरण के लिए, RgF−
6 की RgF−
4से अधिक स्थिर होने की उम्मीद है, जो कि RgF−
2 से अधिक स्थिर होने की उम्मीद है।[2] RgF−
6 की स्थिरता AuF−
6 की स्थिरता के समरूप है ; चांदी का एनालॉग AgF−
6 अज्ञात है और AgF−
4 और F2 अपघटन के लिए केवल अशक्त रूप से स्थिर होने की उम्मीद है। इसके अलावा, Rg2 F10 अपघटन के लिए स्थिर होने की उम्मीद है, Au2F10 के अनुरूप, जबकि Ag2F10, Ag2F6 और F2 के अपघटन के लिए अस्थिर होना चाहिए। जबकि Ag2F10 Ag के अपघटन के लिए अस्थिर होना चाहिए। गोल्ड हेप्टाफ्लोराइड, AuF7, को गोल्ड(V) डिफ्लोराइन कॉम्प्लेक्स AuF5·F2 के रूप में जाना जाता है, जो वास्तविक सोने (VII) हेप्टाफ्लोराइड की तुलना में ऊर्जा में कम होता है; इसके बदले RgF7 की गणना एक सच्चे रेंटजेनियम (VII) हेप्टाफ्लोराइड के रूप में अधिक स्थिर होने के लिए की जाती है, हालांकि यह कुछ हद तक अस्थिर होगा, इसका Rg2F10 और F2 में अपघटन कमरे के तापमान पर थोड़ी मात्रा में ऊर्जा जारी करता है।[7]रेन्टजेनियम(I) को प्राप्त करना कठिन उम्मीद है।[2][25][26] सोना आसानी से साइनाइड कॉम्प्लेक्स Au(CN)−
2 बनाता है, जिसका उपयोग सोने के सायनाइडेशन की प्रक्रिया के माध्यम से अयस्क से इसके निष्कर्षण में किया जाता है; रेन्टजेनियम सूट का पालन करने और Rg(CN)−
2 बनाने की उम्मीद है।[27]
रोएंटजेनियम के संभावित रसायन विज्ञान में दो पिछले तत्वों, मीटनेरियम और डार्मस्टेडियम की तुलना में अधिक रुचि प्राप्त हुई है, क्योंकि समूह 11 तत्वों के वैलेंस एस-सबशेल्स के सापेक्षिक रूप से रोएंटेनियम में सबसे दृढ़ता से अनुबंधित होने की उम्मीद है।[2]आण्विक यौगिक RgH पर गणना से पता चलता है कि सापेक्षतावादी प्रभाव रेन्टजेनियम-हाइड्रोजन बंधन की ताकत को दोगुना करते हैं, भले ही स्पिन-ऑर्बिट इंटरैक्शन भी इसे 0.7 eV (16 kcal/mol) से कमजोर करते हैं। यौगिकों AuX और RgX, जहां X = F, क्लोरीन, ब्रोमिन, ऑक्सीजन, Au, या Rg का भी अध्ययन किया गया।[2][28] Rg+ को सबसे नर्म धातु आयन होने का अनुमान है, जो Au+ से भी नरम है, हालांकि इस बात पर असहमति है कि यह अम्ल या क्षार के रूप में व्यवहार करेगा या नहीं।[29][30] जलीय विलयन में, Rg+ एक्वा आयन [Rg(H2O)2]+ बनाता है, जिसकी Rg–O बॉन्ड दूरी 207.1 पीकोमीटर है। अमोनिया, फॉस्फीन और हाइड्रोजन सल्फाइड के साथ Rg (I) कॉम्प्लेक्स बनाने की भी उम्मीद है।[30]
भौतिक और परमाणु
रेन्टजेनियम सामान्य परिस्थितियों में एक ठोस होने की उम्मीद है और शरीर-केंद्रित क्यूबिक संरचना में क्रिस्टलीकृत होने की उम्मीद है, इसके हल्के जन्मजात के विपरीत, जो चेहरे-केंद्रित क्यूबिक संरचना में क्रिस्टलीकृत होते है, इसकी वजह से अलग-अलग इलेक्ट्रॉन चार्ज घनत्व होने की उम्मीद है।[3] यह लगभग 22–24 g/cm3 के घनत्व के साथ एक बहुत भारी धातु होनी चाहिए; इसकी तुलना में, सबसे घना ज्ञात तत्व जिसका घनत्व मापा गया है, ऑस्मियम, का घनत्व 22.61 g/cm3 है।[4][5] रेंटजेनियम की परमाणु त्रिज्या लगभग 138 pm होने की उम्मीद है।[2]
प्रायोगिक रसायन विज्ञान
रेंटजेनियम की रासायनिक विशेषताओं का स्पष्ट निर्धारण अभी तक स्थापित नहीं किया गया है[31] प्रतिक्रियाओं की कम उत्पादन के कारण जो रोएंजेनियम समस्थानिक उत्पन्न करते हैं।[2]ट्रांसएक्टिनाइड तत्व पर किए जाने वाले रासायनिक अध्ययनों के लिए, कम से कम चार परमाणुओं का उत्पादन किया जाना चाहिए, उपयोग किए गए समस्थानिक का आधा जीवन कम से कम 1 सेकंड होना चाहिए, और उत्पादन की दर प्रति सप्ताह कम से कम एक परमाणु होनी चाहिए।[24]भले ही 282Rg का आधा जीवन, सबसे स्थिर पुष्टि रॉन्टजेनियम समस्थानिक, 100 सेकंड है, जो रासायनिक अध्ययन करने के लिए पर्याप्त लंबा है, एक और बाधा रोएंटेनियम समस्थानिक के उत्पादन की दर को बढ़ाने और प्रयोगों को हफ्तों या महीनों तक चलने देने की आवश्यकता है। सांख्यिकीय रूप से महत्वपूर्ण परिणाम प्राप्त किए जा सकते हैं। रोएंजेनियम समस्थानिकों को अलग करने के लिए पृथक्करण और पता लगाना लगातार किया जाना चाहिए और स्वचालित प्रणालियों को गैस-चरण और रोएंजेनियम के विलयन रसायन पर प्रयोग करने की अनुमति देनी चाहिए, क्योंकि भारी तत्वों की पैदावार हल्के तत्वों की तुलना में कम होने की भविष्यवाणी की जाती है। हालाँकि, रेंटजेनियम के प्रायोगिक रसायन विज्ञान पर उतना ध्यान नहीं दिया गया है जितना कि कोपरनिकस से लिवरमोरियम तक के भारी तत्वों पर ध्यान दिया गया,[2][31][32] सैद्धांतिक भविष्यवाणियों में प्रारंभिक रुचि के बावजूद समूह 11 में एनएस उपधारा पर सापेक्ष प्रभाव के कारण रेंटजेनियम में अधिकतम तक पहुंच गया।[2]समस्थानिक 280Rg और 281Rg रासायनिक प्रयोग के लिए आशाजनक हैं और इन्हें क्रमशः मोस्कोवियम समस्थानिकों 288Mc और 289Mc की पोती के रूप में उत्पादित किए जा सकते हैं क्रमशः एमसी;[33] उनके माता-पिता निहोनियम समस्थानिक 284Nh और 285Nh हैं, जिसकी प्रारंभिक रासायनिक जांच पहले ही हो चुकी है।[34]
यह भी देखें
व्याख्यात्मक नोट्स
उद्धरण
- ↑ Turler, A. (2004). "Gas Phase Chemistry of Superheavy Elements" (PDF). Journal of Nuclear and Radiochemical Sciences. 5 (2): R19–R25. doi:10.14494/jnrs2000.5.R19.
- ↑ 2.00 2.01 2.02 2.03 2.04 2.05 2.06 2.07 2.08 2.09 2.10 2.11 2.12 2.13 2.14 2.15 Hoffman, Darleane C.; Lee, Diana M.; Pershina, Valeria (2006). "Transactinides and the future elements". In Morss; Edelstein, Norman M.; Fuger, Jean (eds.). The Chemistry of the Actinide and Transactinide Elements (3rd ed.). Dordrecht, The Netherlands: Springer Science+Business Media. ISBN 978-1-4020-3555-5.
- ↑ 3.0 3.1 3.2 Östlin, A.; Vitos, L. (2011). "First-principles calculation of the structural stability of 6d transition metals". Physical Review B. 84 (11): 113104. Bibcode:2011PhRvB..84k3104O. doi:10.1103/PhysRevB.84.113104.
- ↑ 4.0 4.1 Gyanchandani, Jyoti; Sikka, S. K. (May 10, 2011). "Physical properties of the 6 d -series elements from density functional theory: Close similarity to lighter transition metals". Physical Review B. 83 (17): 172101. Bibcode:2011PhRvB..83q2101G. doi:10.1103/PhysRevB.83.172101.
- ↑ 5.0 5.1 Kratz; Lieser (2013). Nuclear and Radiochemistry: Fundamentals and Applications (3rd ed.). p. 631.
- ↑ 6.0 6.1 6.2 Fricke, Burkhard (1975). "Superheavy elements: a prediction of their chemical and physical properties". Recent Impact of Physics on Inorganic Chemistry. Structure and Bonding. 21: 89–144. doi:10.1007/BFb0116498. ISBN 978-3-540-07109-9. Retrieved October 4, 2013.
- ↑ 7.0 7.1 Conradie, Jeanet; Ghosh, Abhik (June 15, 2019). "Theoretical Search for the Highest Valence States of the Coinage Metals: Roentgenium Heptafluoride May Exist". Inorganic Chemistry. 2019 (58): 8735–8738. doi:10.1021/acs.inorgchem.9b01139. PMID 31203606.
- ↑ Chemical Data. Roentgenium - Rg, Royal Chemical Society
- ↑ Hofmann, S.; Ninov, V.; Heßberger, F.P.; Armbruster, P.; Folger, H.; Münzenberg, G.; Schött, H. J.; Popeko, A. G.; Yeremin, A. V.; Andreyev, A. N.; Saro, S.; Janik, R.; Leino, M. (1995). "नया तत्व 111". Zeitschrift für Physik A. 350 (4): 281–282. Bibcode:1995ZPhyA.350..281H. doi:10.1007/BF01291182. S2CID 18804192.
- ↑ Barber, R. C.; Greenwood, N. N.; Hrynkiewicz, A. Z.; Jeannin, Y. P.; Lefort, M.; Sakai, M.; Ulehla, I.; Wapstra, A. P.; Wilkinson, D. H. (1993). "Discovery of the transfermium elements. Part II: Introduction to discovery profiles. Part III: Discovery profiles of the transfermium elements". Pure and Applied Chemistry. 65 (8): 1757. doi:10.1351/pac199365081757. S2CID 195819585. (Note: for Part I see Pure Appl. Chem., Vol. 63, No. 6, pp. 879–886, 1991)
- ↑ Karol; Nakahara, H.; Petley, B. W.; Vogt, E. (2001). "On the discovery of the elements 110–112" (PDF). Pure Appl. Chem. 73 (6): 959–967. doi:10.1351/pac200173060959. S2CID 97615948.
- ↑ Hofmann, S.; Heßberger, F. P.; Ackermann, D.; Münzenberg, G.; Antalic, S.; Cagarda, P.; Kindler, B.; Kojouharova, J.; Leino, M.; Lommel, B.; Mann, R.; Popeko, A. G.; Reshitko, S.; Śaro, S.; Uusitalo, J.; Yeremin, A. V. (2002). "New results on elements 111 and 112". European Physical Journal A. 14 (2): 147–157. Bibcode:2002EPJA...14..147H. doi:10.1140/epja/i2001-10119-x. S2CID 8773326.
- ↑ Hofmann; et al. "New results on element 111 and 112" (PDF). GSI report 2000. pp. 1–2. Retrieved April 21, 2018.
- ↑ Karol, P. J.; Nakahara, H.; Petley, B. W.; Vogt, E. (2003). "On the claims for discovery of elements 110, 111, 112, 114, 116, and 118" (PDF). Pure Appl. Chem. 75 (10): 1601–1611. doi:10.1351/pac200375101601. S2CID 95920517.
- ↑ Chatt, J. (1979). "100 से अधिक परमाणु क्रमांक वाले तत्वों के नामकरण के लिए अनुशंसाएँ". Pure and Applied Chemistry. 51 (2): 381–384. doi:10.1351/pac197951020381.
- ↑ 16.0 16.1 16.2 Corish; Rosenblatt, G. M. (2004). "परमाणु संख्या 111 वाले तत्व का नाम और प्रतीक" (PDF). Pure Appl. Chem. 76 (12): 2101–2103. doi:10.1351/pac200476122101. S2CID 195819587.
- ↑ 17.0 17.1 Audi, G.; Kondev, F. G.; Wang, M.; Huang, W. J.; Naimi, S. (2017). "The NUBASE2016 evaluation of nuclear properties" (PDF). Chinese Physics C. 41 (3): 030001. Bibcode:2017ChPhC..41c0001A. doi:10.1088/1674-1137/41/3/030001.
- ↑ 18.0 18.1 18.2 18.3 Oganessian, Yu. Ts.; Utyonkov, V. K.; Kovrizhnykh, N. D.; et al. (2022). "New isotope 286Mc produced in the 243Am+48Ca reaction". Physical Review C. 106 (64306): 064306. Bibcode:2022PhRvC.106f4306O. doi:10.1103/PhysRevC.106.064306. S2CID 254435744.
- ↑ Oganessian, Y.T. (2015). "Super-heavy element research". Reports on Progress in Physics. 78 (3): 036301. Bibcode:2015RPPh...78c6301O. doi:10.1088/0034-4885/78/3/036301. PMID 25746203. S2CID 37779526.
- ↑ Hofmann, S.; Heinz, S.; Mann, R.; et al. (2016). "Remarks on the Fission Barriers of SHN and Search for Element 120". In Peninozhkevich, Yu. E.; Sobolev, Yu. G. (eds.). Exotic Nuclei: EXON-2016 Proceedings of the International Symposium on Exotic Nuclei. Exotic Nuclei. pp. 155–164. doi:10.1142/9789813226548_0024. ISBN 9789813226555.
- ↑ 21.0 21.1 Sonzogni, Alejandro. "न्यूक्लाइड्स का इंटरएक्टिव चार्ट". National Nuclear Data Center: Brookhaven National Laboratory. Archived from the original on July 28, 2018. Retrieved June 6, 2008.
- ↑ Forsberg, U.; et al. (2016). "Recoil-α-fission and recoil-α-α-fission events observed in the reaction 48Ca + 243Am". Nuclear Physics A. 953: 117–138. arXiv:1502.03030. Bibcode:2016NuPhA.953..117F. doi:10.1016/j.nuclphysa.2016.04.025. S2CID 55598355.
- ↑ Cite error: Invalid
<ref>tag; no text was provided for refs namedBloomberg - ↑ 24.0 24.1 Griffith, W. P. (2008). "आवर्त सारणी और प्लेटिनम समूह धातुएँ". Platinum Metals Review. 52 (2): 114–119. doi:10.1595/147106708X297486.
- ↑ Seth, M.; Cooke, F.; Schwerdtfeger, P.; Heully, J.-L.; Pelissier, M. (1998). "The chemistry of the superheavy elements. II. The stability of high oxidation states in group 11 elements: Relativistic coupled cluster calculations for the di-, tetra- and hexafluoro metallates of Cu, Ag, Au, and element 111". J. Chem. Phys. 109 (10): 3935–43. Bibcode:1998JChPh.109.3935S. doi:10.1063/1.476993. S2CID 54803557.
- ↑ Seth, M.; Faegri, K.; Schwerdtfeger, P. (1998). "The Stability of the Oxidation State +4 in Group 14 Compounds from Carbon to Element 114". Angew. Chem. Int. Ed. Engl. 37 (18): 2493–6. doi:10.1002/(SICI)1521-3773(19981002)37:18<2493::AID-ANIE2493>3.0.CO;2-F. PMID 29711350.
- ↑ Demissie, Taye B.; Ruud, Kenneth (February 25, 2017). "डार्मस्टेडियम, रेंटजेनियम और कॉपरनिकियम साइनाइड के साथ मजबूत बंधन बनाते हैं" (PDF). International Journal of Quantum Chemistry. 2017: e25393. doi:10.1002/qua.25393. hdl:10037/13632.
- ↑ Liu, W.; van Wüllen, C. (1999). "Spectroscopic constants of gold and eka-gold (element 111) diatomic compounds: The importance of spin–orbit coupling". J. Chem. Phys. 110 (8): 3730–5. Bibcode:1999JChPh.110.3730L. doi:10.1063/1.478237.
- ↑ Thayer, John S. (2010). "Relativistic Effects and the Chemistry of the Heavier Main Group Elements". कम्प्यूटेशनल रसायन विज्ञान और भौतिकी में चुनौतियाँ और अग्रिम. p. 82. doi:10.1007/978-1-4020-9975-5_2. ISBN 978-1-4020-9974-8.
{{cite book}}:|journal=ignored (help) - ↑ 30.0 30.1 Hancock, Robert D.; Bartolotti, Libero J.; Kaltsoyannis, Nikolas (November 24, 2006). "अतिभारी तत्व 111 के कुछ जलीय-चरण रसायन विज्ञान की घनत्व कार्यात्मक सिद्धांत-आधारित भविष्यवाणी। रोएंटजेनियम (I) 'नरम' धातु आयन है". Inorg. Chem. 45 (26): 10780–5. doi:10.1021/ic061282s. PMID 17173436.
- ↑ 31.0 31.1 Düllmann, Christoph E. (2012). "जीएसआई में अतिभारी तत्व: भौतिकी और रसायन विज्ञान के फोकस में तत्व 114 के साथ एक व्यापक शोध कार्यक्रम". Radiochimica Acta. 100 (2): 67–74. doi:10.1524/ract.2011.1842. S2CID 100778491.
- ↑ Eichler, Robert (2013). "अत्यधिक भारी तत्वों के द्वीप के तट पर रसायन विज्ञान के पहले पदचिन्ह". Journal of Physics: Conference Series. 420 (1): 012003. arXiv:1212.4292. Bibcode:2013JPhCS.420a2003E. doi:10.1088/1742-6596/420/1/012003. S2CID 55653705.
- ↑ Moody, Ken (November 30, 2013). "Synthesis of Superheavy Elements". In Schädel, Matthias; Shaughnessy, Dawn (eds.). अतिभारी तत्वों का रसायन (2nd ed.). Springer Science & Business Media. pp. 24–8. ISBN 9783642374661.
- ↑ Aksenov, Nikolay V.; Steinegger, Patrick; Abdullin, Farid Sh.; Albin, Yury V.; Bozhikov, Gospodin A.; Chepigin, Viktor I.; Eichler, Robert; Lebedev, Vyacheslav Ya.; Mamudarov, Alexander Sh.; Malyshev, Oleg N.; Petrushkin, Oleg V.; Polyakov, Alexander N.; Popov, Yury A.; Sabel'nikov, Alexey V.; Sagaidak, Roman N.; Shirokovsky, Igor V.; Shumeiko, Maksim V.; Starodub, Gennadii Ya.; Tsyganov, Yuri S.; Utyonkov, Vladimir K.; Voinov, Alexey A.; Vostokin, Grigory K.; Yeremin, Alexander; Dmitriev, Sergey N. (July 2017). "On the volatility of nihonium (Nh, Z = 113)". The European Physical Journal A. 53 (158): 158. Bibcode:2017EPJA...53..158A. doi:10.1140/epja/i2017-12348-8. S2CID 125849923.
सामान्य ग्रंथ सूची
- Audi, G.; Kondev, F. G.; Wang, M.; et al. (2017). "NUBASE2016 परमाणु गुणों का मूल्यांकन". Chinese Physics C. 41 (3): 030001. Bibcode:2017ChPhC..41c0001A. doi:10.1088/1674-1137/41/3/030001.
- Beiser, A. (2003). आधुनिक भौतिकी की अवधारणाएँ (6th ed.). McGraw-Hill. ISBN 978-0-07-244848-1. OCLC 48965418.
- Hoffman, D. C.; Ghiorso, A.; Seaborg, G. T. (2000). द ट्रांसयूरेनियम पीपल: द इनसाइड स्टोरी. World Scientific. ISBN 978-1-78-326244-1.
- Kragh, H. (2018). ट्रांसयूरानिक से सुपरहेवी एलिमेंट्स: ए स्टोरी ऑफ़ डिस्प्यूट एंड क्रिएशन. Springer. ISBN 978-3-319-75813-8.
- Zagrebaev, V.; Karpov, A.; Greiner, W. (2013). "अतिभारी तत्व अनुसंधान का भविष्य: अगले कुछ वर्षों में किन नाभिकों का संश्लेषण किया जा सकता है?". Journal of Physics: Conference Series. 420 (1): 012001. arXiv:1207.5700. Bibcode:2013JPhCS.420a2001Z. doi:10.1088/1742-6596/420/1/012001. ISSN 1742-6588. S2CID 55434734.
बाहरी संबंध
- रेन्टजेनियम at The Periodic Table of Videos (University of Nottingham)