प्रोपलीन कार्बोनेट: Difference between revisions
No edit summary |
No edit summary |
||
| Line 53: | Line 53: | ||
}} | }} | ||
'''प्रोपलीन कार्बोनेट''' (सदैव संक्षिप्त '''PC''') कार्बनिक यौगिक माने जाते है जिसका सूत्र C<sub>4</sub>H<sub>6</sub>O<sub>3</sub> है। यह [[प्रोपलीन ग्लाइकोल]] से प्राप्त चक्रीय [[कार्बोनेट एस्टर]] | '''प्रोपलीन कार्बोनेट''' (सदैव संक्षिप्त '''PC''') कार्बनिक यौगिक माने जाते है जिसका सूत्र C<sub>4</sub>H<sub>6</sub>O<sub>3</sub> है। यह [[प्रोपलीन ग्लाइकोल]] से प्राप्त चक्रीय [[कार्बोनेट एस्टर]] होते है।<ref>[http://webbook.nist.gov/cgi/cbook.cgi?ID=C108327 WebBook page for propylene carbonate].</ref> यह रंगहीन और गंधहीन तरल [[रासायनिक ध्रुवीयता]], एप्रोटिक विलायक के रूप में उपयोगी की जाती है।<ref name = ullmann/> और प्रोपलीन कार्बोनेट चिरलिटी (रसायन विज्ञान) है, किंतु अधिकांश संदर्भों में रेसमिक मिश्रण के रूप में उपयोग किया जाता है। | ||
== तैयारी == | == तैयारी == | ||
चूंकि [[ एक विषैली गैस |विषैली गैस]] , प्रोपलीन और एथिलीन कार्बोनेट का उपयोग करके कई कार्बनिक कार्बोनेट का उत्पादन किया जाता है,और अपवाद यह हैं। की वे मुख्य रूप से [[एपॉक्साइड]] के [[कार्बोनेशन]] द्वारा प्रस्तुत किए जाते हैं<ref name = ullmann/>(एपोक्सीप्रोपेन, या [[प्रोपलीन ऑक्साइड]] यहाँ): | चूंकि [[ एक विषैली गैस |विषैली गैस]] , प्रोपलीन और एथिलीन कार्बोनेट का उपयोग करके कई कार्बनिक कार्बोनेट का उत्पादन किया जाता है,और अपवाद यह हैं। की वे मुख्य रूप से [[एपॉक्साइड]] के [[कार्बोनेशन]] द्वारा प्रस्तुत किए जाते हैं<ref name = ullmann/>(एपोक्सीप्रोपेन, या [[प्रोपलीन ऑक्साइड]] यहाँ): | ||
: CH<sub>3</sub>CHCH<sub>2</sub>O + CO<sub>2</sub> → CH<sub>3</sub>C<sub>2</sub>H<sub>3</sub>O<sub>2</sub>CO | : CH<sub>3</sub>CHCH<sub>2</sub>O + CO<sub>2</sub> → CH<sub>3</sub>C<sub>2</sub>H<sub>3</sub>O<sub>2</sub>CO | ||
इस प्रकार से यह प्रक्रिया विशेष रूप से आकर्षक मानी जाती है क्योंकि इन एपॉक्साइड्स के उत्पादन में कार्बन डाइऑक्साइड की अधिक | इस प्रकार से यह प्रक्रिया विशेष रूप से आकर्षक मानी जाती है क्योंकि इन एपॉक्साइड्स के उत्पादन में कार्बन डाइऑक्साइड की अधिक खपत होती है। इस प्रकार यह प्रतिक्रिया हरित प्रक्रिया का सही उदाहरण माना जाता है। और फॉस्जीन के साथ 1,2-प्रोपेनेडियोल की संबंधित प्रतिक्रिया जटिल होती है, न केवल प्रोपीलीन कार्बोनेट किंतु ओलिगोमेरिक उत्पाद भी उत्पन्न कर सकती है। | ||
किंतु प्रोपलीन कार्बोनेट को [[जिंक एसीटेट]] के ऊपर [[यूरिया]] और प्रोपलीन ग्लाइकोल से भी संश्लेषित किया जा सकता है।<ref>Synthesis of propylene carbonate from urea http://pubs.acs.org/doi/abs/10.1021/ie049948i</ref> | किंतु प्रोपलीन कार्बोनेट को [[जिंक एसीटेट]] के ऊपर [[यूरिया]] और प्रोपलीन ग्लाइकोल से भी संश्लेषित किया जा सकता है।<ref>Synthesis of propylene carbonate from urea http://pubs.acs.org/doi/abs/10.1021/ie049948i</ref> | ||
| Line 64: | Line 64: | ||
=== विलायक के रूप में === | === विलायक के रूप में === | ||
इसके अतिरिक्त | इसके अतिरिक्त प्रोपलीन कार्बोनेट का उपयोग ध्रुवीय, [[ aprotic |एप्रोटिक]] विलायक के रूप में किया जाता है।<ref>{{Ullmann|author = Dieter Stoye | title = Solvents | doi = 10.1002/14356007.a24_437}}.</ref> इसमें उच्च [[आणविक द्विध्रुवीय क्षण]] (4.9 [[डेबी]]) पाए जाते है, जोकी [[एसीटोन]] (2.91 डेबी) और [[एथिल एसीटेट]] (1.78 डेबी) की तुलना में अधिक होते है।<ref name = CRC/> इस प्रकार से उदाहरण के लिए, [[ पोटैशियम |पोटैशियम]] , [[सोडियम]] और अन्य क्षार धातुओं को उनके [[क्लोराइड]] के [[ इलेक्ट्रोलीज़ |इलेक्ट्रोलीज़]] द्वारा और प्रोपिलीन कार्बोनेट में भंग अन्य लवणों को प्राप्त करना संभव होता है।<ref name="jorn">{{cite journal | author1 = J. Jorné | author2 = C. W. Tobias | year = 1975 | title = प्रोपलीन कार्बोनेट से क्षार धातुओं का इलेक्ट्रोडोडिशन| journal = J. Appl. Electrochem. | volume = 5 | issue = 4 | pages = 279–290 | doi = 10.1007/BF00608791| s2cid = 93629501 | url = http://www.escholarship.org/uc/item/8m6348vh }}</ref> | ||
=== [[इलेक्ट्रोलाइट]] === | === [[इलेक्ट्रोलाइट]] === | ||
इस प्रकार से इसमें 64 की उच्च [[सापेक्ष पारगम्यता]] (ढांकता हुआ स्थिरांक) के कारण, यह सदैव [[लिथियम बैटरी]] में इलेक्ट्रोलाइट्स के उच्च-पारगम्यता घटक के रूप में उपयोग किया जाता है,सामान्यतः कम-चिपचिपापन विलायक (जैसे [[डाईमेथोक्सीएथेन]]) के साथ उपयुक्त किया जाता है । इसकी उच्च ध्रुवीयता इसे लिथियम आयनों के चारों ओर प्रभावी [[solation|सोलेसन]] शेल बनाने की अनुमति देती है, जिससे प्रवाहकीय इलेक्ट्रोलाइट बनता है। किंतु , इसका उपयोग [[लिथियम आयन बैटरी]] में नहीं किया जाता है। [[ग्रेफाइट इंटरकलेशन कंपाउंड]] पर इसके विनाशकारी प्रभाव के कारण लिथियम-आयन बैटरी का उपयोग नहीं किया जाता है।<ref>{{cite book | author = Doron Aurbach | title = गैर-जलीय इलेक्ट्रोकैमिस्ट्री| publisher = CRC Press | year = 1999 | isbn = 978-0824773342}}</ref> | इस प्रकार से इसमें 64 की उच्च [[सापेक्ष पारगम्यता]] (ढांकता हुआ स्थिरांक) के कारण, यह सदैव [[लिथियम बैटरी]] में इलेक्ट्रोलाइट्स के उच्च-पारगम्यता घटक के रूप में उपयोग किया जाता है,सामान्यतः कम-चिपचिपापन विलायक (जैसे [[डाईमेथोक्सीएथेन]]) के साथ उपयुक्त किया जाता है । इसकी उच्च ध्रुवीयता इसे लिथियम आयनों के चारों ओर प्रभावी [[solation|सोलेसन]] शेल बनाने की अनुमति देती है, जिससे प्रवाहकीय इलेक्ट्रोलाइट बनता है। किंतु , इसका उपयोग [[लिथियम आयन बैटरी]] में नहीं किया जाता है। [[ग्रेफाइट इंटरकलेशन कंपाउंड]] पर इसके विनाशकारी प्रभाव के कारण लिथियम-आयन बैटरी का उपयोग नहीं किया जाता है।<ref>{{cite book | author = Doron Aurbach | title = गैर-जलीय इलेक्ट्रोकैमिस्ट्री| publisher = CRC Press | year = 1999 | isbn = 978-0824773342}}</ref> | ||
Revision as of 13:38, 2 July 2023
|
| |||

| |||
| Names | |||
|---|---|---|---|
| Preferred IUPAC name
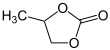
4-मिथाइल-1,3-डाइऑक्सोलन-2-एक | |||
| Other names
(RS)-4-Methyl-1,3-dioxolan-2-one
Cyclic propylene carbonate Carbonic acid propylene ester Cyclic 1,2-propylene carbonate Propylene glycol cyclic carbonate 1,2-Propanediol carbonate 4-Methyl-2-oxo-1,3-dioxolane Arconate 5000 Texacar PC | |||
| Identifiers | |||
3D model (JSmol)
|
|||
| ChemSpider | |||
PubChem CID
|
|||
| UNII | |||
| |||
| |||
| Properties | |||
| C4H6O3 | |||
| Molar mass | 102.089 g·mol−1 | ||
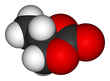
| Appearance | Colorless liquid | ||
| Density | 1.205 g/cm3 | ||
| Melting point | −48.8 °C (−55.8 °F; 224.3 K) | ||
| Boiling point | 242 °C (468 °F; 515 K) | ||
| Very soluble (240 g/L at 20°C) | |||
Refractive index (nD)
|
1.4189 | ||
| Structure | |||
| 4.9 D | |||
| Hazards | |||
| Occupational safety and health (OHS/OSH): | |||
Main hazards
|
Irritant | ||
| GHS labelling:[3] | |||

| |||
| Warning | |||
| H319 | |||
| P305+P351+P338 | |||
| NFPA 704 (fire diamond) | |||
| Flash point | 132 °C (270 °F; 405 K) | ||
| 455 °C (851 °F; 728 K) | |||
| Safety data sheet (SDS) | MSDS by Mallinckrodt Baker | ||
Except where otherwise noted, data are given for materials in their standard state (at 25 °C [77 °F], 100 kPa).
| |||
प्रोपलीन कार्बोनेट (सदैव संक्षिप्त PC) कार्बनिक यौगिक माने जाते है जिसका सूत्र C4H6O3 है। यह प्रोपलीन ग्लाइकोल से प्राप्त चक्रीय कार्बोनेट एस्टर होते है।[4] यह रंगहीन और गंधहीन तरल रासायनिक ध्रुवीयता, एप्रोटिक विलायक के रूप में उपयोगी की जाती है।[5] और प्रोपलीन कार्बोनेट चिरलिटी (रसायन विज्ञान) है, किंतु अधिकांश संदर्भों में रेसमिक मिश्रण के रूप में उपयोग किया जाता है।
तैयारी
चूंकि विषैली गैस , प्रोपलीन और एथिलीन कार्बोनेट का उपयोग करके कई कार्बनिक कार्बोनेट का उत्पादन किया जाता है,और अपवाद यह हैं। की वे मुख्य रूप से एपॉक्साइड के कार्बोनेशन द्वारा प्रस्तुत किए जाते हैं[5](एपोक्सीप्रोपेन, या प्रोपलीन ऑक्साइड यहाँ):
- CH3CHCH2O + CO2 → CH3C2H3O2CO
इस प्रकार से यह प्रक्रिया विशेष रूप से आकर्षक मानी जाती है क्योंकि इन एपॉक्साइड्स के उत्पादन में कार्बन डाइऑक्साइड की अधिक खपत होती है। इस प्रकार यह प्रतिक्रिया हरित प्रक्रिया का सही उदाहरण माना जाता है। और फॉस्जीन के साथ 1,2-प्रोपेनेडियोल की संबंधित प्रतिक्रिया जटिल होती है, न केवल प्रोपीलीन कार्बोनेट किंतु ओलिगोमेरिक उत्पाद भी उत्पन्न कर सकती है।
किंतु प्रोपलीन कार्बोनेट को जिंक एसीटेट के ऊपर यूरिया और प्रोपलीन ग्लाइकोल से भी संश्लेषित किया जा सकता है।[6]
अनुप्रयोग
विलायक के रूप में
इसके अतिरिक्त प्रोपलीन कार्बोनेट का उपयोग ध्रुवीय, एप्रोटिक विलायक के रूप में किया जाता है।[7] इसमें उच्च आणविक द्विध्रुवीय क्षण (4.9 डेबी) पाए जाते है, जोकी एसीटोन (2.91 डेबी) और एथिल एसीटेट (1.78 डेबी) की तुलना में अधिक होते है।[1] इस प्रकार से उदाहरण के लिए, पोटैशियम , सोडियम और अन्य क्षार धातुओं को उनके क्लोराइड के इलेक्ट्रोलीज़ द्वारा और प्रोपिलीन कार्बोनेट में भंग अन्य लवणों को प्राप्त करना संभव होता है।[8]
इलेक्ट्रोलाइट
इस प्रकार से इसमें 64 की उच्च सापेक्ष पारगम्यता (ढांकता हुआ स्थिरांक) के कारण, यह सदैव लिथियम बैटरी में इलेक्ट्रोलाइट्स के उच्च-पारगम्यता घटक के रूप में उपयोग किया जाता है,सामान्यतः कम-चिपचिपापन विलायक (जैसे डाईमेथोक्सीएथेन) के साथ उपयुक्त किया जाता है । इसकी उच्च ध्रुवीयता इसे लिथियम आयनों के चारों ओर प्रभावी सोलेसन शेल बनाने की अनुमति देती है, जिससे प्रवाहकीय इलेक्ट्रोलाइट बनता है। किंतु , इसका उपयोग लिथियम आयन बैटरी में नहीं किया जाता है। ग्रेफाइट इंटरकलेशन कंपाउंड पर इसके विनाशकारी प्रभाव के कारण लिथियम-आयन बैटरी का उपयोग नहीं किया जाता है।[9]
प्रोपलीन कार्बोनेट कुछ चिपकने वाले, रंग खाल उधेड़नेवाला और सौंदर्य प्रसाधनों में भी पाया जा सकता है।[10] इसका उपयोग प्लास्टाइज़र के रूप में भी किया जाता है। प्रोपलीन कार्बोनेट का उपयोग प्राकृतिक गैस और संश्लेषण गैस से CO2 को हटाने के लिए विलायक के रूप में भी किया जाता है जहां H2S भी उपस्तिथ नहीं होते है यह उपयोग 1950 के दशक में ईएल पासो नेचुरल गैस कंपनी और फ्लोर कॉर्पोरेशन द्वारा पश्चिम टेक्सास में टेरेल काउंटी गैस प्लांट में उपयोग के लिए विकसित किया गया था, जो अब ऑक्सिडेंटल पेट्रोलियम के स्वामित्व में है। जो अब ऑक्सिडेंटल पेट्रोलियम के स्वामित्व में है।[11]
अन्य
प्रोपलीन कार्बोनेट उत्पाद को ट्रान्सएस्टरीफिकेशन द्वारा अन्य कार्बोनेट एस्टर में भी परिवर्तित किया जा सकता है (कार्बोनेट एस्टर#कार्बोनेट ट्रांसएस्टरीफिकेशन देखें)।[5]
इस प्रकार से इलेक्ट्रोस्प्रे आयनीकरण मास स्पेक्ट्रोमेट्री में, प्रोपलीन कार्बोनेट को विश्लेषण चार्ज बढ़ाने के लिए कम सतह तनाव समाधान में डोप किया जाता है।[12]
और ग्रिग्नार्ड अभिक्रिया में प्रोपलीन कार्बोनेट (या अधिकांश अन्य कार्बोनेट एस्टर) का उपयोग तृतीयक अल्कोहल बनाने के लिए किया जा सकता है।[13]
सुरक्षा
नैदानिक अध्ययनों से संकेत मिलता है कि कॉस्मेटिक तैयारियों में उपयोग किए जाने पर प्रोपलीन कार्बोनेट त्वचा में जलन या संवेदीकरण का कारण नहीं बनता है, जबकि बिना मिलाए उपयोग किए जाने पर मध्यम त्वचा की जलन देखी जाती है। वाष्प के संपर्क में आने वाले या बिना तरल तरल के संपर्क में आने वाले चूहों में कोई महत्वपूर्ण जहरीला प्रभाव नहीं देखा गया था ।[14] इस प्रकार से अमेरिका में, प्रोपलीन कार्बोनेट को वाष्पशील कार्बनिक यौगिक (वीओसी) के रूप में विनियमित नहीं किया जाता है क्योंकि यह धुंध के गठन में महत्वपूर्ण योगदान नहीं देता है और क्योंकि इसकी वाष्प कैंसर या अन्य जहरीले प्रभाव पैदा करने के लिए ज्ञात या संदिग्ध नहीं होते है।[15]
यह भी देखें
संदर्भ
- ↑ 1.0 1.1 Haynes, William M., ed. (2011). CRC Handbook of Chemistry and Physics (92nd ed.). Boca Raton, FL: CRC Press. ISBN 1-4398-5511-0.
- ↑ Propylene carbonate at Sigma-Aldrich.
- ↑ GHS: GESTIS 070730
- ↑ WebBook page for propylene carbonate.
- ↑ 5.0 5.1 5.2 Hans-Josef Buysch. "Carbonic Esters". Ullmann's Encyclopedia of Industrial Chemistry. Weinheim: Wiley-VCH. doi:10.1002/14356007.a05_197..
- ↑ Synthesis of propylene carbonate from urea http://pubs.acs.org/doi/abs/10.1021/ie049948i
- ↑ Dieter Stoye. "Solvents". Ullmann's Encyclopedia of Industrial Chemistry. Weinheim: Wiley-VCH. doi:10.1002/14356007.a24_437..
- ↑ J. Jorné; C. W. Tobias (1975). "प्रोपलीन कार्बोनेट से क्षार धातुओं का इलेक्ट्रोडोडिशन". J. Appl. Electrochem. 5 (4): 279–290. doi:10.1007/BF00608791. S2CID 93629501.
- ↑ Doron Aurbach (1999). गैर-जलीय इलेक्ट्रोकैमिस्ट्री. CRC Press. ISBN 978-0824773342.
- ↑ प्रोपलीन कार्बोनेट in the Consumer Product Information Database.
- ↑ Schendel, R. "फ्लोर सॉल्वेंट और सेलेक्सोल प्रक्रियाओं की तुलना" (PDF). Retrieved 4 April 2016.
- ↑ Teo C. A., Donald W. A. (May 2014). "इलेक्ट्रोस्प्रे आयनीकरण द्रव्यमान स्पेक्ट्रोमेट्री में सैद्धांतिक अधिकतम प्रोटॉन-स्थानांतरण सीमा से परे सुपरचार्जिंग प्रोटीन के लिए समाधान योजक". Anal. Chem. 86 (9): 4455–62. doi:10.1021/ac500304r. PMID 24712886.
- ↑ Payne, Richard; Theodorou, Ignatius E. (September 1972). "ढांकता हुआ गुण और एथिलीन कार्बोनेट और प्रोपलीन कार्बोनेट में छूट". The Journal of Physical Chemistry. 76 (20): 2892–2900. doi:10.1021/j100664a019. ISSN 0022-3654.
- ↑ "प्रोपलीन कार्बोनेट के लिए पर्यावरण प्रोफ़ाइल". U.S. Environmental Protection Agency. 1998.
- ↑ Johnson, William L. "वाष्पशील कार्बनिक यौगिकों की परिभाषा में संशोधन - प्रोपलीन कार्बोनेट और डाइमिथाइल कार्बोनेट का बहिष्करण". US Environmental Protection Agency. US EPA. Retrieved 11 July 2015.