लोअर सल्फर ऑक्साइड: Difference between revisions
m (10 revisions imported from alpha:लोअर_सल्फर_ऑक्साइड) |
No edit summary |
||
| (One intermediate revision by one other user not shown) | |||
| Line 1: | Line 1: | ||
[[Image:Disulfur-monoxide-2D-dimensions.png|thumb|right|150px|एस की संरचना<sub>2</sub>हे]] | [[Image:Disulfur-monoxide-2D-dimensions.png|thumb|right|150px|एस की संरचना<sub>2</sub>हे]] | ||
[[Image:Disulfur-monoxide-3D-vdW-A.png|thumb|right|150px|S<sub>2</sub> का [[ जगह भरने वाला मॉडल | स्थान भरने वाला मॉडल]] हे]] | [[Image:Disulfur-monoxide-3D-vdW-A.png|thumb|right|150px|S<sub>2</sub> का [[ जगह भरने वाला मॉडल | स्थान भरने वाला मॉडल]] हे]]'''लोअर सल्फर ऑक्साइड''' सूत्र S<sub>m</sub>O<sub>n</sub> के साथ अकार्बनिक यौगिकों का समूह है, जहां 2m > n हैं। ये प्रजातियां प्रायः अस्थिर होती हैं और इस प्रकार रोजमर्रा के जीवन में संभवता ही कभी इसका सामना करना पड़ता है। वे मौलिक सल्फर के दहन में महत्वपूर्ण मध्यवर्ती हैं।<ref name = "Greenwood">{{Greenwood&Earnshaw}}</ref> कुछ उचित प्रकारो से चित्रित उदाहरणों में सम्मिलित है, सल्फर मोनोऑक्साइड (SO), इसका डिमर S<sub>2</sub>O<sub>2</sub> और चक्रीय सल्फर ऑक्साइड की श्रृंखला, S<sub>n</sub>O<sub>x</sub> (x = 1, 2), चक्रीय S<sub>n</sub> छल्लों पर आधारित है। | ||
स्थलीय वायुमंडलीय सल्फर प्रदूषण को समझने की आवश्यकता और | स्थलीय वायुमंडलीय सल्फर प्रदूषण को समझने की आवश्यकता और बृहस्पति के चंद्रमाओं में से, आयो (चंद्रमा), और [[शुक्र]] के बाह्य-स्थलीय वातावरण में सल्फर ऑक्साइड की महत्वपूर्ण मात्रा होने की शोध के कारण लोअर सल्फर ऑक्साइड में रुचि बढ़ी है। प्रारंभिक कार्यकर्ताओं द्वारा रिपोर्ट किए गए कुछ यौगिक जैसे कि ब्लू सेसक्विओक्साइड, S<sub>2</sub>O<sub>3</sub> तरल SO<sub>3</sub> में सल्फर को मिश्रण से बनता है, जो S<sub>4</sub><sup>2+</sup> और S<sub>8</sub><sup>2+</sup> आयनों के पॉलीसल्फेट लवणों का मिश्रण प्रतीत होता है।<ref name = "Greenwood"/> | ||
==सल्फर मोनोऑक्साइड, डाइसल्फ़र डाइऑक्साइड, डाइसल्फ़र मोनोऑक्साइड== | ==सल्फर मोनोऑक्साइड, डाइसल्फ़र डाइऑक्साइड, डाइसल्फ़र मोनोऑक्साइड== | ||
इन प्रजातियों की गैस अवस्था में उत्तम रूप से विशेषता है, किन्तु उन्हें ठोस या तरल के रूप में भिन्न नहीं किया जा सकता है। इसके अतिरिक्त, संघनित होने पर, वे डिमराइज़ेशन और ओलिगोमेराइज़ेशन से प्रवाहित होते हैं, सामान्यतः सल्फर डाइऑक्साइड और मौलिक सल्फर उत्पन्न करते हैं। कुछ मिलीबार दाब पर, सापेक्ष स्थिरता S<sub>2</sub>O > S<sub>2</sub>O<sub>2</sub> > SO होती हैं।<ref name=Steudel/> सल्फर मोनोऑक्साइड (SO) और इसका डिमर (S<sub>2</sub>O<sub>2</sub>) कम तापमान पर फंस गए हैं। | इन प्रजातियों की गैस अवस्था में उत्तम रूप से विशेषता है, किन्तु उन्हें ठोस या तरल के रूप में भिन्न नहीं किया जा सकता है। इसके अतिरिक्त, संघनित होने पर, वे डिमराइज़ेशन और ओलिगोमेराइज़ेशन से प्रवाहित होते हैं, सामान्यतः सल्फर डाइऑक्साइड और मौलिक सल्फर उत्पन्न करते हैं। कुछ मिलीबार दाब पर, सापेक्ष स्थिरता S<sub>2</sub>O > S<sub>2</sub>O<sub>2</sub> > SO होती हैं।<ref name=Steudel/> सल्फर मोनोऑक्साइड (SO) और इसका डिमर (S<sub>2</sub>O<sub>2</sub>) कम तापमान पर फंस गए हैं। डिसल्फर डाइऑक्साइड (S<sub>2</sub>O<sub>2</sub>) सल्फर मोनोऑक्साइड का डिमर है। इसमें C<sub>2v</sub> संरचना (प्लानर) है। | ||
[[डाइसल्फ़ाइड मोनोऑक्साइड]] (S<sub>2</sub>O) [[सल्फर डाइऑक्साइड]] का एनालॉग है। SO<sub>2</sub> के साथ-साथ [[ओजोन]] (O<sub>3</sub>), और [[ट्राइसल्फर]] (S<sub>3</sub>), के जैसे, यह मुड़ी हुई संरचना को ता है। S-S बॉन्ड की लंबाई 188.4 pm है, SO बॉन्ड की लंबाई 146.5 pm है और SSO का कोण 117.88° है। दो द्विध्रुवीय क्षण घटक μa = 0.875 D और μb = 1.18 D हैं।<ref>{{cite journal | [[डाइसल्फ़ाइड मोनोऑक्साइड]] (S<sub>2</sub>O) [[सल्फर डाइऑक्साइड]] का एनालॉग है। SO<sub>2</sub> के साथ-साथ [[ओजोन]] (O<sub>3</sub>), और [[ट्राइसल्फर]] (S<sub>3</sub>), के जैसे, यह मुड़ी हुई संरचना को ता है। S-S बॉन्ड की लंबाई 188.4 pm है, SO बॉन्ड की लंबाई 146.5 pm है और SSO का कोण 117.88° है। दो द्विध्रुवीय क्षण घटक μa = 0.875 D और μb = 1.18 D हैं।<ref>{{cite journal | ||
| Line 45: | Line 45: | ||
==संदर्भ== | ==संदर्भ== | ||
{{reflist}} | {{reflist}} | ||
[[Category:Created On 12/05/2023]] | [[Category:Created On 12/05/2023]] | ||
[[Category:Vigyan Ready]] | [[Category:Machine Translated Page]] | ||
[[Category:Pages with script errors]] | |||
[[Category:Templates Vigyan Ready]] | |||
[[Category:इंटरचेल्कोजेन्स]] | |||
[[Category:सल्फर ऑक्साइड]] | |||
Latest revision as of 16:33, 30 October 2023
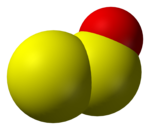
लोअर सल्फर ऑक्साइड सूत्र SmOn के साथ अकार्बनिक यौगिकों का समूह है, जहां 2m > n हैं। ये प्रजातियां प्रायः अस्थिर होती हैं और इस प्रकार रोजमर्रा के जीवन में संभवता ही कभी इसका सामना करना पड़ता है। वे मौलिक सल्फर के दहन में महत्वपूर्ण मध्यवर्ती हैं।[1] कुछ उचित प्रकारो से चित्रित उदाहरणों में सम्मिलित है, सल्फर मोनोऑक्साइड (SO), इसका डिमर S2O2 और चक्रीय सल्फर ऑक्साइड की श्रृंखला, SnOx (x = 1, 2), चक्रीय Sn छल्लों पर आधारित है।
स्थलीय वायुमंडलीय सल्फर प्रदूषण को समझने की आवश्यकता और बृहस्पति के चंद्रमाओं में से, आयो (चंद्रमा), और शुक्र के बाह्य-स्थलीय वातावरण में सल्फर ऑक्साइड की महत्वपूर्ण मात्रा होने की शोध के कारण लोअर सल्फर ऑक्साइड में रुचि बढ़ी है। प्रारंभिक कार्यकर्ताओं द्वारा रिपोर्ट किए गए कुछ यौगिक जैसे कि ब्लू सेसक्विओक्साइड, S2O3 तरल SO3 में सल्फर को मिश्रण से बनता है, जो S42+ और S82+ आयनों के पॉलीसल्फेट लवणों का मिश्रण प्रतीत होता है।[1]
सल्फर मोनोऑक्साइड, डाइसल्फ़र डाइऑक्साइड, डाइसल्फ़र मोनोऑक्साइड
इन प्रजातियों की गैस अवस्था में उत्तम रूप से विशेषता है, किन्तु उन्हें ठोस या तरल के रूप में भिन्न नहीं किया जा सकता है। इसके अतिरिक्त, संघनित होने पर, वे डिमराइज़ेशन और ओलिगोमेराइज़ेशन से प्रवाहित होते हैं, सामान्यतः सल्फर डाइऑक्साइड और मौलिक सल्फर उत्पन्न करते हैं। कुछ मिलीबार दाब पर, सापेक्ष स्थिरता S2O > S2O2 > SO होती हैं।[2] सल्फर मोनोऑक्साइड (SO) और इसका डिमर (S2O2) कम तापमान पर फंस गए हैं। डिसल्फर डाइऑक्साइड (S2O2) सल्फर मोनोऑक्साइड का डिमर है। इसमें C2v संरचना (प्लानर) है।
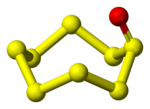
डाइसल्फ़ाइड मोनोऑक्साइड (S2O) सल्फर डाइऑक्साइड का एनालॉग है। SO2 के साथ-साथ ओजोन (O3), और ट्राइसल्फर (S3), के जैसे, यह मुड़ी हुई संरचना को ता है। S-S बॉन्ड की लंबाई 188.4 pm है, SO बॉन्ड की लंबाई 146.5 pm है और SSO का कोण 117.88° है। दो द्विध्रुवीय क्षण घटक μa = 0.875 D और μb = 1.18 D हैं।[3] यह प्रजाति अपघटित होकर पॉलीमेरिक सल्फर ऑक्साइड (पीएसओ) देती है, जिसका अनुमानित सूत्र [S3O]n होता है। पीएसओ कक्ष के तापमान पर मौलिक सल्फर और SO2 में विघटित हो जाता है। आईओ के रंग के लिए पीएसओ को बताया गया है।[4]ट्राइसल्फर मोनोऑक्साइड, S3O अस्थिर अणु है। निराकरण-पुन: आयनीकरण मास स्पेक्ट्रोमेट्री का उपयोग करके गैस चरण में इसकी जानकारी ज्ञात की गयी है। चक्रीय और शृंखला दोनों प्रकार की संरचनाएँ पाई गईं है।[5]
चक्रीय SnOx (x = 1, 2)
बड़ी संख्या में मोनोऑक्साइड SnO ज्ञात हैं जहां n = 5-10 ऑक्सीजन परमाणु बहिर्चक्रीय है।[2] वे होमोसायकल्स को ट्राइफ्लोरोपरोक्सीएसेटिक एसिड के साथ ऑक्सीकरण करके प्रस्तुत किए जा सकते हैं।[1]
- Sn + CF3C(O)OOH → SnO + CF3C(O)OH
यौगिक पीले या नारंगी रंग के होते हैं और कक्ष के तापमान के पास ऊष्मीय रूप से अस्थिर होते हैं।[1]
| सूत्र | रंग (25° C) | m.p. (°C)[2] |
|---|---|---|
| S6O | पीला | 39 |
| S7O | नारंगी | 55 |
| S7O2 | तीव्र नारंगी | 60–62 (विघटन) |
| S8O | नारंगी | 78 (अपघटन) |
| S9O | तीव्र पीला | 32-34 |
| S10O | नारंगी | 51 (विघटित) |
डाइऑक्साइड उचित रूप से विशेषता है: गहरा नारंगी S7O2 (एमपी 60–62 °C अपघटन के साथ), जो ट्राइफ्लोरोपरोक्सोएसेटिक एसिड का उपयोग करके उत्पन्न होता है।[1]
संदर्भ
- ↑ 1.0 1.1 1.2 1.3 1.4 Greenwood, Norman N.; Earnshaw, Alan (1997). Chemistry of the Elements (2nd ed.). Butterworth-Heinemann. ISBN 978-0-08-037941-8.
- ↑ 2.0 2.1 2.2 R. Steudel (2003). "Sulfur-Rich Oxides SnO and SnO2". In Steudel, R. (ed.). एलिमेंटल सल्फर और सल्फर-समृद्ध यौगिक II. Berlin-Heidelberg: Springer. doi:10.1007/b13185. ISBN 9783540449515.
- ↑ Meschi, D.J.; Myers R.J. (1959). "डाइसल्फर मोनोऑक्साइड का माइक्रोवेव स्पेक्ट्रम, संरचना और द्विध्रुवीय क्षण". Journal of Molecular Spectroscopy. 3 (1–6): 405–416. Bibcode:1959JMoSp...3..405M. doi:10.1016/0022-2852(59)90036-0.
- ↑ Baklouti D., D; Schmitt, B.; Brissaud, O. (November 2004). "आयो की सतह पर कम सल्फर ऑक्साइड का इन्फ्रारेड अध्ययन". Bulletin of the American Astronomical Society. 36: 1099. Bibcode:2004DPS....36.1607B.
- ↑ de Petris, G; Rosi M Troiani A (2006). "S3O and S3O+ in the gas phase: ring and open-chain structures". Chemical Communications (42): 4416–4418. doi:10.1039/b609646h. PMID 17057862.