मर्करी(I) क्लोराइड: Difference between revisions
m (Sugatha moved page मरकरी (आई) क्लोराइड to मर्करी(I) क्लोराइड) |
No edit summary |
||
| Line 68: | Line 68: | ||
}} | }} | ||
''' | '''मर्करी(I) क्लोराइड''' Hg<sub>2</sub>Cl<sub>2</sub> सूत्र वाला एक [[रासायनिक यौगिक]] है। इसे [[खनिज]] कैलौमेल (एक दुर्लभ खनिज) या मरक्यूरस क्लोराइड के नाम से भी जाना जाता है, <ref name=EB>{{cite EB1911|wstitle=Calomel}}</ref> यह घना सफेद या पीला-सफेद, गंधहीन ठोस [[पारा (तत्व)|मर्करी (तत्व)]](I) यौगिक का प्रमुख उदाहरण है। यह [[इलेक्ट्रोकैमिस्ट्री]] में संदर्भ विद्युतग्र का एक घटक है। <ref>{{Housecroft2nd|pages=696–697}}</ref><ref>{{cite book |last1=Skoog |first1=Douglas A. |first2=F. James |last2=Holler |first3=Timothy A. |last3=Nieman | title = वाद्य विश्लेषण के सिद्धांत| edition = 5th | publisher = Saunders College Pub. | year = 1998 | pages = 253–271 | isbn = 978-0-03-002078-0}}</ref> | ||
==इतिहास== | ==इतिहास== | ||
माना जाता है कि कैलोमेल नाम ग्रीक καλός "सुंदर", और μέλας "काला" से आया है; या καλός और μέλι "शहद" इसके मीठे स्वाद से आया है। <ref name=EB/> काला नाम (एक सफेद यौगिक के लिए कुछ हद तक आश्चर्यजनक) संभवतः [[अमोनिया]] के साथ इसकी विशिष्ट असंगति प्रतिक्रिया के कारण है, जो सूक्षमतापूर्वक बिखरे हुए धात्विक | माना जाता है कि कैलोमेल नाम ग्रीक καλός "सुंदर", और μέλας "काला" से आया है; या καλός और μέλι "शहद" इसके मीठे स्वाद से आया है। <ref name=EB/> काला नाम (एक सफेद यौगिक के लिए कुछ हद तक आश्चर्यजनक) संभवतः [[अमोनिया]] के साथ इसकी विशिष्ट असंगति प्रतिक्रिया के कारण है, जो सूक्षमतापूर्वक बिखरे हुए धात्विक मर्करी (तत्व) के कारण एक प्रभावशाली काला रंग देता है। इसे खनिज हार्न क्विकसिल्वर या हार्न मर्करी भी कहा जाता है। <ref name=EB/> | ||
कैलोमेल को आंतरिक रूप से लिया गया और रेचक के रूप में उपयोग किया गया, <ref name=EB/> उदाहरण के लिए, 1801 में जॉर्ज III के उपचार के लिए, और कीटाणुनाशक, साथ ही 20वीं सदी की प्रारम्भ तक सिफलिस के उपचार में उपयोग किया गया। अभी हाल तक, इसका उपयोग बागवानी कवकनाशी के रूप में भी किया जाता था, विशेष रूप से [[ब्रैसिसेकी]] समूह की फसलों के बीच [[क्लबरूट]] की घटना को रोकने में सहायता करने के लिए रूट डिप के रूप में उपयोग किया जाता था। <ref>Buczacki, S., ''Pests, Diseases and Disorders of Garden Plants'', Collins, 1998, pp 449-50. {{ISBN|0-00-220063-5}}</ref> | कैलोमेल को आंतरिक रूप से लिया गया और रेचक के रूप में उपयोग किया गया, <ref name=EB/> उदाहरण के लिए, 1801 में जॉर्ज III के उपचार के लिए, और कीटाणुनाशक, साथ ही 20वीं सदी की प्रारम्भ तक सिफलिस के उपचार में उपयोग किया गया। अभी हाल तक, इसका उपयोग बागवानी कवकनाशी के रूप में भी किया जाता था, विशेष रूप से [[ब्रैसिसेकी]] समूह की फसलों के बीच [[क्लबरूट]] की घटना को रोकने में सहायता करने के लिए रूट डिप के रूप में उपयोग किया जाता था। <ref>Buczacki, S., ''Pests, Diseases and Disorders of Garden Plants'', Collins, 1998, pp 449-50. {{ISBN|0-00-220063-5}}</ref> | ||
[[वीर चिकित्सा|द्विपदी चिकित्सा]] के युग में | [[वीर चिकित्सा|द्विपदी चिकित्सा]] के युग में मर्करी विभिन्न प्रकार की शारीरिक और मानसिक बीमारियों के लिए एक लोकप्रिय उपचार बन गया। इसे 18वीं सदी में और क्रांति के उपरान्त अमेरिका में डॉक्टरों द्वारा मरीजों को वमन कराने और उनके शरीर को अशुद्धियों से मुक्त करने के लिए निर्धारित किया गया था। [[बेंजामिन रश]] चिकित्सा में पारे के जाने-माने समर्थक थे और उन्होंने 1793 में [[ फ़िलाडेल्फ़िया |फ़िलाडेल्फ़िया]] में पीत ज्वर के प्रकोप के उपरान्त पीड़ितों के उपचार के लिए कैलोमेल का इस्तेमाल किया था। कैलोमेल को रोगियों को [[रेचक]] या रेचक के रूप में तब तक दिया जाता था जब तक कि उनमें लार आना प्रारम्भ न हो जाए और प्रायः रोगियों को यह दवा दी जाती थी। इतनी भारी मात्रा में कि उनके बाल और दाँत गिर गये। <ref> | ||
{{cite journal | {{cite journal | ||
| title = Heavy Metal Medicine | | title = Heavy Metal Medicine | ||
| Line 94: | Line 94: | ||
==गुण== | ==गुण== | ||
एम-एम आबंध को इतनी आसानी से बनाने की क्षमता के कारण | एम-एम आबंध को इतनी आसानी से बनाने की क्षमता के कारण मर्करी समूह 12 धातुओं में अद्वितीय है। Hg<sub>2</sub>Cl<sub>2</sub> एक रैखिक अणु है। खनिज कैलोमेल अंतरिक्ष समूह I4/m 2/m 2/m के साथ [[ चौकोर | द्विसमलंबाक्ष]] प्रणाली में क्रिस्टलीकृत होता है। क्रिस्टल संरचना की इकाई कोशिका नीचे दिखाई गई है: | ||
{| class="wikitable" style="margin:1em auto; text-align:center;" | {| class="wikitable" style="margin:1em auto; text-align:center;" | ||
| Line 101: | Line 101: | ||
| इकाई कोशिका||Hg का विकृत अष्टफलकीय समन्वय | | इकाई कोशिका||Hg का विकृत अष्टफलकीय समन्वय | ||
|} | |} | ||
Hg-Hg आबंध की लंबाई 253 pm (धातु में Hg-Hg 300 pm है) और रैखिक Hg में Hg-Cl आबंध की Hg<sub>2</sub>Cl<sub>2</sub> इकाई 243 अपराह्न है। <ref name = "Wells">Wells A.F. (1984) ''Structural Inorganic Chemistry'' 5th edition Oxford Science Publications {{ISBN|0-19-855370-6}}</ref> प्रत्येक Hg परमाणु का समग्र समन्वय अष्टफलकीय है, क्योंकि दोपहर 321 बजे दो निकटतम प्रतिवैस के अतिरिक्त, चार अन्य सीएल परमाणु होते हैं। लंबे समय तक [[पारा पॉलीकेशन| | Hg-Hg आबंध की लंबाई 253 pm (धातु में Hg-Hg 300 pm है) और रैखिक Hg में Hg-Cl आबंध की Hg<sub>2</sub>Cl<sub>2</sub> इकाई 243 अपराह्न है। <ref name = "Wells">Wells A.F. (1984) ''Structural Inorganic Chemistry'' 5th edition Oxford Science Publications {{ISBN|0-19-855370-6}}</ref> प्रत्येक Hg परमाणु का समग्र समन्वय अष्टफलकीय है, क्योंकि दोपहर 321 बजे दो निकटतम प्रतिवैस के अतिरिक्त, चार अन्य सीएल परमाणु होते हैं। लंबे समय तक [[पारा पॉलीकेशन|मर्करी पॉलीकेशन]] उपस्थित रहते हैं। | ||
==विरचन और प्रतिक्रिया== | ==विरचन और प्रतिक्रिया== | ||
मौलिक | मौलिक मर्करी और मरक्यूरिक क्लोराइड की प्रतिक्रिया से मर्क्यूरस क्लोराइड बनता है: | ||
:Hg + HgCl<sub>2</sub> → Hg<sub>2</sub>Cl<sub>2</sub> | :Hg + HgCl<sub>2</sub> → Hg<sub>2</sub>Cl<sub>2</sub> | ||
इसे NaCl या HCl सहित विभिन्न क्लोराइड स्रोतों का उपयोग करके जलीय | इसे NaCl या HCl सहित विभिन्न क्लोराइड स्रोतों का उपयोग करके जलीय मर्करी (I) नाइट्रेट से युक्त [[नमक मेटाथिसिस प्रतिक्रिया]] के माध्यम से तैयार किया जा सकता है। | ||
:2 HCl + Hg<sub>2</sub>(NO<sub>3</sub>)<sub>2</sub> → Hg<sub>2</sub>Cl<sub>2</sub> + 2 HNO<sub>3</sub> | :2 HCl + Hg<sub>2</sub>(NO<sub>3</sub>)<sub>2</sub> → Hg<sub>2</sub>Cl<sub>2</sub> + 2 HNO<sub>3</sub> | ||
अमोनिया के कारण Hg<sub>2</sub>Cl<sub>2</sub> अनुपातहीन हो जाता है: | अमोनिया के कारण Hg<sub>2</sub>Cl<sub>2</sub> अनुपातहीन हो जाता है: | ||
| Line 114: | Line 114: | ||
{{main|संतृप्त कैलोमेल विद्युदग्र}} | {{main|संतृप्त कैलोमेल विद्युदग्र}} | ||
इसके ऑक्सीकरण और कमी प्रतिक्रियाओं की आसानी का लाभ उठाते हुए, मर्क्यूरस क्लोराइड को इलेक्ट्रोकैमिस्ट्री में बड़े मापक्रम पर नियोजित किया जाता है। कैलोमेल विद्युतग्र एक संदर्भ विशेष रूप से पुराने प्रकाशनों में विद्युतग्र है। पिछले 50 वर्षों में, इसका स्थान सिल्वर/सिल्वर क्लोराइड (Ag/AgCl) विद्युतग्र ने ले लिया है। हालाँकि | इसके ऑक्सीकरण और कमी प्रतिक्रियाओं की आसानी का लाभ उठाते हुए, मर्क्यूरस क्लोराइड को इलेक्ट्रोकैमिस्ट्री में बड़े मापक्रम पर नियोजित किया जाता है। कैलोमेल विद्युतग्र एक संदर्भ विशेष रूप से पुराने प्रकाशनों में विद्युतग्र है। पिछले 50 वर्षों में, इसका स्थान सिल्वर/सिल्वर क्लोराइड (Ag/AgCl) विद्युतग्र ने ले लिया है। हालाँकि मर्करी (तत्व) की हानिकारक प्रकृति के कारण मर्करी विद्युतग्र को व्यापक रूप से छोड़ दिया गया है, कई रसायनज्ञों का मानना है कि वे अभी भी अधिक सटीक हैं और तब तक हानिकारक नहीं हैं जब तक उन्हें ठीक से संभाला जाता है। प्रयोगात्मक क्षमताओं में अंतर साहित्य मूल्यों से बहुत कम भिन्न होता है। अन्य विद्युतग्र 70 से 100 मिलीवोल्ट तक भिन्न हो सकते हैं। | ||
===प्रकाशरसायन=== | ===प्रकाशरसायन=== | ||
पराबैंगनी प्रकाश के संपर्क में आने पर [[पारा (द्वितीय) क्लोराइड| | पराबैंगनी प्रकाश के संपर्क में आने पर [[पारा (द्वितीय) क्लोराइड|मर्करी (द्वितीय) क्लोराइड]] मर्करी (II) क्लोराइड और मौलिक मर्करी में विघटित हो जाता है। | ||
:Hg<sub>2</sub>Cl<sub>2</sub> → HgCl<sub>2</sub> + Hg | :Hg<sub>2</sub>Cl<sub>2</sub> → HgCl<sub>2</sub> + Hg | ||
एचजी के गठन का उपयोग [[एक्टिनोमीटर]] की तकनीक द्वारा प्रकाश किरण में फोटॉनों की संख्या की गणना करने के लिए किया जा सकता है। | एचजी के गठन का उपयोग [[एक्टिनोमीटर]] की तकनीक द्वारा प्रकाश किरण में फोटॉनों की संख्या की गणना करने के लिए किया जा सकता है। | ||
मर्करी (II) क्लोराइड और [[अमोनियम ऑक्सालेट]] की उपस्थिति में एक हल्की प्रतिक्रिया का उपयोग करके, मर्करी (I) क्लोराइड, [[अमोनियम क्लोराइड]] और [[ कार्बन डाईऑक्साइड |कार्बन डाईऑक्साइड]] का उत्पादन किया जाता है। | |||
:2 HgCl<sub>2</sub> + (NH<sub>4</sub>)<sub>2</sub>C<sub>2</sub>O<sub>4</sub> {{overset|Light|→}} Hg<sub>2</sub>Cl<sub>2(s)</sub> + 2 [{{chem|NH|4|+}}][Cl<sup>−</sup>] + 2 CO<sub>2</sub> | :2 HgCl<sub>2</sub> + (NH<sub>4</sub>)<sub>2</sub>C<sub>2</sub>O<sub>4</sub> {{overset|Light|→}} Hg<sub>2</sub>Cl<sub>2(s)</sub> + 2 [{{chem|NH|4|+}}][Cl<sup>−</sup>] + 2 CO<sub>2</sub> | ||
इस विशेष प्रतिक्रिया की खोज 1880 में जे. एम. एडर (इसलिए इसका नाम एडर प्रतिक्रिया) द्वारा की गई थी और 1929 में डब्ल्यू. ई. रोज़वेरे द्वारा इसकी पुनः जांच की गई। <ref>{{Cite journal |last=Roseveare |first=W. E. | title = पोटेशियम ऑक्सालेट और मर्क्यूरिक क्लोराइड के बीच एक्स-रे फोटोकैमिकल प्रतिक्रिया| journal = [[J. Am. Chem. Soc.]] | year = 1930 | volume = 52 | issue = 7 | pages = 2612–2619 | doi = 10.1021/ja01370a005}}</ref> | इस विशेष प्रतिक्रिया की खोज 1880 में जे. एम. एडर (इसलिए इसका नाम एडर प्रतिक्रिया) द्वारा की गई थी और 1929 में डब्ल्यू. ई. रोज़वेरे द्वारा इसकी पुनः जांच की गई। <ref>{{Cite journal |last=Roseveare |first=W. E. | title = पोटेशियम ऑक्सालेट और मर्क्यूरिक क्लोराइड के बीच एक्स-रे फोटोकैमिकल प्रतिक्रिया| journal = [[J. Am. Chem. Soc.]] | year = 1930 | volume = 52 | issue = 7 | pages = 2612–2619 | doi = 10.1021/ja01370a005}}</ref> | ||
==संबंधित | ==संबंधित मर्करी(I) यौगिक== | ||
[[मरकरी (आई) ब्रोमाइड]], Hg<sub>2</sub>Br<sub>2</sub>, हल्का पीला है, जबकि [[पारा (आई) आयोडाइड| | [[मरकरी (आई) ब्रोमाइड|मर्करी (आई) ब्रोमाइड]], Hg<sub>2</sub>Br<sub>2</sub>, हल्का पीला है, जबकि [[पारा (आई) आयोडाइड|मर्करी (आई) आयोडाइड]], Hg<sub>2</sub>I<sub>2</sub>, हरे रंग का है। दोनों ही खराब घुलनशील हैं। शक्तिशाली अम्ल की अनुपस्थिति में मर्करी (I) फ्लोराइड अस्थिर होता है। | ||
==सुरक्षा संबंधी विचार== | ==सुरक्षा संबंधी विचार== | ||
{{main|पारा विषाक्तता}} | {{main|पारा विषाक्तता}} | ||
मर्क्यूरस क्लोराइड मर्करी विषाक्तता है, हालांकि पानी में इसकी कम घुलनशीलता के कारण यह सामान्यतः अपने [[मरक्यूरिक क्लोराइड]] समकक्ष से कम हानिकारक है। 1700 के दशक के अंत से 1860 के दशक तक [[संयुक्त राज्य अमेरिका]] में इसका उपयोग चिकित्सा में मूत्रवर्धक और रेचक (रेचक) के रूप में किया जाता था। 1954 तक ब्रिटेन में प्रारम्भी पाउडर में कैलोमेल भी एक सामान्य घटक था, जिससे [[एक्रोडिनिया]] के रूप में व्यापक [[पारा विषाक्तता| | मर्क्यूरस क्लोराइड मर्करी विषाक्तता है, हालांकि पानी में इसकी कम घुलनशीलता के कारण यह सामान्यतः अपने [[मरक्यूरिक क्लोराइड]] समकक्ष से कम हानिकारक है। 1700 के दशक के अंत से 1860 के दशक तक [[संयुक्त राज्य अमेरिका]] में इसका उपयोग चिकित्सा में मूत्रवर्धक और रेचक (रेचक) के रूप में किया जाता था। 1954 तक ब्रिटेन में प्रारम्भी पाउडर में कैलोमेल भी एक सामान्य घटक था, जिससे [[एक्रोडिनिया]] के रूप में व्यापक [[पारा विषाक्तता|मर्करी विषाक्तता]] हुई, जिसकी उस समय मृत्यु दर 10 में से 1 थी। <ref>{{cite book | first = Walter | last = Sneader | title = Drug Discovery: A History | url = https://books.google.com/books?id=mYQxRY9umjcC&pg=PA46 | pages = 45–46 | publisher = [[John Wiley and Sons]] | isbn = 978-0-471-89980-8 | year = 2005 | access-date = 2009-02-02}}</ref> बाद में जब यौगिक की विषाक्तता का पता चला तो इन औषधीय उपयोगों को बंद कर दिया गया। | ||
इसका उपयोग सौंदर्य प्रसाधनों में साबुन और त्वचा को गोरा करने वाले लेप के रूप में भी पाया गया है, लेकिन अब अमेरिका, कनाडा, जापान और यूरोपीय संघ सहित कई देशों में इन तैयारियों का निर्माण या आयात करना अवैध है। <ref>{{cite web |url=http://eur-lex.europa.eu/LexUriServ/LexUriServ.do?uri=CONSLEG:1976L0768:20080424:en:PDF |title=Commission Directive 86/199/EEC, OJ L 149, p. 38 of 3.6.1986}}</ref> इन तैयारियों के उत्पादन में सम्मिलित श्रमिकों के एक अध्ययन से पता चला है कि 2,3-डिमरकैप्टो-1-प्रोपेनसल्फोनिक एसिड (डीएमपीएस) का सोडियम नमक शरीर में | इसका उपयोग सौंदर्य प्रसाधनों में साबुन और त्वचा को गोरा करने वाले लेप के रूप में भी पाया गया है, लेकिन अब अमेरिका, कनाडा, जापान और यूरोपीय संघ सहित कई देशों में इन तैयारियों का निर्माण या आयात करना अवैध है। <ref>{{cite web |url=http://eur-lex.europa.eu/LexUriServ/LexUriServ.do?uri=CONSLEG:1976L0768:20080424:en:PDF |title=Commission Directive 86/199/EEC, OJ L 149, p. 38 of 3.6.1986}}</ref> इन तैयारियों के उत्पादन में सम्मिलित श्रमिकों के एक अध्ययन से पता चला है कि 2,3-डिमरकैप्टो-1-प्रोपेनसल्फोनिक एसिड (डीएमपीएस) का सोडियम नमक शरीर में मर्करी के बोझ को कम करने और मूत्र में मर्करी की सांद्रता को सामान्य स्तर तक कम करने में प्रभावी था। <ref>{{cite journal |author1=D. Gonzalez-Ramirez |author2=M. Zuniga-Charles |author3=A. Narro-Juarez |author4=Y. Molina-Recio |author5=K. M. Hurlbut |author6=R. C. Dart |author7=H. V. Aposhian | title = DMPS (2,3-Dimercaptopropane-1-sulfonate, Dimaval) Decreases the Body Burden of Mercury in Humans Exposed to Mercurous Chloride | date=1 October 1998| journal = The Journal of Pharmacology and Experimental Therapeutics| volume = 287 | issue = 1 | pages = 8–12 | url = http://jpet.aspetjournals.org/cgi/content/abstract/287/1/8 | format = free full text | pmid = 9765315 }}</ref> | ||
==संदर्भ== | ==संदर्भ== | ||
{{reflist}} | {{reflist}} | ||
Latest revision as of 12:32, 8 November 2023

| |
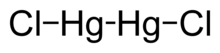
| |

| |
| Names | |
|---|---|
| IUPAC name
Dimercury dichloride
| |
| Other names | |
| Identifiers | |
3D model (JSmol)
|
|
| ChEBI | |
| ChemSpider | |
| EC Number |
|
| 25976 | |
PubChem CID
|
|
| RTECS number |
|
| UNII | |
| UN number | 3077 |
| |
| |
| Properties | |
| Hg2Cl2 | |
| Molar mass | 472.09 g/mol |
| Appearance | White solid |
| Density | 7.150 g/cm3 |
| Melting point | 383 °C (721 °F; 656 K) (sublimes) |
| 0.2 mg/100 mL | |
Solubility product (Ksp)
|
1.43×10−18[1] |
| Solubility | insoluble in ethanol, ether |
| −26.0·10−6 cm3/mol | |
Refractive index (nD)
|
1.973 |
| Structure | |
| tetragonal | |
| Thermochemistry | |
Std molar
entropy (S⦵298) |
196 J·mol−1·K−1[2] |
Std enthalpy of
formation (ΔfH⦵298) |
−265 kJ·mol−1[2] |
| Hazards | |
| GHS labelling: | |
 
| |
| Warning | |
| H302, H315, H319, H335, H410 | |
| P261, P264, P270, P271, P273, P280, P301+P312, P302+P352, P304+P340, P305+P351+P338, P312, P321, P330, P332+P313, P337+P313, P362, P391, P403+P233, P405, P501 | |
| NFPA 704 (fire diamond) | |
| Flash point | Non-flammable |
| Lethal dose or concentration (LD, LC): | |
LD50 (median dose)
|
210 mg/kg (rat, oral)[3] |
| Safety data sheet (SDS) | ICSC 0984 |
| Related compounds | |
Other anions
|
Mercury(I) fluoride Mercury(I) bromide Mercury(I) iodide |
Related compounds
|
Mercury(II) chloride |
Except where otherwise noted, data are given for materials in their standard state (at 25 °C [77 °F], 100 kPa).
| |
मर्करी(I) क्लोराइड Hg2Cl2 सूत्र वाला एक रासायनिक यौगिक है। इसे खनिज कैलौमेल (एक दुर्लभ खनिज) या मरक्यूरस क्लोराइड के नाम से भी जाना जाता है, [4] यह घना सफेद या पीला-सफेद, गंधहीन ठोस मर्करी (तत्व)(I) यौगिक का प्रमुख उदाहरण है। यह इलेक्ट्रोकैमिस्ट्री में संदर्भ विद्युतग्र का एक घटक है। [5][6]
इतिहास
माना जाता है कि कैलोमेल नाम ग्रीक καλός "सुंदर", और μέλας "काला" से आया है; या καλός और μέλι "शहद" इसके मीठे स्वाद से आया है। [4] काला नाम (एक सफेद यौगिक के लिए कुछ हद तक आश्चर्यजनक) संभवतः अमोनिया के साथ इसकी विशिष्ट असंगति प्रतिक्रिया के कारण है, जो सूक्षमतापूर्वक बिखरे हुए धात्विक मर्करी (तत्व) के कारण एक प्रभावशाली काला रंग देता है। इसे खनिज हार्न क्विकसिल्वर या हार्न मर्करी भी कहा जाता है। [4]
कैलोमेल को आंतरिक रूप से लिया गया और रेचक के रूप में उपयोग किया गया, [4] उदाहरण के लिए, 1801 में जॉर्ज III के उपचार के लिए, और कीटाणुनाशक, साथ ही 20वीं सदी की प्रारम्भ तक सिफलिस के उपचार में उपयोग किया गया। अभी हाल तक, इसका उपयोग बागवानी कवकनाशी के रूप में भी किया जाता था, विशेष रूप से ब्रैसिसेकी समूह की फसलों के बीच क्लबरूट की घटना को रोकने में सहायता करने के लिए रूट डिप के रूप में उपयोग किया जाता था। [7]
द्विपदी चिकित्सा के युग में मर्करी विभिन्न प्रकार की शारीरिक और मानसिक बीमारियों के लिए एक लोकप्रिय उपचार बन गया। इसे 18वीं सदी में और क्रांति के उपरान्त अमेरिका में डॉक्टरों द्वारा मरीजों को वमन कराने और उनके शरीर को अशुद्धियों से मुक्त करने के लिए निर्धारित किया गया था। बेंजामिन रश चिकित्सा में पारे के जाने-माने समर्थक थे और उन्होंने 1793 में फ़िलाडेल्फ़िया में पीत ज्वर के प्रकोप के उपरान्त पीड़ितों के उपचार के लिए कैलोमेल का इस्तेमाल किया था। कैलोमेल को रोगियों को रेचक या रेचक के रूप में तब तक दिया जाता था जब तक कि उनमें लार आना प्रारम्भ न हो जाए और प्रायः रोगियों को यह दवा दी जाती थी। इतनी भारी मात्रा में कि उनके बाल और दाँत गिर गये। [8]
पीत ज्वर का उपचार कैलोमेल से भी किया जाता था। [9] लुईस और क्लार्क अभियान अपने अभियान में कैलोमेल लेकर आए। शोधकर्ताओं ने उसी पारे का उपयोग किया, जो शौचालय के गड्ढों की गहराई में पाया जाता है, ताकि उनके संबंधित स्थानों और शिविरों के स्थानों का पता लगाया जा सके। [10]
गुण
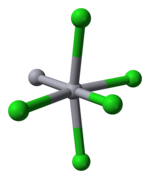
एम-एम आबंध को इतनी आसानी से बनाने की क्षमता के कारण मर्करी समूह 12 धातुओं में अद्वितीय है। Hg2Cl2 एक रैखिक अणु है। खनिज कैलोमेल अंतरिक्ष समूह I4/m 2/m 2/m के साथ द्विसमलंबाक्ष प्रणाली में क्रिस्टलीकृत होता है। क्रिस्टल संरचना की इकाई कोशिका नीचे दिखाई गई है:
 |
|
| इकाई कोशिका | Hg का विकृत अष्टफलकीय समन्वय |
Hg-Hg आबंध की लंबाई 253 pm (धातु में Hg-Hg 300 pm है) और रैखिक Hg में Hg-Cl आबंध की Hg2Cl2 इकाई 243 अपराह्न है। [11] प्रत्येक Hg परमाणु का समग्र समन्वय अष्टफलकीय है, क्योंकि दोपहर 321 बजे दो निकटतम प्रतिवैस के अतिरिक्त, चार अन्य सीएल परमाणु होते हैं। लंबे समय तक मर्करी पॉलीकेशन उपस्थित रहते हैं।
विरचन और प्रतिक्रिया
मौलिक मर्करी और मरक्यूरिक क्लोराइड की प्रतिक्रिया से मर्क्यूरस क्लोराइड बनता है:
- Hg + HgCl2 → Hg2Cl2
इसे NaCl या HCl सहित विभिन्न क्लोराइड स्रोतों का उपयोग करके जलीय मर्करी (I) नाइट्रेट से युक्त नमक मेटाथिसिस प्रतिक्रिया के माध्यम से तैयार किया जा सकता है।
- 2 HCl + Hg2(NO3)2 → Hg2Cl2 + 2 HNO3
अमोनिया के कारण Hg2Cl2 अनुपातहीन हो जाता है:
- Hg2Cl2 + 2 NH3 → Hg + Hg(NH2)Cl + NH4Cl
कैलोमेल विद्युतग्र
इसके ऑक्सीकरण और कमी प्रतिक्रियाओं की आसानी का लाभ उठाते हुए, मर्क्यूरस क्लोराइड को इलेक्ट्रोकैमिस्ट्री में बड़े मापक्रम पर नियोजित किया जाता है। कैलोमेल विद्युतग्र एक संदर्भ विशेष रूप से पुराने प्रकाशनों में विद्युतग्र है। पिछले 50 वर्षों में, इसका स्थान सिल्वर/सिल्वर क्लोराइड (Ag/AgCl) विद्युतग्र ने ले लिया है। हालाँकि मर्करी (तत्व) की हानिकारक प्रकृति के कारण मर्करी विद्युतग्र को व्यापक रूप से छोड़ दिया गया है, कई रसायनज्ञों का मानना है कि वे अभी भी अधिक सटीक हैं और तब तक हानिकारक नहीं हैं जब तक उन्हें ठीक से संभाला जाता है। प्रयोगात्मक क्षमताओं में अंतर साहित्य मूल्यों से बहुत कम भिन्न होता है। अन्य विद्युतग्र 70 से 100 मिलीवोल्ट तक भिन्न हो सकते हैं।
प्रकाशरसायन
पराबैंगनी प्रकाश के संपर्क में आने पर मर्करी (द्वितीय) क्लोराइड मर्करी (II) क्लोराइड और मौलिक मर्करी में विघटित हो जाता है।
- Hg2Cl2 → HgCl2 + Hg
एचजी के गठन का उपयोग एक्टिनोमीटर की तकनीक द्वारा प्रकाश किरण में फोटॉनों की संख्या की गणना करने के लिए किया जा सकता है।
मर्करी (II) क्लोराइड और अमोनियम ऑक्सालेट की उपस्थिति में एक हल्की प्रतिक्रिया का उपयोग करके, मर्करी (I) क्लोराइड, अमोनियम क्लोराइड और कार्बन डाईऑक्साइड का उत्पादन किया जाता है।
- 2 HgCl2 + (NH4)2C2O4 Hg2Cl2(s) + 2 [NH+
4][Cl−] + 2 CO2
इस विशेष प्रतिक्रिया की खोज 1880 में जे. एम. एडर (इसलिए इसका नाम एडर प्रतिक्रिया) द्वारा की गई थी और 1929 में डब्ल्यू. ई. रोज़वेरे द्वारा इसकी पुनः जांच की गई। [12]
संबंधित मर्करी(I) यौगिक
मर्करी (आई) ब्रोमाइड, Hg2Br2, हल्का पीला है, जबकि मर्करी (आई) आयोडाइड, Hg2I2, हरे रंग का है। दोनों ही खराब घुलनशील हैं। शक्तिशाली अम्ल की अनुपस्थिति में मर्करी (I) फ्लोराइड अस्थिर होता है।
सुरक्षा संबंधी विचार
मर्क्यूरस क्लोराइड मर्करी विषाक्तता है, हालांकि पानी में इसकी कम घुलनशीलता के कारण यह सामान्यतः अपने मरक्यूरिक क्लोराइड समकक्ष से कम हानिकारक है। 1700 के दशक के अंत से 1860 के दशक तक संयुक्त राज्य अमेरिका में इसका उपयोग चिकित्सा में मूत्रवर्धक और रेचक (रेचक) के रूप में किया जाता था। 1954 तक ब्रिटेन में प्रारम्भी पाउडर में कैलोमेल भी एक सामान्य घटक था, जिससे एक्रोडिनिया के रूप में व्यापक मर्करी विषाक्तता हुई, जिसकी उस समय मृत्यु दर 10 में से 1 थी। [13] बाद में जब यौगिक की विषाक्तता का पता चला तो इन औषधीय उपयोगों को बंद कर दिया गया।
इसका उपयोग सौंदर्य प्रसाधनों में साबुन और त्वचा को गोरा करने वाले लेप के रूप में भी पाया गया है, लेकिन अब अमेरिका, कनाडा, जापान और यूरोपीय संघ सहित कई देशों में इन तैयारियों का निर्माण या आयात करना अवैध है। [14] इन तैयारियों के उत्पादन में सम्मिलित श्रमिकों के एक अध्ययन से पता चला है कि 2,3-डिमरकैप्टो-1-प्रोपेनसल्फोनिक एसिड (डीएमपीएस) का सोडियम नमक शरीर में मर्करी के बोझ को कम करने और मूत्र में मर्करी की सांद्रता को सामान्य स्तर तक कम करने में प्रभावी था। [15]
संदर्भ
- ↑ John Rumble (June 18, 2018). CRC Handbook of Chemistry and Physics (in English) (99 ed.). CRC Press. pp. 5–188. ISBN 978-1138561632.
- ↑ 2.0 2.1 Zumdahl, Steven S. (2009). Chemical Principles 6th Ed. Houghton Mifflin Company. p. A22. ISBN 978-0-618-94690-7.
- ↑ "Mercury compounds [except (organo) alkyls] (as Hg)". Immediately Dangerous to Life or Health Concentrations (IDLH). National Institute for Occupational Safety and Health (NIOSH).
- ↑ 4.0 4.1 4.2 4.3 Chisholm, Hugh, ed. (1911). . Encyclopædia Britannica (in English) (11th ed.). Cambridge University Press.
- ↑ Housecroft, C. E.; Sharpe, A. G. (2004). Inorganic Chemistry (2nd ed.). Prentice Hall. pp. 696–697. ISBN 978-0-13-039913-7.
- ↑ Skoog, Douglas A.; Holler, F. James; Nieman, Timothy A. (1998). वाद्य विश्लेषण के सिद्धांत (5th ed.). Saunders College Pub. pp. 253–271. ISBN 978-0-03-002078-0.
- ↑ Buczacki, S., Pests, Diseases and Disorders of Garden Plants, Collins, 1998, pp 449-50. ISBN 0-00-220063-5
- ↑ Koehler, Christopher S. W. (January 2001). "Heavy Metal Medicine". Today's Chemist at Work. 10 (1): 61–65. ISSN 1062-094X. Retrieved 2009-02-02.
- ↑ Johnston, Elizabeth Lichtenstein (1901). Recollections of a Georgia Loyalist...written in 1836. New York: Mansfield & Company. p. 82. pp. 82-83.
- ↑ Inglis-Arkell, Esther. "पुरातत्वविदों ने लुईस और क्लार्क को उनके जुलाब के निशान का अनुसरण करके ट्रैक किया". io9 (in English). Retrieved 2018-11-09.
- ↑ Wells A.F. (1984) Structural Inorganic Chemistry 5th edition Oxford Science Publications ISBN 0-19-855370-6
- ↑ Roseveare, W. E. (1930). "पोटेशियम ऑक्सालेट और मर्क्यूरिक क्लोराइड के बीच एक्स-रे फोटोकैमिकल प्रतिक्रिया". J. Am. Chem. Soc. 52 (7): 2612–2619. doi:10.1021/ja01370a005.
- ↑ Sneader, Walter (2005). Drug Discovery: A History. John Wiley and Sons. pp. 45–46. ISBN 978-0-471-89980-8. Retrieved 2009-02-02.
- ↑ "Commission Directive 86/199/EEC, OJ L 149, p. 38 of 3.6.1986".
- ↑ D. Gonzalez-Ramirez; M. Zuniga-Charles; A. Narro-Juarez; Y. Molina-Recio; K. M. Hurlbut; R. C. Dart; H. V. Aposhian (1 October 1998). "DMPS (2,3-Dimercaptopropane-1-sulfonate, Dimaval) Decreases the Body Burden of Mercury in Humans Exposed to Mercurous Chloride" (free full text). The Journal of Pharmacology and Experimental Therapeutics. 287 (1): 8–12. PMID 9765315.
