पोलैनी का संभावित सिद्धांत: Difference between revisions
(Created page with "पोलानी का संभावित सिद्धांत, जिसे पोलानी सोखना संभावित सिद्धांत...") |
No edit summary |
||
| Line 1: | Line 1: | ||
पोलानी का संभावित सिद्धांत, जिसे पोलानी [[सोखना]] संभावित सिद्धांत भी कहा जाता है | पोलानी का संभावित सिद्धांत, जिसे पोलानी [[सोखना|एडसोर्प्शन]] संभावित सिद्धांत भी कहा जाता है और इस प्रकार [[माइकल पोलानी]] द्वारा प्रस्तावित एडसोर्प्शन का एक मॉडल है, जहां सतह के पास गैस की [[रासायनिक क्षमता]] और बड़ी दूरी सतह से गैस की रासायनिक क्षमता के बीच [[रासायनिक संतुलन]] के माध्यम से एडसोर्प्शन को मापा जा सकता है। इस मॉडल में, उन्होंने माना कि सतह पर गैस के वान डर वाल्स बलों के कारण मुख्य रूप से आकर्षण सतह से गैस कण की स्थिति से निर्धारित होता है और गैस संघनन एक [[आदर्श गैस]] के रूप में व्यवहार करती है जहां गैस अपने संतुलन [[वाष्प दबाव]] से अधिक हो जाती है। जबकि [[हेनरी का एडसोर्प्शन सिद्धांत]] कम दबाव में अधिक प्रयुक्त होता है और बीईटी सिद्धांत एडसोर्प्शन इसोथर्म समीकरण 0.05 to 0.35 P/Po पर अधिक उपयोगी होता है और इस प्रकार पोलानी संभावित सिद्धांत का उच्च P/Po (~0.1–0.8) पर बहुत अधिक अनुप्रयोग होता है। | ||
==अवलोकन== | ==अवलोकन== | ||
| Line 5: | Line 5: | ||
===माइकल पोलानी=== | ===माइकल पोलानी=== | ||
{{main|Michael Polanyi}} | {{main|Michael Polanyi}} | ||
माइकल पोलानी, एफआरएस (11 मार्च 1891 - 22 फरवरी 1976) एक हंगेरियन [[बहुश्रुत]] थे, जिन्होंने भौतिक [[रसायन विज्ञान]], अर्थशास्त्र और दर्शनशास्त्र में सैद्धांतिक योगदान दिया। पोलानी एक प्रसिद्ध सैद्धांतिक रसायनज्ञ थे जिन्होंने अध्ययन के तीन मुख्य क्षेत्रों के माध्यम से रसायन विज्ञान में योगदान दिया: ठोस पदार्थों पर गैसों का | माइकल पोलानी, एफआरएस (11 मार्च 1891 - 22 फरवरी 1976) एक हंगेरियन [[बहुश्रुत]] थे, जिन्होंने भौतिक [[रसायन विज्ञान]], अर्थशास्त्र और दर्शनशास्त्र में सैद्धांतिक योगदान दिया। पोलानी एक प्रसिद्ध सैद्धांतिक रसायनज्ञ थे जिन्होंने अध्ययन के तीन मुख्य क्षेत्रों के माध्यम से रसायन विज्ञान में योगदान दिया: ठोस पदार्थों पर गैसों का एडसोर्प्शन , ठोस पदार्थों के गुणों का एक्स-रे संरचना विश्लेषण और रासायनिक प्रतिक्रियाओं की दर। हालाँकि, पोलानी रसायन विज्ञान क्षेत्र में सैद्धांतिक और प्रायोगिक दोनों अध्ययनों में सक्रिय थे। पोलानी ने 1913 में चिकित्सा में डिग्री के साथ-साथ पीएच.डी. भी प्राप्त की। 1917 में [[बुडापेस्ट विश्वविद्यालय]] से भौतिक रसायन विज्ञान में। बाद में अपने जीवन में, उन्होंने बर्लिन में [[कैसर विल्हेम संस्थान]] के साथ-साथ इंग्लैंड के मैनचेस्टर में [[मैनचेस्टर विश्वविद्यालय]] में रसायन विज्ञान के प्रोफेसर के रूप में पढ़ाया। | ||
===इतिहास=== | ===इतिहास=== | ||
====प्रस्तावित सिद्धांत==== | ====प्रस्तावित सिद्धांत==== | ||
1914 में, पोलैनी ने | 1914 में, पोलैनी ने एडसोर्प्शन पर प्रस्तावित अपना पहला पेपर लिखा जहां उन्होंने एक ठोस सतह पर गैस के सोखने के लिए एक मॉडल प्रस्तावित किया।<ref name="polanyi">{{cite journal | last1 = Polanyi | first1 = M | year = 1963 | title = सोखना का संभावित सिद्धांत| journal = Science | volume = 141 | issue = 3585| pages = 1010–013 | doi=10.1126/science.141.3585.1010| pmid = 17739484 | bibcode = 1963Sci...141.1010P }}</ref> बाद में, उन्होंने 1916 में एक पूर्ण विकसित पेपर प्रकाशित किया, जिसमें उनके छात्रों और अन्य लेखकों द्वारा प्रयोगात्मक सत्यापन शामिल था। | ||
बुडापेस्ट विश्वविद्यालय में अपने शोध के दौरान, उनके गुरु प्रोफेसर जॉर्ज ब्रेडिग ने अपने शोध निष्कर्ष [[अल्बर्ट आइंस्टीन]] को भेजे। आइंस्टीन ने ब्रेडिग को जवाब देते हुए लिखा: | बुडापेस्ट विश्वविद्यालय में अपने शोध के दौरान, उनके गुरु प्रोफेसर जॉर्ज ब्रेडिग ने अपने शोध निष्कर्ष [[अल्बर्ट आइंस्टीन]] को भेजे। आइंस्टीन ने ब्रेडिग को जवाब देते हुए लिखा: | ||
<blockquote>आपके एम. पोलानी के कागजात मुझे बहुत प्रसन्न करते हैं। मैंने उनमें आवश्यक चीज़ों की जाँच की है और उन्हें मौलिक रूप से सही पाया है।</blockquote> | <blockquote>आपके एम. पोलानी के कागजात मुझे बहुत प्रसन्न करते हैं। मैंने उनमें आवश्यक चीज़ों की जाँच की है और उन्हें मौलिक रूप से सही पाया है।</blockquote> | ||
| Line 42: | Line 42: | ||
==सिद्धांत== | ==सिद्धांत== | ||
===पोलैनी संभावित | ===पोलैनी संभावित एडसोर्प्शन सिद्धांत=== | ||
[[File:Adsorption of Nitrogen onto the Surface of Carbon.png|thumb|600px|नीले रंग में नाइट्रोजन गैस के अणु भूरे रंग में कार्बन नैनोट्यूब की सतह पर सोख लेते हैं।]]पोलैनी संभावित | [[File:Adsorption of Nitrogen onto the Surface of Carbon.png|thumb|600px|नीले रंग में नाइट्रोजन गैस के अणु भूरे रंग में कार्बन नैनोट्यूब की सतह पर सोख लेते हैं।]]पोलैनी संभावित एडसोर्प्शन सिद्धांत इस धारणा पर आधारित है कि सतह के पास के अणु गुरुत्वाकर्षण या विद्युत क्षेत्र के समान क्षमता के अनुसार चलते हैं।<ref name="Physics and Chemistry of Interfaces">{{cite journal | title = इंटरफेस की भौतिकी और रसायन विज्ञान| author1 = Butt, Hans-Jürgen | author2 = Graf, Karlheinz | author3 = Kappl, Michael | year = 2003 | pages = 193–195}}</ref> यह मॉडल स्थिर तापमान पर सतह पर गैसों के मामले में प्रयुक्त होता है। जब दबाव संतुलन वाष्प दबाव से अधिक होता है तो गैस के अणु उस सतह के करीब चले जाते हैं। सतह से दूरी के सापेक्ष क्षमता में परिवर्तन की गणना रासायनिक क्षमता के अंतर के सूत्र का उपयोग करके की जा सकती है, | ||
:<math> \mathrm{d}\mu = -S_{\rm m} \, \mathrm{d}T + V_{\rm m} \, \mathrm{d}p + \mathrm{d}U_{\rm m} </math> | :<math> \mathrm{d}\mu = -S_{\rm m} \, \mathrm{d}T + V_{\rm m} \, \mathrm{d}p + \mathrm{d}U_{\rm m} </math> | ||
| Line 69: | Line 69: | ||
कहाँ <math>c_{\rm s}</math> अधिशोषक और की संतृप्त सांद्रता है <math>c</math> अधिशोषक की संतुलन सांद्रता है। | कहाँ <math>c_{\rm s}</math> अधिशोषक और की संतृप्त सांद्रता है <math>c</math> अधिशोषक की संतुलन सांद्रता है। | ||
===पोलैनी | ===पोलैनी एडसोर्प्शन सिद्धांत पर आधारित सिद्धांत=== | ||
अपनी पहली रिपोर्ट के बाद से संभावित सिद्धांत में कई वर्षों के दौरान कई परिशोधन और परिवर्तन हुए हैं। पोलैनी के सिद्धांत का उपयोग करके विकसित किए गए प्रमुख सिद्धांतों में से एक डुबिनिन सिद्धांत, डुबिनिन-रादुशकिवेच और डुबिनिन-अस्ताखोव समीकरण थे। | अपनी पहली रिपोर्ट के बाद से संभावित सिद्धांत में कई वर्षों के दौरान कई परिशोधन और परिवर्तन हुए हैं। पोलैनी के सिद्धांत का उपयोग करके विकसित किए गए प्रमुख सिद्धांतों में से एक डुबिनिन सिद्धांत, डुबिनिन-रादुशकिवेच और डुबिनिन-अस्ताखोव समीकरण थे। | ||
एडसोर्प्शन क्षमता का उपयोग करते हुए, एडसोर्प्शन स्थान भरने की डिग्री, <math>\theta</math>, के रूप में गणना की जा सकती है | |||
:<math>\theta = a/a_0 = \mathrm{e}^{{({A / E})}^b }</math> | :<math>\theta = a/a_0 = \mathrm{e}^{{({A / E})}^b }</math> | ||
कहाँ <math>a</math> तापमान T और संतुलन दबाव p पर अधिशोषण का मान है, <math>a_0</math> | कहाँ <math>a</math> तापमान T और संतुलन दबाव p पर अधिशोषण का मान है, <math>a_0</math> एडसोर्प्शन का अधिकतम मूल्य है, और <math>E</math> सोखने की विशिष्ट ऊर्जा kJ/mol में है, <math>A</math> एडसोर्प्शन में [[गिब्स मुक्त ऊर्जा]] में होने वाली हानि के बराबर है <math>\Delta G = - RT \log (p_0/p) </math> और <math>b</math> फिटिंग गुणांक है.<ref>{{Cite journal | last = Dubinin | first = M. M. | author2 = Astakhov, V. A.|title = माइक्रोपोरस अधिशोषक द्वारा गैसों और वाष्पों के अधिशोषण में माइक्रोप्रोर्स की मात्रा भरने की अवधारणाओं का विकास| journal = Bulletin of the Academy of Sciences of the USSR, Division of Chemical Science | volume = 20 | issue = 1 | pages = 3–7 | doi=10.1007/bf00849307| year = 1971 }}</ref> डबिनिन-राडुष्किवेच समीकरण कहां है <math>b</math> 2 के बराबर है और अनुकूलित डुबिनिन-अस्ताखोव समीकरण है <math>b</math> प्रयोगात्मक डेटा के लिए उपयुक्त है इसे सरल बनाया जा सकता है | ||
:<math>\log a = \log a_0 + 0.434 \left(\frac{A}{E}\right)^b</math> | :<math>\log a = \log a_0 + 0.434 \left(\frac{A}{E}\right)^b</math> | ||
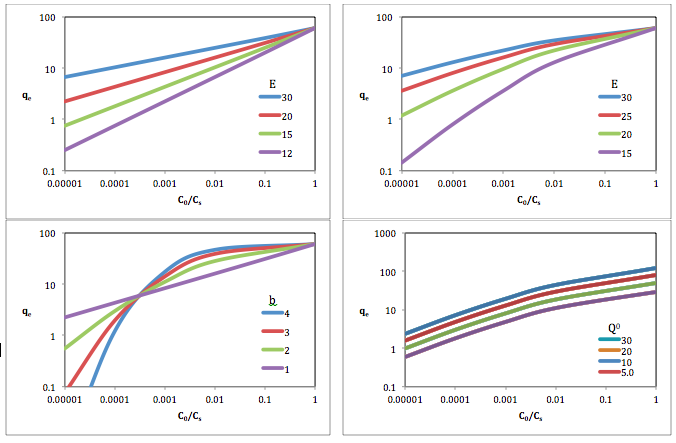
[[File:Dubinin-Astakhov Curves.png|thumb|800px|क्यू में वृद्धि के कारण डुबिनिन-अस्ताखोव वक्र में परिवर्तन<sup>0</sup>, ई, और बी एक शर्बत बनाम सापेक्ष विलेय सांद्रता पर विलेय | [[File:Dubinin-Astakhov Curves.png|thumb|800px|क्यू में वृद्धि के कारण डुबिनिन-अस्ताखोव वक्र में परिवर्तन<sup>0</sup>, ई, और बी एक शर्बत बनाम सापेक्ष विलेय सांद्रता पर विलेय इसोथर्म के लॉग-लॉग स्केल प्लॉट पर। <br />ऊपर-बाएँ: प्र<sup>0</sup>=60; बी = 1 | ||
<br />ऊपर-दाएं: प्र<sup>0</sup>=60; बी = 1.5 | <br />ऊपर-दाएं: प्र<sup>0</sup>=60; बी = 1.5 | ||
<br />नीचे-बाएं: प्र<sup>0</sup>=60; ई = 20 | <br />नीचे-बाएं: प्र<sup>0</sup>=60; ई = 20 | ||
| Line 86: | Line 86: | ||
<math>\log q_{\rm e} = \log Q^0 + (\varepsilon_{\rm sw}/E)^b</math>, | <math>\log q_{\rm e} = \log Q^0 + (\varepsilon_{\rm sw}/E)^b</math>, | ||
कहाँ <math>q_{\rm e}</math> एमजी/जी में अधिशोषक की संतुलन अधिशोषित सांद्रता है, <math>Q^0</math> अधिशोषक की अधिकतम अधिशोषित सांद्रता mg/g में है, <math>\varepsilon_{\rm sw}</math> प्रभावी | कहाँ <math>q_{\rm e}</math> एमजी/जी में अधिशोषक की संतुलन अधिशोषित सांद्रता है, <math>Q^0</math> अधिशोषक की अधिकतम अधिशोषित सांद्रता mg/g में है, <math>\varepsilon_{\rm sw}</math> प्रभावी एडसोर्प्शन क्षमता है, जहां के बराबर है <math>\varepsilon_{\rm sw} = -RT \ln (c_{\rm e}/c_{\rm s})</math>, <math>c_{\rm e}</math> समाधान चरण में अधिशोषक की संतुलन सांद्रता mg/L में है, और <math>c_{\rm s}</math> पानी में अधिशोषक घुलनशीलता mg/L है।<ref name=Xing /> | ||
अधिशोषण की विशिष्ट ऊर्जा को एक ही सतह पर एक मानक वाष्प के लिए अधिशोषण की विशिष्ट ऊर्जा से संबंधित किया जा सकता है, <math>E_0</math>, एक आत्मीयता गुणांक के उपयोग के माध्यम से, <math>\beta</math> | अधिशोषण की विशिष्ट ऊर्जा को एक ही सतह पर एक मानक वाष्प के लिए अधिशोषण की विशिष्ट ऊर्जा से संबंधित किया जा सकता है, <math>E_0</math>, एक आत्मीयता गुणांक के उपयोग के माध्यम से, <math>\beta</math> | ||
| Line 93: | Line 93: | ||
:<math>\beta = \frac{\alpha}{\alpha_0}</math> | :<math>\beta = \frac{\alpha}{\alpha_0}</math> | ||
कहाँ <math>\alpha</math> और <math>\alpha_0</math> क्रमशः नमूने और मानक वाष्प की ध्रुवीकरण क्षमताएं हैं। इष्टतम फिटिंग गुणांक निर्धारित करने के लिए कई अध्ययन किए गए हैं, <math>b</math>, और आत्मीयता गुणांक, <math>\beta</math>, ठोस पदार्थों पर गैसों और वाष्पों के सोखने का सर्वोत्तम वर्णन करने के लिए। परिणामस्वरूप, प्रयोगात्मक परिणामों के साथ फिट होने पर प्राप्त होने वाली सटीकता के कारण डबिनिन-अस्ताखोव समीकरण | कहाँ <math>\alpha</math> और <math>\alpha_0</math> क्रमशः नमूने और मानक वाष्प की ध्रुवीकरण क्षमताएं हैं। इष्टतम फिटिंग गुणांक निर्धारित करने के लिए कई अध्ययन किए गए हैं, <math>b</math>, और आत्मीयता गुणांक, <math>\beta</math>, ठोस पदार्थों पर गैसों और वाष्पों के सोखने का सर्वोत्तम वर्णन करने के लिए। परिणामस्वरूप, प्रयोगात्मक परिणामों के साथ फिट होने पर प्राप्त होने वाली सटीकता के कारण डबिनिन-अस्ताखोव समीकरण एडसोर्प्शन अध्ययन में उपयोग में रहता है। | ||
====वाष्प और गैसों के लिए डबिनिन-अस्ताखोव पैरामीटर==== | ====वाष्प और गैसों के लिए डबिनिन-अस्ताखोव पैरामीटर==== | ||
| Line 122: | Line 122: | ||
==आवेदन== | ==आवेदन== | ||
कई आधुनिक अध्ययनों में, सक्रिय कार्बन या कार्बन ब्लैक के अध्ययन में पोलैनी सिद्धांत का व्यापक रूप से उपयोग किया जाता है। सिद्धांत का उपयोग विभिन्न प्रकार के परिदृश्यों जैसे सक्रिय कार्बन पर गैस | कई आधुनिक अध्ययनों में, सक्रिय कार्बन या कार्बन ब्लैक के अध्ययन में पोलैनी सिद्धांत का व्यापक रूप से उपयोग किया जाता है। सिद्धांत का उपयोग विभिन्न प्रकार के परिदृश्यों जैसे सक्रिय कार्बन पर गैस एडसोर्प्शन और नॉनऑनिक [[पॉलीसाइक्लिक एरोमैटिक हाइड्रोकार्बन]] की सोखने की प्रक्रिया को मॉडल करने के लिए सफलतापूर्वक किया गया है।<ref>{{Cite journal | last = Yang | first = K. | author2 = Wu, W. | author3 = Jing, Q & Zhu, L. | title = बहु-दीवार वाले कार्बन नैनोट्यूब द्वारा एनिलिन, फिनोल और उनके विकल्प का जलीय सोखना| journal = Environmental Science and Technology | volume = 42 | issue = 21 | pages = 7931–6 | doi=10.1021/es801463v| pmid = 19031883 | year = 2008 | bibcode = 2008EnST...42.7931Y }}</ref> बाद में, प्रयोगों से यह भी पता चला कि यह [[फिनोल]] और [[रंगों का रासायनिक आधार]] जैसे [[आयनिक यौगिक]] पॉलीसाइक्लिक एरोमैटिक हाइड्रोकार्बन का मॉडल बना सकता है। हाल ही में, पॉलीनी एडसोर्प्शन इसोथर्म का उपयोग [[कार्बन नैनोकण]]ों के सोखने के मॉडल के लिए किया गया है। | ||
===कार्बन नैनोकणों का लक्षण वर्णन=== | ===कार्बन नैनोकणों का लक्षण वर्णन=== | ||
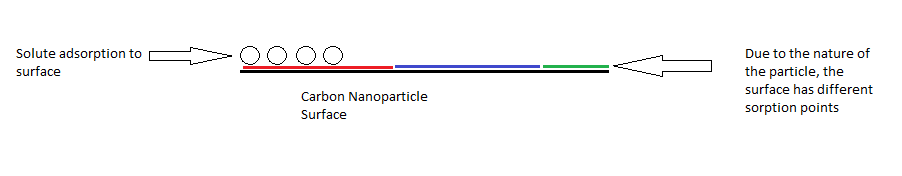
ऐतिहासिक रूप से, सिद्धांत का उपयोग गैर-समान अधिशोषक और बहु-घटक विलेय को मॉडल करने के लिए किया गया था। अधिशोषक और अधिशोषक के कुछ जोड़े के लिए, पॉलीनी सिद्धांत के गणितीय पैरामीटर अधिशोषक और अधिशोषक दोनों के भौतिक रासायनिक गुणों से संबंधित हो सकते हैं। सिद्धांत का उपयोग कार्बन नैनोट्यूब और कार्बन नैनोकणों के सोखने के मॉडल के लिए किया गया है। यांग और ज़िंग द्वारा किए गए अध्ययन में,<ref name=Xing>{{Cite journal | last = Yang | first = K. | author2 = Xing, B. | title = Adsorption of organic compounds by carbon nanomaterials in aqueous phase: Polanyi theory and its application | journal = Chemical Reviews | volume = 110 | issue = 10 | pages = 5989–6008 | doi=10.1021/cr100059s | pmid=20518459| year = 2010 }}</ref> सिद्धांत को [[लैंगमुइर सोखना मॉडल]], फ्रायंडलिच समीकरण और विभाजन की तुलना में | ऐतिहासिक रूप से, सिद्धांत का उपयोग गैर-समान अधिशोषक और बहु-घटक विलेय को मॉडल करने के लिए किया गया था। अधिशोषक और अधिशोषक के कुछ जोड़े के लिए, पॉलीनी सिद्धांत के गणितीय पैरामीटर अधिशोषक और अधिशोषक दोनों के भौतिक रासायनिक गुणों से संबंधित हो सकते हैं। सिद्धांत का उपयोग कार्बन नैनोट्यूब और कार्बन नैनोकणों के सोखने के मॉडल के लिए किया गया है। यांग और ज़िंग द्वारा किए गए अध्ययन में,<ref name=Xing>{{Cite journal | last = Yang | first = K. | author2 = Xing, B. | title = Adsorption of organic compounds by carbon nanomaterials in aqueous phase: Polanyi theory and its application | journal = Chemical Reviews | volume = 110 | issue = 10 | pages = 5989–6008 | doi=10.1021/cr100059s | pmid=20518459| year = 2010 }}</ref> सिद्धांत को [[लैंगमुइर सोखना मॉडल|लैंगमुइर एडसोर्प्शन मॉडल]], फ्रायंडलिच समीकरण और विभाजन की तुलना में एडसोर्प्शन इसोथर्म के लिए बेहतर रूप से फिट दिखाया गया है। प्रयोग में कार्बन नैनोकणों और कार्बन नैनोट्यूब पर कार्बनिक अणुओं के सोखने का अध्ययन किया गया। पॉलीनी सिद्धांत के अनुसार कार्बन नैनोकणों की सतह दोष वक्रता उनके सोखने को प्रभावित कर सकती है। कणों पर सपाट सतह अधिक सतह परमाणुओं को सोखने वाले कार्बनिक अणुओं के पास जाने की अनुमति देगी जिससे क्षमता में वृद्धि होगी, जिससे मजबूत अंतःक्रिया होगी। यह सिद्धांत कार्बन नैनोकणों पर कार्बनिक यौगिकों के सोखने के तंत्र को समझने और सोखने की क्षमता और आत्मीयता का अनुमान लगाने में फायदेमंद रहा है। इस सिद्धांत का उपयोग करके, शोधकर्ता विशिष्ट आवश्यकताओं के लिए कार्बन नैनोकणों को डिजाइन करने में सक्षम होने की उम्मीद कर रहे हैं जैसे कि उन्हें पर्यावरण अध्ययन में शर्बत के रूप में उपयोग करना। | ||
[[File:Surface adsorption onto carbon nanoparticles.png|कार्बन नैनोकणों पर सतह सोखना]] | [[File:Surface adsorption onto carbon nanoparticles.png|कार्बन नैनोकणों पर सतह सोखना]] | ||
===विभिन्न प्रणालियों से अवशोषण=== | ===विभिन्न प्रणालियों से अवशोषण=== | ||
मैन्स, एम., और होफ़र, एल. जे. ई. द्वारा किए गए पहले अध्ययनों में से एक में,<ref>{{Cite journal | last = Manes | first = M. | author2 = Hofer, B.J.E.|title = सक्रिय कार्बन पर समाधान से सोखने के लिए पोलैनी सोखना संभावित सिद्धांत का अनुप्रयोग| journal = The Journal of Physical Chemistry | volume = 73 | issue = 3 | pages = 584–590 | doi=10.1021/j100723a018| year = 1969 }}</ref> पॉलीनी सिद्धांत का उपयोग कार्बनिक विलायक की एक विस्तृत श्रृंखला का उपयोग करके सक्रिय कार्बन के विभिन्न सांद्रता पर तरल-चरण | मैन्स, एम., और होफ़र, एल. जे. ई. द्वारा किए गए पहले अध्ययनों में से एक में,<ref>{{Cite journal | last = Manes | first = M. | author2 = Hofer, B.J.E.|title = सक्रिय कार्बन पर समाधान से सोखने के लिए पोलैनी सोखना संभावित सिद्धांत का अनुप्रयोग| journal = The Journal of Physical Chemistry | volume = 73 | issue = 3 | pages = 584–590 | doi=10.1021/j100723a018| year = 1969 }}</ref> पॉलीनी सिद्धांत का उपयोग कार्बनिक विलायक की एक विस्तृत श्रृंखला का उपयोग करके सक्रिय कार्बन के विभिन्न सांद्रता पर तरल-चरण एडसोर्प्शन इसोथर्म को चिह्नित करने के लिए किया गया था। पोलियानी सिद्धांत को इन विभिन्न प्रणालियों के लिए उपयुक्त दिखाया गया है। परिणामों के कारण, अध्ययन ने न्यूनतम डेटा का उपयोग करके समान प्रणालियों के लिए इसोथर्म की भविष्यवाणी करने की संभावना पेश की। हालाँकि, सीमा यह है कि बड़ी संख्या में सॉल्वैंट्स के लिए एडसोर्प्शन इसोथर्म केवल एक सीमित सीमा तक ही फिट हो सकते हैं। वक्र उच्च क्षमता सीमा पर डेटा को फिट करने में सक्षम नहीं था। अध्ययन ने यह भी निष्कर्ष निकाला कि परिणामों में कुछ विसंगतियाँ थीं। सक्रिय कार्बन पर [[कार्बन टेट्राक्लोराइड]], [[ cyclohexane ]] और [[कार्बन डाइसल्फ़ाइड]] से एडसोर्प्शन वक्र में अच्छी तरह से फिट नहीं हो पा रहा था, और इसे समझाया जाना बाकी है। प्रयोग करने वाले शोधकर्ताओं का अनुमान है कि कार्बन टेट्राक्लोराइड और साइक्लोहेक्सेन के स्टेरिक प्रभावों ने इसमें भूमिका निभाई होगी। यह अध्ययन विभिन्न प्रणालियों के साथ किया गया है जैसे कि पानी के घोल से कार्बनिक तरल पदार्थ और पानी के घोल से कार्बनिक ठोस। | ||
===प्रतिस्पर्धी | ===प्रतिस्पर्धी एडसोर्प्शन === | ||
चूंकि विभिन्न प्रणालियों की जांच की गई है, इसलिए मिश्रित समाधान के व्यक्तिगत सोखने की जांच के लिए एक अध्ययन किया गया था। इस घटना को लैंगमुइर | चूंकि विभिन्न प्रणालियों की जांच की गई है, इसलिए मिश्रित समाधान के व्यक्तिगत सोखने की जांच के लिए एक अध्ययन किया गया था। इस घटना को लैंगमुइर एडसोर्प्शन मॉडल#प्रतिस्पर्धी एडसोर्प्शन भी कहा जाता है क्योंकि विलेय समान एडसोर्प्शन साइटों के लिए प्रतिस्पर्धा करते हैं। रोसेन और मेन्स द्वारा किए गए प्रयोग में,<ref>{{Cite journal | last = Manes | first = M.R. | author2 = Manes, M.|title = सक्रिय कार्बन पर समाधान से सोखने के लिए पोलैनी सोखना संभावित सिद्धांत का अनुप्रयोग। सातवीं. जल विलयन से ठोस पदार्थों का प्रतिस्पर्धी अधिशोषण| journal = The Journal of Physical Chemistry | volume = 80 | issue = 9 | pages = 953–959 |doi = 10.1021/j100550a007 | year = 1976 }}</ref> [[ग्लूकोज]], [[यूरिया]], [[ बेंज़ोइक एसिड ]], [[थैलाइड]] और [[पी nitrophenol]] का प्रतिस्पर्धी एडसोर्प्शन । पोलैनी एडसोर्प्शन मॉडल का उपयोग करके, वे सक्रिय कार्बन की सतह पर प्रत्येक यौगिक के सापेक्ष एडसोर्प्शन की गणना करने में सक्षम थे। | ||
==यह भी देखें== | ==यह भी देखें== | ||
Revision as of 00:23, 27 July 2023
पोलानी का संभावित सिद्धांत, जिसे पोलानी एडसोर्प्शन संभावित सिद्धांत भी कहा जाता है और इस प्रकार माइकल पोलानी द्वारा प्रस्तावित एडसोर्प्शन का एक मॉडल है, जहां सतह के पास गैस की रासायनिक क्षमता और बड़ी दूरी सतह से गैस की रासायनिक क्षमता के बीच रासायनिक संतुलन के माध्यम से एडसोर्प्शन को मापा जा सकता है। इस मॉडल में, उन्होंने माना कि सतह पर गैस के वान डर वाल्स बलों के कारण मुख्य रूप से आकर्षण सतह से गैस कण की स्थिति से निर्धारित होता है और गैस संघनन एक आदर्श गैस के रूप में व्यवहार करती है जहां गैस अपने संतुलन वाष्प दबाव से अधिक हो जाती है। जबकि हेनरी का एडसोर्प्शन सिद्धांत कम दबाव में अधिक प्रयुक्त होता है और बीईटी सिद्धांत एडसोर्प्शन इसोथर्म समीकरण 0.05 to 0.35 P/Po पर अधिक उपयोगी होता है और इस प्रकार पोलानी संभावित सिद्धांत का उच्च P/Po (~0.1–0.8) पर बहुत अधिक अनुप्रयोग होता है।
अवलोकन
माइकल पोलानी
माइकल पोलानी, एफआरएस (11 मार्च 1891 - 22 फरवरी 1976) एक हंगेरियन बहुश्रुत थे, जिन्होंने भौतिक रसायन विज्ञान, अर्थशास्त्र और दर्शनशास्त्र में सैद्धांतिक योगदान दिया। पोलानी एक प्रसिद्ध सैद्धांतिक रसायनज्ञ थे जिन्होंने अध्ययन के तीन मुख्य क्षेत्रों के माध्यम से रसायन विज्ञान में योगदान दिया: ठोस पदार्थों पर गैसों का एडसोर्प्शन , ठोस पदार्थों के गुणों का एक्स-रे संरचना विश्लेषण और रासायनिक प्रतिक्रियाओं की दर। हालाँकि, पोलानी रसायन विज्ञान क्षेत्र में सैद्धांतिक और प्रायोगिक दोनों अध्ययनों में सक्रिय थे। पोलानी ने 1913 में चिकित्सा में डिग्री के साथ-साथ पीएच.डी. भी प्राप्त की। 1917 में बुडापेस्ट विश्वविद्यालय से भौतिक रसायन विज्ञान में। बाद में अपने जीवन में, उन्होंने बर्लिन में कैसर विल्हेम संस्थान के साथ-साथ इंग्लैंड के मैनचेस्टर में मैनचेस्टर विश्वविद्यालय में रसायन विज्ञान के प्रोफेसर के रूप में पढ़ाया।
इतिहास
प्रस्तावित सिद्धांत
1914 में, पोलैनी ने एडसोर्प्शन पर प्रस्तावित अपना पहला पेपर लिखा जहां उन्होंने एक ठोस सतह पर गैस के सोखने के लिए एक मॉडल प्रस्तावित किया।[1] बाद में, उन्होंने 1916 में एक पूर्ण विकसित पेपर प्रकाशित किया, जिसमें उनके छात्रों और अन्य लेखकों द्वारा प्रयोगात्मक सत्यापन शामिल था। बुडापेस्ट विश्वविद्यालय में अपने शोध के दौरान, उनके गुरु प्रोफेसर जॉर्ज ब्रेडिग ने अपने शोध निष्कर्ष अल्बर्ट आइंस्टीन को भेजे। आइंस्टीन ने ब्रेडिग को जवाब देते हुए लिखा:
आपके एम. पोलानी के कागजात मुझे बहुत प्रसन्न करते हैं। मैंने उनमें आवश्यक चीज़ों की जाँच की है और उन्हें मौलिक रूप से सही पाया है।
पोलानी ने बाद में इस घटना का वर्णन यह कहकर किया:
<ब्लॉककोट>धमाका! मैं एक वैज्ञानिक था.
पोलानी और आइंस्टीन अगले 20 वर्षों तक एक-दूसरे को लिखते रहे।
आलोचना
पोलानी के सोखने के मॉडल को प्रकाशन वर्षों के बाद कई दशकों तक बहुत आलोचना का सामना करना पड़ा। अधिशोषण के निर्धारण के लिए उनका सरलीकृत मॉडल विद्युत द्विध्रुव आघूर्ण|डेबी के निश्चित द्विध्रुव, बोह्र परमाणु मॉडल|बोह्र के परमाणु मॉडल की खोज के समय बनाया गया था, और साथ ही रसायन विज्ञान की दुनिया में प्रमुख हस्तियों द्वारा अंतर-आणविक बलों और इलेक्ट्रोस्टैटिक बलों के विकासशील सिद्धांत के दौरान बनाया गया था। विलियम हेनरी ब्रैग सहित|डब्ल्यू.एच. ब्रैग, विलियम लॉरेंस ब्रैग|डब्ल्यू.एल. ब्रैग, और विलेम हेंड्रिक कीसोम। उनके मॉडल के विरोधियों ने दावा किया कि पोलैनी के सिद्धांत ने इन उभरते सिद्धांतों को ध्यान में नहीं रखा। आलोचना में यह शामिल था कि मॉडल ने गैस और सतह की विद्युतीय अंतःक्रियाओं को ध्यान में नहीं रखा, और अन्य अणुओं की उपस्थिति सतह पर गैस के आकर्षण को रोक देगी। 1916 से 1918 तक लैंगमुइर समीकरण के बाद पोलानी के मॉडल को जांच के दायरे में रखा गया, जिसके शोध के माध्यम से अंततः 1932 में नोबेल पुरस्कार जीता गया। हालाँकि, पोलानी इनमें से कई चर्चाओं में भाग लेने में सक्षम नहीं थे क्योंकि उन्होंने प्रथम विश्व युद्ध में हंगरी के दौरान 1914-1916 में ऑस्ट्रिया-हंगरी #सर्बियाई मोर्चे पर ऑस्ट्रिया-हंगरी|ऑस्ट्रो-हंगेरियन सेना के लिए एक चिकित्सा अधिकारी के रूप में कार्य किया था। पोलानी ने लिखा इस अनुभव के बारे में कह रहे हैं: <ब्लॉककोट>अगस्त 1914 से अक्टूबर 1918 तक ऑस्ट्रो-हंगेरियन सेना में एक चिकित्सा अधिकारी के रूप में सेवा करके, और 1919 के अंत तक चली बाद की क्रांतियों और जवाबी क्रांतियों द्वारा, मैं खुद कुछ समय के लिए इन विकासों के बारे में किसी भी जानकारी से सुरक्षित था। अन्यत्र कम-अच्छी जानकारी वाले मंडल के सदस्य कुछ समय तक मेरे सिद्धांत की सरलता और इसके व्यापक प्रयोगात्मक सत्यापन से प्रभावित होते रहे।[1]</ब्लॉककोट>
रक्षा
पोलानी ने वर्णन किया कि उनके सोखने के मॉडल की स्वीकृति का "महत्वपूर्ण मोड़" तब आया जब फ़्रिट्ज़ हैबर ने उन्हें बर्लिन, जर्मनी में भौतिक रसायन विज्ञान के लिए कैसर विल्हेम संस्थान में अपने सिद्धांत का पूर्ण बचाव करने के लिए कहा। इस बैठक में अल्बर्ट आइंस्टीन सहित वैज्ञानिक जगत के कई प्रमुख खिलाड़ी उपस्थित थे। अपने मॉडल के बारे में पोलैनी की पूरी व्याख्या सुनने के बाद, हैबर और आइंस्टीन ने दावा किया कि पोलैनी ने "इस मामले की वैज्ञानिक रूप से स्थापित संरचना के प्रति पूर्ण उपेक्षा प्रदर्शित की थी"। वर्षों बाद, पोलैनी ने निष्कर्ष निकालते हुए अपनी आपबीती का वर्णन किया,
पेशेवर तौर पर, मैं इस अवसर पर केवल अपने दांतों की खाल के सहारे बच गया।
पोलानी ने इस बैठक के बाद अपने मॉडल वर्षों की वैधता को साबित करने के लिए सहायक साक्ष्य प्रदान करना जारी रखा।[1]
खंडन
अपने मॉडल की इन अस्वीकृतियों और आलोचना से पोलानी की 'मुक्ति' (जैसा कि उन्होंने इसका वर्णन किया) 1930 में हुई, जब फ़्रिट्ज़ लंदन ने इलेक्ट्रॉनिक प्रणालियों के ध्रुवीकरण पर क्वांटम यांत्रिकी के सिद्धांतों पर स्थापित एकजुट बलों का एक नया सिद्धांत प्रस्तावित किया। पोलानी ने लंदन को पत्र लिखकर पूछा, <ब्लॉकक्वॉट>“क्या ये बल हस्तक्षेप करने वाले अणुओं द्वारा स्क्रीनिंग के अधीन हैं? क्या इन बलों के ठोस कार्य में स्थानिक रूप से निश्चित सोखने की क्षमता होगी? </ब्लॉककोट> कम्प्यूटेशनल विश्लेषण के बाद, पोलानी और लंदन के बीच एक संयुक्त प्रकाशन किया गया जिसमें दावा किया गया कि सोखने वाली ताकतें उस मॉडल के समान व्यवहार करती हैं जो पोलानी ने प्रस्तावित किया था।[1]
आगे का शोध
पोलैनी के सिद्धांत का ऐतिहासिक महत्व है, जिनके काम का उपयोग अन्य मॉडलों के लिए एक आधार के रूप में किया गया है, जैसे कि वॉल्यूम भरने वाले माइक्रोप्रोर्स (टीवीएफएम) का सिद्धांत और डुबिनिन-राडशकेविच सिद्धांत। पोलैनी के संभावित सिद्धांत को शामिल करते हुए अन्य शोध किए गए हैं जैसे कि ज़्सिग्मोंडी द्वारा खोजी गई केशिका संघनन घटना। पोयलानी के सिद्धांत के विपरीत, जिसमें एक सपाट सतह शामिल है, ज़िग्मोंडी के शोध में सिलिका सामग्री जैसी छिद्रपूर्ण संरचना शामिल है। उनके शोध ने साबित किया कि वाष्प का संघनन मानक संतृप्त वाष्प दबाव के नीचे संकीर्ण छिद्रों में हो सकता है।[2]
सिद्धांत
पोलैनी संभावित एडसोर्प्शन सिद्धांत
पोलैनी संभावित एडसोर्प्शन सिद्धांत इस धारणा पर आधारित है कि सतह के पास के अणु गुरुत्वाकर्षण या विद्युत क्षेत्र के समान क्षमता के अनुसार चलते हैं।[3] यह मॉडल स्थिर तापमान पर सतह पर गैसों के मामले में प्रयुक्त होता है। जब दबाव संतुलन वाष्प दबाव से अधिक होता है तो गैस के अणु उस सतह के करीब चले जाते हैं। सतह से दूरी के सापेक्ष क्षमता में परिवर्तन की गणना रासायनिक क्षमता के अंतर के सूत्र का उपयोग करके की जा सकती है,
कहाँ रासायनिक क्षमता है, दाढ़ एन्ट्रापी है, दाढ़ की मात्रा है, और दाढ़ आंतरिक ऊर्जा है.
संतुलन पर, दूरी पर गैस की रासायनिक क्षमता किसी सतह से, , सतह से असीम रूप से बड़ी दूरी पर गैस की रासायनिक क्षमता के बराबर है, . परिणामस्वरूप, सतह से अनंत दूरी से r दूरी तक एकीकरण होता है
कहाँ दूरी r और पर आंशिक दबाव है सतह से अनंत दूरी पर आंशिक दबाव है।
चूँकि तापमान स्थिर रहता है, रासायनिक क्षमता सूत्र में अंतर को दबाव पर एकीकृत किया जा सकता है और
सेटिंग करके , समीकरण को सरल बनाया जा सकता है
आदर्श गैस नियम का उपयोग करते हुए, , निम्नलिखित सूत्र प्राप्त होता है
चूंकि गैस किसी सतह पर तब संघनित होकर तरल में बदल जाती है जब गैस का दबाव संतुलन वाष्प दबाव से अधिक हो जाता है, , हम मान सकते हैं कि मोटाई की सतह पर एक तरल फिल्म बनती है, . पर ऊर्जा है
यह मानते हुए कि गैसों का आंशिक दबाव सांद्रता, सोखने की क्षमता से संबंधित है, के रूप में गणना की जा सकती है
कहाँ अधिशोषक और की संतृप्त सांद्रता है अधिशोषक की संतुलन सांद्रता है।
पोलैनी एडसोर्प्शन सिद्धांत पर आधारित सिद्धांत
अपनी पहली रिपोर्ट के बाद से संभावित सिद्धांत में कई वर्षों के दौरान कई परिशोधन और परिवर्तन हुए हैं। पोलैनी के सिद्धांत का उपयोग करके विकसित किए गए प्रमुख सिद्धांतों में से एक डुबिनिन सिद्धांत, डुबिनिन-रादुशकिवेच और डुबिनिन-अस्ताखोव समीकरण थे।
एडसोर्प्शन क्षमता का उपयोग करते हुए, एडसोर्प्शन स्थान भरने की डिग्री, , के रूप में गणना की जा सकती है
कहाँ तापमान T और संतुलन दबाव p पर अधिशोषण का मान है, एडसोर्प्शन का अधिकतम मूल्य है, और सोखने की विशिष्ट ऊर्जा kJ/mol में है, एडसोर्प्शन में गिब्स मुक्त ऊर्जा में होने वाली हानि के बराबर है और फिटिंग गुणांक है.[4] डबिनिन-राडुष्किवेच समीकरण कहां है 2 के बराबर है और अनुकूलित डुबिनिन-अस्ताखोव समीकरण है प्रयोगात्मक डेटा के लिए उपयुक्त है इसे सरल बनाया जा सकता है
अन्य अध्ययनों में डुबिनिन-अस्ताखोव का उपयोग इसी रूप में किया गया है
,
कहाँ एमजी/जी में अधिशोषक की संतुलन अधिशोषित सांद्रता है, अधिशोषक की अधिकतम अधिशोषित सांद्रता mg/g में है, प्रभावी एडसोर्प्शन क्षमता है, जहां के बराबर है , समाधान चरण में अधिशोषक की संतुलन सांद्रता mg/L में है, और पानी में अधिशोषक घुलनशीलता mg/L है।[5]
अधिशोषण की विशिष्ट ऊर्जा को एक ही सतह पर एक मानक वाष्प के लिए अधिशोषण की विशिष्ट ऊर्जा से संबंधित किया जा सकता है, , एक आत्मीयता गुणांक के उपयोग के माध्यम से,
आत्मीयता गुणांक नमूना और मानक वाष्प के गुणों का अनुपात है
कहाँ और क्रमशः नमूने और मानक वाष्प की ध्रुवीकरण क्षमताएं हैं। इष्टतम फिटिंग गुणांक निर्धारित करने के लिए कई अध्ययन किए गए हैं, , और आत्मीयता गुणांक, , ठोस पदार्थों पर गैसों और वाष्पों के सोखने का सर्वोत्तम वर्णन करने के लिए। परिणामस्वरूप, प्रयोगात्मक परिणामों के साथ फिट होने पर प्राप्त होने वाली सटीकता के कारण डबिनिन-अस्ताखोव समीकरण एडसोर्प्शन अध्ययन में उपयोग में रहता है।
वाष्प और गैसों के लिए डबिनिन-अस्ताखोव पैरामीटर
| Compound | Activated carbon | , kJ/mol | Source | ||
|---|---|---|---|---|---|
| Benzene | Carbon molecular sieve | 1.78 | 11.52 | 1.00 | [6] |
| Acetone | Carbon molecular sieve | 2.00 | 9.774 | 0.85 | [6] |
| Benzene | CAL AC | 2 | 18.23 | 1.00 | [7] |
| Acetone | CAL AC | 2 | 13.21 | 0.72 | [7] |
| Acetone | Carbon molecular sieve | 2.8 | 20.29 | 0.72 | [8] |
| Benzene | Carbon molecular sieve | 3.1 | 28.87 | 1.00 | [8] |
| Nitrogen | Carbon molecular sieve | 2.6 | 11.72 | 0.41 | [8] |
| Oxygen | Carbon molecular sieve | 2.3 | 9.21 | 0.32 | [8] |
| Hydrogen | Carbon molecular sieve | 2.5 | 5.44 | 0.19 | [8] |
आवेदन
कई आधुनिक अध्ययनों में, सक्रिय कार्बन या कार्बन ब्लैक के अध्ययन में पोलैनी सिद्धांत का व्यापक रूप से उपयोग किया जाता है। सिद्धांत का उपयोग विभिन्न प्रकार के परिदृश्यों जैसे सक्रिय कार्बन पर गैस एडसोर्प्शन और नॉनऑनिक पॉलीसाइक्लिक एरोमैटिक हाइड्रोकार्बन की सोखने की प्रक्रिया को मॉडल करने के लिए सफलतापूर्वक किया गया है।[9] बाद में, प्रयोगों से यह भी पता चला कि यह फिनोल और रंगों का रासायनिक आधार जैसे आयनिक यौगिक पॉलीसाइक्लिक एरोमैटिक हाइड्रोकार्बन का मॉडल बना सकता है। हाल ही में, पॉलीनी एडसोर्प्शन इसोथर्म का उपयोग कार्बन नैनोकणों के सोखने के मॉडल के लिए किया गया है।
कार्बन नैनोकणों का लक्षण वर्णन
ऐतिहासिक रूप से, सिद्धांत का उपयोग गैर-समान अधिशोषक और बहु-घटक विलेय को मॉडल करने के लिए किया गया था। अधिशोषक और अधिशोषक के कुछ जोड़े के लिए, पॉलीनी सिद्धांत के गणितीय पैरामीटर अधिशोषक और अधिशोषक दोनों के भौतिक रासायनिक गुणों से संबंधित हो सकते हैं। सिद्धांत का उपयोग कार्बन नैनोट्यूब और कार्बन नैनोकणों के सोखने के मॉडल के लिए किया गया है। यांग और ज़िंग द्वारा किए गए अध्ययन में,[5] सिद्धांत को लैंगमुइर एडसोर्प्शन मॉडल, फ्रायंडलिच समीकरण और विभाजन की तुलना में एडसोर्प्शन इसोथर्म के लिए बेहतर रूप से फिट दिखाया गया है। प्रयोग में कार्बन नैनोकणों और कार्बन नैनोट्यूब पर कार्बनिक अणुओं के सोखने का अध्ययन किया गया। पॉलीनी सिद्धांत के अनुसार कार्बन नैनोकणों की सतह दोष वक्रता उनके सोखने को प्रभावित कर सकती है। कणों पर सपाट सतह अधिक सतह परमाणुओं को सोखने वाले कार्बनिक अणुओं के पास जाने की अनुमति देगी जिससे क्षमता में वृद्धि होगी, जिससे मजबूत अंतःक्रिया होगी। यह सिद्धांत कार्बन नैनोकणों पर कार्बनिक यौगिकों के सोखने के तंत्र को समझने और सोखने की क्षमता और आत्मीयता का अनुमान लगाने में फायदेमंद रहा है। इस सिद्धांत का उपयोग करके, शोधकर्ता विशिष्ट आवश्यकताओं के लिए कार्बन नैनोकणों को डिजाइन करने में सक्षम होने की उम्मीद कर रहे हैं जैसे कि उन्हें पर्यावरण अध्ययन में शर्बत के रूप में उपयोग करना।
विभिन्न प्रणालियों से अवशोषण
मैन्स, एम., और होफ़र, एल. जे. ई. द्वारा किए गए पहले अध्ययनों में से एक में,[10] पॉलीनी सिद्धांत का उपयोग कार्बनिक विलायक की एक विस्तृत श्रृंखला का उपयोग करके सक्रिय कार्बन के विभिन्न सांद्रता पर तरल-चरण एडसोर्प्शन इसोथर्म को चिह्नित करने के लिए किया गया था। पोलियानी सिद्धांत को इन विभिन्न प्रणालियों के लिए उपयुक्त दिखाया गया है। परिणामों के कारण, अध्ययन ने न्यूनतम डेटा का उपयोग करके समान प्रणालियों के लिए इसोथर्म की भविष्यवाणी करने की संभावना पेश की। हालाँकि, सीमा यह है कि बड़ी संख्या में सॉल्वैंट्स के लिए एडसोर्प्शन इसोथर्म केवल एक सीमित सीमा तक ही फिट हो सकते हैं। वक्र उच्च क्षमता सीमा पर डेटा को फिट करने में सक्षम नहीं था। अध्ययन ने यह भी निष्कर्ष निकाला कि परिणामों में कुछ विसंगतियाँ थीं। सक्रिय कार्बन पर कार्बन टेट्राक्लोराइड, cyclohexane और कार्बन डाइसल्फ़ाइड से एडसोर्प्शन वक्र में अच्छी तरह से फिट नहीं हो पा रहा था, और इसे समझाया जाना बाकी है। प्रयोग करने वाले शोधकर्ताओं का अनुमान है कि कार्बन टेट्राक्लोराइड और साइक्लोहेक्सेन के स्टेरिक प्रभावों ने इसमें भूमिका निभाई होगी। यह अध्ययन विभिन्न प्रणालियों के साथ किया गया है जैसे कि पानी के घोल से कार्बनिक तरल पदार्थ और पानी के घोल से कार्बनिक ठोस।
प्रतिस्पर्धी एडसोर्प्शन
चूंकि विभिन्न प्रणालियों की जांच की गई है, इसलिए मिश्रित समाधान के व्यक्तिगत सोखने की जांच के लिए एक अध्ययन किया गया था। इस घटना को लैंगमुइर एडसोर्प्शन मॉडल#प्रतिस्पर्धी एडसोर्प्शन भी कहा जाता है क्योंकि विलेय समान एडसोर्प्शन साइटों के लिए प्रतिस्पर्धा करते हैं। रोसेन और मेन्स द्वारा किए गए प्रयोग में,[11] ग्लूकोज, यूरिया, बेंज़ोइक एसिड , थैलाइड और पी nitrophenol का प्रतिस्पर्धी एडसोर्प्शन । पोलैनी एडसोर्प्शन मॉडल का उपयोग करके, वे सक्रिय कार्बन की सतह पर प्रत्येक यौगिक के सापेक्ष एडसोर्प्शन की गणना करने में सक्षम थे।
यह भी देखें
- अवशोषण
- कार्बन नैनोट्यूब
- सक्रिय कार्बन
- फ़्रायंडलिच समीकरण
- शर्त सिद्धांत
संदर्भ
- ↑ 1.0 1.1 1.2 1.3 Polanyi, M (1963). "सोखना का संभावित सिद्धांत". Science. 141 (3585): 1010–013. Bibcode:1963Sci...141.1010P. doi:10.1126/science.141.3585.1010. PMID 17739484.
- ↑ http://web.iitd.ac.in/~arunku/files/CEL311_Y13/Adsorption%20Theory%20to%20practice_Dabrowski.pdf[bare URL PDF]
- ↑ Butt, Hans-Jürgen; Graf, Karlheinz; Kappl, Michael (2003). "इंटरफेस की भौतिकी और रसायन विज्ञान": 193–195.
{{cite journal}}: Cite journal requires|journal=(help) - ↑ Dubinin, M. M.; Astakhov, V. A. (1971). "माइक्रोपोरस अधिशोषक द्वारा गैसों और वाष्पों के अधिशोषण में माइक्रोप्रोर्स की मात्रा भरने की अवधारणाओं का विकास". Bulletin of the Academy of Sciences of the USSR, Division of Chemical Science. 20 (1): 3–7. doi:10.1007/bf00849307.
- ↑ 5.0 5.1 Yang, K.; Xing, B. (2010). "Adsorption of organic compounds by carbon nanomaterials in aqueous phase: Polanyi theory and its application". Chemical Reviews. 110 (10): 5989–6008. doi:10.1021/cr100059s. PMID 20518459.
- ↑ 6.0 6.1 Doong, S. J.; Yang, R. T. (1988). "A simple potential theory model for predicting mixed-gas adsorption". Industrial & Engineering Chemistry Research. 27 (4): 630–635. doi:10.1021/ie00076a017.
- ↑ 7.0 7.1 Tamon, H.; Okazaki, M. (1996). "Influence of acidic surface oxides of activated carbon on gas adsorption characteristics". Carbon. 34 (6): 741–746. doi:10.1016/0008-6223(96)00029-2.
- ↑ 8.0 8.1 8.2 8.3 8.4 Kawazoe, K.; Kawai, T.; Eguchi, Y.; Itoga, K. (1974). "Correlation of adsorption equilibrium data of various gases and vapors on molecular-sieving carbon". Journal of Chemical Engineering of Japan. 7 (3): 158–162. doi:10.1252/jcej.7.158.
- ↑ Yang, K.; Wu, W.; Jing, Q & Zhu, L. (2008). "बहु-दीवार वाले कार्बन नैनोट्यूब द्वारा एनिलिन, फिनोल और उनके विकल्प का जलीय सोखना". Environmental Science and Technology. 42 (21): 7931–6. Bibcode:2008EnST...42.7931Y. doi:10.1021/es801463v. PMID 19031883.
{{cite journal}}: CS1 maint: multiple names: authors list (link) - ↑ Manes, M.; Hofer, B.J.E. (1969). "सक्रिय कार्बन पर समाधान से सोखने के लिए पोलैनी सोखना संभावित सिद्धांत का अनुप्रयोग". The Journal of Physical Chemistry. 73 (3): 584–590. doi:10.1021/j100723a018.
- ↑ Manes, M.R.; Manes, M. (1976). "सक्रिय कार्बन पर समाधान से सोखने के लिए पोलैनी सोखना संभावित सिद्धांत का अनुप्रयोग। सातवीं. जल विलयन से ठोस पदार्थों का प्रतिस्पर्धी अधिशोषण". The Journal of Physical Chemistry. 80 (9): 953–959. doi:10.1021/j100550a007.