कैंसर इम्यूनोथेरेपी: Difference between revisions
m (14 revisions imported from alpha:कैंसर_इम्यूनोथेरेपी) |
No edit summary |
||
| Line 56: | Line 56: | ||
Sipuleucel-T (बदला) को 2010 में स्पर्शोन्मुख या न्यूनतम रोगसूचक मेटास्टैटिक कैस्ट्रेशन-प्रतिरोधी [[प्रोस्टेट कैंसर]] के उपचार के लिए अनुमोदित किया गया था। उपचार में [[ल्यूकेफेरेसिस]] द्वारा रक्त [[एंटीजन-प्रेजेंटिंग सेल]] कोशिकाओं को हटाना और उन्हें GM- से बने [[संलयन प्रोटीन]] PA2024 के साथ बढ़ाना शामिल है। CSF और प्रोस्टेट-विशिष्ट [[प्रोस्टेटिक एसिड फॉस्फेट]] (PAP) और पुन: उपयोग किया जाता है। यह प्रक्रिया तीन बार दोहराई जाती है।<ref>{{cite journal | vauthors = Gardner TA, Elzey BD, Hahn NM | title = Sipuleucel-T (बदला) ऑटोलॉगस वैक्सीन स्पर्शोन्मुख या न्यूनतम लक्षण वाले कैटरेट-प्रतिरोधी मेटास्टेटिक प्रोस्टेट कैंसर वाले पुरुषों के उपचार के लिए स्वीकृत| journal = Human Vaccines & Immunotherapeutics | volume = 8 | issue = 4 | pages = 534–39 | date = April 2012 | pmid = 22832254 | doi = 10.4161/hv.19795 | doi-access = free }}</ref><ref>{{cite journal | vauthors = Oudard S | title = उन्नत प्रोस्टेट कैंसर के लिए उभरते उपचारों में प्रगति| journal = Cancer Treatment Reviews | volume = 39 | issue = 3 | pages = 275–89 | date = May 2013 | pmid = 23107383 | doi = 10.1016/j.ctrv.2012.09.005 }}</ref><ref>{{cite journal | vauthors = Sims RB | title = सिपुलेसेल-टी का विकास: मेटास्टैटिक कैस्ट्रेट प्रतिरोधी प्रोस्टेट कैंसर के उपचार के लिए ऑटोलॉगस सेलुलर इम्यूनोथेरेपी| journal = Vaccine | volume = 30 | issue = 29 | pages = 4394–97 | date = June 2012 | pmid = 22122856 | doi = 10.1016/j.vaccine.2011.11.058 | doi-access = free }}</ref><ref>{{cite journal | vauthors = Shore ND, Mantz CA, Dosoretz DE, Fernandez E, Myslicki FA, McCoy C, Finkelstein SE, Fishman MN | title = कैस्ट्रेशन-प्रतिरोधी प्रोस्टेट कैंसर के इम्यूनोलॉजिक उपचार के लिए सिपुलेसेल-टी पर निर्माण| journal = Cancer Control | volume = 20 | issue = 1 | pages = 7–16 | date = January 2013 | pmid = 23302902 | doi = 10.1177/107327481302000103 | doi-access = free }}</ref> | Sipuleucel-T (बदला) को 2010 में स्पर्शोन्मुख या न्यूनतम रोगसूचक मेटास्टैटिक कैस्ट्रेशन-प्रतिरोधी [[प्रोस्टेट कैंसर]] के उपचार के लिए अनुमोदित किया गया था। उपचार में [[ल्यूकेफेरेसिस]] द्वारा रक्त [[एंटीजन-प्रेजेंटिंग सेल]] कोशिकाओं को हटाना और उन्हें GM- से बने [[संलयन प्रोटीन]] PA2024 के साथ बढ़ाना शामिल है। CSF और प्रोस्टेट-विशिष्ट [[प्रोस्टेटिक एसिड फॉस्फेट]] (PAP) और पुन: उपयोग किया जाता है। यह प्रक्रिया तीन बार दोहराई जाती है।<ref>{{cite journal | vauthors = Gardner TA, Elzey BD, Hahn NM | title = Sipuleucel-T (बदला) ऑटोलॉगस वैक्सीन स्पर्शोन्मुख या न्यूनतम लक्षण वाले कैटरेट-प्रतिरोधी मेटास्टेटिक प्रोस्टेट कैंसर वाले पुरुषों के उपचार के लिए स्वीकृत| journal = Human Vaccines & Immunotherapeutics | volume = 8 | issue = 4 | pages = 534–39 | date = April 2012 | pmid = 22832254 | doi = 10.4161/hv.19795 | doi-access = free }}</ref><ref>{{cite journal | vauthors = Oudard S | title = उन्नत प्रोस्टेट कैंसर के लिए उभरते उपचारों में प्रगति| journal = Cancer Treatment Reviews | volume = 39 | issue = 3 | pages = 275–89 | date = May 2013 | pmid = 23107383 | doi = 10.1016/j.ctrv.2012.09.005 }}</ref><ref>{{cite journal | vauthors = Sims RB | title = सिपुलेसेल-टी का विकास: मेटास्टैटिक कैस्ट्रेट प्रतिरोधी प्रोस्टेट कैंसर के उपचार के लिए ऑटोलॉगस सेलुलर इम्यूनोथेरेपी| journal = Vaccine | volume = 30 | issue = 29 | pages = 4394–97 | date = June 2012 | pmid = 22122856 | doi = 10.1016/j.vaccine.2011.11.058 | doi-access = free }}</ref><ref>{{cite journal | vauthors = Shore ND, Mantz CA, Dosoretz DE, Fernandez E, Myslicki FA, McCoy C, Finkelstein SE, Fishman MN | title = कैस्ट्रेशन-प्रतिरोधी प्रोस्टेट कैंसर के इम्यूनोलॉजिक उपचार के लिए सिपुलेसेल-टी पर निर्माण| journal = Cancer Control | volume = 20 | issue = 1 | pages = 7–16 | date = January 2013 | pmid = 23302902 | doi = 10.1177/107327481302000103 | doi-access = free }}</ref> | ||
=== CAR-T कोशिका उपचार === | === CAR-T कोशिका उपचार === | ||
| Line 293: | Line 293: | ||
एक अन्य दृष्टिकोण एक स्वस्थ दाता से अगुणित γδ T कोशिकाओं या Nk कोशिकाओं का दत्तक हस्तांतरण है।<ref>{{cite journal | vauthors = Barros MS, de Araújo ND, Magalhães-Gama F, Pereira Ribeiro TL, Alves Hanna FS, Tarragô AM, Malheiro A, Costa AG | display-authors = 6 | title = γδ टी सेल फॉर ल्यूकेमिया इम्यूनोथेरेपी: न्यू एंड एक्सपेंडिंग ट्रेंड्स| journal = Frontiers in Immunology | volume = 12 | pages = 729085 | date = 22 September 2021 | pmid = 34630403 | doi = 10.3389/fimmu.2021.729085 | pmc = 8493128 | doi-access = free }}</ref> इस दृष्टिकोण का प्रमुख लाभ यह है कि ये कोशिकाएँ [[GVHD]] का कारण नहीं बनती हैं। स्थानांतरित कोशिकाओं का नुकसान प्रायः बिगड़ा हुआ कार्य है।<ref name="pmid = 24528541">{{cite journal | vauthors = Wilhelm M, Smetak M, Schaefer-Eckart K, Kimmel B, Birkmann J, Einsele H, Kunzmann V | title = सफल दत्तक हस्तांतरण और अगुणित γδ टी कोशिकाओं के विवो विस्तार में| journal = Journal of Translational Medicine | volume = 12 | pages = 45 | date = February 2014 | pmid = 24528541 | pmc = 3926263 | doi = 10.1186/1479-5876-12-45 }}</ref> | एक अन्य दृष्टिकोण एक स्वस्थ दाता से अगुणित γδ T कोशिकाओं या Nk कोशिकाओं का दत्तक हस्तांतरण है।<ref>{{cite journal | vauthors = Barros MS, de Araújo ND, Magalhães-Gama F, Pereira Ribeiro TL, Alves Hanna FS, Tarragô AM, Malheiro A, Costa AG | display-authors = 6 | title = γδ टी सेल फॉर ल्यूकेमिया इम्यूनोथेरेपी: न्यू एंड एक्सपेंडिंग ट्रेंड्स| journal = Frontiers in Immunology | volume = 12 | pages = 729085 | date = 22 September 2021 | pmid = 34630403 | doi = 10.3389/fimmu.2021.729085 | pmc = 8493128 | doi-access = free }}</ref> इस दृष्टिकोण का प्रमुख लाभ यह है कि ये कोशिकाएँ [[GVHD]] का कारण नहीं बनती हैं। स्थानांतरित कोशिकाओं का नुकसान प्रायः बिगड़ा हुआ कार्य है।<ref name="pmid = 24528541">{{cite journal | vauthors = Wilhelm M, Smetak M, Schaefer-Eckart K, Kimmel B, Birkmann J, Einsele H, Kunzmann V | title = सफल दत्तक हस्तांतरण और अगुणित γδ टी कोशिकाओं के विवो विस्तार में| journal = Journal of Translational Medicine | volume = 12 | pages = 45 | date = February 2014 | pmid = 24528541 | pmc = 3926263 | doi = 10.1186/1479-5876-12-45 }}</ref> | ||
=== प्रति-CD[[सीडी47|47]] उपचार === | === प्रति-CD[[सीडी47|47]] उपचार === | ||
| Line 425: | Line 425: | ||
{{Chemotherapeutic agents}} | {{Chemotherapeutic agents}} | ||
{{Breakthrough of the Year}} | {{Breakthrough of the Year}} | ||
[[Category:All articles with unsourced statements]] | |||
[[Category: | [[Category:Articles with hatnote templates targeting a nonexistent page]] | ||
[[Category:Articles with invalid date parameter in template]] | |||
[[Category:Articles with short description]] | |||
[[Category:Articles with unsourced statements from December 2019]] | |||
[[Category:Articles with unsourced statements from July 2019]] | |||
[[Category:CS1 English-language sources (en)]] | |||
[[Category:CS1 errors]] | |||
[[Category:CS1 français-language sources (fr)]] | |||
[[Category:CS1 maint]] | |||
[[Category:CS1 Ελληνικά-language sources (el)]] | |||
[[Category:Citation Style 1 templates|W]] | |||
[[Category:Collapse templates]] | |||
[[Category:Created On 11/12/2022]] | [[Category:Created On 11/12/2022]] | ||
[[Category:Vigyan Ready]] | [[Category:Machine Translated Page]] | ||
[[Category:Navigational boxes| ]] | |||
[[Category:Navigational boxes without horizontal lists]] | |||
[[Category:Pages with broken file links]] | |||
[[Category:Pages with reference errors]] | |||
[[Category:Pages with script errors]] | |||
[[Category:Short description with empty Wikidata description]] | |||
[[Category:Sidebars with styles needing conversion]] | |||
[[Category:Template documentation pages|Documentation/doc]] | |||
[[Category:Templates Vigyan Ready]] | |||
[[Category:Templates based on the Citation/CS1 Lua module]] | |||
[[Category:Templates generating COinS|Cite web]] | |||
[[Category:Templates generating microformats]] | |||
[[Category:Templates that are not mobile friendly]] | |||
[[Category:Templates used by AutoWikiBrowser|Cite web]] | |||
[[Category:Templates using TemplateData]] | |||
[[Category:Use dmy dates from December 2018]] | |||
[[Category:Wikipedia articles needing clarification from April 2016]] | |||
[[Category:Wikipedia articles needing page number citations from February 2018]] | |||
[[Category:Wikipedia fully protected templates|Cite web]] | |||
[[Category:Wikipedia metatemplates]] | |||
[[Category:इम्यूनोलॉजी की शाखाएं]] | |||
[[Category:कैंसर इम्यूनोथेरेपी| ]] | |||
[[Category:ट्यूमर के लिए मोनोक्लोनल एंटीबॉडी]] | |||
Revision as of 18:09, 22 December 2022
| कैंसर इम्यूनोथेरेपी | |
|---|---|
| File:रिट्क्सिमाब FAB के लिए पेप्टाइड बाध्य.png |
कैंसर प्रतिरक्षा चिकित्सा (कभी-कभी प्रतिरक्षित-ऑन्कोलॉजी कहा जाता है) कैंसर का इलाज करने के लिए प्रतिरक्षा प्रणाली की उत्तेजना है, जिससे रोग से लड़ने की प्रतिरक्षा प्रणाली की प्राकृतिक क्षमता में सुधार होता है। यह कैंसर प्रतिरक्षा विज्ञान के बुनियादी शोध और कैंसर विज्ञान की बढ़ती उप-विशिष्टता का एक अनुप्रयोग है।
कैंसर रोगक्षमता चिकित्सा इस तथ्य का फायदा उठाती है कि कैंसर कोशिकाओं में प्रायः उनकी सतह पर अर्बुद प्रतिजन, अणु होते हैं जिन्हें प्रतिरक्षा प्रणाली के रोगप्रतिकारक प्रोटीन द्वारा पता लगाया जा सकता है, जो उन्हें बांधता है। अर्बुद प्रतिजन प्रायः प्रोटीन या अन्य वृहत् अणु (जैसे, कार्बोहाइड्रेट) होते हैं। सामान्य रोगप्रतिकारक बाहरी रोगजनकों से बंधते हैं, लेकिन संशोधित रोगक्षमता चिकित्सा रोगप्रतिकारक अर्बुद प्रतिजन को बांधते हैं और प्रतिरक्षा प्रणाली को रोकने या मारने के लिए कैंसर कोशिकाओं की पहचान करते हैं। कैंसर रोगक्षमता चिकित्सा की नैदानिक सफलता कैंसर के विभिन्न रूपों के बीच अत्यधिक परिवर्तनशील है; उदाहरण के लिए, अमाशय का कैंसर के कुछ उपप्रकार दृष्टिकोण के लिए अच्छी तरह से प्रतिक्रिया करते हैं जबकि रोगक्षमता चिकित्सा अन्य उपप्रकारों के लिए प्रभावी नहीं है।[1]
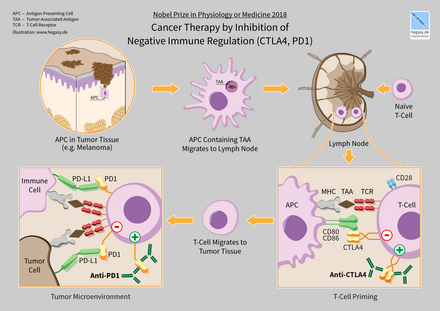
2018 में, अमेरिकी प्रतिरक्षाविज्ञानी जेम्स पी. एलिसन और जापानी प्रतिरक्षाविज्ञानी तासुकु होन्जो को नकारात्मक प्रतिरक्षित नियन्त्रण के अवरोधन द्वारा कैंसर उपचार की खोज के लिए जीवन पद्वति या औषधि में नोबेल पुरस्कार मिला।[2]
इतिहास
17वीं और 18वीं शताब्दी के दौरान, कैंसर में रोगक्षमता चिकित्सा के विभिन्न रूप व्यापक हो गए। 18वीं और 19वीं शताब्दी में, व्रणकारी अर्बुद को बंद करने वाली पूतिक मरहमपट्टी का उपयोग कैंसर के उपचार के लिए किया जाता था। संक्रमण के विकास को सुविधाजनक बनाने के लिए शल्यक घावों को खुला छोड़ दिया गया था, और मवाद वाले घावों को जानबूझकर बनाया गया था। 1891 में कैंसर पर सूक्ष्मजीवों के सबसे प्रसिद्ध प्रभावों में से एक बताया गया, जब एक अमेरिकी सर्जन विलियम कोली ने टीका लगाया था। [स्ट्रेप्टोकोकस पाइोजेन्स] के साथ निष्क्रिय अर्बुद वाले रोगी[3] कोली [था] ने उस समय उपलब्ध साहित्य की पूरी तरह से समीक्षा की और आकस्मिक या चिकित्साजन्य ज्वरग्रस्त विसर्प वाले कैंसर रोगियों की 38 रिपोर्टें पाईं। 12 रोगियों में, पिशितार्बुद या कर्कट पूरी तरह से गायब हो गया था; दूसरों में काफी सुधार हुआ था। कोली ने चिकित्साजन्य विसर्प के उपचारात्मक उपयोग का प्रयास करने का निर्णय लिया...[4] कोली ने एक विष विकसित किया जिसमें गर्मी से मारे गए किटाणु [रोगाणु पूयन और सेराटिया शुष्कप्राय] सम्मिलित थे। 1963 तक, इस उपचार का उपयोग मांसार्बुद के उपचार के लिए किया जाता था।[3] Coley ने 1000 से अधिक कैंसर रोगियों को किटाणु या जीवाणु उत्पादों के साथ इंजेक्शन लगाया।[5] 51.9% [कोली के] रोगियों में निष्क्रिय नरम-ऊतक मांसार्बुद ने पूर्ण अर्बुद प्रतिगमन दिखाया और 5 से अधिक वर्षों तक जीवित रहे, और 21.2% रोगियों में इस उपचार के कम से कम 20 वर्षों के बाद अर्बुद का कोई नैदानिक प्रमाण नहीं था ...[3] 20वीं शताब्दी में तुलाने यूनिवर्सिटी स्कूल ऑफ मेडिसिन में डॉ. मारिया ओ'कॉनर हॉर्नुंग के नेतृत्व में अनुसंधान जारी रहा[6][7]
श्रेणियां
रोगक्षमता चिकित्सा को सक्रिय या निष्क्रिय के रूप में वर्गीकृत किया जा सकता है। सक्रिय रोगक्षमता चिकित्सा विशेष रूप से प्रतिरक्षा प्रणाली के माध्यम से अर्बुद कोशिकाओं को लक्षित करती है। उदाहरणों में चिकित्सीय कैंसर के टीके CAR-T कोशिका, और लक्षित रोगप्रतिकारक उपचार सम्मिलित हैं (जिन्हें उपचार के टीके के रूप में भी जाना जाता है,[8] जिसे कैंसर से लड़ने के लिए शरीर की प्रतिरक्षा प्रणाली को बढ़ावा देने के लिए परिकलन किया गया है)। इसके विपरीत, निष्क्रिय रोगक्षमता चिकित्सा सीधे अर्बुद कोशिकाओं को लक्षित नहीं करती है, लेकिन कैंसर कोशिकाओं पर हमला करने के लिए प्रतिरक्षा प्रणाली की क्षमता को बढ़ाती है। उदाहरणों चेकप्वाइंट निरोधक और कोशिका द्रव्य विभाजन सम्मिलित हैं।
सक्रिय कोशिकीय उपचारों का उद्देश्य प्रतिजन के रूप में ज्ञात विशिष्ट अनुचिह्नक की पहचान करके कैंसर कोशिकाओं को नष्ट करना है। कैंसर के टीकों में, एक टीके के माध्यम से इन प्रतिजनों के प्रति प्रतिरक्षा प्रतिक्रिया उत्पन्न करने का लक्ष्य होता है। वर्तमान में, केवल एक टीका (प्राँस्टैट कैंसर के लिए सिपुलेकोशिका-T) को मंजूरी दी गई है। CAR-T कोशिका उपचार जैसे कोशिका-मध्यस्थ चिकित्सा में, रोगी से प्रतिरक्षा कोशिकाओं को निकाला जाता है, अर्बुद विशिष्ट प्रतिजन को पहचानने के लिए आनुवंशिक रूप से अभियन्ता किया जाता है, और रोगी को वापस कर दिया जाता है। कोशिका जो इस तरह से इस्तेमाल किए जा सकते हैं वे हैं प्राकृतिक मारक (NK) कोशिका, लिम्फोकाइन-सक्रिय मारक कोशिका, कोशिका विषी T कोशिका और द्रुमिका कोशिका अंत में, विशिष्ट रोगप्रतिकारक विकसित किए जा सकते हैं जो कैंसर कोशिकाओं को पहचानते हैं और उन्हें प्रतिरक्षा प्रणाली द्वारा विनाश के लिए लक्षित करते हैं। इस तरह के रोगप्रतिकारक के उदाहरणों में सम्मुचयुक्सीमब (CD-20 को लक्षित करना), ट्रैस्टुजुमाब (HER-2 को लक्षित करना) और सम्मुचयुक्सीमैब (EGFR को लक्षित करना) सम्मिलित हैं।
निष्क्रिय रोगप्रतिकारक उपचारों का उद्देश्य विशेष रूप से कैंसर कोशिकाओं को लक्षित किए बिना प्रतिरक्षा प्रणाली की गतिविधि को बढ़ाना है। उदाहरण के लिए, कोशिका द्रव्य विभाजन सीधे प्रतिरक्षा प्रणाली को उत्तेजित करते हैं और प्रतिरक्षा गतिविधि को बढ़ाते हैं। चेकप्वाइंट अवरोधक प्रोटीन (प्रतिरक्षा चेकप्वाइंट) को लक्षित करते हैं जो सामान्य रूप से प्रतिरक्षा प्रतिक्रिया को कम कर देते हैं। यह कैंसर कोशिकाओं पर हमला करने की प्रतिरक्षा प्रणाली की क्षमता को बढ़ाता है। वर्तमान शोध प्रतिरक्षा कार्य को बढ़ाने के लिए नए संभावित लक्ष्यों की पहचान कर रहा है। स्वीकृत चेकपॉइंट निरोधक में रोगप्रतिकारक जैसे कि इपिलीमुमाब, निवोलुमाब और पेम्ब्रोलिज़ुमाब सम्मिलित हैं।
कोशिकीय रोगक्षमता चिकित्सा
द्रुमिका कोशिका उपचार
द्रुमिका कोशिका उपचार लसीकाणुओं के लिए अर्बुद प्रतिजन पेश करने के लिए द्रुमिका कोशिकाओं के कारण प्रति-अर्बुद प्रतिक्रियाओं को भड़काती है, जो उन्हें सक्रिय करती है, प्रतिजन पेश करने वाली अन्य कोशिकाओं को मारने के लिए उन्हें भड़काती है। स्तनधारी प्रतिरक्षा प्रणाली में वृक्ष के समान कोशिकाएं प्रतिजन पेश करने वाली कोशिकाएं (APCs) हैं।[9] कैंसर के उपचार में वे कैंसर प्रतिजन लक्ष्यीकरण में सहायता करते हैं।[10] द्रुमिका कोशिकाओं पर आधारित एकमात्र स्वीकृत कोशिकीय कैंसर उपचार सिपुलेकोशिका-T है।
अर्बुद प्रतिजन पेश करने के लिए द्रुमिका कोशिकाओं को प्रेरित करने का एक तरीका स्वजात अर्बुद अपघट्य [11] या छोटे पेप्टाइड्स (प्रोटीन के छोटे हिस्से जो कैंसर कोशिकाओं पर प्रोटीन प्रतिजन के अनुरूप होते हैं) के साथ टीकाकरण है।। इन पेप्टाइड्स को प्रायः प्रतिरक्षा और प्रति-अर्बुद प्रतिक्रियाओं को बढ़ाने के लिए सहायक (अत्यधिक इम्युनोजेनिक पदार्थ) के संयोजन में दिया जाता है। अन्य सहायक में प्रोटीन या अन्य रसायन सम्मिलित होते हैं जो द्रुमिका कोशिकाओं को आकर्षित और / या सक्रिय करते हैं, जैसे कि कणिकाणु बृहत्भक्षकाणु उपनिवेश-उत्तेजक कारक (GM-CSF)। आक्रामक ब्रेन अर्बुद के रूप में ग्लयोब्लास्टोमा (GBM) में द्रुमिका कोशिका टीका के लिए उपयोग किए जाने वाले प्रतिजन का सबसे सामान्य स्रोत संपूर्ण अर्बुद अपघट्य, CMV प्रतिजन RNA और अर्बुद से जुड़े पेप्टाइड्स जैसे EGFRvIII थे।[12]
ट्यूमर कोशिकाओं को GM-CSF व्यक्त करके विवो में डेंड्राइटिक कोशिकाओं को भी सक्रिय किया जा सकता है। यह जीएम-सीएसएफ का उत्पादन करने के लिए आनुवंशिक रूप से इंजीनियरिंग ट्यूमर कोशिकाओं द्वारा या जीएम-सीएसएफ को व्यक्त करने वाले ओंकोलिटिक वायरस के साथ ट्यूमर कोशिकाओं को संक्रमित करके प्राप्त किया जा सकता है।
एक अन्य रणनीति रोगी के रक्त से डेंड्राइटिक कोशिकाओं को निकालना और उन्हें शरीर के बाहर सक्रिय करना है। डेंड्राइटिक कोशिकाएं ट्यूमर एंटीजन की उपस्थिति में सक्रिय होती हैं, जो एकल ट्यूमर-विशिष्ट पेप्टाइड/प्रोटीन या ट्यूमर सेल लाइसेट (टूटी हुई ट्यूमर कोशिकाओं का समाधान) हो सकता है। ये कोशिकाएं (वैकल्पिक सहायक के साथ) संक्रमित होती हैं और एक प्रतिरक्षा प्रतिक्रिया को उत्तेजित करती हैं।
डेंड्राइटिक सेल थेरेपी में एंटीबॉडी का उपयोग शामिल है जो डेंड्राइटिक कोशिकाओं की सतह पर रिसेप्टर्स को बांधता है। एंटीजन को एंटीबॉडी में जोड़ा जा सकता है और डेंड्राइटिक कोशिकाओं को परिपक्व होने और ट्यूमर को प्रतिरक्षा प्रदान करने के लिए प्रेरित कर सकता है। टीएलआर3, टीएलआर7, टीएलआर8 या सीडी 40 जैसे डेंड्रिटिक सेल रिसेप्टर्स को एंटीबॉडी लक्ष्य के रूप में इस्तेमाल किया गया है।[10]इम्यूनोथेरेपी में डेंड्राइटिक सेल-एनके सेल इंटरफेस की भी महत्वपूर्ण भूमिका है। नई डेंड्राइटिक सेल-आधारित टीकाकरण रणनीतियों के डिजाइन में एनके सेल-उत्तेजक क्षमता भी शामिल होनी चाहिए। एंटीट्यूमर डीसी-आधारित नैदानिक परीक्षणों में परिणाम के रूप में एनके कोशिकाओं की निगरानी को व्यवस्थित रूप से शामिल करना महत्वपूर्ण है।[citation needed]
ड्रग्स
Sipuleucel-T (बदला) को 2010 में स्पर्शोन्मुख या न्यूनतम रोगसूचक मेटास्टैटिक कैस्ट्रेशन-प्रतिरोधी प्रोस्टेट कैंसर के उपचार के लिए अनुमोदित किया गया था। उपचार में ल्यूकेफेरेसिस द्वारा रक्त एंटीजन-प्रेजेंटिंग सेल कोशिकाओं को हटाना और उन्हें GM- से बने संलयन प्रोटीन PA2024 के साथ बढ़ाना शामिल है। CSF और प्रोस्टेट-विशिष्ट प्रोस्टेटिक एसिड फॉस्फेट (PAP) और पुन: उपयोग किया जाता है। यह प्रक्रिया तीन बार दोहराई जाती है।[13][14][15][16]
CAR-T कोशिका उपचार
CAR-T रोगक्षमता चिकित्सा का आधार कैंसर कोशिकाओं को अधिक प्रभावी ढंग से लक्षित करने और उन्हें नष्ट करने के लिए T कोशिकाओं को संशोधित करना है। वैज्ञानिक लोगों से T कोशिकाओं को निकालते हैं, आनुवंशिक रूप से उन्हें एक असाध्य प्रतिजन ग्राही (CAR) जोड़ने के लिए बदलते हैं जो विशेष रूप से कैंसर कोशिकाओं को पहचानता है, फिर परिणामी CAR-T कोशिकाओं को रोगियों में उनके अर्बुद पर हमला करने के लिए संक्रमित करता है।
स्वीकृत दवाएं
टीसाजेनलेकलेउकोशिका ( केरिया), एक असाध्य प्रतिजन ग्राही (CAR-T) उपचार है, जिसे अत्यधिक लिम्फोब्लासटिक श्वेताणु रक्तता (ALL) के इलाज के लिए 2017 में FDA द्वारा अनुमोदित किया गया था।[17] यह उपचार शरीर से CD19 सकारात्मक कोशिकाओं (B-कोशिकाओं) को हटा देता है (रोगग्रस्त कोशिकाओं सहित, लेकिन सामान्य रोगप्रतिकारक उत्पादक कोशिकाएं भी)।
एक्सिकैबटेजीन सिलोल्यूकोशिका (यसकार्टा) एक अन्य CAR-T चिकित्सीय है, जिसे 2017 में बड़े B-कोशिका लसीकाबुर्दको फैलाना (DLBCL) के उपचार के लिए अनुमोदित किया गया है।[18]
T कोशिका ग्राही T कोशिका उपचार
TCR-T उपचार प्रमुख विषमद्वितय जटिल-प्रस्तुत पेप्टाइड अंश अणुओं को पहचानने के लिए अल्फा और बीटा पेप्टाइड श्रृंखलाओं से बने प्रोटीन डिमर का उपयोग करते हैं। CAR-T के कोशिका सतह प्रतिजन के विपरीत, TCR-T अंतःकोशिकी प्रतिजन अंशों के उस बड़े सम्मुचय को पहचान सकता है। हालांकि, TCR-T कोशिका उपचार MHC अणुओं पर निर्भर करती है, जिससे इसकी उपयोगिता सीमित हो जाती है।[19]
T कोशिका अभियान्त्रिकी और अवमुक्त के लिए बहुक्रियाशील एल्गिनेट मचान
T कोशिका अभियान्त्रिकी और अवमुक्त के लिए बहुआयामी एल्गिनेट मचान सीटू अभियान्त्रिकी, प्रतिकृति और आनुवंशिक रूप से अभियन्ता T कोशिकाओं की रिहाई के लिए एक तकनीक है। यह काल्पनिक प्रतिजन ग्राही T कोशिका उपचार का विकास है। T कोशिकाओं को रोगी से निकाला जाता है और आनुवंशिक रूप से अभियन्ता विषाणु के साथ मिलाया जाता है जिसमें कैंसर लक्ष्यीकरण प्त्रैक होता है (CAR T के साथ)। फिर मिश्रण को एक विशारद (मचान) में जोड़ा जाता है, जो उन्हें अवशोषित करता है। विशारद में रोगप्रतिकारकहोते हैं जो T कोशिकाओं और इंटरल्यूकिन को सक्रिय करते हैं जो कोशिका प्रसार को ट्रिगर करते हैं। विशारद को तब रोगी में प्रत्यारोपित किया जाता है। सक्रिय T कोशिकाएं CAR T कोशिकाएं बनने के लिए विषाणु को प्रभावित करती हैं। इंटरल्यूकिन्स इन CAR T कोशिकाओं को बढ़ने के लिए उत्तेजित करते हैं, और CAR T कोशिकाएं कैंसर पर हमला करने के लिए विशारद से बाहर निकलती हैं। तकनीक में हफ्तों के बजाय घंटों का समय लगता है। और क्योंकि कोशिकाएं छोटी होती हैं, वे शरीर में लंबे समय तक रहती हैं, कैंसर के खिलाफ मजबूत शक्ति दिखाती हैं, और थकावट के कम अनुचिह्नक प्रदर्शित करती हैं। इन विशेषताओं को चूहे प्रतिरूप में प्रदर्शित किया गया था। लसीकाबुर्द के खिलाफ उपचार अधिक प्रभावी और लंबे समय तक चलने वाला था।[20][21]
रोगप्रतिकारक उपचार
रोगप्रतिकारक अनुकूली प्रतिरक्षा प्रणाली का एक प्रमुख घटक है, जो बाह्री प्रतिजन को पहचानने और प्रतिरक्षा प्रतिक्रिया को उत्तेजित करने में केंद्रीय भूमिका निभाता है। रोगप्रतिकारक Y-आकार के प्रोटीन होते हैं जो कुछ B कोशिकाओं द्वारा निर्मित होते हैं और दो क्षेत्रों से बने होते हैं: एक खंड प्रतिजन-बाध्यकारी, प्रतिजन-बाध्यकारी (Fab), जो प्रतिजन को बांधता है, और खंड क्रिस्टलीय क्षेत्र, जो बृहत्भक्षकाणु, उदासीनरागी और NK कोशिकाओं सहित विभिन्न प्रतिरक्षा कोशिका प्रकारों की सतह पर व्यक्त तथाकथित Fc ग्राही्स के साथ बातचीत करता है। कई प्रतिरक्षा चिकित्सा पथ्यापथ्य नियम में रोगप्रतिकारक सम्मिलित हैं। एकक्लोनी प्रतिरक्षी प्रौद्योगिकी अभियन्ता और विशिष्ट प्रतिजन के खिलाफ रोगप्रतिकारक उत्पन्न करते हैं, जैसे कि अर्बुद सतहों पर मौजूद है। ये रोगप्रतिकारक जो अर्बुद के प्रतिजन के लिए विशिष्ट हैं, फिर उन्हें अर्बुद में इंजेक्ट किया जा सकता है।
रोगप्रतिकारक प्रकार
संयुग्मन
कैंसर के उपचार में दो प्रकार का उपयोग किया जाता है:[22]
- नग्न एकक्लोनी प्रतिरक्षी जोड़े गए तत्वों के बिना रोगप्रतिकारक हैं। अधिकांश रोगप्रतिकारक उपचार इस रोगप्रतिकारक प्रकार का उपयोग करते हैं।
- संयुग्मित एकक्लोनी प्रतिरक्षी दूसरे अणु से जुड़े होते हैं, जो या तो कोशिका विषी या विघटनाभिक होते हैं। जहरीले रसायन सामान्यतः कीमोथेरपी दवाओं के रूप में उपयोग किए जाते हैं, लेकिन अन्य विषाक्त पदार्थों का उपयोग भी किया जा सकता है। रोगप्रतिकारक कैंसर कोशिका की सतहों पर विशिष्ट प्रतिजन को बांधता है, जिससे अर्बुद को उपचार निर्देशित किया जाता है। विघटनाभिक यौगिक- सहलग्न रोगप्रतिकारक को रेडियोलेबल कहा जाता है। केमोलेबेल्ड या इम्युनोटॉक्सिन रोगप्रतिकारक को क्रमशः रसोचिकित्सीय अणुओं या विषाक्त पदार्थों के साथ प्रचिह्न किया जाता है।[23]अनुसंधान ने एक प्रति-अर्बुद एकक्लोनी प्रतिरक्षी के लिए एक TLR-जैसे ग्राही के संयुग्मन का भी प्रदर्शन किया है।[24]
Fc क्षेत्र
Fc ग्राही को बांधने की Fc की क्षमता महत्वपूर्ण है क्योंकि यह रोगप्रतिकारक को प्रतिरक्षा प्रणाली को सक्रिय करने की अनुमति देती है। Fc क्षेत्र विविध हैं: वे कई उपप्रकारों में मौजूद हैं और इन्हें और संशोधित किया जा सकता है, उदाहरण के लिए ग्लाइकोसाइलीकरण नामक प्रक्रिया में शर्करा का संकलन। Fc क्षेत्र में परिवर्तन Fc ग्राही्स को संलग्न करने के लिए रोगप्रतिकारक की क्षमता को बदल सकते हैं और विस्तार से, रोगप्रतिकारक सक्रियकृत की प्रतिरक्षा प्रतिक्रिया के प्रकार को निर्धारित करेंगे।[25] उदाहरण के लिए, PD-1 को लक्षित करने वाले प्रतिरक्षा चेकपॉइंट अवरोधक T कोशिकाओं द्वारा व्यक्त Pd-1 को बांधने और अर्बुद को खत्म करने के लिए इन कोशिकाओं को पुन: सक्रिय करने के लिए प्रारुप किए गए रोगप्रतिकारक हैं।[26] प्रति-Pd-1 दवाओं में न केवल एक फैब क्षेत्र होता है जो Pd-1 को बांधता है बल्कि एक Fc क्षेत्र भी होता है। प्रायोगिक कार्य इंगित करता है कि कैंसर रोगक्षमता चिकित्सा दवाओं का Fc भाग उपचार के परिणाम को प्रभावित कर सकता है। उदाहरण के लिए, Fc क्षेत्रों के साथ प्रति-Pd-1 दवाएं जो निरोधात्मक Fc ग्राही को बांधती हैं वे चिकित्सीय प्रभावकारिता को कम कर सकती हैं।[27] प्रतिबिंबन अध्ययनों ने आगे दिखाया है कि प्रति-Pd-1 दवाओं का Fc क्षेत्र अर्बुद से जुड़े बृहत्भक्षकाणु द्वारा व्यक्त Fc ग्राही को बांध सकता है। यह प्रक्रिया दवाओं को उनके इच्छित लक्ष्य (यानी T कोशिकाओं की सतह पर व्यक्त Pd-1 अणु) से हटा देती है और चिकित्सीय प्रभावकारिता को सीमित कर देती है।[28] इसके अलावा, सह-उत्तेजक प्रोटीन CD40 को लक्षित करने वाले रोगप्रतिकारक को इष्टतम चिकित्सीय प्रभावकारिता के लिए चयनात्मक Fc ग्राही के साथ जुड़ाव की आवश्यकता होती है।[29] साथ में, ये अध्ययन रोगप्रतिकारक-आधारित प्रतिरक्षा जांच चौकी लक्ष्यीकरण रणनीतियों में Fc स्थिति के महत्व को रेखांकित करते हैं।
मानव/गैर-मानव रोगप्रतिकारक
रोगप्रतिकारक विभिन्न स्रोतों से आ सकते हैं, जिनमें मानव कोशिकाएं, चूहे और दोनों का संयोजन (काल्पनिक रोगप्रतिकारक) सम्मिलित हैं। रोगप्रतिकारक के विभिन्न स्रोत विभिन्न प्रकार की प्रतिरक्षा प्रतिक्रियाओं को भड़का सकते हैं। उदाहरण के लिए, मानव प्रतिरक्षा प्रणाली चूहे के रोगप्रतिकारक (जिसे मुरीन रोगप्रतिकारक के रूप में भी जाना जाता है) को पहचान सकती है और उनके खिलाफ प्रतिरक्षा प्रतिक्रिया को प्रेरित कर सकती है। यह उपचार के रूप में रोगप्रतिकारक की प्रभावशीलता को कम कर सकता है और प्रतिरक्षा प्रतिक्रिया का कारण बन सकता है। काल्पनिक रोगप्रतिकारक रोगप्रतिकारक के हिस्से को संबंधित मानव समकक्ष के साथ बदलकर मूषक रोगप्रतिकारक की प्रतिरक्षाजनकता को कम करने का प्रयास करते हैं। मानवकृत रोगप्रतिकारक लगभग पूरी तरह से मानव हैं; चर क्षेत्रों के केवल संपूरकता निर्धारित करने वाले क्षेत्र मूषक स्रोतों से प्राप्त होते हैं। असंशोधित मानव DNA का उपयोग करके मानव रोगप्रतिकारक का उत्पादन किया गया है।[23]
क्रिया का तंत्र
रोगप्रतिकारक-निर्भर कोशिका-मध्यस्थता कोशिका विषाक्तता (ADCC)
रोगप्रतिकारक-निर्भर कोशिका-मध्यस्थता कोशिका विषाक्तता (ADCC) को कोशिका सतहों को लक्षित करने के लिए बाध्य करने के लिए रोगप्रतिकारक की आवश्यकता होती है। रोगप्रतिकारक एक बाध्यकारी क्षेत्र (FAB) और Fc क्षेत्र से बनते हैं जिन्हें प्रतिरक्षा प्रणाली की कोशिकाओं द्वारा उनके Fc ग्राही के माध्यम से पता लगाया जा सकता है। Fc ग्राही Nk कोशिकाओं सहित कई प्रतिरक्षा प्रणाली कोशिकाओं पर पाए जाते हैं। जब Nk कोशिकाएं रोगप्रतिकारक-लेपित कोशिकाओं का सामना करती हैं, तो बाद के Fc क्षेत्र अपने Fc ग्राही के साथ बातचीत करते हैं, अर्बुद कोशिका को मारने के लिए पेर्फोरिन और ग्रैनजाइम B जारी करते हैं। उदाहरणों में रीटक्सिमैब, ओफातुमुमब, एलोटुजुमैब और आलेमतुजुमब सम्मिलित हैं। विकास के तहत रोगप्रतिकारक ने Fc क्षेत्रों को बदल दिया है जो एक विशिष्ट प्रकार के Fc ग्राही, FcγRIIIA के लिए उच्च संबंध रखते हैं, जो नाटकीय रूप से प्रभावशीलता में वृद्धि कर सकते हैं।[30][31]
पूरक सक्रियण
पूरक प्रणाली में रक्त प्रोटीन सम्मिलित होते हैं जो कोशिका की सतह पर रोगप्रतिकारक के बंधन के बाद कोशिका मृत्यु का कारण बन सकते हैं (पूरक सक्रियण के तरीकों के बीच शास्त्रीय पूरक मार्ग)। सामान्यतः प्रणाली बाह्री रोगजनकों से निपटती है, लेकिन कैंसर में उपचारात्मक रोगप्रतिकारक के साथ सक्रिय किया जा सकता है। यदि रोगप्रतिकारक काल्पनिक, मानवकृत या मानव है; जब तक इसमें IgG1 Fc क्षेत्र सम्मिलित है तब तक प्रणाली को प्रेरित किया जा सकता है। पूरक झिल्ली हमले परिसर के सक्रियण से कोशिका मृत्यु का कारण बन सकता है, जिसे पूरक-निर्भर कोशिका विषाक्तता; रोगप्रतिकारक-निर्भर कोशिका-मध्यस्थता कोशिका विषाक्तता की वृद्धि; और CR3-निर्भर कोशिकीय कोशिका विषाक्तता के रूप में जाना जाता है। पूरक-निर्भर कोशिका विषाक्तता तब होती है जब रोगप्रतिकारक कैंसर कोशिका की सतह से जुड़ते हैं, C1 संकुल इन रोगप्रतिकारक से जुड़ते हैं और बाद में कैंसर कोशिका झिल्ली में प्रोटीन छिद्र बन जाते हैं।[32]
अवरोधन
रोगप्रतिकारक उपचार प्रोटीन से जुड़कर और उन्हें अन्य प्रोटीन को प्रभावित करने से भौतिक रूप से अवरुद्ध करके भी कार्य कर सकते हैं। चेकप्वाइंट इनहिबिटर (CTLA-4, PD-1, और PD-L1) इस तंत्र द्वारा संचालित होते हैं। संक्षेप में, चेकप्वाइंट अवरोधक प्रोटीन होते हैं जो सामान्यतः प्रतिरक्षा प्रतिक्रिया को धीमा करने में मदद करते हैं और प्रतिरक्षा प्रणाली को सामान्य कोशिकाओं पर हमला करने से रोकते हैं। चेकप्वाइंट अवरोधक इन प्रोटीनों को बांधते हैं और उन्हें सामान्य रूप से कार्य करने से रोकते हैं, जिससे प्रतिरक्षा प्रणाली की गतिविधि बढ़ जाती है। उदाहरणों में दुर्वालूमब, आईपिलिमुमैब, निवोलुमैब और पेम्ब्रोलिज़ुमाब सम्मिलित हैं।
FDA-अनुमोदित रोगप्रतिकारक
| रोग प्रतिकारक | ब्राण्ड नाम | प्रकार | लक्ष्य | स्वीकृति तिथि | अनुमोदित उपचार |
|---|---|---|---|---|---|
| अलेमतुजुमाब | कैंपथ | मानवीकृत | CD52 | 2001 | B-कोशिका दीर्घकालिक लसीका श्वेत रक्तता (CLL)[34] |
| एटेज़ोलिज़ुमाब | टेसेंट्रिक | मानवीकृत | PD-L1 | 2016 | मलाशय का कैंसर[35] |
| एवेलुमाब | बावेंसियो | मानव | PD-L1 | 2017 | विक्षेपी मर्केल कोशिका कर्कट[36] |
| इपिलिमुमैब | यर्वॉय | मानव | CTLA4 | 2011 | विक्षेपी मिलैनोमा[37] |
| एलोटुजुमाब | एम्प्लिसीटी | मानवीकृत | SLAMF7 | 2015 | बहुल मज्जार्बुद[38] |
| ओफतुमुमाब | अरज़ेरा | मानव | CD20 | 2009 | दुर्दम्य CLL[39] |
| निवोलुमाब | ओपदिवो | मानव | PD-1 | 2014 | अयोग्य या विक्षेपी मेलेनोमा, पट्टक नॉन-स्मॉल कोशिका फेफड़े का कैंसर, गुर्दे संबंधी कोशिका कर्कट, कोलोरेक्टल कैंसर, हेपैटोकोशिकाुलर कर्कट, क्लासिकल हॉजकिन लसीकाबुर्द [40][41] |
| पेम्ब्रोलिज़ुमाब | कीट्रोडा | मानवीकृत | PD-1 | 2014 | अयोग्य या विक्षेपी मेलेनोमा, पट्टक नॉन-स्मॉल कोशिका फेफड़े का कैंसर, (NSCLC), हॉजकिन का लसीकाबुर्द, मर्केल-कोशिका कर्कट (MCC), प्राथमिक मध्यस्थानिका बी-कोशिका लसीकाबुर्द (PMBCL), पेट का कैंसर, सर्वाइकल कैंसर |
| रिट्क्सिमैब | ऋतुक्सन, मबथेरा | काल्पनिक | CD20 | 1997 | गैर - हॉजकिन लसीकाबुर्द[42] |
| दुर्वालुमाब | इम्फिनज़ी | मानव | PD-L1 | 2017 | मलाशय का कैंसर गैर-छोटे कोशिका फेफड़ों का कैंसर[43] |
अलेम्तुजुमाब
एलेमटुजुमाब (कैम्पथ-1एच) एक प्रति-CD52 मानवीकृत IGg1 एकक्लोनी प्रतिरक्षी है जो फ्लूडरबाइन- दुर्दम्य दीर्घकालिक लसकोशिका श्वेताणुरक्तता (CLL), त्वचीय T-कोशिका लसीकाबुर्द , परिधीय T-कोशिका लसीकाबुर्द और T-कोशिका प्रोलसकोशिका श्वेताणुरक्तता के उपचार के लिए संकेतित है। CD52 परिधीय रक्त लसीकाणुओं (दोनों T-कोशिकाओं और B-कोशिकाओं) और एककेंद्रक श्वेतकोशिका्स के 95% से अधिक पर पाया जाता है, लेकिन लसीकाणुओं में इसका कार्य अज्ञात है। यह CD52 से जुड़ता है और पूरक निर्धारण और ADCC तंत्र द्वारा इसके कोशिका विषी प्रभाव की शुरुआत करता है। रोगप्रतिकारक लक्ष्य (प्रतिरक्षा प्रणाली की कोशिकाएं) के कारण एलेमटुजुमाब उपचार की सामान्य जटिलताएं संक्रमण, विषाक्तता और अस्थिमज्जा दमन हैं।[44][45][46]
दुर्वालुमाब
दुर्वालुमाब (इम्फिनज़ी) एक मानव प्रतिरक्षा ग्लोबुलिन G1 कप्पा (IgG1κ) एकक्लोनी प्रतिरक्षी है जो PD-1 और CD80 (B7.1) अणुओं के साथ योजनाबद्ध कोशिका मृत्यु संलग्नी 1 (PD-L1) के पारस्परिक प्रभाव को रोकता है। दुर्वालुमाब स्थानीय रूप से उन्नत या विक्षेपी यूरोटेलियल कर्कट वाले मरीजों के इलाज के लिए अनुमोदित है:
- प्लैटिनम युक्त रसोचिकित्सा के दौरान या उसके बाद बीमारी बढ़ती है।
- प्लेटिनम युक्त रसोचिकित्सा के साथ नवसहायक या सहायक उपचार के 12 महीनों के भीतर रोग बढ़ता है।
16 फरवरी 2018 को, खाद्य एवं औषधि प्रशासन ने अयोग्य चरण III ग़ैर - लघु कोशिका फेफड़े का (NSCLC) वाले रोगियों के लिए दुर्वालुमैब को मंजूरी दी, जिनकी बीमारी समवर्ती प्लैटिनम-आधारित रसोचिकित्सा और विकिरण चिकित्सा के बाद आगे नहीं बढ़ी है।[47]
इपिलिमुमैब
इपिलिमुमैब (यर्वॉय) एक मानव IgG1 रोगप्रतिकारक है जो सतह प्रोटीन CTLA4 को बांधता है। सामान्य शरीरविज्ञान में T-कोशिकाएं दो संकेतों से सक्रिय होती हैं: T-कोशिका ग्राही एक प्रतिजन- प्रमुख MHC संकुल और T-कोशिका सतह ग्राही CD28 बाध्यकारी CD80 या CD86 प्रोटीन के लिए CTLA4 CD80 या CD86 से जुड़ता है, इन सतह प्रोटीनों के लिए CD28 के बंधन को रोकता है और इसलिए T-कोशिकाओं की सक्रियता को नकारात्मक रूप से नियंत्रित करता है।[48][49][50][51]
मेलेनोमा कोशिकाओं पर हमला करने के लिए प्रतिरक्षा प्रणाली के लिए सक्रिय कोशिका विषी T-कोशिकाओं की आवश्यकता होती है। सामान्य रूप से बाधित सक्रिय मेलेनोमा-विशिष्ट कोशिका विषी T-कोशिकाएं एक प्रभावी प्रति-अर्बुद प्रतिक्रिया उत्पन्न कर सकती हैं। इपिलिमुमैब प्रति-अर्बुद प्रतिक्रिया को बढ़ाने के लिए नियामक टी-कोशिकाओं को कोशिका विषी T-कोशिकाओं के अनुपात में बदलाव का कारण बन सकता है। नियामक T-कोशिकाएं अन्य T-कोशिकाओं को रोकती हैं, जिससे अर्बुद को फायदा हो सकता है।[48][49][50][51]
निवोलुमाब
निवोलुमाब एक मानव IgG4 रोगप्रतिकारक है जो PD-L1 या क्रमादेशित कोशिका मृत्यु 1 संलग्नी 2 (PD-L1 या PD-L2) के बंधन को अवरुद्ध करके T-कोशिका निष्क्रियता को रोकता है, कैंसर कोशिकाओं द्वारा व्यक्त प्रोटीन, क्रमादेशित कोशिका मृत्यु प्रोटीन 1 के साथ PD-1, एक प्रोटीन जो सक्रिय T-कोशिकाओं की सतह पर पाया जाता है।[52][53] निवोलुमाब का उपयोग उन्नत मेलेनोमा, विक्षेपी गुर्दे संबंधी कोशिका कर्कट, उन्नत फेफड़े के कैंसर, उन्नत सिर और गर्दन के कैंसर और हॉजकिन के लसीकाबुर्द में किया जाता है।[54]
ओफतुमुमाब
ओफतुमुमाब एक दूसरे युग का मानव IgG1 रोगप्रतिकारक है जो CD20 से जुड़ता है। इसका उपयोग दीर्घकालिक लसकोशिका श्वेताणुरक्तता (CLL) के उपचार में किया जाता है क्योंकि CLL की कैंसर कोशिकाएं सामान्यतः CD 20-व्यक्त B-कोशिकाएं होती हैं। रीटक्सिमैब के विपरीत, जो CD20 प्रोटीन के एक बड़े परिपथ से जुड़ता है, ओटाटुमुमैब एक अलग, छोटे परिपथ से जुड़ता है। यह उनकी विभिन्न विशेषताओं की व्याख्या कर सकता है। रीटक्सिमैब की तुलना में, ओफतुमुमाब कम प्रतिरक्षाजनत्व के साथ कम खुराक पर पूरक-निर्भर कोशिका विषाक्तता को प्रेरित करता है।[55][56]
पेम्ब्रोलिज़ुमाब
2019 तक, पेम्ब्रोलिज़ुमाब, जो PD-1, क्रमादेशित कोशिका मृत्यु प्रोटीन 1 को अवरुद्ध करता है, का उपयोग अंतःशिरा जलसेक के माध्यम से कुछ स्थितियों में निष्क्रिय या विक्षेपी मेलेनोमा, विक्षेपी गैर-छोटे कोशिका फेफड़ों के कैंसर (NSCLC) के इलाज के लिए किया गया है, दूसरी पंक्ति के रूप में सिर और गर्दन के स्क्वैमस कोशिका कर्कट (HNSCC) के लिए उपचार, प्लेटिनम आधारित प्रतिनोप्लास्टिक | प्लैटिनम-आधारित रसोचिकित्सा के बाद, और दुर्दम्य क्लासिक हॉजकिन के लसीकाबुर्द(cHL) वाले वयस्क और बाल रोगियों के उपचार के लिए।[57][58] यह यूरोटेलियल कर्कट, पेट के कैंसर और गर्भाशय ग्रीवा के कैंसर वाले कुछ रोगियों के लिए भी संकेत दिया गया है।[59]
रितुक्सिमैब
रितुक्सिमैब एक काल्पनिक मोनोक्लोनल IgG1 रोगप्रतिकारक है जो CD20 के लिए विशिष्ट है, जिसे इसके मूल रोगप्रतिकारक इब्रिट्यूमोमैब से विकसित किया गया है। इब्रिट्यूमोमैब की तरह, रीटक्सिमैब CD20 को लक्षित करता है, जिससे यह कुछ B-कोशिका दुर्दमताओं के इलाज में प्रभावी हो जाता है। इनमें आक्रामक और अकर्मण्य लसीकाबुर्द जैसे फैलाना बड़े B-कोशिका लसीकाबुर्द और पुटकीय लसीकाबुर्द और लेकिमिया जैसे B-कोशिका दीर्घकालिक लसकोशिका श्वेताणुरक्तता सम्मिलित हैं। हालाँकि CD20 का कार्य अपेक्षाकृत अज्ञात है, CD20 B-कोशिका सक्रियण में सम्मिलित एक कैल्शियम माध्यम हो सकता है। रोगप्रतिकारक की कार्रवाई का तरीका मुख्य रूप से ADCC और पूरक-मध्यस्थता कोशिका विषाक्तता के प्रेरण के माध्यम से होता है। अन्य तंत्रों में एपोप्टोसिस सम्मिलित है[clarification needed] और कोशिकीय विकास गिरफ्तारी। रितुक्सिमैब रसोचिकित्सा के लिए कैंसर की B-कोशिकाओं की संवेदनशीलता को भी बढ़ाता है।[60]<रेफरी नाम = प्लॉस्कर 2003 803–43 >Plosker GL, Figgitt DP (2003). "Rituximab: गैर-हॉजकिन के लिंफोमा और क्रोनिक लिम्फोसाइटिक ल्यूकेमिया में इसके उपयोग की समीक्षा". Drugs. 63 (8): 803–43. doi:10.2165/00003495-200363080-00005. PMID 12662126.</रेफरी>[61][62][63]
साइटोकिन उपचार
कोशिका द्रव्य विभाजन एक अर्बुद के भीतर मौजूद कई प्रकार की कोशिकाओं द्वारा निर्मित प्रोटीन होते हैं। वे प्रतिरक्षा प्रतिक्रियाओं को संशोधित कर सकते हैं। अर्बुद प्रायः उन्हें बढ़ने और प्रतिरक्षा प्रतिक्रिया को कम करने की अनुमति देने के लिए उन्हें नियोजित करता है। ये प्रतिरक्षा- स्वर बलाघात प्रभाव उन्हें प्रतिरक्षा प्रतिक्रिया को भड़काने के लिए औषधि के रूप में उपयोग करने की अनुमति देते हैं। सामान्यतः इस्तेमाल होने वाले दो कोशिका द्रव्य विभाजन इंटरफेरॉन और इंटरल्यूकिन हैं।[64] इंटरल्यूकिन-2 और इंटरफेरॉन-α कोशिका द्रव्य विभाजन, प्रोटीन हैं जो प्रतिरक्षा प्रणाली के व्यवहार को विनियमित और समन्वयित करते हैं। उनके पास प्रति-अर्बुद गतिविधि को बढ़ाने की क्षमता है और इस प्रकार निष्क्रिय कैंसर उपचार के रूप में इसका उपयोग किया जा सकता है। इंटरफेरॉन-α का उपयोग बालों वाली कोशिका श्वेताणुरक्तता, एड्स से संबंधित कपोसी के पिशितार्बुद, पुटकीय लसीकाबुर्द, दीर्घकालिक मज्जाभ श्वेताणुरक्तता और घातक मेलेनोमा के उपचार में किया जाता है। इंटरल्यूकिन-2 का इस्तेमाल मैलिग्नेंट मेलेनोमा और गुर्दे कोशिका कर्कट के इलाज में किया जाता है।[citation needed]
इंटरफेरॉन
इंटरफेरॉन प्रतिरक्षा प्रणाली द्वारा निर्मित होते हैं। वे सामान्यतः प्रति- विषाणुज प्रतिक्रिया में सम्मिलित होते हैं, लेकिन कैंसर के लिए भी इसका उपयोग होता है। वे तीन समूहों में आते हैं: इंटरफेरॉन टाइप I (IFNα और IFNβ), इंटरफेरॉन टाइप II (IFNγ) और टाइप III इंटरफेरॉन (IFNλ)। IFNα को बालों वाली कोशिका श्वेताणुरक्तता, एड्स से संबंधित कपोसी के पिशितार्बुद, कूपिक लसीकाबुर्द, दीर्घकालिक मज्जाभ श्वेताणुरक्तता और मेलेनोमा में उपयोग के लिए अनुमोदित किया गया है। टाइप I और II IFNs पर बड़े पैमाने पर शोध किया गया है और हालांकि दोनों प्रकार के प्रति-अर्बुद प्रतिरक्षा प्रणाली प्रभाव को बढ़ावा देते हैं, केवल I IFN प्रकार को चिकित्सकीय रूप से प्रभावी दिखाया गया है। IFNλ पशु प्रतिरूप में इसके प्रति-अर्बुद प्रभावों के लिए वचन देता है।[65][66]
टाइप I IFNs के विपरीत, इंटरफेरॉन गामा अभी तक किसी भी कैंसर के इलाज के लिए स्वीकृत नहीं है। हालांकि, जब इंटरफेरॉन गामा को मूत्राशय कर्कट और मेलेनोमा कैंसर वाले रोगियों को दिया गया तो उत्तरजीविता में सुधार देखा गया। डिम्बग्रंथि कर्कट के चरण 2 और 3 के रोगियों में सबसे आशाजनक परिणाम प्राप्त हुआ। कैंसर कोशिकाओं में IFN-गामा का कृत्रिम परिवेशीय अध्ययन अधिक व्यापक है और परिणाम IFN-गामा की प्रसार-रोधी गतिविधि का संकेत देते हैं, जो विकास अवरोध या कोशिका मृत्यु की ओर ले जाता है, जो सामान्यतः एपोप्टोसिस से लेकिन कभी-कभी ऑटोफैगी द्वारा प्रेरित होता है ।[67]
इंटरल्युकिन
इंटरल्यूकिन्स में प्रतिरक्षा प्रणाली प्रभावों की एक श्रृंखला होती है। इंटरल्यूकिन-2 का इस्तेमाल मैलिग्नेंट मेलेनोमा और गुर्दे संबंधी कोशिका कर्कट के इलाज में किया जाता है। सामान्य शरीरविज्ञान में यह प्रभावी T कोशिकाओं और T-नियामक कोशिकाओं दोनों को बढ़ावा देता है, लेकिन इसकी क्रिया का सटीक तंत्र अज्ञात है।[64][68]
संयोजन रोगक्षमता चिकित्सा
PD1 और CTLA4 निरोधक जैसे विभिन्न प्रतिरक्षा चिकित्सा का संयोजन अर्बुद-रोधी प्रतिक्रिया को बढ़ा सकता है जिससे टिकाऊ प्रतिक्रिया हो सकती है।[69][70]
प्रतिरक्षा चिकित्सा के साथ अर्बुद के अंशोच्छेदन चिकित्सा का संयोजन इम्यूनोस्टिम्युलेटिंग प्रतिक्रिया को बढ़ाता है और उपचारात्मक विक्षेपी कैंसर उपचार के लिए सहक्रियात्मक प्रभाव डालता है।[71]
औषधीय अभिकर्ता के साथ चेकप्वाइंट इम्यूनोथेरैपी के संयोजन में प्रतिक्रिया में सुधार करने की क्षमता होती है, और इस तरह के संयोजन उपचार नैदानिक जांच का एक उच्च जांच क्षेत्र है।[72] इम्यूनोस्टिम्युलेटरी दवाएं जैसे CSF-1R अवरोधक और TLR प्रचालक इस समायोजन में विशेष रूप से प्रभावी रहे हैं।[73][74]
पॉलीसेकेराइड-K
जापान के स्वास्थ्य, श्रम और कल्याण मंत्रालय ने 1980 के दशक में मशरूम, कोरिओलस वर्ण परिवर्ती से निकाले गए पॉलीसेकेराइड-K के उपयोग को मंजूरी दी, ताकि रसोचिकित्सा से गुजरने वाले रोगियों की प्रतिरक्षा प्रणाली को उत्तेजित किया जा सके। यह अमेरिका और अन्य न्यायालयों में एक आहार पूरक है।[75]
चिकित्सीय महत्व के लिए आनुवंशिक पूर्व-परीक्षण
प्रतिरक्षा चिकित्सा दवाओं में से कई की उच्च लागत और चिकित्सा बीमा कंपनियों की उनके नुस्खे के लिए प्राथमिक चुकौती करने की अनिच्छा के कारण, इन दवाओं की प्रभावशीलता का पूर्वानुमान लगाने का प्रयास करने के लिए विभिन्न परीक्षण विधियों का प्रस्ताव दिया गया है। PD-L1 प्रोटीन का पता लगाना कई रोगक्षमता चिकित्सा दवाओं के लिए अतिसंवेदनशील कैंसर का संकेत प्रतीत होता है, लेकिन शोध में पाया गया कि इस प्रोटीन की कमी या कैंसर के ऊतकों में इसका समावेश दोनों ही अनिर्णायक थे, कम समझ में आने वाली अलग-अलग मात्रा के कारण संक्रमित कोशिकाओं और ऊतकों के भीतर अलग-अलग समय और स्थानों के दौरान प्रोटीन है।[76][77][78]2018 में कुछ आनुवंशिक संकेत जैसे कि अर्बुद उत्परिवर्ती ज़िम्मेदारी (TMB, कैंसर कोशिका के DNA में एक लक्षित आनुवंशिक क्षेत्र के भीतर परिवर्तन की संख्या), और माइक्रोसेटेलाइट अस्थिरता (MSI, बिगड़ा हुआ DNA बेमेल की मात्रा जो संभावित परिवर्तन की ओर ले जाती है) को मंजूरी दी गई है, FDA द्वारा कुछ कैंसर के लिए रोगक्षमता चिकित्सा दवा के प्रभावी उपचार की संभावना के लिए अच्छे संकेतक के रूप में, लेकिन अनुसंधान अभी भी प्रगति पर है।[79][80] TMB पर आधारित रोगक्षमता चिकित्सा के लिए रोगी की प्राथमिकता अभी भी अत्यधिक विवादास्पद है।[81][82]
कुछ मामलों में FDA ने दवाओं के लिए आनुवंशिक परीक्षणों को मंजूरी दी है जो कुछ आनुवंशिक अनुचिह्नक के लिए विशिष्ट है। उदाहरण के लिए, FDA ने विक्षेपी मेलेनोमा के लिए BRAF (आनुवान्शिकी) से जुड़ी दवा को मंजूरी दे दी है, जिसे BRF आनुवंशिक उत्परिवर्तन के परीक्षण के बाद रोगियों को दिया जाना है।[83]
सामान्य कैंसर उपचार के लिए इस प्रकार के परीक्षण महंगे हैं और व्यापक रूप से विज्ञापित किए जा रहे हैं। अतीत में, कैंसर के उपचार के लिए कुछ अनुवांशिक परीक्षण अनिल पोट्टी जैसे घोटालों में सम्मिलित रहे हैं, या धोखाधड़ी होने का दावा किया गया है।[84][85][86]
अनुसंधान
दत्तक T-कोशिका उपचार
दत्तक T कोशिका उपचार T-कोशिकाओं (दत्तक कोशिका स्थानांतरण) के आधान द्वारा निष्क्रिय टीकाकरण का एक रूप है। वे रक्त और ऊतक में पाए जाते हैं और सामान्यतः तब सक्रिय होते हैं जब उन्हें बाह्री रोगजनक मिलते हैं। विशेष रूप से वे तब सक्रिय होते हैं जब टी-कोशिका की सतह के ग्राही्स कोशिकाओं का सामना करते हैं जो बाह्री प्रोटीन के कुछ हिस्सों को उनकी सतह के प्रतिजनों पर प्रदर्शित करते हैं। ये या तो संक्रमित कोशिकाएं या प्रतिजन- प्रत्यक्ष कोशिका (APCs) हो सकते हैं। वे सामान्य ऊतक और अर्बुद ऊतक में पाए जाते हैं, जहां उन्हें अर्बुद घुसपैठ करने वाले लसीकाणु (TIL) के रूप में जाना जाता है। वे APC's जैसे द्रुमिका कोशिकाओं की उपस्थिति से सक्रिय होते हैं जो अर्बुद प्रतिजन पेश करते हैं। हालांकि ये कोशिकाएं अर्बुद पर हमला कर सकती हैं, अर्बुद के भीतर का वातावरण अत्यधिक प्रतिरक्षादमनकारी है, जो प्रतिरक्षा-मध्यस्थ अर्बुद की मृत्यु को रोकता है।[87]
अर्बुद लक्षित T-कोशिकाओं के उत्पादन और प्राप्त करने के कई तरीके विकसित किए गए हैं। अर्बुद प्रतिजन के लिए विशिष्ट T-कोशिकाओं को अर्बुद के नमूने (TIL) से हटाया जा सकता है या रक्त से निस्यंदन किया जा सकता है। इसके बाद के सक्रियण और संवर्धन को पूर्व विवो में किया जाता है, जिसके परिणामों को फिर से जोड़ा जाता है। सक्रियण जीन उपचार के माध्यम से, या T कोशिकाओं को अर्बुद प्रतिजन के संपर्क में लाकर किया जा सकता है।
2014 तक, कई ACT क्लिनिकल परीक्षण चल रहे थे।[88][89][90][91][92] महत्वपूर्ण रूप से, 2018 के एक अध्ययन से पता चला है कि विक्षेपी मेलेनोमा वाले रोगियों में नैदानिक प्रतिक्रियाएं प्राप्त की जा सकती हैं, जो पिछले कई प्रतिरक्षा चिकित्सा के लिए प्रतिरोधी हैं।[93] 2017 में FDA द्वारा पहले 2 दत्तक T-कोशिका उपचार, टिसजेनलेक्ल्यूकोशिका और एक्सिकैबटेजीन सिलोल्यूकोशिका को मंजूरी दी गई थी।[94][18]
एक अन्य दृष्टिकोण एक स्वस्थ दाता से अगुणित γδ T कोशिकाओं या Nk कोशिकाओं का दत्तक हस्तांतरण है।[95] इस दृष्टिकोण का प्रमुख लाभ यह है कि ये कोशिकाएँ GVHD का कारण नहीं बनती हैं। स्थानांतरित कोशिकाओं का नुकसान प्रायः बिगड़ा हुआ कार्य है।[96]
प्रति-CD47 उपचार
मेजबान प्रतिरक्षा प्रणाली के प्रतिरक्षण निगरानी से बचने के लिए कई अर्बुद कोशिकाएं CD47 को अतिअभिव्यक्त करती हैं। CD47 अपने ग्राही संकेत-नियामक प्रोटीन अल्फा (SIRPα) को बांधता है और अर्बुद कोशिका के भक्षकोशिकता को कम करता है।[97] इसलिए, प्रति-CD47 उपचार का उद्देश्य अर्बुद कोशिकाओं की निकासी बहाल करना है। इसके अतिरिक्त, बढ़ते सबूत प्रति-सीडी47 उपचार के जवाब में अर्बुद प्रतिजन-विशिष्ट कोशिका-मध्यस्थता प्रतिरक्षा के रोजगार का समर्थन करते हैं।[98][99] कई चिकित्सीय विकसित किए जा रहे हैं, जिनमें प्रति-CD47 रोगप्रतिकारक, अभियन्ता डिकॉय ग्राही्स, प्रति-SIRPα रोगप्रतिकारक और द्विविशिष्ट अभिकर्ता सम्मिलित हैं।[98]2017 तक, ठोस और रुधिरविज्ञान दुर्दमताओं की विस्तृत श्रृंखला का चिकित्सकीय परीक्षण किया जा रहा था।[98][100]
प्रति-GD2 रोगप्रतिकारक
कोशिकाओं की सतह पर कार्बोहाइड्रेट प्रतिजन रोगक्षमता चिकित्सा के लक्ष्य के रूप में इस्तेमाल किया जा सकता है। GD2 एक गैंग्लियोसाइड है जो कई प्रकार के कैंसर कोशिका की सतह पर पाया जाता है जिसमें न्यूरोब्लास्टोमा, दृष्टिपटलकोरकार्बुद, मेलेनोमा, छोटे कोशिका फेफड़े का कैंसर, मस्तिष्क का अर्बुद, ऑस्टियो पिशितार्बुद, मांसपेशीगत सार्कोमा, इविंग का मांसार्बुद, वसा सार्कोमा, तंतु सार्कोमा, लेयोमायोसार्कोमा और अन्य नरम ऊतक पिशितार्बुद सम्मिलित हैं। यह सामान्यतः सामान्य ऊतकों की सतह पर व्यक्त नहीं होता है, जिससे यह रोगक्षमता चिकित्सा के लिए एक अच्छा लक्ष्य बन जाता है। 2014 तक, नैदानिक परीक्षण चल रहे थे।[101]
प्रतिरक्षा चौकियों
प्रतिरक्षा चौकियां प्रतिरक्षा प्रणाली के कार्य को प्रभावित करती हैं। प्रतिरक्षा चौकियां उत्तेजक या निरोधात्मक हो सकती हैं। प्रतिरक्षा प्रणाली के हमलों से खुद को बचाने के लिए अर्बुद इन चौकियों का उपयोग कर सकते हैं। वर्तमान में स्वीकृत चेकपॉइंट थैरेपी निरोधात्मक चेकपॉइंट ग्राही्स को अवरूध्द करती है। प्रतिरक्षा कोशिकाओं को संकेत देने वाली नकारात्मक प्रतिक्रिया की नाकाबंदी के परिणामस्वरूप अर्बुद के खिलाफ एक बढ़ी हुई प्रतिरक्षा प्रतिक्रिया होती है।[53] प्रतिरक्षित चेकपॉइंट नाकाबंदी उपचारों में विविध प्रभावशीलता होती है। हॉजकिन लसीकाबुर्द और प्राकृतिक किलर T-कोशिका लसीकाबुर्द में, प्रतिक्रिया की दर 50-60% अधिक होती है। हालाँकि, स्तन और प्रोस्टेट कैंसर के लिए प्रतिक्रिया दर काफी कम है।[102]
जांच के तहत एक संलग्नी-ग्राही पारस्परिक प्रभाव ट्रांसमेम्ब्रेन प्रोग्रामेड कोशिका डेथ 1 प्रोटीन (PDCD1, PD-1; जिसे CD279 के रूप में भी जाना जाता है) और इसके संलग्नी, [[क्रमादेशित कोशिका मृत्यु 1 संलग्नी 1]] | PD-1 संलग्नी 1 (PD-L1) के बीच का योजनाबद्ध है , CD 274)। कोशिका की सतह पर PD-L1 एक प्रतिरक्षा कोशिका की सतह पर PD1 से जुड़ता है, जो प्रतिरक्षा कोशिका गतिविधि को रोकता है। PD-L1 कार्यों में टी कोशिका गतिविधियों पर एक महत्वपूर्ण नियामक भूमिका है। ऐसा प्रतीत होता है कि (कैंसर-मध्यस्थता) कोशिका की सतह पर PD-L1 का अपरेगुलेशन T कोशिकाओं को बाधित कर सकता है जो अन्यथा हमला कर सकती हैं। कैंसर कोशिकाओं पर PD-L1 भी FAS- और इंटरफेरॉन-आश्रित एपोप्टोसिस को रोकता है, T कोशिकाओं द्वारा उत्पादित कोशिका विषी अणुओं से कोशिकाओं की रक्षा करता है। रोगप्रतिकारकजो या तो PD-1 या PD-L1 से बंधते हैं और इसलिए बातचीत को अवरुद्ध करते हैं, T-कोशिकाओं को अर्बुद पर हमला करने की अनुमति दे सकते हैं।[103]
CTLA-4 नाकाबंदी
FDA द्वारा अनुमोदित पहला चेकपॉइंट रोगप्रतिकारकipilimumab था, जिसे मेलेनोमा के उपचार के लिए 2011 में अनुमोदित किया गया था।[104] यह प्रतिरक्षा जांच चौकी अणु CTLA-4 को अवरुद्ध करता है। क्लिनिकल परीक्षणों ने फेफड़ों के कैंसर या अग्नाशय के कैंसर पर प्रति-CTLA -4 उपचार के कुछ लाभ भी दिखाए हैं, विशेष रूप से अन्य दवाओं के संयोजन में।[105][106] चल रहे परीक्षणों में पीडी-1 या पीडी-एल1 अवरोधकों के साथ सीटीएलए-4 नाकाबंदी के संयोजन का परीक्षण विभिन्न प्रकार के कैंसर पर किया जाता है।[107] हालांकि, चेक-पॉइंट नाकाबंदी (विशेष रूप से CTLA-4 ब्लॉकिंग रोगप्रतिकारक), या चेक-पॉइंट ब्लॉकिंग रोगप्रतिकारकके संयोजन के साथ इलाज किए गए रोगियों में प्रतिरक्षा संबंधी प्रतिकूल घटनाओं जैसे डर्माटोलॉजिक, गैस्ट्रोइंटेस्टाइनल, एंडोक्राइन, या यकृत ऑटोइम्युनिटी होने का उच्च जोखिम होता है। प्रतिक्रियाएँ।[52] जब प्रति-सीटीएलए-4 रोगप्रतिकारकको रक्त प्रवाह में इंजेक्शन द्वारा प्रशासित किया जाता है, तो प्रेरित टी-कोशिका सक्रियण की चौड़ाई के कारण ये सबसे अधिक संभावना होती हैं।
मूत्राशय के कैंसर के एक चूहे प्रतिरूप का उपयोग करते हुए, शोधकर्ताओं ने पाया है कि अर्बुद क्षेत्र में कम खुराक वाले प्रति-CTSL-4 के एक स्थानीय इंजेक्शन में अर्बुद को रोकने की क्षमता उतनी ही थी जितनी कि रक्त में रोगप्रतिकारक वितरित होने पर।[108] उसी समय परिसंचारी रोगप्रतिकारक के स्तर कम थे, यह सुझाव देते हुए कि प्रति- -4 उपचार के स्थानीय प्रशासन के परिणामस्वरूप कम प्रतिकूल घटनाएं हो सकती हैं।[108]
PD-1 अवरोधक
IgG4 PD1 रोगप्रतिकारक निवोलुमाब के साथ प्रारंभिक नैदानिक परीक्षण के परिणाम 2010 में प्रकाशित हुए थे।[53]इसे 2014 में मंजूरी दी गई थी। निवोलुमैब मेलेनोमा, फेफड़े के कैंसर, गुर्दे के कैंसर, मूत्राशय के कैंसर, सिर और गर्दन के कैंसर और हॉजकिन के लसीकाबुर्द के इलाज के लिए स्वीकृत है।[109] गैर-छोटे कोशिका फेफड़ों के कैंसर के लिए 2016 का नैदानिक परीक्षण पहली पंक्ति के समुच्चयन में उपचार के लिए अपने प्राथमिक समापन बिंदु को पूरा करने में विफल रहा, लेकिन FDA ने चिकित्सा की बाद की पंक्तियों में मंजूरी दे दी है।[110]
पेम्ब्रोलिज़ुमाब (कीट्रूडा) एक अन्य PD1 अवरोधक है जिसे 2014 में FDA द्वारा अनुमोदित किया गया था। पेम्ब्रोलिज़ुमाब को मेलेनोमा और फेफड़ों के कैंसर के इलाज के लिए अनुमोदित किया गया है।[109]
प्रारंभिक नैदानिक परीक्षणों में रोगप्रतिकारक BGB-A317 एक PD-1 अवरोधक (Fc गामा ग्राही को बाध्य नहीं करने के लिए अभिकल्पित किया गया) है।[111]
PD-L1 अवरोधक
मई 2016 में, PD-L1 अवरोधक एटेज़ोलिज़ुमाब[112] मूत्राशय के कैंसर के इलाज के लिए अनुमोदित किया गया था।
विकास में वर्तमान में प्रति-PD-L 1 रोगप्रतिकारक में एक निरोधात्मक प्रभाव के अलावा एवलुमाब और दुर्वालुमाब सम्मिलित है[113] ,[114] ।[115]
CIS
रोगक्षम-उपचार को बढ़ाने के अन्य तरीकों में तथाकथित आंतरिक चेकपॉइंट अवरोधों को लक्षित करना सम्मिलित है उदा। CISH (जीन)। कई कैंसर रोगी प्रतिरक्षा जांच चौकी नाकाबंदी का जवाब नहीं देते हैं। T कोशिका घुसपैठ को प्रोत्साहित करने वाले अतिरिक्त तर्कसंगत रूप से चयनित प्रति कैंसर उपचारों के साथ प्रतिरक्षा जांच चौकी नाकाबंदी के संयोजन से प्रतिक्रिया दर में सुधार किया जा सकता है। उदाहरण के लिए, लक्षित उपचार जैसे रेडियोउपचार, वास्कुलचर लक्ष्यीकरण एजेंट, और इम्युनोजेनिक रसोचिकित्सा[116] पशु प्रतिरूप में प्रतिरक्षा चेकपॉइंट नाकाबंदी प्रतिक्रिया में सुधार कर सकते हैं।
ऑनकोलिटिक विषाणु
एक ओंकोलिटिक विषाणु एक विषाणु है जो अधिमानतः कैंसर कोशिकाओं को संक्रमित करता है और मारता है। चूंकि संक्रमित कैंसर कोशिकाएं ओंकोलिसिस द्वारा नष्ट हो जाती हैं, वे शेष अर्बुद को नष्ट करने में मदद करने के लिए नए संक्रामक विषाणु कण या विषाणु छोड़ते हैं। ओंकोलिटिक विषाणु को न केवल अर्बुद कोशिकाओं के प्रत्यक्ष विनाश का कारण माना जाता है, बल्कि दीर्घकालिक रोगक्षमता चिकित्सा के लिए मेजबान प्रति-अर्बुद प्रतिरक्षा प्रतिक्रिया को उत्तेजित करने के लिए भी माना जाता है।[117][118][119]
प्रति-कैंसर एजेंटों के रूप में विषाणु की क्षमता को पहली बार बीसवीं सदी की शुरुआत में महसूस किया गया था, हालांकि समन्वित अनुसंधान प्रयास 1960 के दशक तक शुरू नहीं हुए थे। एडीनोविषाणु, रीओविषाणु, खसरा मोरबिलीविषाणु, हर्पीज सिंप्लेक्स, न्यूकैसल रोग विषाणु और टीकािया सहित कई विषाणु का अब नैदानिक रूप से ऑनकोलिटिक एजेंटों के रूप में परीक्षण किया गया है। T-Vec मेलेनोमा के उपचार के लिए पहला FDA-अनुमोदित ऑनकोलिटिक विषाणु है। कई अन्य ओंकोलिटिक विषाणु चरण II-III के विकास में हैं।[120]
बहुशर्करा्स
औषधीय मशरूम में पाए जाने वाले कुछ यौगिक, मुख्य रूप से पॉलीसेकेराइड, प्रतिरक्षा प्रणाली को विनियमित कर सकते हैं और इसमें कैंसर विरोधी गुण हो सकते हैं। उदाहरण के लिए, बीटा glucans | बीटा-ग्लूकेन्स जैसे लेंटिनन को बृहतभक्षककोशिका, Nk कोशिकाओं, T कोशिकाओं और प्रतिरक्षा प्रणाली कोशिका द्रव्य विभाजन को उत्तेजित करने के लिए प्रयोगशाला अध्ययनों में दिखाया गया है और नैदानिक परीक्षणों में प्रतिरक्षितोलॉजिक सहायक के रूप में जांच की गई है।[121]
नवप्रतिजन
कई अर्बुद परिवर्तन व्यक्त करते हैं। ये उत्परिवर्तन संभावित रूप से T कोशिका रोगक्षमता चिकित्सा में उपयोग के लिए नए लक्ष्य योग्य प्रतिजन (नियोएन्टीजेन्स) बनाते हैं। कैंसर के घावों में CD8+ T कोशिकाओं की उपस्थिति, जैसा कि RNA अनुक्रमण डेटा का उपयोग करके पहचाना गया है, एक उच्च अर्बुद परिवर्तनल बर्डन वाले अर्बुद में अधिक है। प्राकृतिक हत्यारे कोशिकाओं और T कोशिकाओं की साइटोलिटिक गतिविधि से जुड़े टेप का स्तर सकारात्मक रूप से कई मानव अर्बुद में उत्परिवर्तनीय भार के साथ संबंध रखता है। गैर-छोटे कोशिका फेफड़ों के कैंसर रोगियों में लैम्ब्रोलिज़ुमाब के साथ इलाज किया जाता है, उत्परिवर्तनीय भार नैदानिक प्रतिक्रिया के साथ एक मजबूत सहसंबंध दिखाता है। मेलेनोमा रोगियों में िपिलीमुमड के साथ इलाज किया जाता है, दीर्घकालिक लाभ भी उच्च उत्परिवर्तनीय भार से जुड़ा होता है, हालांकि कम महत्वपूर्ण होता है। लंबे समय तक नैदानिक लाभ वाले रोगियों में अनुमानित MHC बाध्यकारी नियोएंटिजेन्स को टेट्रापेप्टाइड रूपांकनों की एक श्रृंखला के लिए समृद्ध किया गया था जो बिना या न्यूनतम नैदानिक लाभ वाले रोगियों के अर्बुद में नहीं पाए गए थे।[122] हालांकि, अन्य अध्ययनों में पहचाने गए मानव नवजातजन टेट्रापेप्टाइड हस्ताक्षरों के प्रति पूर्वाग्रह नहीं दिखाते हैं।[123]
यह भी देखें
- कैंसर का टीका
- 5T4
- कोली के विष
- कॉम्बिनेटरियल एब्लेशन और रोगक्षमता चिकित्सा
- क्रायोरोगक्षमता चिकित्सा
- फोटोरोगक्षमता चिकित्सा
संदर्भ
- ↑ Kodach LL, Peppelenbosch MP (August 2021). "इम्यून चेकप्वाइंट नाकाबंदी के प्रति प्रतिक्रिया को प्रेरित करने के लिए माइलॉयड-व्युत्पन्न सप्रेसर सेल कम्पार्टमेंट को लक्षित करना गैस्ट्रिक कैंसर के विशिष्ट उपप्रकारों तक सीमित है।". Gastroenterology. 161 (2): 727. doi:10.1053/j.gastro.2021.03.047. PMID 33798523.
- ↑ "फिजियोलॉजी या मेडिसिन 2018 में नोबेल पुरस्कार". NobelPrize.org (in English). Retrieved 4 August 2019.
- ↑ 3.0 3.1 3.2 Kucerova P, Cervinkova M (April 2016). "ट्यूमर का सहज प्रतिगमन और माइक्रोबियल संक्रमण की भूमिका - कैंसर के उपचार की संभावनाएं". Anti-Cancer Drugs. 27 (4): 269–77. doi:10.1097/CAD.0000000000000337. PMC 4777220. PMID 26813865.
- ↑ Kienle GS (March 2012). "कैंसर के उपचार में बुखार: कोली की थेरेपी और महामारी संबंधी अवलोकन". Global Advances in Health and Medicine. 1 (1): 92–100. doi:10.7453/gahmj.2012.1.1.016. PMC 3833486. PMID 24278806.
- ↑ McCarthy EF (2006). "विलियम बी कोली के विष और हड्डी और कोमल-ऊतक सार्कोमा का उपचार". The Iowa Orthopaedic Journal. 26: 154–8. PMC 1888599. PMID 16789469.
- ↑ निबंध सार इंटरनेशनल: पूर्वव्यापी सूचकांक, वॉल्यूम I-XXIX। (in English). University Microfilms. 1970.
- ↑ "प्रारंभ वक्ता प्रशंसा करते हैं, स्थानीय स्नातकों को सलाह देते हैं। . ". Washington Post (in English). ISSN 0190-8286. Retrieved 9 July 2021.
- ↑ "कैंसर के टीके क्या हैं?". Cancer.Net (in English). 30 September 2013. Retrieved 15 August 2021.
- ↑ Riddell SR (July 2001). "बढ़ी हुई स्व-प्रस्तुति द्वारा कैंसर के टीकों में प्रगति". Proceedings of the National Academy of Sciences of the United States of America. 98 (16): 8933–35. Bibcode:2001PNAS...98.8933R. doi:10.1073/pnas.171326398. PMC 55350. PMID 11481463.
- ↑ 10.0 10.1 Palucka K, Banchereau J (July 2013). "डेंड्राइटिक-सेल-आधारित चिकित्सीय कैंसर के टीके". Immunity. 39 (1): 38–48. doi:10.1016/j.immuni.2013.07.004. PMC 3788678. PMID 23890062.
- ↑ Hirayama M, Nishimura Y (July 2016). "पेप्टाइड-आधारित कैंसर टीकों की वर्तमान स्थिति और भविष्य की संभावनाएं". International Immunology. 28 (7): 319–28. doi:10.1093/intimm/dxw027. PMID 27235694.
- ↑ Dastmalchi F, Karachi A, Mitchell D (June 2018). "Dendritic Cell Therapy". एल्स. American Cancer Society. pp. 1–27. doi:10.1002/9780470015902.a0024243. ISBN 9780470015902. S2CID 155185753.
- ↑ Gardner TA, Elzey BD, Hahn NM (April 2012). "Sipuleucel-T (बदला) ऑटोलॉगस वैक्सीन स्पर्शोन्मुख या न्यूनतम लक्षण वाले कैटरेट-प्रतिरोधी मेटास्टेटिक प्रोस्टेट कैंसर वाले पुरुषों के उपचार के लिए स्वीकृत". Human Vaccines & Immunotherapeutics. 8 (4): 534–39. doi:10.4161/hv.19795. PMID 22832254.
- ↑ Oudard S (May 2013). "उन्नत प्रोस्टेट कैंसर के लिए उभरते उपचारों में प्रगति". Cancer Treatment Reviews. 39 (3): 275–89. doi:10.1016/j.ctrv.2012.09.005. PMID 23107383.
- ↑ Sims RB (June 2012). "सिपुलेसेल-टी का विकास: मेटास्टैटिक कैस्ट्रेट प्रतिरोधी प्रोस्टेट कैंसर के उपचार के लिए ऑटोलॉगस सेलुलर इम्यूनोथेरेपी". Vaccine. 30 (29): 4394–97. doi:10.1016/j.vaccine.2011.11.058. PMID 22122856.
- ↑ Shore ND, Mantz CA, Dosoretz DE, Fernandez E, Myslicki FA, McCoy C, Finkelstein SE, Fishman MN (January 2013). "कैस्ट्रेशन-प्रतिरोधी प्रोस्टेट कैंसर के इम्यूनोलॉजिक उपचार के लिए सिपुलेसेल-टी पर निर्माण". Cancer Control. 20 (1): 7–16. doi:10.1177/107327481302000103. PMID 23302902.
- ↑ Office of the Commissioner. "प्रेस घोषणाएँ - FDA अनुमोदन संयुक्त राज्य अमेरिका में पहली जीन थेरेपी लाता है". fda.gov. Retrieved 13 December 2017.
- ↑ 18.0 18.1 "एफडीए कुछ प्रकार के बड़े बी-सेल लिंफोमा वाले वयस्कों के इलाज के लिए सीएआर-टी सेल थेरेपी को मंजूरी देता है". fda.gov. 18 October 2017. Retrieved 8 November 2017.
- ↑ Zhao L, Cao YJ (2019). "क्लिनिक में कैंसर के लिए इंजीनियर टी सेल थेरेपी". Frontiers in Immunology. 10: 2250. doi:10.3389/fimmu.2019.02250. PMC 6798078. PMID 31681259.
- ↑ Irving M (29 March 2022). "इम्प्लांटेबल इम्यूनोथेरेपी "फैक्टरी" तेजी से, अधिक प्रभावी ढंग से कैंसर से लड़ती है". New Atlas (in English). Retrieved 29 March 2022.
- ↑ Agarwalla P, Ogunnaike EA, Ahn S, Froehlich KA, Jansson A, Ligler FS, et al. (March 2022). "तेजी से विवो निर्माण और सीएआर-टी कोशिकाओं की रिहाई के लिए बायोइंस्ट्रक्टिव इम्प्लांटेबल मचान". Nature Biotechnology. 40 (8): 1250–1258. doi:10.1038/s41587-022-01245-x. PMC 9376243. PMID 35332339.
- ↑ 22.0 22.1 Scott AM, Wolchok JD, Old LJ (March 2012). "Antibody therapy of cancer". Nature Reviews. Cancer. 12 (4): 278–87. doi:10.1038/nrc3236. PMID 22437872. S2CID 205469234.
- ↑ 23.0 23.1 Harding FA, Stickler MM, Razo J, DuBridge RB (May–June 2010). "मानवकृत और पूरी तरह से मानव एंटीबॉडी की इम्यूनोजेनेसिटी: अवशिष्ट इम्यूनोजेनेसिटी सीडीआर क्षेत्रों में रहती है". mAbs. 2 (3): 256–65. doi:10.4161/mabs.2.3.11641. PMC 2881252. PMID 20400861.
- ↑ Gadd AJ, Greco F, Cobb AJ, Edwards AD (August 2015). "टोल-लाइक रिसेप्टर्स का लक्षित सक्रियण: एक मोनोक्लोनल एंटीबॉडी के लिए टोल-लाइक रिसेप्टर 7 एगोनिस्ट का संयुग्मन एंटीजन बाइंडिंग और विशिष्टता को बनाए रखता है" (PDF). Bioconjugate Chemistry (in English). 26 (8): 1743–52. doi:10.1021/acs.bioconjchem.5b00302. PMID 26133029. S2CID 26307107.
हम यहां पहली बार एंटीजन विशिष्टता से समझौता किए बिना एक एंटीट्यूमर एमएबी (एंटी-एचसीडी20 रीटक्सिमैब) के लिए एक छोटे अणु टीएलआर7 एगोनिस्ट के सफल संयुग्मन को प्रदर्शित करते हैं।
- ↑ Pincetic A, Bournazos S, DiLillo DJ, Maamary J, Wang TT, Dahan R, Fiebiger BM, Ravetch JV (August 2014). "टाइप I और टाइप II एफसी रिसेप्टर्स जन्मजात और अनुकूली प्रतिरक्षा को नियंत्रित करते हैं". Nature Immunology. 15 (8): 707–16. doi:10.1038/ni.2939. PMC 7430760. PMID 25045879.
- ↑ Topalian SL, Hodi FS, Brahmer JR, Gettinger SN, Smith DC, McDermott DF, Powderly JD, Carvajal RD, Sosman JA, Atkins MB, Leming PD, Spigel DR, Antonia SJ, Horn L, Drake CG, Pardoll DM, Chen L, Sharfman WH, Anders RA, Taube JM, McMiller TL, Xu H, Korman AJ, Jure-Kunkel M, Agrawal S, McDonald D, Kollia GD, Gupta A, Wigginton JM, Sznol M (June 2012). "कैंसर में एंटी-पीडी-1 एंटीबॉडी की सुरक्षा, गतिविधि और प्रतिरक्षा सहसंबंध". The New England Journal of Medicine. 366 (26): 2443–54. doi:10.1056/NEJMoa1200690. PMC 3544539. PMID 22658127.
- ↑ Dahan R, Sega E, Engelhardt J, Selby M, Korman AJ, Ravetch JV (October 2015). "FcγRs PD-1/PD-L1 अक्ष को लक्षित करने वाली एंटीबॉडी की ट्यूमर-विरोधी गतिविधि को संशोधित करते हैं". Cancer Cell. 28 (4): 543. doi:10.1016/j.ccell.2015.09.011. PMID 28854351.
- ↑ Arlauckas SP, Garris CS, Kohler RH, Kitaoka M, Cuccarese MF, Yang KS, Miller MA, Carlson JC, Freeman GJ, Anthony RM, Weissleder R, Pittet MJ (May 2017). "विवो इमेजिंग में एंटी-पीडी-1 थेरेपी में ट्यूमर से जुड़े मैक्रोफेज-मध्यस्थता प्रतिरोध मार्ग का पता चलता है". Science Translational Medicine. 9 (389): eaal3604. doi:10.1126/scitranslmed.aal3604. PMC 5734617. PMID 28490665.
- ↑ Dahan R, Barnhart BC, Li F, Yamniuk AP, Korman AJ, Ravetch JV (July 2016). "एगोनिस्टिक, ह्यूमन एंटी-सीडी40 मोनोक्लोनल एंटीबॉडीज की चिकित्सीय गतिविधि के लिए चुनिंदा एफसीआर एंगेजमेंट की आवश्यकता होती है". Cancer Cell. 29 (6): 820–31. doi:10.1016/j.ccell.2016.05.001. PMC 4975533. PMID 27265505.
- ↑ Weiner LM, Surana R, Wang S (May 2010). "मोनोक्लोनल एंटीबॉडी: कैंसर इम्यूनोथेरेपी के लिए बहुमुखी प्लेटफॉर्म". Nature Reviews. Immunology. 10 (5): 317–27. doi:10.1038/nri2744. PMC 3508064. PMID 20414205.
- ↑ Seidel UJ, Schlegel P, Lang P (2013). "चिकित्सीय एंटीबॉडी के साथ ट्यूमर इम्यूनोथेरेपी में प्राकृतिक किलर सेल मध्यस्थता एंटीबॉडी-निर्भर सेलुलर साइटोटोक्सिसिटी". Frontiers in Immunology. 4: 76. doi:10.3389/fimmu.2013.00076. PMC 3608903. PMID 23543707.
- ↑ Gelderman KA, Tomlinson S, Ross GD, Gorter A (March 2004). "एमएबी-मध्यस्थता कैंसर इम्यूनोथेरेपी में पूरक कार्य". Trends in Immunology. 25 (3): 158–64. doi:10.1016/j.it.2004.01.008. PMID 15036044.
- ↑ Waldmann TA (March 2003). "Immunotherapy: past, present and future". Nature Medicine. 9 (3): 269–77. doi:10.1038/nm0303-269. PMID 12612576. S2CID 9745527.
- ↑ Demko S, Summers J, Keegan P, Pazdur R (February 2008). "FDA drug approval summary: alemtuzumab as single-agent treatment for B-cell chronic lymphocytic leukemia". The Oncologist. 13 (2): 167–74. CiteSeerX 10.1.1.503.6960. doi:10.1634/theoncologist.2007-0218. PMID 18305062.
- ↑ "FDA approves new, targeted treatment for bladder cancer". FDA. 18 May 2016. Retrieved 20 May 2016.
- ↑ "US Food and Drug Administration – Avelumab Prescribing Label" (PDF).
- ↑ Pazdur R. "FDA approval for Ipilimumab". Retrieved 7 November 2013.
- ↑ "Bristol-Myers Squibb and AbbVie Receive U.S. FDA Breakthrough Therapy Designation for Elotuzumab, an Investigational Humanized Monoclonal Antibody for Multiple Myeloma | BMS Newsroom".
- ↑ Lemery SJ, Zhang J, Rothmann MD, Yang J, Earp J, Zhao H, McDougal A, Pilaro A, Chiang R, Gootenberg JE, Keegan P, Pazdur R (September 2010). "U.S. Food and Drug Administration approval: ofatumumab for the treatment of patients with chronic lymphocytic leukemia refractory to fludarabine and alemtuzumab". Clinical Cancer Research. 16 (17): 4331–38. doi:10.1158/1078-0432.CCR-10-0570. PMID 20601446.
- ↑ Sharma P, Allison JP (April 2015). "The future of immune checkpoint therapy". Science. 348 (6230): 56–61. Bibcode:2015Sci...348...56S. doi:10.1126/science.aaa8172. PMID 25838373. S2CID 4608450.
- ↑ "Opdivo Drug Approval History".
- ↑ James JS, Dubs G (December 1997). "FDA approves new kind of lymphoma treatment. Food and Drug Administration". AIDS Treatment News (284): 2–3. PMID 11364912.
- ↑ "FDA approves durvalumab after chemoradiation for unresectable stage III NSCLC". FDA. 9 February 2019.
- ↑ Byrd JC, Stilgenbauer S, Flinn IW (1 January 2004). "पुरानी लिम्फोसाईटिक ल्यूकेमिया". Hematology. American Society of Hematology. Education Program. 2004 (1): 163–83. doi:10.1182/asheducation-2004.1.163. PMID 15561682.
- ↑ Domagała A, Kurpisz M (2001). "CD52 एंटीजन - एक समीक्षा". Medical Science Monitor. 7 (2): 325–31. PMID 11257744.
- ↑ Dearden C (July 2012). "मैं प्रोलिम्फोसाइटिक ल्यूकेमिया का इलाज कैसे करता हूं". Blood. 120 (3): 538–51. doi:10.1182/blood-2012-01-380139. PMID 22649104.
- ↑ "एफडीए ने अनपेक्टेबल स्टेज III एनएससीएलसी के लिए कीमोराडिएशन के बाद डुरवालुमाब को मंजूरी दी". FDA. 9 February 2019.
- ↑ 48.0 48.1 Sondak VK, Smalley KS, Kudchadkar R, Grippon S, Kirkpatrick P (June 2011). "Ipilimumab". Nature Reviews. Drug Discovery. 10 (6): 411–12. doi:10.1038/nrd3463. PMID 21629286.
- ↑ 49.0 49.1 Lipson EJ, Drake CG (November 2011). "Ipilimumab: मेटास्टैटिक मेलेनोमा के लिए एक एंटी-CTLA-4 एंटीबॉडी". Clinical Cancer Research. 17 (22): 6958–62. doi:10.1158/1078-0432.CCR-11-1595. PMC 3575079. PMID 21900389.
- ↑ 50.0 50.1 Thumar JR, Kluger HM (December 2010). "Ipilimumab: मेलेनोमा के लिए एक आशाजनक इम्यूनोथेरेपी". Oncology. 24 (14): 1280–88. PMID 21294471.
- ↑ 51.0 51.1 Chambers CA, Kuhns MS, Egen JG, Allison JP (2001). "टी सेल प्रतिक्रियाओं के नियमन में सीटीएलए-4-मध्यस्थता निषेध: ट्यूमर इम्यूनोथेरेपी में तंत्र और हेरफेर". Annual Review of Immunology. 19: 565–94. doi:10.1146/annurev.immunol.19.1.565. PMID 11244047.
- ↑ 52.0 52.1 Postow MA, Callahan MK, Wolchok JD (June 2015). "कैंसर थेरेपी में इम्यून चेकपॉइंट नाकाबंदी". Journal of Clinical Oncology. 33 (17): 1974–82. doi:10.1200/JCO.2014.59.4358. PMC 4980573. PMID 25605845.
- ↑ 53.0 53.1 53.2 Pardoll DM (March 2012). "कैंसर इम्यूनोथेरेपी में प्रतिरक्षा चौकियों की नाकाबंदी". Nature Reviews. Cancer. 12 (4): 252–64. doi:10.1038/nrc3239. PMC 4856023. PMID 22437870.
- ↑ Kumar V, Chaudhary N, Garg M, Floudas CS, Soni P, Chandra AB (2017). "इम्यून चेकपॉइंट इनहिबिटर थेरेपी द्वारा प्रेरित प्रतिरक्षा संबंधित प्रतिकूल घटनाओं (आईआरएई) का वर्तमान निदान और प्रबंधन". Frontiers in Pharmacology. 8: 49. doi:10.3389/fphar.2017.00049. PMC 5296331. PMID 28228726.
- ↑ Castillo J, Perez K (2010). "पिछले उपचारों के लिए प्रतिरोधी पुरानी लिम्फोसाइटिक ल्यूकेमिया के उपचार में ofatumumab की भूमिका". Journal of Blood Medicine. 1: 1–8. doi:10.2147/jbm.s7284. PMC 3262337. PMID 22282677.
- ↑ Zhang B (July–August 2009). "Ofatumumab". mAbs. 1 (4): 326–31. doi:10.4161/mabs.1.4.8895. PMC 2726602. PMID 20068404.
- ↑ "पेम्ब्रोलिज़ुमाब लेबल" (PDF). FDA. May 2017. linked from Index page at FDA website November 2016
- ↑ "ईएमसी पर पेम्ब्रोलिज़ुमाब लेबल". UK Electronic Medicines Compendium. 27 January 2017.
- ↑ "निर्धारित जानकारी की मुख्य विशेषताएं - कीट्रूडा (पेम्ब्रोलिज़ुमाब)" (PDF). fda.gov. June 2018. Retrieved 27 February 2019.
- ↑ Keating GM (July 2010). "Rituximab: क्रोनिक लिम्फोसाइटिक ल्यूकेमिया, लो-ग्रेड या कूपिक लिंफोमा में इसके उपयोग की समीक्षा और बड़े बी-सेल लिंफोमा को फैलाना". Drugs. 70 (11): 1445–76. doi:10.2165/11201110-000000000-00000. PMID 20614951.
- ↑ Cerny T, Borisch B, Introna M, Johnson P, Rose AL (November 2002). "रीटक्सिमैब की क्रिया का तंत्र". Anti-Cancer Drugs. 13 (Suppl 2): S3–10. doi:10.1097/00001813-200211002-00002. PMID 12710585. S2CID 25061294.
- ↑ Janeway C, Travers P, Walport M, Shlomchik M (2001). इम्यूनोबायोलॉजी (Fifth ed.). New York and London: Garland Science. ISBN 978-0-8153-4101-7.[page needed]
- ↑ Weiner GJ (April 2010). "Rituximab: क्रिया का तंत्र". Seminars in Hematology. 47 (2): 115–23. doi:10.1053/j.seminhematol.2010.01.011. PMC 2848172. PMID 20350658.
- ↑ 64.0 64.1 Dranoff G (January 2004). "कैंसर रोगजनन और कैंसर चिकित्सा में साइटोकिन्स". Nature Reviews. Cancer. 4 (1): 11–22. doi:10.1038/nrc1252. PMID 14708024. S2CID 42092046.
- ↑ Dunn GP, Koebel CM, Schreiber RD (November 2006). "इंटरफेरॉन, प्रतिरक्षा और कैंसर इम्यूनोएडिटिंग". Nature Reviews. Immunology. 6 (11): 836–48. doi:10.1038/nri1961. PMID 17063185. S2CID 223082.
- ↑ Lasfar A, Abushahba W, Balan M, Cohen-Solal KA (2011). "इंटरफेरॉन लैम्ब्डा: कैंसर इम्यूनोथेरेपी में एक नई तलवार". Clinical & Developmental Immunology. 2011: 349575. doi:10.1155/2011/349575. PMC 3235441. PMID 22190970.
- ↑ Razaghi A, Owens L, Heimann K (December 2016). "एक इम्यूनोथेरेप्यूटिक के रूप में पुनः संयोजक मानव इंटरफेरॉन गामा की समीक्षा: उत्पादन प्लेटफार्मों और ग्लाइकोसिलेशन के प्रभाव". Journal of Biotechnology. 240: 48–60. doi:10.1016/j.jbiotec.2016.10.022. PMID 27794496.
- ↑ Coventry BJ, Ashdown ML (2012). "इंटरल्यूकिन-2 चिकित्सा की 20वीं वर्षगांठ: पूर्ण नैदानिक प्रतिक्रियाओं के दीर्घकालीन यादृच्छिक प्रेरण की व्याख्या करने वाली द्विपक्षीय भूमिका". Cancer Management and Research. 4: 215–21. doi:10.2147/cmar.s33979. PMC 3421468. PMID 22904643.
{{cite journal}}: zero width space character in|title=at position 57 (help) - ↑ Ott PA, Hodi FS, Kaufman HL, Wigginton JM, Wolchok JD (2017). "संयोजन इम्यूनोथेरेपी: एक रोड मैप". Journal for Immunotherapy of Cancer. 5: 16. doi:10.1186/s40425-017-0218-5. PMC 5319100. PMID 28239469.
- ↑ Mahoney KM, Rennert PD, Freeman GJ (August 2015). "संयोजन कैंसर इम्यूनोथेरेपी और नए इम्यूनोमॉड्यूलेटरी लक्ष्य". Nature Reviews. Drug Discovery. 14 (8): 561–84. doi:10.1038/nrd4591. PMID 26228759. S2CID 2220735.
- ↑ Mehta A, Oklu R, Sheth RA (2015). "थर्मल एब्लेटिव थैरेपी और इम्यून चेकपॉइंट मॉड्यूलेशन: क्या स्थानीय दृष्टिकोण प्रणालीगत प्रतिक्रिया को प्रभावित कर सकते हैं?". Gastroenterology Research and Practice. 2016: 9251375. doi:10.1155/2016/9251375. PMC 4802022. PMID 27051417.
- ↑ Tang J, Shalabi A, Hubbard-Lucey VM (January 2018). "क्लिनिकल इम्यूनो-ऑन्कोलॉजी परिदृश्य का व्यापक विश्लेषण". Annals of Oncology. 29 (1): 84–91. doi:10.1093/annonc/mdx755. PMID 29228097.
- ↑ Perry CJ, Muñoz-Rojas AR, Meeth KM, Kellman LN, Amezquita RA, Thakral D, Du VY, Wang JX, Damsky W, Kuhlmann AL, Sher JW, Bosenberg M, Miller-Jensen K, Kaech SM (March 2018). "माइलॉयड-लक्षित इम्युनोथैरेपी सूजन और एंटीट्यूमर इम्युनिटी को प्रेरित करने के लिए तालमेल में कार्य करते हैं". The Journal of Experimental Medicine. 215 (3): 877–93. doi:10.1084/jem.20171435. PMC 5839759. PMID 29436395.
- ↑ Rodell CB, Arlauckas SP, Cuccarese MF, Garris CS, Li R, Ahmed MS, Kohler RH, Pittet MJ, Weissleder R (21 May 2018). "TLR7/8-एगोनिस्ट-लोडेड नैनोपार्टिकल्स कैंसर इम्यूनोथेरेपी को बढ़ाने के लिए ट्यूमर से जुड़े मैक्रोफेज के ध्रुवीकरण को बढ़ावा देते हैं". Nature Biomedical Engineering. 2 (8): 578–588. doi:10.1038/s41551-018-0236-8. PMC 6192054. PMID 31015631.
- ↑ "कोरिओलस वर्सिकलर". American Cancer Society. Archived from the original on 15 February 2006.
- ↑ "कैंसर जेनेटिक्स KEYTRUDA® के लिए FDA-अनुमोदित DAKO PD-L1 IHC 22C3 PharmaDx सहयोगी नैदानिक परीक्षण की पेशकश करता है". 3 February 2016.
{{cite web}}: zero width space character in|title=at position 91 (help) - ↑ Udall M, Rizzo M, Kenny J, Doherty J, Dahm S, Robbins P, Faulkner E (February 2018). "PD-L1 डायग्नोस्टिक टेस्ट: स्कोरिंग एल्गोरिदम और टेस्ट-वैलिडेशन मेट्रिक्स की एक व्यवस्थित साहित्य समीक्षा". Diagnostic Pathology. 13 (1): 12. doi:10.1186/s13000-018-0689-9. PMC 5807740. PMID 29426340.
- ↑ Dacic S (April 2018). "फेफड़े के कैंसर में PD-L1 परीक्षण मानकीकरण का समय पूरा हो गया है". Annals of Oncology. 29 (4): 791–792. doi:10.1093/annonc/mdy069. PMID 29688334.
- ↑ Goodman AM, Kato S, Bazhenova L, Patel SP, Frampton GM, Miller V, Stephens PJ, Daniels GA, Kurzrock R (November 2017). "विविध कैंसर में इम्यूनोथेरेपी के प्रति प्रतिक्रिया के एक स्वतंत्र भविष्यवक्ता के रूप में ट्यूमर पारस्परिक बोझ". Molecular Cancer Therapeutics. 16 (11): 2598–2608. doi:10.1158/1535-7163.MCT-17-0386. PMC 5670009. PMID 28835386.
- ↑ "एफडीए ने ट्यूमर म्यूटेशनल बर्डन ≥ 10 म्यूट/एमबी के साथ एनएससीएलसी में फर्स्ट-लाइन निवोलुमैब प्लस लो-डोस इपिलिमैटैब के लिए एसबीएलए स्वीकार किया". ASCO Post. American Society of Clinical Oncology. 7 February 2018.
- ↑ Liu D, Schilling B, Liu D, Sucker A, Livingstone E, Jerby-Arnon L, et al. (December 2019). "मेटास्टैटिक मेलेनोमा वाले मरीजों में पीडी1 नाकाबंदी के नैदानिक परिणामों के एकीकृत आणविक और नैदानिक मॉडलिंग". Nature Medicine. 25 (12): 1916–1927. doi:10.1038/s41591-019-0654-5. PMC 6898788. PMID 31792460.
{{cite journal}}: zero width space character in|title=at position 64 (help) - ↑ Motzer RJ, Robbins PB, Powles T, Albiges L, Haanen JB, Larkin J, et al. (September 2020). "एडवांस्ड रीनल सेल कार्सिनोमा में एवलुमैब प्लस एक्सिटिनिब बनाम सुनीतिनिब: फेज 3 जेवेलिन रीनल 101 ट्रायल का बायोमार्कर विश्लेषण". Nature Medicine. 26 (11): 1733–1741. doi:10.1038/s41591-020-1044-8. PMC 8493486. PMID 32895571.
- ↑ "एफडीए ने बीआरएफ म्यूटेशन के साथ अनरेक्टेबल या मेटास्टैटिक मेलानोमा के संयोजन में एनकोराफेनीब और बिनीमेटिनिब को मंजूरी दी". U.S. Food and Drug Administration. 27 June 2018.
- ↑ Duke U Cancer Fraud Scandal: A Cautionary Tale For Obama's Precision Medicine Push, Faye Flam, 17 February 2015 (Forbes website)
- ↑ "Liquid biopsies" for cancer screening: Life-saving tests, or overdiagnosis and overtreatment taken to a new level? David Gorski, September 2015, Science-Based Medicine website
- ↑ A public discussion by cancer patients from 2011 on the melanoma.org website shows costs and claims.
- ↑ Restifo NP, Dudley ME, Rosenberg SA (March 2012). "कैंसर के लिए दत्तक इम्यूनोथेरेपी: टी सेल प्रतिक्रिया का दोहन". Nature Reviews. Immunology. 12 (4): 269–81. doi:10.1038/nri3191. PMC 6292222. PMID 22437939.
- ↑ Carroll J (December 2013). "नोवार्टिस/पेन की अनुकूलित टी सेल ने एएसएच को तारकीय ल्यूकेमिया डेटा से प्रभावित किया". Fierce Biotech.
- ↑ Carroll J (February 2014). "सर्वर नोवार्टिस के साथ हाई-स्टेक सीएआर-टी शोडाउन में प्रवेश करता है". FierceBiotech.
- ↑ Regalado A (June 2015). "बायोटेक आ रहा है कैंसर का इलाज: कैंसर को हराने के लिए अपनी प्रतिरक्षा कोशिकाओं को सुपरचार्ज करें? जूनो थेरेप्यूटिक्स का मानना है कि इसके उपचार ठीक यही कर सकते हैं". MIT Technology Review. Archived from the original on 20 June 2015.
{{cite web}}: zero width space character in|title=at position 127 (help) - ↑ "कार टी-सेल थेरेपी: इंजीनियरिंग मरीजों की प्रतिरक्षा कोशिकाएं उनके कैंसर का इलाज करती हैं". cancer.gov. 6 December 2013. Retrieved 9 May 2014.
- ↑ "एनआईएच के अध्ययन से पता चलता है कि कैंसर की एक विस्तृत श्रृंखला के खिलाफ एक नई कैंसर इम्यूनोथेरेपी पद्धति प्रभावी हो सकती है". nih.gov. 8 May 2014. Retrieved 9 May 2014.
- ↑ Andersen R, Borch TH, Draghi A, Gokuldass A, Rana MA, Pedersen M, Nielsen M, Kongsted P, Kjeldsen JW, Westergaard MC, Radic HD, Chamberlain CA, Holmich LR, Hendel HW, Larsen MS, Met O, Svane IM, Donia M (April 2018). "चेकपॉइंट इनहिबिटर रेसिस्टेंट-मेलेनोमा वाले मरीजों से अलग की गई टी कोशिकाएं कार्यात्मक हैं और ट्यूमर के प्रतिगमन में मध्यस्थता कर सकती हैं।". Ann. Oncol. 29 (7): 1575–1581. doi:10.1093/annonc/mdy139. PMID 29688262.
- ↑ "एफडीए की मंजूरी संयुक्त राज्य अमेरिका में पहली जीन थेरेपी लाती है". fda.gov. 30 August 2017. Retrieved 8 November 2017.
- ↑ Barros MS, de Araújo ND, Magalhães-Gama F, Pereira Ribeiro TL, Alves Hanna FS, Tarragô AM, et al. (22 September 2021). "γδ टी सेल फॉर ल्यूकेमिया इम्यूनोथेरेपी: न्यू एंड एक्सपेंडिंग ट्रेंड्स". Frontiers in Immunology. 12: 729085. doi:10.3389/fimmu.2021.729085. PMC 8493128. PMID 34630403.
- ↑ Wilhelm M, Smetak M, Schaefer-Eckart K, Kimmel B, Birkmann J, Einsele H, Kunzmann V (February 2014). "सफल दत्तक हस्तांतरण और अगुणित γδ टी कोशिकाओं के विवो विस्तार में". Journal of Translational Medicine. 12: 45. doi:10.1186/1479-5876-12-45. PMC 3926263. PMID 24528541.
- ↑ Jaiswal S, Chao MP, Majeti R, Weissman IL (June 2010). "मैक्रोफेज ट्यूमर इम्यूनोसर्वेविरेंस के मध्यस्थ के रूप में". Trends in Immunology. 31 (6): 212–19. doi:10.1016/j.it.2010.04.001. PMC 3646798. PMID 20452821.
- ↑ 98.0 98.1 98.2 Weiskopf K (May 2017). "CD47/SIRPα अक्ष को लक्षित कर कैंसर इम्यूनोथेरेपी". European Journal of Cancer. 76: 100–09. doi:10.1016/j.ejca.2017.02.013. PMID 28286286.
- ↑ Matlung HL, Szilagyi K, Barclay NA, van den Berg TK (March 2017). "CD47-SIRPα सिग्नलिंग अक्ष कैंसर में एक सहज प्रतिरक्षा जांच बिंदु के रूप में". Immunological Reviews. 276 (1): 145–64. doi:10.1111/imr.12527. PMID 28258703. S2CID 6275163.
- ↑ Veillette A, Chen J (March 2018). "SIRPα-CD47 एंटीकैंसर थेरेपी में इम्यून चेकपॉइंट नाकाबंदी". Trends in Immunology. 39 (3): 173–84. doi:10.1016/j.it.2017.12.005. PMID 29336991.
- ↑ Ahmed M, Cheung NK (January 2014). "कैंसर इम्यूनोथेरेपी के लिए इंजीनियरिंग एंटी-जीडी2 मोनोक्लोनल एंटीबॉडी". FEBS Letters. 588 (2): 288–97. doi:10.1016/j.febslet.2013.11.030. PMID 24295643.
- ↑ Ganesan S, Mehnert J (9 March 2020). "इम्यून चेकपॉइंट नाकाबंदी के जवाब के लिए बायोमार्कर". Annual Review of Cancer Biology. 4 (1): 331–351. doi:10.1146/annurev-cancerbio-030419-033604.
- ↑ Granier C, De Guillebon E, Blanc C, Roussel H, Badoual C, Colin E, Saldmann A, Gey A, Oudard S, Tartour E (2017). "कैंसर में चेकप्वाइंट अवरोधकों के उपयोग के लिए क्रियाविधि और तर्काधार". ESMO Open. 2 (2): e000213. doi:10.1136/esmoopen-2017-000213. PMC 5518304. PMID 28761757.
- ↑ Cameron F, Whiteside G, Perry C (May 2011). "Ipilimumab: पहली वैश्विक स्वीकृति". Drugs. 71 (8): 1093–104. doi:10.2165/11594010-000000000-00000. PMID 21668044.
- ↑ Lynch TJ, Bondarenko I, Luft A, Serwatowski P, Barlesi F, Chacko R, Sebastian M, Neal J, Lu H, Cuillerot JM, Reck M (June 2012). "चरण IIIB/IV गैर-लघु-कोशिका फेफड़ों के कैंसर में प्रथम-पंक्ति उपचार के रूप में पैक्लिटैक्सेल और कार्बोप्लाटिन के साथ संयोजन में Ipilimumab: एक यादृच्छिक, डबल-ब्लाइंड, बहुकेंद्रीय चरण II अध्ययन के परिणाम". Journal of Clinical Oncology. 30 (17): 2046–54. doi:10.1200/JCO.2011.38.4032. PMID 22547592.
- ↑ Le DT, Lutz E, Uram JN, Sugar EA, Onners B, Solt S, Zheng L, Diaz LA, Donehower RC, Jaffee EM, Laheru DA (September 2013). "पहले इलाज किए गए अग्नाशय के कैंसर में जीएम-सीएसएफ जीन के साथ ट्रांसफ़ेक्ट किए गए एलोजेनिक अग्नाशय ट्यूमर कोशिकाओं के साथ संयोजन में आईपिलिमैब का मूल्यांकन". Journal of Immunotherapy. 36 (7): 382–89. doi:10.1097/CJI.0b013e31829fb7a2. PMC 3779664. PMID 23924790.
- ↑ Clinical trial number NCT01928394 for "A Study of Nivolumab by Itself or Nivolumab Combined With Ipilimumab in Patients With Advanced or Metastatic Solid Tumors" at ClinicalTrials.gov
- ↑ 108.0 108.1 van Hooren L, Sandin LC, Moskalev I, Ellmark P, Dimberg A, Black P, Tötterman TH, Mangsbo SM (February 2017). "मोनोथेरापी के रूप में या एंटी-पीडी1 के साथ संयोजन में सीटीएलए-4 का स्थानीय चेकप्वाइंट अवरोध मुराइन ब्लैडर कैंसर के विकास को रोकता है". European Journal of Immunology. 47 (2): 385–93. doi:10.1002/eji.201646583. PMID 27873300. S2CID 2463514.
- ↑ 109.0 109.1 Pollack A (18 May 2016). "एफ.डी.ए. ब्लैडर कैंसर के लिए एक इम्यूनोथेरेपी दवा को मंज़ूरी दी". The New York Times. ISSN 0362-4331. Retrieved 21 May 2016.
- ↑ Steele A (5 August 2016). "ब्रिस्टल मायर्स: प्रमुख फेफड़े-कैंसर अध्ययन में Opdivo समापन बिंदु को पूरा करने में विफल रहा". The Wall Street Journal. ISSN 0099-9660. Retrieved 5 August 2016.
- ↑ BeiGene, Ltd. (2016). "2016 अमेरिकन सोसाइटी ऑफ क्लिनिकल ऑन्कोलॉजी की वार्षिक बैठक में बीजीन ने पीडी-1 एंटीबॉडी बीजीबी-ए317 पर आरंभिक क्लिनिकल डेटा प्रस्तुत किया". Globe Newswire.
- ↑ Roche. "विशिष्ट प्रकार के फेफड़ों के कैंसर में रोशे के कैंसर इम्यूनोथेरेपी एटेज़ोलिज़ुमाब के लिए एफडीए प्राथमिकता समीक्षा प्रदान करता है".
- ↑ Merck Group. "इम्यूनो-ऑन्कोलॉजी एवेलुमाब".
- ↑ Cure today. "Durvalumab उन्नत मूत्राशय कैंसर के उपचार में प्रगति जारी है।".
- ↑ Avacta Life Sciences. "एफिमर बायोथेरेप्यूटिक्स पीडी-एल1 इनहिबिटर के साथ कैंसर के ऑफ-स्विच को लक्षित करता है". Archived from the original on 6 August 2016. Retrieved 16 May 2016.
- ↑ Pfirschke C, Engblom C, Rickelt S, Cortez-Retamozo V, Garris C, Pucci F, et al. (February 2016). "इम्यूनोजेनिक कीमोथेरेपी चेकपॉइंट नाकाबंदी थेरेपी के लिए ट्यूमर को संवेदनशील बनाती है". Immunity. 44 (2): 343–54. doi:10.1016/j.immuni.2015.11.024. PMC 4758865. PMID 26872698.
- ↑ Fukuhara H, Ino Y, Todo T (October 2016). "ओंकोलिटिक वायरस थेरेपी: भोर में कैंसर के उपचार का एक नया युग". Cancer Science. 107 (10): 1373–79. doi:10.1111/cas.13027. PMC 5084676. PMID 27486853.
- ↑ Haddad D (2017). "जेनेटिकली इंजीनियर्ड वैक्सीनिया वायरस कैंसर के उपचार, इमेजिंग और ट्रांसजेन डिलीवरी के एजेंट के रूप में". Frontiers in Oncology. 7: 96. doi:10.3389/fonc.2017.00096. PMC 5440573. PMID 28589082.
- ↑ Marin-Acevedo JA, Soyano AE, Dholaria B, Knutson KL, Lou Y (January 2018). "प्रतिरक्षा जांच चौकी अवरोधकों से परे कैंसर इम्यूनोथेरेपी". Journal of Hematology & Oncology. 11 (1): 8. doi:10.1186/s13045-017-0552-6. PMC 5767051. PMID 29329556.
- ↑ Lawler SE, Speranza MC, Cho CF, Chiocca EA (June 2017). "कैंसर उपचार में ओंकोलिटिक वायरस: एक समीक्षा". JAMA Oncology. 3 (6): 841–849. doi:10.1001/jamaoncol.2016.2064. PMID 27441411. S2CID 39321536.
- ↑ Aleem E (June 2013). "β-ग्लूकेन्स और कैंसर थेरेपी में उनके अनुप्रयोग: मानव अध्ययन पर ध्यान केंद्रित करें". Anti-Cancer Agents in Medicinal Chemistry. 13 (5): 709–19. doi:10.2174/1871520611313050007. PMID 23293888.
- ↑ Snyder A, Makarov V, Merghoub T, Yuan J, Zaretsky JM, Desrichard A, Walsh LA, Postow MA, Wong P, Ho TS, Hollmann TJ, Bruggeman C, Kannan K, Li Y, Elipenahli C, Liu C, Harbison CT, Wang L, Ribas A, Wolchok JD, Chan TA (December 2014). "मेलेनोमा में CTLA-4 नाकाबंदी के नैदानिक प्रतिक्रिया के लिए आनुवंशिक आधार". The New England Journal of Medicine. 371 (23): 2189–99. doi:10.1056/NEJMoa1406498. PMC 4315319. PMID 25409260.
{{cite journal}}: zero width space character in|title=at position 41 (help) - ↑ Schumacher TN, Schreiber RD (April 2015). "कैंसर इम्यूनोथेरेपी में नियोएंटीजेन". Science. 348 (6230): 69–74. Bibcode:2015Sci...348...69S. doi:10.1126/science.aaa4971. PMID 25838375.
इस पेज में लापता आंतरिक लिंक की सूची
- बुनियादी अनुसंधान
- प्रतिरक्षा तंत्र
- कैंसर की कोशिकाएं
- कैंसर विज्ञान
- साइटोकाइन
- rituximab
- गुणवर्धक औषधि
- लाइव
- प्रमुख उतक अनुरूपता जटिल
- बी कोशिकाएं
- पूरकता निर्धारण क्षेत्रों
- elotuzumab
- झिल्ली हमला परिसर
- फ्लूडाराबाइन
- कोशिका विषी टी-कोशिका
- फेफड़ों की छोटी कोशिकाओं में कोई कैंसर नहीं
- ग्रीवा कैंसर
- आमाशय का कैंसर
- भोजी
- रोगज़नक़
- Nk कोशिका
- कोष्ठिका मध्यस्थित उन्मुक्ति
- कोमल ऊतक मांसार्बुद
- छोटे कोशिका फेफड़ों का कैंसर
- avelumab
- आंतरिक चौकी नाकाबंदी
- reovirus
- प्रतिरक्षाविज्ञानी सहायक
बाहरी संबंध
- A primer on "Immunotherapy to Treat Cancer", NIH
- Immunotherapy – Using the Immune System to Treat Cancer
- Cancer Research Institute – What is Cancer Immunotherapy
- Society for Immunotherapy of Cancer
- "And Then There Were Five". Economist.
- "Discover the Science of Immuno-Oncology". Bristol-Myers Squibb. Archived from the original on 10 October 2014. Retrieved 13 March 2014.
- Eggermont A, Finn O (September 2012). "Advances in immuno-oncology. Foreword". Annals of Oncology. 23 (Suppl 8): viii5. doi:10.1093/annonc/mds255. PMID 22918929.