हाइड्रोसिलिलेशन: Difference between revisions
No edit summary |
No edit summary |
||
| Line 12: | Line 12: | ||
==असममित हाइड्रोसिलिलेशन== | ==असममित हाइड्रोसिलिलेशन== | ||
दर्शक[[ लिगैंड ]]के रूप में | दर्शक[[ लिगैंड ]]के रूप में इंगित (रसायन विज्ञान) फॉस्फीन का उपयोग करते हुए, उत्प्रेरक असममित हाइड्रोसिलेशन के लिए उत्प्रेरक विकसित किए गए हैं। अच्छी तरह से अध्ययन की गई प्रतिक्रिया 1-फिनाइल-1- (ट्राइक्लोरोसिलिल) इथेन देने के लिए [[ स्टाइरीन |स्टाइरीन]] में [[ trichlorosilane |ट्राईक्लोरोसिलेन]] को मिलाना है | ||
: | :Cl<sub>3</sub>SiH + PhCH=CH<sub>2</sub> → (Ph)(CH<sub>3</sub>)CHSiCl<sub>3</sub> | ||
पैलेडियम-उत्प्रेरित युग्मन प्रतिक्रियाओं का उपयोग करके लगभग पूर्ण [[ एनैन्टीओमर ]] (ईई) प्राप्त किया जा सकता है, जो कि बिनाफ्थिल-प्रतिस्थापित मोनोफॉस्फीन लिगैंड द्वारा समर्थित है।<ref>{{Cite book|first1=T.|last1=Hayashi|first2=K.|last2=Yamasaki|chapter=C–E Bond Formation through Asymmetric Hydrosilylation of Alkenes|title=व्यापक ऑर्गेनोमेटेलिक रसायन विज्ञान III|editor1-first=Robert H.|editor1-last=Crabtree|editor2 =D. Michael P. Mingos|editor2-link =D. Michael P. Mingos|location=Amsterdam|publisher=Elsevier|year=2007|isbn=978-0-08-045047-6|doi=10.1016/B0-08-045047-4/00140-0}}</ref> | पैलेडियम-उत्प्रेरित युग्मन प्रतिक्रियाओं का उपयोग करके लगभग पूर्ण[[ एनैन्टीओमर ]](ईई) प्राप्त किया जा सकता है, जो कि बिनाफ्थिल-प्रतिस्थापित मोनोफॉस्फीन लिगैंड द्वारा समर्थित है।<ref>{{Cite book|first1=T.|last1=Hayashi|first2=K.|last2=Yamasaki|chapter=C–E Bond Formation through Asymmetric Hydrosilylation of Alkenes|title=व्यापक ऑर्गेनोमेटेलिक रसायन विज्ञान III|editor1-first=Robert H.|editor1-last=Crabtree|editor2 =D. Michael P. Mingos|editor2-link =D. Michael P. Mingos|location=Amsterdam|publisher=Elsevier|year=2007|isbn=978-0-08-045047-6|doi=10.1016/B0-08-045047-4/00140-0}}</ref> | ||
==सतह हाइड्रोसिलिलेशन== | ==सतह हाइड्रोसिलिलेशन== | ||
मूल ऑक्साइड को हटाने और [[ हाइड्रोजन-समाप्त सिलिकॉन सतह ]] बनाने के लिए [[ सिलिकॉन बिस्किट ]] | मूल ऑक्साइड को हटाने और[[ हाइड्रोजन-समाप्त सिलिकॉन सतह | हाइड्रोजन-निलंबित सिलिकॉन सतह]] बनाने के लिए [[ सिलिकॉन बिस्किट |सिलिकॉन पटलिका]] को [[ हाइड्रोफ्लुओरिक अम्ल |हाइड्रोफ्लुओरिक अम्ल]] में उकेरा जा सकता है। हाइड्रोजन-निलंबित सतहें एक स्थिर एकल परत बनाने के लिए असंतृप्त यौगिकों जैसे, टर्मिनल एल्केन्स और अल्काइन्स के साथ हाइड्रोसिलेशन से गुजरती हैं। | ||
: | उदाहरण के लिए: | ||
:Si-''H'' + H<sub>2</sub>C=CH(CH<sub>2</sub>)<sub>7</sub>CH<sub>3</sub> → Si-CH<sub>2</sub>CH''H''-(CH<sub>2</sub>)<sub>7</sub>CH<sub>3</sub> | |||
हाइड्रोसिलिलेशन प्रतिक्रिया कमरे के तापमान पर या गर्मी (सामान्य प्रतिक्रिया तापमान 120-200 डिग्री सेल्सियस), नमी और ऑक्सीजन मुक्त परिस्थितियों में यूवी प्रकाश के साथ शुरू की जा सकती है।<ref>"Photoreactivity of Unsaturated Compounds with Hydrogen-Terminated Silicon (111)," R. L. Cicero, M. R. Linford, C. E. D. Chidsey, Langmuir 16, 5688-5695 (2000)</ref> परिणामी मोनोलेयर, जो स्थिर और निष्क्रिय है, विभिन्न डिवाइस अनुप्रयोगों के लिए प्रासंगिक, बेस सिलिकॉन परत के ऑक्सीकरण को रोकता है।<ref>Direct electrical detection of DNA Hybridization at DNA-modified silicon surfaces, W.Cai, J. Peck, D. van der Weide, and R.J. Hamers, Biosensors and Bioelectronics 19, 1013-1019 (2004)</ref> | हाइड्रोसिलिलेशन प्रतिक्रिया कमरे के तापमान पर या गर्मी (सामान्य प्रतिक्रिया तापमान 120-200 डिग्री सेल्सियस), नमी और ऑक्सीजन मुक्त परिस्थितियों में यूवी प्रकाश के साथ शुरू की जा सकती है।<ref>"Photoreactivity of Unsaturated Compounds with Hydrogen-Terminated Silicon (111)," R. L. Cicero, M. R. Linford, C. E. D. Chidsey, Langmuir 16, 5688-5695 (2000)</ref> परिणामी मोनोलेयर, जो स्थिर और निष्क्रिय है, विभिन्न डिवाइस अनुप्रयोगों के लिए प्रासंगिक, बेस सिलिकॉन परत के ऑक्सीकरण को रोकता है।<ref>Direct electrical detection of DNA Hybridization at DNA-modified silicon surfaces, W.Cai, J. Peck, D. van der Weide, and R.J. Hamers, Biosensors and Bioelectronics 19, 1013-1019 (2004)</ref> | ||
Revision as of 10:33, 14 February 2023
हाइड्रोसिलिलेशन, जिसे उत्प्रेरक हाइड्रोसिलेशन भी कहा जाता है, यह संतृप्त और असंतृप्त यौगिक में एसआई-एच बांड को जोड़ने का वर्णन करता है।[1] प्रतिक्रिया प्रायः उत्प्रेरक रूप से आयोजित की जाती है और सामान्यतः सब्सट्रेट असंतृप्त कार्बनिक यौगिक होते हैं। अल्केन और अल्काइन्स ऐल्किल विनाइल सिलाने देते हैं; एवं एल्डिहाइड और कीटोन सिलील ईथर देते हैं। हाइड्रोसिलिलेशन को सजातीय उत्प्रेरण में प्लैटिनम का सबसे महत्वपूर्ण अनुप्रयोग कहा गया है।[2]
कार्यक्षेत्र और तंत्र
एल्केन्स का हाइड्रोसिलिलेशन अर्गैनोसिलिकान यौगिक तैयार करने के लिए व्यावसायिक रूप से महत्वपूर्ण विधि का प्रतिनिधित्व करता है। यह प्रक्रिया यांत्रिक रूप से एल्केन्स के हाइड्रोजनीकरण के समान है। वास्तव में, समान उत्प्रेरक कभी-कभी दो उत्प्रेरक प्रक्रियाओं के लिए नियोजित होते हैं।
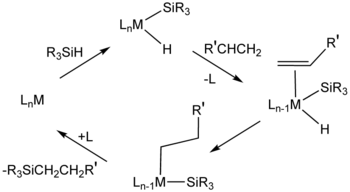
प्रचलित तंत्र, जिसे चाक-हैरोड तंत्र कहा जाता है, मध्यवर्ती धातु परिसर को मानता है जिसमें एक हाइड्राइड, एक सिलील लिगैंड (R3Si), और एल्केन कर्यद्रव होता है। सिग्मा-कॉम्प्लेक्स की मध्यस्थता से ऑक्सीडेटिव जोड़ आगे बढ़ता है, जिसमें एसआई-एच बांड पूरी तरह से टूटा नहीं है।
एल्केन्स का हाइड्रोसिलिलेशन सामान्यतः एंटी-मार्कोवनिकोव जोड़ के माध्यम से होता है, अर्थात, सिलिकॉन टर्मिनल कार्बन पर रखा जाता है, जब एक टर्मिनल एल्केन को हाइड्रोसिलिलेट किया जाता है।[1] चाक-हैरोड तंत्र की विविधताएं मौजूद हैं। कुछ मामलों में एलकेन को एम-सी बन्ध में शामिल किया जाता है, जिसके बाद बीटा-हाइड्राइड उन्मूलन होता है, चाक-हैरोड तंत्र में अनुक्रम के विपरीत कुछ मामलों में, हाइड्रोसिलिलेशन का परिणाम बीटा-हाइड्राइड उन्मूलन के परिणामस्वरूप विनाइल या एलिलिक सिलेन में होता है।[3] अल्काइन्स भी हाइड्रोसिलिलेशन से गुजरते हैं, उदाहरण के लिए, ट्राइएथिल सिलेन को डिपेनिलसैटिलीन में जोड़ना:[4]
- Et3SiH + PhC≡CPh → Et3Si(Ph)C=CH(Ph)
असममित हाइड्रोसिलिलेशन
दर्शकलिगैंड के रूप में इंगित (रसायन विज्ञान) फॉस्फीन का उपयोग करते हुए, उत्प्रेरक असममित हाइड्रोसिलेशन के लिए उत्प्रेरक विकसित किए गए हैं। अच्छी तरह से अध्ययन की गई प्रतिक्रिया 1-फिनाइल-1- (ट्राइक्लोरोसिलिल) इथेन देने के लिए स्टाइरीन में ट्राईक्लोरोसिलेन को मिलाना है
- Cl3SiH + PhCH=CH2 → (Ph)(CH3)CHSiCl3
पैलेडियम-उत्प्रेरित युग्मन प्रतिक्रियाओं का उपयोग करके लगभग पूर्णएनैन्टीओमर (ईई) प्राप्त किया जा सकता है, जो कि बिनाफ्थिल-प्रतिस्थापित मोनोफॉस्फीन लिगैंड द्वारा समर्थित है।[5]
सतह हाइड्रोसिलिलेशन
मूल ऑक्साइड को हटाने और हाइड्रोजन-निलंबित सिलिकॉन सतह बनाने के लिए सिलिकॉन पटलिका को हाइड्रोफ्लुओरिक अम्ल में उकेरा जा सकता है। हाइड्रोजन-निलंबित सतहें एक स्थिर एकल परत बनाने के लिए असंतृप्त यौगिकों जैसे, टर्मिनल एल्केन्स और अल्काइन्स के साथ हाइड्रोसिलेशन से गुजरती हैं।
उदाहरण के लिए:
- Si-H + H2C=CH(CH2)7CH3 → Si-CH2CHH-(CH2)7CH3
हाइड्रोसिलिलेशन प्रतिक्रिया कमरे के तापमान पर या गर्मी (सामान्य प्रतिक्रिया तापमान 120-200 डिग्री सेल्सियस), नमी और ऑक्सीजन मुक्त परिस्थितियों में यूवी प्रकाश के साथ शुरू की जा सकती है।[6] परिणामी मोनोलेयर, जो स्थिर और निष्क्रिय है, विभिन्न डिवाइस अनुप्रयोगों के लिए प्रासंगिक, बेस सिलिकॉन परत के ऑक्सीकरण को रोकता है।[7]
उत्प्रेरक
स्पीयर द्वारा प्लैटिनम उत्प्रेरक की शुरुआत से पहले, हाइड्रोसिलिलेशन का व्यापक रूप से अभ्यास नहीं किया गया था। 1947 में अकादमिक साहित्य में पेरोक्साइड-उत्प्रेरित प्रक्रिया की सूचना मिली थी,[8] लेकिन स्पीयर के उत्प्रेरक (क्लोरोप्लाटिनिक एसिड | एच .) की शुरूआत2पीटीसीएल6) एक बड़ी सफलता थी।
कारस्टेड के उत्प्रेरक को बाद में पेश किया गया था। यह एक लिपोफिलिक परिसर है जो औद्योगिक हित के कार्बनिक सबस्ट्रेट्स में घुलनशील है।[9] हाइड्रोजनीकरण को उत्प्रेरित करने वाले परिसर और यौगिक अक्सर हाइड्रोसिलिलेशन के लिए प्रभावी उत्प्रेरक होते हैं, उदा। विल्किंसन के उत्प्रेरक।
संदर्भ
- ↑ 1.0 1.1 "Hydrosilylation A Comprehensive Review on Recent Advances" B. Marciniec (ed.), Advances in Silicon Science, Springer Science, 2009. doi:10.1007/978-1-4020-8172-9
- ↑ Renner, H.; Schlamp, G.; Kleinwächter, I.; Drost, E.; Lüschow, H. M.; Tews, P.; Panster, P.; Diehl, M.; Lang, J.; Kreuzer, T.; Knödler, A.; Starz, K. A.; Dermann, K.; Rothaut, J.; Drieselman, R. (2002). "Platinum group metals and compounds". उलमन का औद्योगिक रसायन विज्ञान का विश्वकोश. Wiley. doi:10.1002/14356007.a21_075. ISBN 3527306730.
- ↑ Troegel, D.; Stohrer, J. (2011). "औद्योगिक दृष्टिकोण से ओलेफिन के लेट ट्रांजिशन मेटल उत्प्रेरित हाइड्रोसिलिलेशन में हालिया प्रगति और वास्तविक चुनौतियां". Coord. Chem. Rev. 255 (13–14): 1440–1459. doi:10.1016/j.ccr.2010.12.025.
- ↑ James L. Fry, Ronald J. Rahaim Jr., Robert E. Maleczka, Jr. "Triethylsilane", Encyclopedia of Reagents for Organic Synthesis, John Wiley & Sons, 2007. doi:10.1002/047084289X.rt226.pub2
- ↑ Hayashi, T.; Yamasaki, K. (2007). "C–E Bond Formation through Asymmetric Hydrosilylation of Alkenes". In Crabtree, Robert H.; D. Michael P. Mingos (eds.). व्यापक ऑर्गेनोमेटेलिक रसायन विज्ञान III. Amsterdam: Elsevier. doi:10.1016/B0-08-045047-4/00140-0. ISBN 978-0-08-045047-6.
- ↑ "Photoreactivity of Unsaturated Compounds with Hydrogen-Terminated Silicon (111)," R. L. Cicero, M. R. Linford, C. E. D. Chidsey, Langmuir 16, 5688-5695 (2000)
- ↑ Direct electrical detection of DNA Hybridization at DNA-modified silicon surfaces, W.Cai, J. Peck, D. van der Weide, and R.J. Hamers, Biosensors and Bioelectronics 19, 1013-1019 (2004)
- ↑ Sommer, L.; Pietrusza, E.; Whitmore, F. (1947). "1-ऑक्टीन में ट्राइक्लोरोसिलेन का पेरोक्साइड-उत्प्रेरित योग". J. Am. Chem. Soc. 69 (1): 188. doi:10.1021/ja01193a508.
- ↑ C. Elschenbroich, Organometallics (2006) Wiley and Sons-VCH: Weinheim. ISBN 978-3-527-29390-2
अग्रिम पठन
Books
- Applied homogeneous catalysis with organometallic compounds : a comprehensive handbook : applications, developments. Boy Cornils; W A Herrmann. Publisher: Weinheim ; New York : Wiley-VCH, 2000.
- Comprehensive handbook on hydrosilylation. Bogdan Marciniec. Publisher: Oxford [u.a.] : Pergamon Press, 1992.
- Rhodium complexes as hydrosilylation catalysts. N.K. Skvortsov. // Rhodium Express. 1994. No 4 (May). P. 3 - 36 (Eng). [1] ISSN 0869-7876
Articles
- "Alkyl Monolayers on Silicon Prepared from 1-Alkenes and Hydrogen-Terminated Silicon," M. R. Linford, P. Fenter, P. M. Eisenberger and C. E. D. Chidsey, J. Am. Chem. Soc. 117, 3145-3155 (1995).
- "Synthesis and characterization of DNA-modified Si(111) Surfaces," T. Strother, W. CAi, X. Zhao, R.J. Hamers, and L.M. Smith, J. Am. Chem. Soc. 122, 1205-1209 (2000).
- "T. Strother, R.J. Hamers, and L.M. Smith, "Surface Chemistry of DNA Covalent Attachment to the Silicon(100) Surface". Langmuir, 2002, 18, 788-796.
- "Covalently Modified Silicon and Diamond Surfaces: Resistance to Non-Specific Protein Adsorption and Optimization for Biosensing," T.L. Lasseter, B.H. Clare, N.L. Abbott, and R.J. Hamers. J. Am. Chem. Soc. 2004, 126, 10220-10221.