जल-गैस शिफ्ट प्रतिक्रिया: Difference between revisions
No edit summary |
No edit summary |
||
| Line 1: | Line 1: | ||
{{Short description|Reaction of carbon monoxide and water vapor}} | {{Short description|Reaction of carbon monoxide and water vapor}} | ||
''' | '''वाटर गैस शिफ्ट रिएक्शन ''' (डब्ल्यूजीएसआर) कार्बन डाइऑक्साइड और हाइड्रोजन बनाने के लिए कार्बन मोनोऑक्साइड और जल वाष्प की प्रतिक्रिया का वर्णन करता है: | ||
: CO + H<sub>2</sub>O ⇌ CO<sub>2</sub> + H<sub>2</sub> | : CO + H<sub>2</sub>O ⇌ CO<sub>2</sub> + H<sub>2</sub> | ||
वाटर गैस शिफ्ट रिएक्शन की खोज इटली के भौतिक विज्ञानी फेलिस फोंटाना ने 1780 में की थी। इस प्रतिक्रिया के औद्योगिक मूल्य का एहसास बहुत बाद में हुआ था। 20 वीं सदी की शुरुआत से पहले, आयरन ऑक्साइड और हाइड्रोजन का उत्पादन करने के लिए लोहे के साथ उच्च दबाव में भाप की प्रतिक्रिया करके हाइड्रोजन प्राप्त किया जाता था। हाइड्रोजन की आवश्यकता वाली औद्योगिक प्रक्रियाओं के विकास के साथ, जैसे कि हैबर-बॉश अमोनिया संश्लेषण, हाइड्रोजन उत्पादन के एक कम खर्चीले और अधिक कुशल तरीके की आवश्यकता थी। इस समस्या के समाधान के रूप में, शुद्ध हाइड्रोजन उत्पाद का उत्पादन करने के लिए डब्ल्यूजीएसआर को कोयले के गैसीकरण के साथ जोड़ा गया था। चूंकि हाइड्रोजन अर्थव्यवस्था का विचार लोकप्रियता प्राप्त कर रहा है, हाइड्रोकार्बन के प्रतिस्थापन ईंधन स्रोत के रूप में हाइड्रोजन पर ध्यान बढ़ रहा है। | वाटर गैस शिफ्ट रिएक्शन की खोज इटली के भौतिक विज्ञानी फेलिस फोंटाना ने 1780 में की थी। इस प्रतिक्रिया के औद्योगिक मूल्य का एहसास बहुत बाद में हुआ था। 20 वीं सदी की शुरुआत से पहले, आयरन ऑक्साइड और हाइड्रोजन का उत्पादन करने के लिए लोहे के साथ उच्च दबाव में भाप की प्रतिक्रिया करके हाइड्रोजन प्राप्त किया जाता था। हाइड्रोजन की आवश्यकता वाली औद्योगिक प्रक्रियाओं के विकास के साथ, जैसे कि हैबर-बॉश अमोनिया संश्लेषण, हाइड्रोजन उत्पादन के एक कम खर्चीले और अधिक कुशल तरीके की आवश्यकता थी। इस समस्या के समाधान के रूप में, शुद्ध हाइड्रोजन उत्पाद का उत्पादन करने के लिए डब्ल्यूजीएसआर को कोयले के गैसीकरण के साथ जोड़ा गया था। चूंकि हाइड्रोजन अर्थव्यवस्था का विचार लोकप्रियता प्राप्त कर रहा है, हाइड्रोकार्बन के प्रतिस्थापन ईंधन स्रोत के रूप में हाइड्रोजन पर ध्यान बढ़ रहा है। | ||
Latest revision as of 11:49, 4 September 2023
वाटर गैस शिफ्ट रिएक्शन (डब्ल्यूजीएसआर) कार्बन डाइऑक्साइड और हाइड्रोजन बनाने के लिए कार्बन मोनोऑक्साइड और जल वाष्प की प्रतिक्रिया का वर्णन करता है:
- CO + H2O ⇌ CO2 + H2
वाटर गैस शिफ्ट रिएक्शन की खोज इटली के भौतिक विज्ञानी फेलिस फोंटाना ने 1780 में की थी। इस प्रतिक्रिया के औद्योगिक मूल्य का एहसास बहुत बाद में हुआ था। 20 वीं सदी की शुरुआत से पहले, आयरन ऑक्साइड और हाइड्रोजन का उत्पादन करने के लिए लोहे के साथ उच्च दबाव में भाप की प्रतिक्रिया करके हाइड्रोजन प्राप्त किया जाता था। हाइड्रोजन की आवश्यकता वाली औद्योगिक प्रक्रियाओं के विकास के साथ, जैसे कि हैबर-बॉश अमोनिया संश्लेषण, हाइड्रोजन उत्पादन के एक कम खर्चीले और अधिक कुशल तरीके की आवश्यकता थी। इस समस्या के समाधान के रूप में, शुद्ध हाइड्रोजन उत्पाद का उत्पादन करने के लिए डब्ल्यूजीएसआर को कोयले के गैसीकरण के साथ जोड़ा गया था। चूंकि हाइड्रोजन अर्थव्यवस्था का विचार लोकप्रियता प्राप्त कर रहा है, हाइड्रोकार्बन के प्रतिस्थापन ईंधन स्रोत के रूप में हाइड्रोजन पर ध्यान बढ़ रहा है।
आवेदन
डब्लूजीएसआर एक अत्यधिक मूल्यवान औद्योगिक प्रतिक्रिया है जिसका प्रयोग अमोनिया, हाइड्रोकार्बन, मेथनॉल और हाइड्रोजन के निर्माण में किया जाता है। इसका सबसे महत्वपूर्ण अनुप्रयोग हाइड्रोजन के उत्पादन में मीथेन या अन्य हाइड्रोकार्बन के भाप सुधार से कार्बन मोनोऑक्साइड के रूपांतरण के संयोजन में है।[1] फिशर-ट्रॉप्स प्रक्रिया में, डब्ल्यूजीएसआर H2/CO अनुपात को संतुलित करने के लिए इस्तेमाल की जाने वाली सबसे महत्वपूर्ण प्रतिक्रियाओं में से एक है। यह कार्बन मोनोऑक्साइड की कीमत पर हाइड्रोजन का स्रोत प्रदान करता है, जो अमोनिया संश्लेषण में इस्तेमाल के लिए उच्च शुद्धता वाले हाइड्रोजन के उत्पादन के लिए महत्वपूर्ण है।
पानी और कार्बन मोनोऑक्साइड को सम्मिलित करने वाली प्रक्रियाओं में जल-गैस शिफ्ट प्रतिक्रिया एक अवांछित पक्ष प्रतिक्रिया हो सकती है, उदा। रोडियाम आधारित मोनसेंटो प्रक्रिया। इरिडियम आधारित कैटिवा प्रक्रिया में कम पानी का उपयोग होता है, जो इस प्रतिक्रिया को दबा देता है।
ईंधन सेल
डब्लूजीएसआर हाइड्रोजन उत्पादन को बढ़ाकर ईंधन कोशिकाओं की दक्षता में सहायता कर सकता है। डब्लूजीएसआर को कोशिकाओं में कार्बन मोनोऑक्साइड सांद्रता को कम करने में एक महत्वपूर्ण घटक माना जाता है जो कार्बन मोनोऑक्साइड विषाक्तता जैसे प्रोटॉन-एक्सचेंज झिल्ली (पीईएम) ईंधन सेल के लिए अतिसंवेदनशील होते हैं।[2] इस प्रयोग के लाभ दो गुना हैं: न केवल जल गैस शिफ्ट प्रतिक्रिया कार्बन मोनोऑक्साइड की एकाग्रता को प्रभावी ढंग से कम कर देगी, बल्कि यह हाइड्रोजन उत्पादन को बढ़ाकर ईंधन कोशिकाओं की दक्षता में भी वृद्धि करेगी।[2] दुर्भाग्य से, वर्तमान वाणिज्यिक उत्प्रेरक जो औद्योगिक जल गैस शिफ्ट प्रक्रियाओं में उपयोग किए जाते हैं, ईंधन सेल अनुप्रयोगों के साथ संगत नहीं हैं।[3] स्वच्छ ईंधन की उच्च मांग और हाइड्रोजन ईंधन कोशिकाओं में जल गैस शिफ्ट प्रतिक्रिया की महत्वपूर्ण भूमिका के साथ, ईंधन सेल प्रौद्योगिकी में अनुप्रयोग के लिए जल गैस शिफ्ट उत्प्रेरक का विकास वर्तमान अनुसंधान हित का क्षेत्र है।
ईंधन सेल अनुप्रयोग के लिए उत्प्रेरकों को कम तापमान पर काम करना होगा। चूंकि डब्ल्यूजीएसआर कम तापमान पर धीमा होता है जहां संतुलन हाइड्रोजन उत्पादन के पक्ष में होता है, डब्ल्यूजीएस रिएक्टरों को बड़ी मात्रा में उत्प्रेरक की आवश्यकता होती है, जो व्यावहारिक अनुप्रयोग से परे उनकी लागत और आकार को बढ़ा देता है।[2] बड़े पैमाने के औद्योगिक संयंत्रों में उपयोग किया जाने वाला वाणिज्यिक एलटीएस उत्प्रेरक अपनी निष्क्रिय अवस्था में पायरोफोरिक भी होता है और इसलिए उपभोक्ता अनुप्रयोगों के लिए सुरक्षा चिंताओं को प्रस्तुत करता है।[3] एक ऐसे उत्प्रेरक का विकास करना जो इन सीमाओं को पार कर सके, हाइड्रोजन अर्थव्यवस्था के कार्यान्वयन के लिए प्रासंगिक है।
अवशोषण-वर्धित जल गैस बदलाव
सिनगैस से एक उच्च दबाव हाइड्रोजन धारा का उत्पादन करने के लिए सोखना-वर्धित जल गैस शिफ्ट (एसईडब्ल्यूजीएस) में CO2 के ठोस सोखना के संयोजन में डब्ल्यूजीएस प्रतिक्रिया का उपयोग किया जाता है।[4]
प्रतिक्रिया की स्थिति
इस प्रतिक्रिया का संतुलन एक महत्वपूर्ण तापमान निर्भरता को दर्शाता है और तापमान में वृद्धि के साथ संतुलन स्थिरांक घटता है, अर्थात उच्च हाइड्रोजन गठन कम तापमान पर मनाया जाता है।
तापमान निर्भरता
बढ़ते तापमान के साथ, प्रतिक्रिया की दर बढ़ जाती है, लेकिन हाइड्रोजन का उत्पादन ऊष्मागतिक रूप से कम अनुकूल हो जाता है[5] क्योंकि जल गैस शिफ्ट प्रतिक्रिया मध्यम रूप से ऊष्माक्षेपी होती है; रासायनिक संतुलन में इस बदलाव की व्याख्या ले शाटेलियर के सिद्धांत के अनुसार की जा सकती है। 600–2000 K की तापमान सीमा से अधिक, डब्ल्यूजीएसआर के लिए संतुलन स्थिरांक का निम्नलिखित संबंध है:[3]
व्यावहारिक प्रसंग
प्रतिक्रिया के ऊष्मप्रवैगिकी और कैनेटीक्स दोनों का लाभ उठाने के लिए, औद्योगिक-पैमाने पर जल गैस शिफ्ट प्रतिक्रिया कई एडियाबेटिक चरणों में आयोजित की जाती है जिसमें उच्च तापमान शिफ्ट (एचटीएस) होता है, जिसके बाद कम तापमान शिफ्ट (एलटीएस) होता है। इंटरसिस्टम कूलिंग।[6] प्रारंभिक एचटीएस उच्च प्रतिक्रिया दर का लाभ उठाता है लेकिन कार्बन मोनोऑक्साइड के अधूरे रूपांतरण के परिणामस्वरूप होता है। बाद में कम तापमान शिफ्ट रिएक्टर कार्बन मोनोऑक्साइड सामग्री को <1% तक कम कर देता है। व्यावसायिक एचटीएस उत्प्रेरक आयरन ऑक्साइड-क्रोमियम ऑक्साइड पर आधारित हैं और एलटीएस उत्प्रेरक कॉपर आधारित है। तांबा उत्प्रेरक सल्फर द्वारा विषाक्तता के लिए अतिसंवेदनशील है। एलटीएस रिएक्टर से पहले गार्ड बेड द्वारा सल्फर यौगिकों को हटा दिया जाता है। एचटीएस की एक महत्वपूर्ण सीमा H2O/CO अनुपात है जहां कम अनुपात से पार्श्व प्रतिक्रियाएं हो सकती हैं जैसे कि धातु लोहा, मिथेनेशन, कार्बन जमाव और फिशर-ट्रॉप्स प्रतिक्रिया।
उच्च तापमान बदलाव उत्प्रेरण
वाणिज्यिक एचटीएस उत्प्रेरकों की विशिष्ट संरचना को 74.2% Fe2O3, 10.0% Cr2O3, 0.2% MgO (शेष प्रतिशत अस्थिर घटकों के लिए जिम्मेदार ठहराया गया) के रूप में रिपोर्ट किया गया है।[7] क्रोमियम आयरन ऑक्साइड को स्थिर करने का काम करता है और सिंटरिंग को रोकता है। एचटीएस उत्प्रेरक का संचालन 310 डिग्री सेल्सियस से 450 डिग्री सेल्सियस के तापमान सीमा के भीतर होता है। प्रतिक्रिया की उष्माक्षेपी प्रकृति के कारण रिएक्टर की लंबाई के साथ तापमान बढ़ता है। इस प्रकार, निकास तापमान को 550 डिग्री सेल्सियस से अधिक होने से रोकने के लिए इनलेट तापमान 350 डिग्री सेल्सियस पर बनाए रखा जाता है। औद्योगिक रिएक्टर वायुमंडलीय दबाव से 8375 kPa (82.7 atm) की सीमा में काम करते हैं।[7] रसायन विज्ञान और सामग्री विज्ञान के क्षेत्र में उच्च प्रदर्शन वाले एचटी डब्ल्यूजीएस उत्प्रेरकों की खोज अनुसंधान का एक गहन विषय बना हुआ है। डब्ल्यूजीएस प्रतिक्रियाओं में उत्प्रेरक प्रदर्शन के मूल्यांकन के लिए सक्रियण ऊर्जा एक महत्वपूर्ण मानदंड है। आज तक, सेरिया सपोर्ट सामग्री पर तांबे के नैनोकणों से युक्त उत्प्रेरकों के लिए सबसे कम सक्रियण ऊर्जा मूल्यों में से कुछ पाए गए हैं, [8] हाइड्रोजन उत्पादन के सापेक्ष Ea = 34 kJ/mol रिपोर्ट किए गए मानों के साथ।
कम तापमान बदलाव उत्प्रेरण
कम तापमान डब्ल्यूजीएस प्रतिक्रिया के लिए उत्प्रेरक आमतौर पर कॉपर या कॉपर ऑक्साइड-लोडेड सिरेमिक चरणों पर आधारित होते हैं, जबकि सबसे आम सपोर्ट में जिंक ऑक्साइड के साथ एल्यूमिना या एल्यूमिना सम्मिलित हैं, अन्य सपोर्ट में रेयर अर्थ ऑक्साइड, स्पिनल्स या पेरोसाइट्स सम्मिलित हो सकते हैं।[8] एक वाणिज्यिक एलटीएस उत्प्रेरक की एक विशिष्ट रचना को32-33% CuO, 34-53% ZnO, 15-33% Al2O3 के रूप में सूचित किया गया है।[3] सक्रिय उत्प्रेरक प्रजाति CuO है। ZnO का कार्य संरचनात्मक सहायता प्रदान करने के साथ-साथ सल्फर द्वारा तांबे के जहर को रोकना है। Al2O3 फैलाव और पेलेट सिकुड़न को रोकता है। एलटीएस शिफ्ट रिएक्टर 200-250 डिग्री सेल्सियस की सीमा पर संचालित होता है। ऊपरी तापमान की सीमा तांबे की थर्मल सिंटरिंग की संवेदनशीलता के कारण होती है। ये कम तापमान एचटीएस के मामले में देखी जाने वाली पार्श्व प्रतिक्रियाओं की घटना को भी कम करते हैं। सेरिया पर समर्थित प्लेटिनम जैसी महान धातुओं का भी एलटीएस के लिए उपयोग किया गया है।[9]
क्रियाविधि
डब्ल्यूजीएसआर का अध्ययन सौ वर्षों से अधिक समय से किया जा रहा है। काइनेटिक रूप से प्रासंगिक तंत्र उत्प्रेरक संरचना और तापमान पर निर्भर करता है। [6][13] दो तंत्र प्रस्तावित किए गए हैं: एक सहयोगी लैंगमुइर-हिंसलवुड तंत्र और एक रेडॉक्स तंत्र। रेडॉक्स तंत्र को आमतौर पर औद्योगिक लौह-क्रोमियम उत्प्रेरक पर उच्च तापमान डब्ल्यूजीएसआर (>350 °C) के दौरान गतिज रूप से प्रासंगिक माना जाता है।[5] ऐतिहासिक रूप से, कम तापमान पर तंत्र के बारे में बहुत विवाद रहा है। हाल के प्रायोगिक अध्ययन इस बात की पुष्टि करते हैं कि संबंधित कार्बोक्सिल तंत्र धातु-ऑक्साइड-समर्थित संक्रमण धातु कटैलिसीस पर प्रमुख निम्न-तापमान मार्ग है।[14][12]
सहयोगी तंत्र
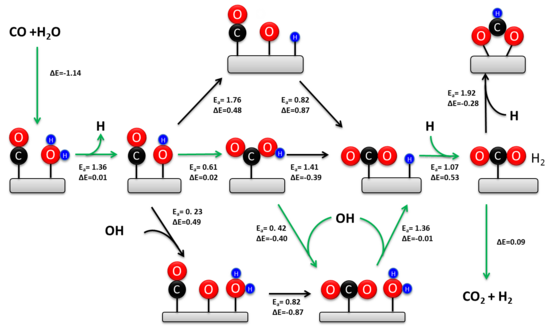
1920 में आर्मस्ट्रांग और हिल्डिच ने पहली बार साहचर्य तंत्र का प्रस्ताव रखा। इस क्रियाविधि में, CO और H2O को उत्प्रेरक की सतह पर अधिशोषित किया जाता है, इसके बाद एक मध्यवर्ती का निर्माण होता है और H2 और CO2 का विशोषण होता है। सामान्य तौर पर, H2O उत्प्रेरक पर विघटित होकर OH और H का उत्पादन करता है। पृथक्कृत जल CO के साथ प्रतिक्रिया करके कार्बोक्सिल बनाता है या मध्यवर्ती बनाता है। मध्यवर्ती बाद में CO2 उत्पन्न करने के लिए डीहाइड्रोजेनेट करता है और H को अधिशोषित करता है। दो अधिशोषित H परमाणु H2 बनाने के लिए पुन: संयोजित होते हैं।
सहयोगी तंत्र के दौरान गतिशील रूप से प्रासंगिक मध्यवर्ती के आसपास महत्वपूर्ण विवाद रहा है। प्रायोगिक अध्ययनों से संकेत मिलता है कि दोनों मध्यवर्ती धातु ऑक्साइड समर्थित संक्रमण धातु उत्प्रेरक पर प्रतिक्रिया दर में योगदान करते हैं।[14][12] हालांकि, ऑक्साइड समर्थन पर अधिशोषित फॉर्मेट की थर्मोडायनामिक स्थिरता के कारण कार्बोक्सिल मार्ग समग्र दर का लगभग 90% है। कार्बोक्सिल गठन के लिए सक्रिय साइट में एक अवशोषित हाइड्रॉक्सिल से सटे एक धातु परमाणु होते हैं। यह धातु-ऑक्साइड इंटरफेस पर आसानी से बनता है और विस्तारित धातु सतहों के सापेक्ष ऑक्साइड-समर्थित संक्रमण धातुओं की उच्च गतिविधि की व्याख्या करता है।[12] डब्ल्यूजीएसआर के लिए टर्न-ओवर-फ्रीक्वेंसी हाइड्रॉक्सिल गठन के संतुलन स्थिरांक के समानुपाती होती है, जो गैर-कमजोर समर्थन (जैसे SiO2) और विस्तारित धातु सतहों की तुलना में रिड्यूसिबल ऑक्साइड सपोर्ट (जैसे CeO2) पर तर्कसंगत बनाता है। जैसे पं.) आप अधिक सक्रिय क्यों हैं? कार्बोक्सिल गठन के लिए सक्रिय साइट के विपरीत, विस्तारित धातु सतहों पर फॉर्मेट गठन होता है। ऑक्साइड-समर्थित परमाणु रूप से फैले हुए संक्रमण धातु उत्प्रेरक का उपयोग करके डब्ल्यूजीएसआर के दौरान फॉर्मेट इंटरमीडिएट को समाप्त किया जा सकता है, आगे कार्बोक्सिल मार्ग के गतिज प्रभुत्व की पुष्टि करता है।[15]
रेडॉक्स तंत्र
रेडॉक्स तंत्र में उत्प्रेरक सामग्री के ऑक्सीकरण अवस्था में परिवर्तन सम्मिलित है। इस तंत्र में, CO2 बनाने के लिए उत्प्रेरक सामग्री से आंतरिक रूप से जुड़े एक O-परमाणु द्वारा CO का ऑक्सीकरण किया जाता है। एक पानी का अणु दो हाइड्रॉक्सिल उत्पन्न करने के लिए नवगठित ओ-रिक्ति पर विघटनकारी सोखना से गुजरता है। हाइड्रॉक्सिल्स अनुपातहीन होकर H2 उत्पन्न करते हैं और उत्प्रेरक सतह को उसकी पूर्व-प्रतिक्रिया अवस्था में लौटा देते हैं।
समरूप मॉडल
तंत्र में M-CO केंद्र पर पानी या हाइड्रॉक्साइड का न्यूक्लियोफिलिक हमला होता है, जिससे मेटालैकारबॉक्सिलिक एसिड उत्पन्न होता है।[2][16]
ऊष्मप्रवैगिकी
कमरे के तापमान (298 K) पर निम्न थर्मोडायनेमिक पैरामीटर के साथ डब्ल्यूजीएसआर एक्सर्जोनिक है:
Free energy ΔG⊖ = –6.82 kcal Enthalpy ΔH⊖ = –9.84 kcal Entropy ΔS⊖ = –10.1 cal/deg
जलीय घोल में, प्रतिक्रिया कम ऊर्जा उत्पन्न करने वाली होती है।[17]
रिवर्स वाटर-गैस शिफ्ट
चूँकि वाटर-गैस शिफ्ट रिएक्शन एक संतुलन प्रतिक्रिया है, इसलिए 'रिवर्स' वॉटर-गैस शिफ्ट रिएक्शन नहीं होता है। जल गैस को मुख्य रूप से कार्बन मोनोऑक्साइड (CO) और हाइड्रोजन (H2) से युक्त ईंधन गैस के रूप में परिभाषित किया जाता है। वाटर-गैस शिफ्ट में 'शिफ्ट' शब्द का अर्थ जल-गैस संरचना (CO: H2) अनुपात को बदलना है। रिएक्टर में CO2 मिलाकर अनुपात बढ़ाया जा सकता है या भाप जोड़कर कम किया जा सकता है।
यह भी देखें
- स्वस्थानी संसाधनों का उपयोग
- लेन हाइड्रोजन उत्पादक
- प्रॉक्सी
- औद्योगिक उत्प्रेरक
- सोरशन वर्धित जल गैस शिफ्ट
- सिनगैस
संदर्भ
- ↑ Water Gas Shift Catalysis a combined experimental and computational study
- ↑ 2.0 2.1 2.2 2.3 Vielstich, Wolf; Lamm, Arnold; Gasteiger, Hubert A., eds. (2003). ईंधन कोशिकाओं की पुस्तिका: मूल बातें, प्रौद्योगिकी, अनुप्रयोग. New York: Wiley. ISBN 978-0-471-49926-8.
- ↑ 3.0 3.1 3.2 3.3 Callaghan, Caitlin (2006). जल-गैस-शिफ्ट प्रतिक्रिया का काइनेटिक्स और उत्प्रेरण: एक सूक्ष्म गतिज और ग्राफ सैद्धांतिक दृष्टिकोण (PDF) (PhD). Worcester Polytechnic Institute.
- ↑ Jansen, Daniel; van Selow, Edward; Cobden, Paul; Manzolini, Giampaolo; Macchi, Ennio; Gazzani, Matteo; Blom, Richard; Heriksen, Partow Pakdel; Beavis, Rich; Wright, Andrew (2013-01-01). "SEWGS प्रौद्योगिकी अब स्केल-अप के लिए तैयार है!". Energy Procedia (in English). 37: 2265–2273. doi:10.1016/j.egypro.2013.06.107. ISSN 1876-6102.
- ↑ 5.0 5.1 Ratnasamy, Chandra; Wagner, Jon P. (September 2009). "जल गैस शिफ्ट कटैलिसीस". Catalysis Reviews. 51 (3): 325–440. doi:10.1080/01614940903048661. S2CID 98530242.
- ↑ 6.0 6.1 Smith R J, Byron; Muruganandam Loganthan; Murthy Shekhar Shantha (2010). "जल गैस शिफ्ट प्रतिक्रिया की समीक्षा". International Journal of Chemical Reactor Engineering. 8: 1–32. doi:10.2202/1542-6580.2238. S2CID 96769998.
- ↑ 7.0 7.1 Newsome, David S. (1980). "जल-गैस शिफ्ट रिएक्शन". Catalysis Reviews: Science and Engineering. 21 (2): 275–318. doi:10.1080/03602458008067535.
- ↑ Coletta, Vitor C.; Gonçalves, Renato V.; Bernardi, Maria I. B.; Hanaor, Dorian A. H.; Assadi, M. Hussein N.; Marcos, Francielle C. F.; Nogueira, Francisco G. E.; Assaf, Elisabete M.; Mastelaro, Valmor R. (2021). "Cu-संशोधित SrTiO3 पेरोव्स्काइट्स टुवर्ड्स एन्हांस्ड वाटर-गैस शिफ्ट कटैलिसीस: एक संयुक्त प्रायोगिक और कम्प्यूटेशनल अध्ययन". ACS Applied Energy Materials. 4: 452–461. arXiv:2104.06739. doi:10.1021/acsaem.0c02371. S2CID 233231670.
- ↑ Jain, Rishabh; Maric, Radenka (April 2014). "रिएक्टिव स्प्रे डिपोजिशन टेक्नोलॉजी द्वारा जल-गैस शिफ्ट रिएक्शन के लिए उत्प्रेरक के रूप में नैनो-पीटी ऑन सेरिया सपोर्ट का संश्लेषण". Applied Catalysis A: General. 475: 461–468. doi:10.1016/j.apcata.2014.01.053.
- ↑ Gokhale, Amit A.; Dumesic, James A.; Mavrikakis, Manos (2008-01-01). "कॉपर पर कम तापमान वाली जल गैस शिफ्ट रिएक्शन के तंत्र पर". Journal of the American Chemical Society. 130 (4): 1402–1414. doi:10.1021/ja0768237. ISSN 0002-7863. PMID 18181624.
- ↑ Grabow, Lars C.; Gokhale, Amit A.; Evans, Steven T.; Dumesic, James A.; Mavrikakis, Manos (2008-03-01). "पीटी पर जल गैस शिफ्ट रिएक्शन का तंत्र: प्रथम सिद्धांत, प्रयोग, और माइक्रोकाइनेटिक मॉडलिंग". The Journal of Physical Chemistry C. 112 (12): 4608–4617. doi:10.1021/jp7099702. ISSN 1932-7447.
- ↑ 12.0 12.1 12.2 12.3 Nelson, Nicholas C.; Szanyi, János (2020-05-15). "हेटरोलाइटिक हाइड्रोजन सक्रियण: जल-गैस शिफ्ट, हाइड्रोडीऑक्सीजनेशन, और सीओ ऑक्सीकरण कटैलिसीस में समर्थन प्रभावों को समझना". ACS Catalysis. 10 (10): 5663–5671. doi:10.1021/acscatal.0c01059. OSTI 1656557. S2CID 218798723.
- ↑ Yao, Siyu; Zhang, Xiao; Zhou, Wu; Gao, Rui; Xu, Wenqian; Ye, Yifan; Lin, Lili; Wen, Xiaodong; Liu, Ping; Chen, Bingbing; Crumlin, Ethan (2017-06-22). "निम्न-तापमान जल-गैस शिफ्ट प्रतिक्रिया के लिए उत्प्रेरक के रूप में α-MoC पर परमाणु-स्तरित Au क्लस्टर". Science (in English). 357 (6349): 389–393. Bibcode:2017Sci...357..389Y. doi:10.1126/science.aah4321. ISSN 0036-8075. PMID 28642235. S2CID 206651887.
- ↑ 14.0 14.1 Nelson, Nicholas C.; Nguyen, Manh-Thuong; Glezakou, Vassiliki-Alexandra; Rousseau, Roger; Szanyi, János (October 2019). "वाटर-गैस शिफ्ट कटैलिसीस के दौरान स्वस्थानी-जनित मेटास्टेबल सक्रिय साइट के माध्यम से कार्बोक्सिल मध्यवर्ती गठन". Nature Catalysis (in English). 2 (10): 916–924. doi:10.1038/s41929-019-0343-2. ISSN 2520-1158. S2CID 202729116.
- ↑ Nelson, Nicholas C.; Chen, Linxiao; Meira, Debora; Kovarik, Libor; Szanyi, János (2020). "TiO2 पर पैलेडियम के सीटू फैलाव में रिवर्स वॉटर-गैस शिफ्ट रिएक्शन के दौरान: परमाणु रूप से बिखरे हुए पैलेडियम का निर्माण". Angewandte Chemie International Edition (in English). 59 (40): 17657–17663. doi:10.1002/anie.202007576. ISSN 1521-3773. OSTI 1661896. PMID 32589820. S2CID 220118889.
- ↑ Barakat, Tarek; Rooke, Joanna C.; Genty, Eric; Cousin, Renaud; Siffert, Stéphane; Su, Bao-Lian (1 January 2013). "पर्यावरणीय उपचार और जल-गैस शिफ्ट प्रौद्योगिकियों में स्वर्ण उत्प्रेरक". Energy & Environmental Science. 6 (2): 371. doi:10.1039/c2ee22859a.
- ↑ King, A. D.; King, R. B.; Yang, D. B., "Homogeneous catalysis of the water gas shift reaction using iron pentacarbonyl", J. Am. Chem. Soc. 1980, vol. 102, pp. 1028-1032. doi:10.1021/ja00523a020