डिसोडियम टेट्राकार्बोनिलफेरेट: Difference between revisions
(Created page with "{{chembox |verifiedrevid = 449831753 |ImageFile = Disodium tetracarbonylferrate.png |IUPACName = disodium tetracarbonylferrate |SystematicName = disodium tetracarbonylferrate...") |
|||
| Line 42: | Line 42: | ||
== संश्लेषण == | == संश्लेषण == | ||
[[अभिकर्मक]] मूल रूप से सोडियम अमलगम के साथ लोहे के पेंटाकारबोनील को कम करके सीटू में उत्पन्न किया गया था।<ref name=Cooke>{{ cite journal | author = Cooke, M. P. | title = सोडियम टेट्राकार्बोनिलफेरेट (-II) का उपयोग करके अल्काइल ब्रोमाइड्स का एल्डिहाइड में सुगम रूपांतरण| journal = [[Journal of the American Chemical Society]] | year = 1970 | volume = 92 | issue = 20 | pages = 6080–6082 | doi = 10.1021/ja00723a056 }}</ref> आधुनिक संश्लेषण [[सोडियम नेफ़थलीन]] या सोडियम बेंजोफेनोन केटिल्स का उपयोग रिड्यूसेंट्स के रूप में करते हैं:<ref name = RJA/><ref>{{cite journal |author=Richard G. Finke, Thomas N. Sorrell|doi=10.15227/orgsyn.059.0102|title=Nucleophilic Acylation with Disodium Tetracarbonylferrate: Methyl 7-Oxoheptanoate and Methyl 7-Oxoöctanoate|journal=Organic Syntheses|year=1979|volume=59|page=102}}</ref> | [[अभिकर्मक]] मूल रूप से सोडियम अमलगम के साथ लोहे के पेंटाकारबोनील को कम करके सीटू में उत्पन्न किया गया था।<ref name=Cooke>{{ cite journal | author = Cooke, M. P. | title = सोडियम टेट्राकार्बोनिलफेरेट (-II) का उपयोग करके अल्काइल ब्रोमाइड्स का एल्डिहाइड में सुगम रूपांतरण| journal = [[Journal of the American Chemical Society]] | year = 1970 | volume = 92 | issue = 20 | pages = 6080–6082 | doi = 10.1021/ja00723a056 }}</ref> आधुनिक संश्लेषण [[सोडियम नेफ़थलीन]] या सोडियम बेंजोफेनोन केटिल्स का उपयोग रिड्यूसेंट्स के रूप में करते हैं:<ref name = RJA/><ref>{{cite journal |author=Richard G. Finke, Thomas N. Sorrell|doi=10.15227/orgsyn.059.0102|title=Nucleophilic Acylation with Disodium Tetracarbonylferrate: Methyl 7-Oxoheptanoate and Methyl 7-Oxoöctanoate|journal=Organic Syntheses|year=1979|volume=59|page=102}}</ref> | ||
: | :: Fe(CO)<sub>5</sub> + 2 Na → Na<sub>2</sub>[Fe(CO)<sub>4</sub>] + CO | ||
:: जब सोडियम की कमी का उपयोग किया जाता है, तो कमी गहरे पीले रंग के ऑक्टाकारबोनील अलग-अलग होती है: | |||
: 2 Fe(CO)<sub>5</sub> + 2 Na → Na<sub>2</sub>[Fe<sub>2</sub>(CO)<sub>8</sub>] + 2 CO | |||
<ref name="RJA" /> | |||
कुछ विशिष्ट विधियाँ आयरन कार्बोनिल से शुरू नहीं होती हैं।<ref name="ref1">{{cite book | author = Scholsser, M. | year = 2013 | title = सिंथेसिस में ऑर्गेनोमेटेलिक्स, तीसरा मैनुअल| location = Chicester, England | publisher = Wiley }}</ref> | |||
| Line 54: | Line 58: | ||
डिसोडियम टेट्राकार्बोनिलफेरेट का उपयोग [[एसिड क्लोराइड]] को एल्डिहाइड में बदलने के लिए किया जा सकता है। यह प्रतिक्रिया आयरन [[एसाइल]] कॉम्प्लेक्स की मध्यस्थता के माध्यम से आगे बढ़ती है। | डिसोडियम टेट्राकार्बोनिलफेरेट का उपयोग [[एसिड क्लोराइड]] को एल्डिहाइड में बदलने के लिए किया जा सकता है। यह प्रतिक्रिया आयरन [[एसाइल]] कॉम्प्लेक्स की मध्यस्थता के माध्यम से आगे बढ़ती है। | ||
: | :: Na<sub>2</sub>[Fe(CO)<sub>4</sub>] + RBr → Na[RFe(CO)<sub>4</sub>] + NaBr | ||
: | :: Na<sub>2</sub>[Fe(CO)<sub>4</sub>] + RCOCl → Na[RC(O)Fe(CO)<sub>4</sub>] + NaCl | ||
:: Na[RC(O)Fe(CO)<sub>4</sub>] + HCl → RCHO + "Fe(CO)<sub>4</sub>" + NaCl | |||
:: Na<sub>2</sub>[Fe(CO)<sub>4</sub>] + RX → Na[RFe(CO)<sub>4</sub>] + NaX | |||
डिसोडियम टेट्राकार्बोनिलफेरेट अल्काइल कॉम्प्लेक्स बनाने के लिए [[ अल्काइल हलाइड्स ]] (आरएक्स) के साथ प्रतिक्रिया करता है: | डिसोडियम टेट्राकार्बोनिलफेरेट अल्काइल कॉम्प्लेक्स बनाने के लिए [[ अल्काइल हलाइड्स ]] (आरएक्स) के साथ प्रतिक्रिया करता है: | ||
: | :: Na[RFe(CO)<sub>4</sub>] + O<sub>2</sub>, H<sup>+</sup> →→ RCO<sub>2</sub>H + Fe... | ||
इस तरह के लोहे के एल्किलों को संबंधित [[कार्बोज़ाइलिक तेजाब]] और [[एसिड हलाइड]]्स में परिवर्तित किया जा सकता है: | इस तरह के लोहे के एल्किलों को संबंधित [[कार्बोज़ाइलिक तेजाब]] और [[एसिड हलाइड]]्स में परिवर्तित किया जा सकता है: | ||
: | :: Na[RFe(CO)<sub>4</sub>] + 2 X<sub>2</sub> → RC(O)X + FeX<sub>2</sub> + 3 CO + NaX | ||
: | : | ||
<!-- Lithium (or CO) can be added to form the complex [LFe(CO)<sub>3</sub>(C(O)R)]Na, then R<sup>'</sup>X can be added to form RC(O)R<sup>'</sup>.<ref name="ref1"></ref> | <!-- Lithium (or CO) can be added to form the complex [LFe(CO)<sub>3</sub>(C(O)R)]Na, then R<sup>'</sup>X can be added to form RC(O)R<sup>'</sup>.<ref name="ref1"></ref> | ||
Revision as of 21:34, 25 March 2023
| |
| Names | |
|---|---|
| IUPAC name
disodium tetracarbonylferrate
| |
| Systematic IUPAC name
disodium tetracarbonylferrate | |
| Other names
disodium iron tetracarbonyl,
Collman's reagent
| |
| Identifiers | |
3D model (JSmol)
|
|
| EC Number |
|
PubChem CID
|
|
| |
| |
| Properties | |
| C4FeNa2O4 | |
| Molar mass | 213.87 |
| Appearance | Colorless solid |
| Density | 2.16 g/cm3, solid |
| Decomposes | |
| Solubility | tetrahydrofuran, dimethylformamide, dioxane |
| Structure | |
| Distorted tetrahedron | |
| Tetrahedral | |
| Hazards | |
| Occupational safety and health (OHS/OSH): | |
Main hazards
|
Pyrophoric |
| Related compounds | |
Related compounds
|
Iron pentacarbonyl |
Except where otherwise noted, data are given for materials in their standard state (at 25 °C [77 °F], 100 kPa).
| |
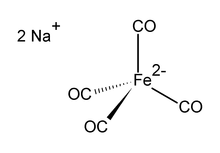
डिसोडियम टेट्राकार्बोनिलफेरेट सूत्र ना के साथ ऑर्गेनोआयरन यौगिक है2[फे (सीओ)4]। यह हमेशा सॉल्वेट के रूप में प्रयोग किया जाता है, उदाहरण के लिए, टेट्राहाइड्रोफ्यूरान या डाईमेथोक्सीएथेन के साथ, जो सोडियम केशन से जुड़ता है।[1] एक ऑक्सीजन-संवेदनशील रंगहीन ठोस, यह ऑर्गोनोमेटिक और कार्बनिक रासायनिक अनुसंधान में एक अभिकर्मक है। डाइऑक्सेन सॉल्वेटेड सोडियम नमक को कोलमैन के अभिकर्मक के रूप में जाना जाता है, जेम्स पी। कोलमैन की मान्यता में, इसके उपयोग के शुरुआती लोकप्रिय।[2]
संरचना
डायनियन [Fe(CO)]4]2− Ni(CO) के साथ समइलेक्ट्रॉनिक है4.[3][4] लोहे का केंद्र Na के साथ टेट्राहेड्रल है+---OCFe इंटरैक्शन। यह आमतौर पर सोडियम केशन के लिए जटिल डाइअॉॉक्सिन के साथ प्रयोग किया जाता है।
संश्लेषण
अभिकर्मक मूल रूप से सोडियम अमलगम के साथ लोहे के पेंटाकारबोनील को कम करके सीटू में उत्पन्न किया गया था।[5] आधुनिक संश्लेषण सोडियम नेफ़थलीन या सोडियम बेंजोफेनोन केटिल्स का उपयोग रिड्यूसेंट्स के रूप में करते हैं:[1][6]
- Fe(CO)5 + 2 Na → Na2[Fe(CO)4] + CO
- जब सोडियम की कमी का उपयोग किया जाता है, तो कमी गहरे पीले रंग के ऑक्टाकारबोनील अलग-अलग होती है:
- 2 Fe(CO)5 + 2 Na → Na2[Fe2(CO)8] + 2 CO
[1] कुछ विशिष्ट विधियाँ आयरन कार्बोनिल से शुरू नहीं होती हैं।[7]
प्रतिक्रियाएं
इसका उपयोग एल्काइल हलाइड्स से एल्डिहाइड को संश्लेषित करने के लिए किया जाता है।[8] अभिकर्मक को मूल रूप से दो-चरण, एक-पॉट प्रतिक्रिया में संबंधित एल्डिहाइड में प्राथमिक एल्काइल ब्रोमाइड के रूपांतरण के लिए वर्णित किया गया था:[5]: नहीं2[फे (सीओ)4] + आरबीआर → ना[आरएफई(सीओ)4] + नाबर इसके बाद इस घोल को ट्राइफेनिलफॉस्फीन | पीपीएच के साथ क्रमिक रूप से उपचारित किया जाता है3और फिर एल्डिहाइड, RCHO देने के लिए एसीटिक अम्ल ।
डिसोडियम टेट्राकार्बोनिलफेरेट का उपयोग एसिड क्लोराइड को एल्डिहाइड में बदलने के लिए किया जा सकता है। यह प्रतिक्रिया आयरन एसाइल कॉम्प्लेक्स की मध्यस्थता के माध्यम से आगे बढ़ती है।
- Na2[Fe(CO)4] + RBr → Na[RFe(CO)4] + NaBr
- Na2[Fe(CO)4] + RCOCl → Na[RC(O)Fe(CO)4] + NaCl
- Na[RC(O)Fe(CO)4] + HCl → RCHO + "Fe(CO)4" + NaCl
- Na2[Fe(CO)4] + RX → Na[RFe(CO)4] + NaX
डिसोडियम टेट्राकार्बोनिलफेरेट अल्काइल कॉम्प्लेक्स बनाने के लिए अल्काइल हलाइड्स (आरएक्स) के साथ प्रतिक्रिया करता है:
- Na[RFe(CO)4] + O2, H+ →→ RCO2H + Fe...
इस तरह के लोहे के एल्किलों को संबंधित कार्बोज़ाइलिक तेजाब और एसिड हलाइड्स में परिवर्तित किया जा सकता है:
- Na[RFe(CO)4] + 2 X2 → RC(O)X + FeX2 + 3 CO + NaX
संदर्भ
- ↑ 1.0 1.1 1.2 Strong, H.; Krusic, P. J.; San Filippo, J. (1990). "Sodium Carbonyl Ferrates, Na2[Fe(CO)4], Na2[Fe2(CO)8], and Na2[Fe3(CO)11]. Bis[μ-Nitrido-Bis(triphenylphosphorus)1+] Undeca-Carbonyltriferrate2−, [(Ph3P)2N]2[Fe3(CO)11]". Inorganic Syntheses. 28: 203–207. doi:10.1002/9780470132593.ch52. ISBN 0-471-52619-3.
- ↑ Miessler, G. L.; Tarr, D. A. (2004). अकार्बनिक रसायन शास्त्र. Upper Saddle River, NJ: Pearson.
- ↑ Chin, H. B.; Bau, R. (1976). "The Crystal Structure of Disodium Tetracarbonylferrate. Distortion of the Tetracarbonylferrate2− Anion in the Solid State". Journal of the American Chemical Society. 98 (9): 2434–2439. doi:10.1021/ja00425a009.
- ↑ Teller, R. G.; Finke, R. G.; Collman, J. P.; Chin, H. B.; Bau, R. (1977). "Dependence of the tetracarbonylferrate(2-) geometry on counterion: crystal structures of dipotassium tetracarbonylferrate and bis(sodium crypt) tetracarbonylferrate [crypt = N(CH2CH2OCH2CH2OCH2CH2)3N]". Journal of the American Chemical Society. 99 (4): 1104–1111. doi:10.1021/ja00446a022.
{{cite journal}}: CS1 maint: uses authors parameter (link) - ↑ 5.0 5.1 Cooke, M. P. (1970). "सोडियम टेट्राकार्बोनिलफेरेट (-II) का उपयोग करके अल्काइल ब्रोमाइड्स का एल्डिहाइड में सुगम रूपांतरण". Journal of the American Chemical Society. 92 (20): 6080–6082. doi:10.1021/ja00723a056.
- ↑ Richard G. Finke, Thomas N. Sorrell (1979). "Nucleophilic Acylation with Disodium Tetracarbonylferrate: Methyl 7-Oxoheptanoate and Methyl 7-Oxoöctanoate". Organic Syntheses. 59: 102. doi:10.15227/orgsyn.059.0102.
- ↑ Scholsser, M. (2013). सिंथेसिस में ऑर्गेनोमेटेलिक्स, तीसरा मैनुअल. Chicester, England: Wiley.
- ↑ Pike, R. D. (2001). "डिसोडियम टेट्राकार्बोनिलफेरेट (-II)". Encyclopedia of Reagents for Organic Synthesis. doi:10.1002/047084289X.rd465.
अग्रिम पठन
- Collman, J. P. (1975). "Disodium Tetracarbonylferrate, a Transition Metal Analog of a Grignard Reagent". Accounts of Chemical Research. 8 (10): 342–347. doi:10.1021/ar50094a004.
- Ungurenasu, C.; Cotzur, C. (1982). "Disodium Tetracarbonylferrate: A Reagent for Acid Functionalization of Halogenated Polymers". Polymer Bulletin. 6 (5–6): 299–303. doi:10.1007/BF00255401. S2CID 101154955.
- Hieber, V. W.; Braun, G. (1959). "Notizen: "Rheniumcarbonylwasserstoff" und Methylpentacarbonylrhenium". Zeitschrift für Naturforschung B. 14 (2): 132–133. doi:10.1515/znb-1959-0214. S2CID 94402946.