एथिलबेन्जीन: Difference between revisions
No edit summary |
No edit summary |
||
| Line 114: | Line 114: | ||
3 जून 2014 को डच [[मोरडिज्क]] औद्योगिक क्षेत्र में एक विस्फोट हुआ। यह [[ शैल पीएलसी | शैल पीएलसी]] द्वारा संचालित एक रासायनिक रिएक्टर में हुआ, <ref>https://www.onderzoeksraad.nl/nl/media/attachment/2018/7/10/06d477404859summary_shell_moerdijk.pdf {{bare URL PDF|date=July 2023}}</ref>जो धातु ऑक्साइड उत्प्रेरक और एथिलबेंजीन के बीच एक अतितापी अस्थायी प्रतिक्रिया या [[बेलगाम उष्म वायु प्रवाह|अनियंत्रित उष्म वायु प्रवाह]] के कारण अधिक गरम हो गया। | 3 जून 2014 को डच [[मोरडिज्क]] औद्योगिक क्षेत्र में एक विस्फोट हुआ। यह [[ शैल पीएलसी | शैल पीएलसी]] द्वारा संचालित एक रासायनिक रिएक्टर में हुआ, <ref>https://www.onderzoeksraad.nl/nl/media/attachment/2018/7/10/06d477404859summary_shell_moerdijk.pdf {{bare URL PDF|date=July 2023}}</ref>जो धातु ऑक्साइड उत्प्रेरक और एथिलबेंजीन के बीच एक अतितापी अस्थायी प्रतिक्रिया या [[बेलगाम उष्म वायु प्रवाह|अनियंत्रित उष्म वायु प्रवाह]] के कारण अधिक गरम हो गया। | ||
==स्वास्थ्य प्रभाव== | ==स्वास्थ्य प्रभाव== | ||
एथिलबेंजीन की तीव्र [[विषाक्तता]] कम होती है, जिसका LD<sub>50</sub> लगभग 4 ग्राम प्रति किलोग्राम शरीर वजन होता है। लंबे समय तक विषाक्तता और कैंसर के प्रभाव में अस्पष्टता होती है।<ref name="Ullmann">Vincent A.Welch, Kevin J. Fallon, Heinz-Peter Gelbke “Ethylbenzene” ''Ullmann’s Encyclopedia of Industrial Chemistry'', Wiley-VCH, Weinheim, 2005. {{doi|10.1002/14356007.a10_035.pub2}}</ref> उच्च स्तर के वायु में एथिलबेंजीन के उच्च स्तर के असर के साथ आँखों और गले की संवेदनशीलता हो सकती है। उच्चस्तर के संपर्क में, एथिलबेंजीन चक्कर आने का कारण बन सकता है।<ref name="Ethylbenzene1" /> शरीर में पहुंचने के बाद, एथिलबेंजीन का जैविक अपघटन होता है और इसे 1-फिनाइलइथेनॉल, ऐसिटोफीनोन, [[फेनिलग्लॉक्सिलिक एसिड]], [[मैंडेलिक एसिड]], [[ बेंज़ोइक एसिड |बेंज़ोइक एसिड]] और [[हिप्पुरिक एसिड]] में बदल जाता है। एथिलबेंजीन के संपर्क में आने पर मूत्र में विघटन उत्पादों की जांच करके एक्सपोजर का निर्धारण किया जा सकता है। | |||
सितंबर 2007 तक, संयुक्त राज्य पर्यावरण संरक्षण एजेंसी (ईपीए) ने निर्धारित किया कि एक दिन के लिए 30 भाग प्रति मिलियन (पीपीएम) या दस दिनों के लिए 3 पीपीएम की सांद्रता वाला पानी पीने से बच्चों में कोई प्रतिकूल प्रभाव पड़ने की | सितंबर 2007 तक, संयुक्त राज्य पर्यावरण संरक्षण एजेंसी (ईपीए) ने निर्धारित किया कि एक दिन के लिए 30 भाग प्रति मिलियन (पीपीएम) या दस दिनों के लिए 3 पीपीएम की सांद्रता वाला पानी पीने से बच्चों में कोई प्रतिकूल प्रभाव पड़ने की संभावना नहीं है। एथिलबेंजीन की 0.7 पीपीएम की जीवनकालिक अवसरण का कोई भी नकारात्मक प्रभाव का उम्मीद नहीं किया जाता है। यह यू.एस. के मानकों और नियंत्रण नियमों के अनुसार होता है। अमेरिकी व्यावसायिक सुरक्षा और स्वास्थ्य प्रशासन श्रमिकों के संपर्क को 8-घंटे के कार्यदिवस, 40-घंटे के कार्यसप्ताह के लिए औसतन 100 पीपीएम तक सीमित करता है।<ref name="Ethylbenzene1" /> | ||
[[अंतरराष्ट्रीय कैंसर अनुसंधान संस्था]] (आईएआरसी) द्वारा एथिलबेन्जीन को संभावित कार्सिनोजेन के रूप में वर्गीकृत किया गया है,यद्यपि, ईपीए ने एथिलबेन्जीन को कार्सिनोजेन निर्धारित नहीं किया है। नेशनल टॉक्सिकोलॉजी प्रोग्राम ने चूहों और चुहियों में एक इनहेलेशन अध्ययन किया। एथिलबेन्जीन के संपर्क में आने से नर चूहों में गुर्दे और वृषण ट्यूमर की घटनाओं में वृद्धि हुई, और मादा चूहों में गुर्दे के ट्यूमर, नर चूहों में फेफड़ों के ट्यूमर और मादा चूहों में यकृत ट्यूमर की प्रवृत्ति में वृद्धि हुई। | |||
सभी कार्बनिक यौगिकों की तरह, एथिलबेन्जीन वाष्प हवा के साथ एक विस्फोटक मिश्रण बनाते हैं।<ref name="ref4" /> एथिलबेन्जीन का परिवहन करते समय, इसे कक्षा 3, [[पैकिंग समूह]] में एक ज्वलनशील तरल के रूप में वर्गीकृत किया जाता है।<ref name="ref4" /> | |||
===पर्यावरणीय प्रभाव=== | ===पर्यावरणीय प्रभाव=== | ||
एथिलबेंजीन अधिकतर वायु में वाष्प के रूप में पाया जाता है<ref name="Ethylbenzene1" /> क्योंकि यह जल और मिट्टी से आसानी से भ्रमण कर सकता है। 1999 में नगरीय वायु में औसत अधिकार एक प्रतिमिल्लियन की मात्रा के 0.62 पार्ट्स प्रति बिलियन में पाया गया था।<ref name="Ref 3">{{cite web|title=Technology Transfer Network Air Toxics Web Site: Ethylbenzene|url=http://www.epa.gov/ttnatw01/hlthef/ethylben.html|publisher=US Environmental Protection Agency|access-date=13 February 2013}}</ref> 2012 में किए गए एक अध्ययन में पाया गया कि देश की हवा में औसत सांद्रता 0.01 पीपीबी और घर के अंदर औसत सांद्रता 1.0 पीपीबी पाई गई। इसे [[कोयला]], गैस और [[तेल]] के जलने से भी हवा में छोड़ा जा सकता है। उद्योग में एथिलबेन्जीन का उपयोग हवा में एथिलबेन्जीन वाष्प में योगदान देता है। हवा में लगभग तीन दिनों तक सूरज की रोशनी की मदद से रहने के बाद, अन्य रसायन एथिलबेन्जीन को ऐसे रसायनों में तोड़ देते हैं जो [[ धुंध | धुंध]] में पाए जा सकते हैं।<ref name="Ethylbenzene1" />चूँकि यह आसानी से मिट्टी से नहीं जुड़ता है इसलिए यह सरलता से [[भूजल]] में भी चला जाता है। सतही जल में, यह तब टूट जाता है जब यह पानी में प्राकृतिक रूप से पाए जाने वाले रसायनों के साथ प्रतिक्रिया करता है।<ref name="Ref 2">{{cite web|title=एथिलबेन्जीन|url=http://www.eco-usa.net/toxics/chemicals/ethylbenzene.shtml|publisher=eco-usa.net|access-date=12 February 2013|url-status=dead|archive-url=https://web.archive.org/web/20121225134046/http://www.eco-usa.net/toxics/chemicals/ethylbenzene.shtml|archive-date=25 December 2012}}</ref> सामान्यतः, एथिलबेन्जीन पीने के पानी में नहीं पाया जाता है, यद्यपि यह आवासीय पेयजल कुओं में पाया जा सकता है या निवासीय पेयजल के कुएं में एथिलबेंजीन पाया जा सकता है। | |||
2012 | 2012 के अनुसार, यूरोपीय संघ के संकटमय पदार्थ निदेशिका के अनुसार, एथिलबेंजीन पर्यावरण के लिए खतरनाक कटिबद्ध नहीं किया गया है।<ref name="ref4" /> | ||
इथाइलबेन्जीन तंबाकू के धुएं का एक घटक है।<ref name="TalhoutSchulz2011">{{cite journal|last1=Talhout|first1=Reinskje|last2=Schulz|first2=Thomas|last3=Florek|first3=Ewa|last4=Van Benthem|first4=Jan|last5=Wester|first5=Piet|last6=Opperhuizen|first6=Antoon|title=तम्बाकू के धुएँ में खतरनाक यौगिक|journal=International Journal of Environmental Research and Public Health|volume=8|issue=12|year=2011|pages=613–628|issn=1660-4601|doi=10.3390/ijerph8020613|pmid=21556207|pmc=3084482|doi-access=free}}</ref> | इथाइलबेन्जीन तंबाकू के धुएं का एक घटक है।<ref name="TalhoutSchulz2011">{{cite journal|last1=Talhout|first1=Reinskje|last2=Schulz|first2=Thomas|last3=Florek|first3=Ewa|last4=Van Benthem|first4=Jan|last5=Wester|first5=Piet|last6=Opperhuizen|first6=Antoon|title=तम्बाकू के धुएँ में खतरनाक यौगिक|journal=International Journal of Environmental Research and Public Health|volume=8|issue=12|year=2011|pages=613–628|issn=1660-4601|doi=10.3390/ijerph8020613|pmid=21556207|pmc=3084482|doi-access=free}}</ref> | ||
===जैव निम्नीकरण=== | ===जैव निम्नीकरण=== | ||
कवक [[क्लैडोफियालोफोरा]] के कुछ उपभेद एथिलबेन्जीन पर विकसित हो सकते हैं।<ref>{{cite journal | title=वाष्पशील सुगंधित हाइड्रोकार्बन पर उनके एकमात्र कार्बन और ऊर्जा स्रोत के रूप में उगने वाले कवक का अलगाव और लक्षण वर्णन|author1=Francesc X. PRENAFETA-BOLDU|author2=Andrea KUHN|author3=Dion M. A. M. LUYKX|author4=Heidrun ANKE|author5=Johan W. van GROENESTIJN|author6=Jan A. M. de BONT|volume=105|issue=4|pages=477–484|date=April 2001|doi=10.1017/s0953756201003719|journal=Mycological Research}}</ref> जीवाणु [[सुगंधित तेल]] ईबीएन1 की खोज एथिलबेन्जीन पर बढ़ने की क्षमता के कारण की गई थी।<ref>{{Cite journal | last1 = Rabus | first1 = R. | last2 = Widdel | first2 = F. | कवक [[क्लैडोफियालोफोरा]] के कुछ उपभेद एथिलबेन्जीन पर विकसित हो सकते हैं।<ref>{{cite journal | title=वाष्पशील सुगंधित हाइड्रोकार्बन पर उनके एकमात्र कार्बन और ऊर्जा स्रोत के रूप में उगने वाले कवक का अलगाव और लक्षण वर्णन|author1=Francesc X. PRENAFETA-BOLDU|author2=Andrea KUHN|author3=Dion M. A. M. LUYKX|author4=Heidrun ANKE|author5=Johan W. van GROENESTIJN|author6=Jan A. M. de BONT|volume=105|issue=4|pages=477–484|date=April 2001|doi=10.1017/s0953756201003719|journal=Mycological Research}}</ref> जीवाणु [[सुगंधित तेल]] ईबीएन1 की खोज एथिलबेन्जीन पर बढ़ने की क्षमता के कारण की गई थी।<ref>{{Cite journal | last1 = Rabus | first1 = R. | last2 = Widdel | first2 = F. | ||
Revision as of 11:20, 27 July 2023

| |||
|
| |||
| Names | |||
|---|---|---|---|
| IUPAC name
Ethylbenzene
| |||
| Other names
Ethylbenzol; Phenylethane; alpha-Methyltoluene; EB
| |||
| Identifiers | |||
3D model (JSmol)
|
|||
| Abbreviations | EB | ||
| 1901871 | |||
| ChEBI | |||
| ChEMBL | |||
| ChemSpider | |||
| DrugBank | |||
| KEGG | |||
PubChem CID
|
|||
| RTECS number |
| ||
| UNII | |||
| |||
| |||
| Properties | |||
| C8H10 | |||
| Molar mass | 106.168 g·mol−1 | ||
| Appearance | colorless liquid | ||
| Odor | aromatic[1] | ||
| Density | 0.8665 g/mL | ||
| Melting point | −95 °C (−139 °F; 178 K) | ||
| Boiling point | 136 °C (277 °F; 409 K) | ||
| 0.015 g/100 mL (20 °C) | |||
| log P | 3.27 | ||
| Vapor pressure | 9.998 mmHg | ||
| -77.20·10−6 cm3/mol | |||
Refractive index (nD)
|
1.495 | ||
| Viscosity | 0.669 cP at 20 °C | ||
| 0.58 D[2] | |||
| Thermochemistry | |||
Heat capacity (C)
|
1.726 J/(gK) | ||
| Hazards | |||
| Occupational safety and health (OHS/OSH): | |||
Main hazards
|
Flammable | ||
| GHS labelling: | |||
   
| |||
| Danger | |||
| H225, H304, H320, H332, H335, H336, H351, H360, H373, H400, H411 | |||
| P201, P202, P210, P233, P240, P241, P242, P243, P260, P261, P264, P271, P273, P280, P281, P301+P310, P303+P361+P353, P304+P312, P304+P340, P305+P351+P338, P308+P313, P312, P314, P331, P337+P313, P370+P378, P391, P403+P233, P403+P235, P405, P501 | |||
| NFPA 704 (fire diamond) | |||
| Flash point | 22.22 °C (72.00 °F; 295.37 K) | ||
| 430 °C (806 °F; 703 K) | |||
| Explosive limits | 1–7.8% | ||
| Lethal dose or concentration (LD, LC): | |||
LD50 (median dose)
|
5460 mg/kg | ||
LCLo (lowest published)
|
4000 ppm (rat, 4 hr)[3] | ||
| NIOSH (US health exposure limits): | |||
PEL (Permissible)
|
TWA 100 ppm (435 mg/m3)[1] | ||
REL (Recommended)
|
TWA 100 ppm (435 mg/m3) ST 125 ppm (545 mg/m3)[1] | ||
IDLH (Immediate danger)
|
800 ppm[1] | ||
| Related compounds | |||
Related aromatic
hydrocarbons |
styrene, toluene | ||
Related compounds
|
benzene polystyrene | ||
Except where otherwise noted, data are given for materials in their standard state (at 25 °C [77 °F], 100 kPa).
| |||
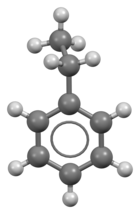
एथिलबेन्जीन सूत्र वाला एक कार्बनिक यौगिक है जिसका रासायनिक सूत्र C6H5CH2CH3 है। यह अत्यधिक ज्वलनशील, रंगहीन तरल है जिसकी गंध पेट्रोल के समान होती है।
यह एकचक्रीय सुगंधित हाइड्रोकार्बन है जो पेट्रोकेमिकल उद्योग में महत्वपूर्ण है, क्योंकि इसे स्टाइरीन के उत्पादन में एक प्रतिक्रिया मध्यवर्ती के रूप में उपयोग किया जाता है। स्टाइरीन पॉलिस्टाइरीन, एक सामान्य प्लास्टिक सामग्री, का पूर्वावस्था उत्पन्न करता है। 2012 में, एथिलबेंजीन के उत्पादन का 99% से अधिक स्टाइरीन के उत्पादन में खपत किया गया था।
घटना और अनुप्रयोग
एथिलबेन्जीन प्राकृतिक रूप से कोयला टार और पेट्रोलियम में पाया जाता है।[4]एथिलबेंजीन का प्रमुख उपयोग पॉलिस्टाइरीन के उत्पादन में एक बाधक के रूप में होता है। एथिलबेंजीन की कैटलिटिक डाइहाइड्रोजनीकरण से हाइड्रोजन और स्टाइरीन मिलता है:
- C
6H
5CH
2CH
3 → C6H5CH=CH2 + H
2
मई 2012 तक, सभी एथिलबेंजीन के उत्पादन का 99% से अधिक भाग इस उद्देश्य के लिए उपयोग किया जाता था।
एथिलबेन्जीन हाइड्रोपेरोक्साइड, एक अभिकर्मक और रेडिकल प्रेरक, एथिलबेन्जीन के ऑटोऑक्सीकरण से उत्पन्न होता है।
C6H5CH2CH3 + O2 → C6H5CH(O2H)CH3
आला उपयोग
एथिलबेंजीन को गैसोलीन में जोड़ा जाता है जिससे इंजन की खटखटाहट को कम करने और ऑक्टेन रेटिंग को बढ़ाने के लिए एक एंटी-नॉक एजेंट के रूप में जोड़ा जाता है। एथिलबेंजीन प्रायः अन्य उत्पादों में भी पाया जाता है, जिनमें कीटनाशक, सेल्युलोज ऐसिटेट, सिंथेटिक रबर, पेंट और स्याही सहित अन्य उत्पादों में पाया जाता है। प्राकृतिक गैस की पुनर्प्राप्ति में प्रयोग होने वाले एथिलबेंजीन को भूमि में इंजेक्शन किया जा सकता है।[4]
उत्पादन
एसिड-उत्प्रेरित रासायनिक प्रतिक्रिया में बेंजीन और ईथेन के संयोजन से एथिलबेन्जीन का बड़े पैमाने पर उत्पादन किया जाता है:
- C
6H
6 + C
2H
4 → C
6H
5CH
2CH
3
2012 में, 99% से अधिक एथिलबेनज़ीन का उत्पादन इसी तरह से किया गया था।
आसवन प्रक्रिया के विस्तार, सुपरफ्रैक्शनिंग द्वारा जाइलीन के मिश्रण से थोड़ी मात्रा में एथिलबेन्जीन प्राप्त किया जाता है।[5]
1980 के दशक में, वाष्प चरण ऑल्केलेशन का जियोलाइट पर आधारित प्रक्रिया उच्च शुद्धता और उत्पादन देती थी। फिर जियोलाइट उत्प्रेरक का उपयोग करके एक तरल स्थिति प्रक्रिया को प्रस्तुत किया गया। इसमें कम बेंजीन-टू-इथिलीन अनुपात का प्रदान किया गया, जिससे आवश्यक उपकरण का आकार और उपजाऊ उत्पादन कम हो गया ।[6]
औद्योगिक दुर्घटनाएँ
3 जून 2014 को डच मोरडिज्क औद्योगिक क्षेत्र में एक विस्फोट हुआ। यह शैल पीएलसी द्वारा संचालित एक रासायनिक रिएक्टर में हुआ, [7]जो धातु ऑक्साइड उत्प्रेरक और एथिलबेंजीन के बीच एक अतितापी अस्थायी प्रतिक्रिया या अनियंत्रित उष्म वायु प्रवाह के कारण अधिक गरम हो गया।
स्वास्थ्य प्रभाव
एथिलबेंजीन की तीव्र विषाक्तता कम होती है, जिसका LD50 लगभग 4 ग्राम प्रति किलोग्राम शरीर वजन होता है। लंबे समय तक विषाक्तता और कैंसर के प्रभाव में अस्पष्टता होती है।[8] उच्च स्तर के वायु में एथिलबेंजीन के उच्च स्तर के असर के साथ आँखों और गले की संवेदनशीलता हो सकती है। उच्चस्तर के संपर्क में, एथिलबेंजीन चक्कर आने का कारण बन सकता है।[4] शरीर में पहुंचने के बाद, एथिलबेंजीन का जैविक अपघटन होता है और इसे 1-फिनाइलइथेनॉल, ऐसिटोफीनोन, फेनिलग्लॉक्सिलिक एसिड, मैंडेलिक एसिड, बेंज़ोइक एसिड और हिप्पुरिक एसिड में बदल जाता है। एथिलबेंजीन के संपर्क में आने पर मूत्र में विघटन उत्पादों की जांच करके एक्सपोजर का निर्धारण किया जा सकता है।
सितंबर 2007 तक, संयुक्त राज्य पर्यावरण संरक्षण एजेंसी (ईपीए) ने निर्धारित किया कि एक दिन के लिए 30 भाग प्रति मिलियन (पीपीएम) या दस दिनों के लिए 3 पीपीएम की सांद्रता वाला पानी पीने से बच्चों में कोई प्रतिकूल प्रभाव पड़ने की संभावना नहीं है। एथिलबेंजीन की 0.7 पीपीएम की जीवनकालिक अवसरण का कोई भी नकारात्मक प्रभाव का उम्मीद नहीं किया जाता है। यह यू.एस. के मानकों और नियंत्रण नियमों के अनुसार होता है। अमेरिकी व्यावसायिक सुरक्षा और स्वास्थ्य प्रशासन श्रमिकों के संपर्क को 8-घंटे के कार्यदिवस, 40-घंटे के कार्यसप्ताह के लिए औसतन 100 पीपीएम तक सीमित करता है।[4]
अंतरराष्ट्रीय कैंसर अनुसंधान संस्था (आईएआरसी) द्वारा एथिलबेन्जीन को संभावित कार्सिनोजेन के रूप में वर्गीकृत किया गया है,यद्यपि, ईपीए ने एथिलबेन्जीन को कार्सिनोजेन निर्धारित नहीं किया है। नेशनल टॉक्सिकोलॉजी प्रोग्राम ने चूहों और चुहियों में एक इनहेलेशन अध्ययन किया। एथिलबेन्जीन के संपर्क में आने से नर चूहों में गुर्दे और वृषण ट्यूमर की घटनाओं में वृद्धि हुई, और मादा चूहों में गुर्दे के ट्यूमर, नर चूहों में फेफड़ों के ट्यूमर और मादा चूहों में यकृत ट्यूमर की प्रवृत्ति में वृद्धि हुई।
सभी कार्बनिक यौगिकों की तरह, एथिलबेन्जीन वाष्प हवा के साथ एक विस्फोटक मिश्रण बनाते हैं।[5] एथिलबेन्जीन का परिवहन करते समय, इसे कक्षा 3, पैकिंग समूह में एक ज्वलनशील तरल के रूप में वर्गीकृत किया जाता है।[5]
पर्यावरणीय प्रभाव
एथिलबेंजीन अधिकतर वायु में वाष्प के रूप में पाया जाता है[4] क्योंकि यह जल और मिट्टी से आसानी से भ्रमण कर सकता है। 1999 में नगरीय वायु में औसत अधिकार एक प्रतिमिल्लियन की मात्रा के 0.62 पार्ट्स प्रति बिलियन में पाया गया था।[9] 2012 में किए गए एक अध्ययन में पाया गया कि देश की हवा में औसत सांद्रता 0.01 पीपीबी और घर के अंदर औसत सांद्रता 1.0 पीपीबी पाई गई। इसे कोयला, गैस और तेल के जलने से भी हवा में छोड़ा जा सकता है। उद्योग में एथिलबेन्जीन का उपयोग हवा में एथिलबेन्जीन वाष्प में योगदान देता है। हवा में लगभग तीन दिनों तक सूरज की रोशनी की मदद से रहने के बाद, अन्य रसायन एथिलबेन्जीन को ऐसे रसायनों में तोड़ देते हैं जो धुंध में पाए जा सकते हैं।[4]चूँकि यह आसानी से मिट्टी से नहीं जुड़ता है इसलिए यह सरलता से भूजल में भी चला जाता है। सतही जल में, यह तब टूट जाता है जब यह पानी में प्राकृतिक रूप से पाए जाने वाले रसायनों के साथ प्रतिक्रिया करता है।[10] सामान्यतः, एथिलबेन्जीन पीने के पानी में नहीं पाया जाता है, यद्यपि यह आवासीय पेयजल कुओं में पाया जा सकता है या निवासीय पेयजल के कुएं में एथिलबेंजीन पाया जा सकता है।
2012 के अनुसार, यूरोपीय संघ के संकटमय पदार्थ निदेशिका के अनुसार, एथिलबेंजीन पर्यावरण के लिए खतरनाक कटिबद्ध नहीं किया गया है।[5]
इथाइलबेन्जीन तंबाकू के धुएं का एक घटक है।[11]
जैव निम्नीकरण
कवक क्लैडोफियालोफोरा के कुछ उपभेद एथिलबेन्जीन पर विकसित हो सकते हैं।[12] जीवाणु सुगंधित तेल ईबीएन1 की खोज एथिलबेन्जीन पर बढ़ने की क्षमता के कारण की गई थी।[13]
संदर्भ
- ↑ 1.0 1.1 1.2 1.3 NIOSH Pocket Guide to Chemical Hazards. "#0264". National Institute for Occupational Safety and Health (NIOSH).
- ↑ Lange's Handbook of Chemistry (15th ed.). 1999.
- ↑ "Ethyl benzene". Immediately Dangerous to Life or Health Concentrations (IDLH). National Institute for Occupational Safety and Health (NIOSH).
- ↑ 4.0 4.1 4.2 4.3 4.4 4.5 "एथिलबेन्जीन टॉक्सअक्सर पूछे जाने वाले प्रश्न" (PDF). Agency for Toxic Substances and Disease Registry. Retrieved 21 May 2018.
- ↑ 5.0 5.1 5.2 5.3 "ETHYLBENZENE : ENVIRONMENTAL, HEALTH & SAFETY GUIDELINES". CEFIC. Archived from the original on 19 September 2014. Retrieved 14 February 2013.
- ↑ "एथिलबेन्जीन (ईबी) उत्पादन और विनिर्माण प्रक्रिया". PIERS. Retrieved 14 February 2013.
- ↑ https://www.onderzoeksraad.nl/nl/media/attachment/2018/7/10/06d477404859summary_shell_moerdijk.pdf[bare URL PDF]
- ↑ Vincent A.Welch, Kevin J. Fallon, Heinz-Peter Gelbke “Ethylbenzene” Ullmann’s Encyclopedia of Industrial Chemistry, Wiley-VCH, Weinheim, 2005. doi:10.1002/14356007.a10_035.pub2
- ↑ "Technology Transfer Network Air Toxics Web Site: Ethylbenzene". US Environmental Protection Agency. Retrieved 13 February 2013.
- ↑ "एथिलबेन्जीन". eco-usa.net. Archived from the original on 25 December 2012. Retrieved 12 February 2013.
- ↑ Talhout, Reinskje; Schulz, Thomas; Florek, Ewa; Van Benthem, Jan; Wester, Piet; Opperhuizen, Antoon (2011). "तम्बाकू के धुएँ में खतरनाक यौगिक". International Journal of Environmental Research and Public Health. 8 (12): 613–628. doi:10.3390/ijerph8020613. ISSN 1660-4601. PMC 3084482. PMID 21556207.
- ↑ Francesc X. PRENAFETA-BOLDU; Andrea KUHN; Dion M. A. M. LUYKX; Heidrun ANKE; Johan W. van GROENESTIJN; Jan A. M. de BONT (April 2001). "वाष्पशील सुगंधित हाइड्रोकार्बन पर उनके एकमात्र कार्बन और ऊर्जा स्रोत के रूप में उगने वाले कवक का अलगाव और लक्षण वर्णन". Mycological Research. 105 (4): 477–484. doi:10.1017/s0953756201003719.
- ↑ Rabus, R.; Widdel, F. (1995). "नए डिनाइट्रिफाइंग बैक्टीरिया द्वारा एथिलबेन्जीन और अन्य सुगंधित हाइड्रोकार्बन का अवायवीय क्षरण". Archives of Microbiology. 163 (2): 96–103. doi:10.1007/s002030050177. PMID 7710331.
- National Toxicology Program. Toxicology and Carcinogenesis Studies of Ethylbenzene (CAS No. 100-41-4) in F344/N Rats and B6C3F1 Mice (Inhalation Studies). TR No. 466. U.S. Department of Health and Human Services, Public Health Service, National Institutes of Health, Bethesda, MD. 1999.