डेस्मोप्लास्टिक स्मॉल-राउंड-सेल ट्यूमर: Difference between revisions
(TEXT EDITING) |
m (TEXT EDITING) |
||
| Line 49: | Line 49: | ||
पहली बार इकाई का वर्णन 1989 में रोगविज्ञानी विलियम एल गेराल्ड और [[जुआन रोसाई]] द्वारा गया था।<ref>{{cite journal |last1=Gerald |first1=W. L. |last2=Rosai |first2=J. |title=Case 2. Desmoplastic small cell tumor with divergent differentiation |journal=Pediatr. Pathol. |volume=9 |issue=2 |pages=177–83 |year=1989 |pmid=2473463 |doi=10.3109/15513818909022347}}</ref> पैथोलॉजी घने डिस्मोप्लास्टिक [[स्ट्रोमा (पशु ऊतक)]] के भीतर अच्छी तरह से परिचालित ठोस ट्यूमर नोड्यूल का खुलासा करती है। अक्सर केंद्रीय परिगलन के क्षेत्र मौजूद होते हैं। ट्यूमर कोशिकाओं में बढ़े हुए परमाणु / साइटोप्लाज्मिक अनुपात के साथ हाइपरक्रोमैटिक नाभिक होते हैं।{{citation needed|date=June 2020}} | पहली बार इकाई का वर्णन 1989 में रोगविज्ञानी विलियम एल गेराल्ड और [[जुआन रोसाई]] द्वारा गया था।<ref>{{cite journal |last1=Gerald |first1=W. L. |last2=Rosai |first2=J. |title=Case 2. Desmoplastic small cell tumor with divergent differentiation |journal=Pediatr. Pathol. |volume=9 |issue=2 |pages=177–83 |year=1989 |pmid=2473463 |doi=10.3109/15513818909022347}}</ref> पैथोलॉजी घने डिस्मोप्लास्टिक [[स्ट्रोमा (पशु ऊतक)]] के भीतर अच्छी तरह से परिचालित ठोस ट्यूमर नोड्यूल का खुलासा करती है। अक्सर केंद्रीय परिगलन के क्षेत्र मौजूद होते हैं। ट्यूमर कोशिकाओं में बढ़े हुए परमाणु / साइटोप्लाज्मिक अनुपात के साथ हाइपरक्रोमैटिक नाभिक होते हैं।{{citation needed|date=June 2020}} | ||
इम्यूनोहिस्टोकेमिस्ट्री पर, इन कोशिकाओं में एपिथेलियल मार्कर साइटोकैटिन, मेसेनकाइमा मार्कर डेस्मिन और विमिन, और न्यूरोनल मार्कर न्यूरॉन-विशिष्ट एनोलेज़ सहित ट्रिलिनियर सह-अभिव्यक्ति है। इस प्रकार, हालांकि शुरू में प्रस्तुति के स्थानों के कारण मेसोथेलियल मूल का माना जाता था, अब इसे मल्टीफेनोटाइपिक भेदभाव के साथ पूर्वज कोशिका से उत्पन्न होने की परिकल्पना है।{{cn|date=March 2022}} | इम्यूनोहिस्टोकेमिस्ट्री पर, इन कोशिकाओं में एपिथेलियल मार्कर साइटोकैटिन, मेसेनकाइमा मार्कर डेस्मिन और विमिन, और न्यूरोनल मार्कर न्यूरॉन-विशिष्ट एनोलेज़ सहित ट्रिलिनियर सह-अभिव्यक्ति है। इस प्रकार, हालांकि शुरू में प्रस्तुति के स्थानों के कारण मेसोथेलियल मूल का माना जाता था, अब इसे मल्टीफेनोटाइपिक भेदभाव के साथ पूर्वज कोशिका से उत्पन्न होने की परिकल्पना की गई है।{{cn|date=March 2022}} | ||
== निदान == | == निदान == | ||
Revision as of 17:22, 14 August 2023
| Desmoplastic small-round-cell tumor | |
|---|---|
| अन्य नाम | DSRCT[1] |
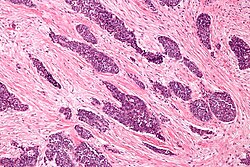 | |
| Micrograph of a desmoplastic small round cell tumor, showing the characteristic desmoplastic stroma and angulated nests of small round cells. H&E stain. | |
| Specialty | Oncology |
| रोग का निदान | Five-year survival rate 15%[2] |
| आवृत्ति | ~200 cases reported[2][3] |
डेस्मोप्लास्टिक स्मॉल-राउंड-सेल ट्यूमर (DSRCT) एक आक्रामक और दुर्लभ कैंसर है जो मुख्य रूप से पेट में द्रव्यमान के रूप में होता है।[4] प्रभावित अन्य क्षेत्रों में लसीकापर्व , पेट की परत, डायाफ्राम (शरीर रचना), प्लीहा, यकृत, छाती की दीवार, खोपड़ी, रीढ़ की हड्डी, बड़ी आंत, छोटी आंत, मूत्राशय, मस्तिष्क, फेफड़े, अंडकोष और अंडाशय शामिल हो सकते हैं। श्रोणि मेटास्टैटिक फैलाव की रिपोर्ट में की गई साइटों में यकृत, फेफड़े, लिम्फ नोड्स, मस्तिष्क, खोपड़ी और हड्डियां शामिल हैं। यह EWS-WT1 फ्यूजन प्रोटीन की विशेषता है।
फोडा को नरम ऊतक सरकोमा और एक छोटे गोल नीले सेल ट्यूमर के रूप में वर्गीकृत किया गया है। यह अक्सर पुरुष बच्चों में होता है। महिलाओं में यह बीमारी शायद ही कभी होती है, लेकिन जब ऐसा होता है तो ट्यूमर को डिम्बग्रंथि के कैंसर के रूप में देखा जा सकता है।[5]
संकेत और लक्षण
कुछ प्रारंभिक चेतावनी संकेत हैं कि अगर किसी मरीज के पास डीएसआरसीटी है तो रोगी अक्सर युवा और स्वस्थ होते हैं. क्योंकि ट्यूमर बढ़ते है और उदर गुहा के भीतर निर्बाध रूप से फैल जाते हैं ये दुर्लभ ट्यूमर होते हैं और अक्सर चिकित्सकों द्वारा गलत लक्षण के निदान किए जाते हैं। रोगी द्वारा देखे जाने से पहले उदर द्रव्यमान विशाल आकार तक बढ़ सकता है। पेट को टटोल कर ट्यूमर को कठोर, गोल पिंड के रूप में महसूस किया जा सकता है।[citation needed]
रोग के पहले लक्षणों में अक्सर पेट का फूलना, पेट का द्रव्यमान, पेट या पीठ में दर्द, जठरांत्र संबंधी रुकावट, भूख की कमी, जलोदर, रक्ताल्पता और दुर्बलता [ शामिल होते हैं।[citation needed]
अन्य अन्य सूचित लक्षणों में अज्ञात गांठें, थायरॉयड की स्थिति, हार्मोनल स्थिति, रक्त के थक्के, गुर्दे और मूत्र संबंधी समस्याएं, अंडकोष, स्तन, गर्भाशय, योनि और डिम्बग्रंथि द्रव्यमान शामिल हैं।[citation needed]
अनुवांशिकी
ऐसे कोई ज्ञात जोखिम कारक नहीं हैं जिन्हें रोग के लिए विशिष्ट रूप से पहचान की गई हो हो। ऐसा प्रतीत होता है कि ट्यूमर बचपन की आदिम कोशिकाओं से उत्पन्न होता है, और इसे बचपन का कैंसर माना जाता है।[citation needed]
अनुसंधान ने संकेत दिया है कि डीएसआरसीटी और विल्म्स ट्यूमर और इविंग सरकोमा के बीच एक काइमेरिक संबंध है। न्यूरोब्लास्टोमा और गैर-हॉजकिन के लिंफोमा के साथ मिलकर, वे लघु-कोशिका ट्यूमर बनाते हैं।[citation needed]
डीएसआरसीटी एक अद्वितीय क्रोमोसोमल ट्रांसलोकेशन (टी (11; 22) (पी 13: क्यू 12) के रूप में जाना जाता है)से जुड़ा है[6] जो सामान्य रूप से क्रोमोसोम की लंबी (या "q") भुजा के बैंड 12 पर स्थित पर स्थित EWSR1 FET प्रोटीन परिवार को विलीन करता है गुणसूत्र 22 WT1 प्रतिलेखन कारक जीन के हिस्से के साथ सामान्य रूप से गुणसूत्र 11 की छोटी भुजा के बैंड 13 पर स्थित होती है।[7] परिणामी EWSR1-WT1 फ्यूजन जीन को फ्यूजन ट्रांसक्रिप्ट में बदल दिया जाता है[8] जो EWSR1-WT1 काइमेरिक प्रोटीन के निर्माण को निर्देशित करता है।[9] EWSR1-WT1 काइमेरिक प्रोटीन में EWSR1 का एन-टर्मिनल लेन-देन डोमेन और WT1 का डीएनए-बाध्यकारी डोमेन शामिल है। यह स्थानान्तरण डीएसआरसीटी के लगभग सभी मामलों में देखा जाता है।[10] EWS/WT1 ट्रांसलोकेशन उत्पाद ENT4 को लक्षित करता है।[11] ईएनटी4 को पीएमएटी के नाम से भी जाना जाता है।
पैथोलॉजी
पहली बार इकाई का वर्णन 1989 में रोगविज्ञानी विलियम एल गेराल्ड और जुआन रोसाई द्वारा गया था।[12] पैथोलॉजी घने डिस्मोप्लास्टिक स्ट्रोमा (पशु ऊतक) के भीतर अच्छी तरह से परिचालित ठोस ट्यूमर नोड्यूल का खुलासा करती है। अक्सर केंद्रीय परिगलन के क्षेत्र मौजूद होते हैं। ट्यूमर कोशिकाओं में बढ़े हुए परमाणु / साइटोप्लाज्मिक अनुपात के साथ हाइपरक्रोमैटिक नाभिक होते हैं।[citation needed]
इम्यूनोहिस्टोकेमिस्ट्री पर, इन कोशिकाओं में एपिथेलियल मार्कर साइटोकैटिन, मेसेनकाइमा मार्कर डेस्मिन और विमिन, और न्यूरोनल मार्कर न्यूरॉन-विशिष्ट एनोलेज़ सहित ट्रिलिनियर सह-अभिव्यक्ति है। इस प्रकार, हालांकि शुरू में प्रस्तुति के स्थानों के कारण मेसोथेलियल मूल का माना जाता था, अब इसे मल्टीफेनोटाइपिक भेदभाव के साथ पूर्वज कोशिका से उत्पन्न होने की परिकल्पना की गई है।[citation needed]
निदान
विभेदक निदान
क्योंकि यह एक दुर्लभ ट्यूमर है, बहुत से पारिवारिक चिकित्सक या ऑन्कोलॉजिस्ट इस बीमारी से परिचित नहीं हैं। युवा रोगियों में डीएसआरसीटी को गलती से rhabdomyosarcoma, न्यूरोब्लास्टोमा और मेसेन्टेरिक कार्सिनॉइड सहित पेट के अन्य ट्यूमर समझ लिया जा सकता है । पुराने रोगियों में डीएसआरसीटी लिंफोमा, पेरिटोनियल मेसोथेलियोमा और पेरिटोनियल कार्सिनोमैटोसिस के समान हो सकता है। पुरुषों में डीएसआरसीटी को गलत तरीके से जर्म सेल कैंसर या वृषण कैंसर समझा जा सकता है, जबकि महिलाओं में डीएसआरसीटी को गलती से डिम्बग्रंथि का कैंसर समझा जा सकता है। डीएसआरसीटी अन्य छोटे-गोल नीले सेल कैंसर के साथ अन्य जिसमें इविंग का सारकोमा, तीव्र ल्यूकेमिया, लघु कोशिका मेसोथेलियोमा, न्यूरोब्लास्टोमा, आदिम neuroectodermal ट्यूमर, रबडोमायोसार्कोमा और विल्म्स ट्यूमर शामिल हैं. के विशेषताओं को साझा करता है[citation needed]
उपचार
DSRCT का अक्सर गलत निदान किया जाता है। वयस्क रोगियों को हमेशा सारकोमा विशेषज्ञ के पास भेजा जाना चाहिए। यह एक आक्रामक, दुर्लभ, तेजी से फैलने वाला ट्यूमर है और बाल चिकित्सा और वयस्क रोगियों दोनों का इलाज सारकोमा केंद्र में किया जाना चाहिए।[citation needed]
रोग के लिए कोई मानक प्रोटोकॉल नहीं है;[13] हालांकि, हाल की पत्रिकाओं और अध्ययनों ने बताया है कि कुछ रोगी उच्च-खुराक (पी6 प्रोटोकॉल) कीमोथेरपी , रखरखाव कीमोथेरेपी, डिबल्किंग ऑपरेशन, साइटोर्डेक्टिव सर्जरी और विकिरण चिकित्सा का जवाब देते हैं। अन्य उपचार विकल्पों में शामिल हेमेटोपोएटिक स्टेम सेल प्रत्यारोपण, तीव्रता-संग्राहक विकिरण थेरेपी, रेडियो आवृति पृथककरण , स्टीरियोटैक्टिक बॉडी रेडिएशन थेरेपी, इंट्रापेरिटोनियल हाइपरथर्मिक केमोपरफ्यूजन , और क्लिनिकल परीक्षण।
पूर्वानुमान
DSRCT के लिए पूर्वानुमान खराब बना रहता है।[14] पूर्वानुमान कैंसर के चरण पर निर्भर करता है। क्योंकि रोग का गलत निदान किया जा सकता है या पता नहीं चल पाता है, ट्यूमर अक्सर पेट के भीतर बड़े हो जाते हैं और शरीर के अन्य भागों में रूप-परिवर्तन या फैल जाते हैं।
इसका कोई ज्ञात अंग या उत्पत्ति का क्षेत्र नहीं है। डीएसआरसीटी लिम्फ नोड्स या रक्त प्रवाह के माध्यम से मेटास्टेसिस कर सकता है। मेटास्टेसिस की साइटों में प्लीहा, डायाफ्राम, यकृत, बड़ी और छोटी आंत, फेफड़े, केंद्रीय तंत्रिका तंत्र, हड्डियां, गर्भाशय, मूत्राशय, जननांग, उदर गुहा और मस्तिष्क शामिल हैं।
उच्च-खुराक कीमोथेरेपी, आक्रामक सर्जिकल शोधन का एक बहु-साधन दृष्टिकोण,[15] विकिरण, और स्टेम सेल बचाव कुछ रोगियों के लिए जीवित रहने में सुधार करता है। रिपोर्टों ने संकेत दिया है कि मरीज शुरू में पहली पंक्ति की कीमोथेरेपी और उपचार का जवाब देंगे लेकिन यह पुनरावृत्ति सामान्य है।
सुधार की स्थिति में या निष्क्रिय ट्यूमर वाले कुछ रोगियों को लंबे समय तक कम खुराक वाली कीमोथेरेपी से लाभ होता है, जिससे डीएसआरसीटी एक पुरानी बीमारी बन जाती है।
अनुसंधान
The examples and perspective in this section may not represent a worldwide view of the subject. (July 2016) (Learn how and when to remove this template message) |
स्टेलिन फाउंडेशन[16] वर्तमान में DSRCT रोगियों को परीक्षण के लिए अपने ट्यूमर के नमूने नि:शुल्क भेजने का अवसर प्रदान करता है। अनुसंधान वैज्ञानिक नग्न चूहों पर नमूने विकसित कर रहे हैं और विभिन्न रासायनिक घटको का परीक्षण कर रहे हैं ताकि पता चल सके कि व्यक्ति के ट्यूमर के खिलाफ कौन सबसे प्रभावी है।
उन्नत डीएसआरसीटी वाले रोगी नैदानिक परीक्षणों में भाग लेने के योग्य हो सकते हैं जो रोग के इलाज के लिए नई दवाओं पर शोध कर रहे हैं।
Cory Monzingo Foundation एक 501(c)(3) संगठन है जो डीएसआरसीटी के उपचार और इलाज के लिए अनुसंधान का समर्थन करता है। कोरी मोनजिंगो फाउंडेशन एमडी एंडरसन कैंसर सेंटर को फंडिंग प्रदान करता है, और अन्य गैर-लाभकारी कैंसर अनुसंधान संगठनों को भी फंडिंग प्रदान कर सकता है।
2002 में, निशियो और अल,[17] जेएन-डीएसआरसीटी-1 नामक एक विशिष्ट इंट्रा-एब्डोमिनल डीएसआरसीटी के साथ एक रोगी के फुफ्फुस बहाव से प्राप्त एक उपन्यास मानव ट्यूमर सेल लाइन की स्थापना की।[18] जिसका अब शोध में उपयोग किया जा सकता है।
सेंट जूड चिल्ड्रन रिसर्च हॉस्पिटल ने 2018 में, चाइल्डहुड सॉलिड ट्यूमर नेटवर्क से संसाधन उपलब्ध कराए हैं, जो अनुरोध पर रोगी-व्युत्पन्न ऑर्थोटोपिक ज़ेनोग्राफ़्ट तक पहुँच प्रदान करता है।[19]
वैकल्पिक नाम
इस रोग को इस रूप में भी जाना जाता है: डेस्मोप्लास्टिक छोटा गोल नीला कोशिका ट्यूमर; इंट्रा-एब्डोमिनल डिस्मोप्लास्टिक छोटे गोल ब्लू सेल ट्यूमर; डिस्मोप्लास्टिक छोटे सेल ट्यूमर; डिस्मोप्लास्टिक कैंसर; डेस्मोप्लास्टिक सारकोमा , डीएसआरसीटी।
पेरिटोनियल मेसोथेलियोमा से कोई संबंध नहीं है जो एक अन्य बीमारी है जिसे कभी-कभी डिस्मोप्लास्टिक के रूप में वर्णित किया जाता है।
यह भी देखें
- डिस्मोप्लासिया
- केट ग्रेंजर (1981-2016), एक अंग्रेजी चिकित्सक, जिनके डीएसआरसीटी के साथ निदान के कारण उन्होंने बेहतर रोगी देखभाल के लिए अभियान चलाया, और कैंसर अनुसंधान के लिए धन जुटाया।
संदर्भ
- ↑ RESERVED, INSERM US14-- ALL RIGHTS. "Orphanet: Desmoplastic small round cell tumor". www.orpha.net (in English). Retrieved 17 November 2019.
- ↑ 2.0 2.1 "Desmoplastic Small Round Cell Tumor". St. Jude Children's Research Hospital. Retrieved March 22, 2023.
- ↑ "Desmoplastic Small Round Cell Tumors (DSRCT)". National Cancer Institute. Retrieved March 22, 2023.
- ↑ Lee YS, Hsiao CH: Desmoplastic small round cell tumor: a clinicopathologic, immunohistochemical and molecular study of four patients. J Formos Med Assoc 2007; 106: 854–860.
- ↑ Bland AE, Shah AA, Piscitelli JT, Bentley RC, Secord AA (2007). "डेस्मोप्लास्टिक छोटे गोल सेल ट्यूमर उन्नत डिम्बग्रंथि के कैंसर के रूप में". International Journal of Gynecological Cancer. 18 (4): 847–50. doi:10.1111/j.1525-1438.2007.01110.x. PMID 18081791.
- ↑ Murphy AJ, Bishop K, Pereira C, et al. (December 2008). "A new molecular variant of desmoplastic small round cell tumor: significance of WT1 immunostaining in this entity". Hum. Pathol. 39 (12): 1763–70. doi:10.1016/j.humpath.2008.04.019. PMID 18703217.
- ↑ Flucke U, van Noesel MM, Siozopoulou V, Creytens D, Tops BB, van Gorp JM, Hiemcke-Jiwa LS (June 2021). "EWSR1-The Most Common Rearranged Gene in Soft Tissue Lesions, Which Also Occurs in Different Bone Lesions: An Updated Review". Diagnostics (Basel, Switzerland). 11 (6): 1093. doi:10.3390/diagnostics11061093. PMC 8232650. PMID 34203801.
- ↑ Gerald WL, Haber DA (June 2005). "डिस्मोप्लास्टिक छोटे गोल सेल ट्यूमर में EWS-WT1 जीन फ्यूजन". Semin. Cancer Biol. 15 (3): 197–205. doi:10.1016/j.semcancer.2005.01.005. PMID 15826834.
- ↑ Lee YS, Hsiao CH (2007). "Desmoplastic small round cell tumor: a clinicopathologic, immunohistochemical and molecular study of four patients". J. Formos. Med. Assoc. 106 (10): 854–60. doi:10.1016/S0929-6646(08)60051-0. PMID 17964965.
- ↑ Martínez-Trufero J, Cruz Jurado J, Hernández-León CN, Correa R, Asencio JM, Bernabeu D, Alvarez R, Hindi N, Mata C, Marquina G, Martínez V, Redondo A, Floría LJ, Gómez-Mateo MC, Lavernia J, Sebio A, Garcia Del Muro X, Martin-Broto J, Valverde-Morales C (September 2021). "Uncommon and peculiar soft tissue sarcomas: Multidisciplinary review and practical recommendations. Spanish Group for Sarcoma research (GEIS -GROUP). Part II". Cancer Treatment Reviews. 99: 102260. doi:10.1016/j.ctrv.2021.102260. PMID 34340159.
- ↑ Li H, Smolen GA, Beers LF, et al. (2008). "Adenosine transporter ENT4 is a direct target of EWS/WT1 translocation product and is highly expressed in desmoplastic small round cell tumor". PLOS ONE. 3 (6): e2353. Bibcode:2008PLoSO...3.2353L. doi:10.1371/journal.pone.0002353. PMC 2394657. PMID 18523561.

- ↑ Gerald, W. L.; Rosai, J. (1989). "Case 2. Desmoplastic small cell tumor with divergent differentiation". Pediatr. Pathol. 9 (2): 177–83. doi:10.3109/15513818909022347. PMID 2473463.
- ↑ Talarico F, Iusco D, Negri L, Belinelli D: Combined resection and multi-agent adjuvant chemotherapy for intra-abdominal desmoplastic small round cell tumour: case report and review of the literature. G Chir 2007; 28: 367–370.
- ↑ Lal DR, Su WT, Wolden SL, Loh KC, Modak S, La Quaglia MP (January 2005). "डिस्मोप्लास्टिक छोटे गोल सेल ट्यूमर के लिए मल्टीमॉडल उपचार के परिणाम". J. Pediatr. Surg. 40 (1): 251–5. doi:10.1016/j.jpedsurg.2004.09.046. PMID 15868593.
- ↑ Talarico F, Iusco D, Negri L, Belinelli D (October 2007). "Combined resection and multi-agent adjuvant chemotherapy for intra-abdominal desmoplastic small round cell tumour: case report and review of the literature". G Chir. 28 (10): 367–70. PMID 17915050.
- ↑ Official website for Stehlin Foundation
- ↑ Nishio, Jun; Iwasaki, Hiroshi; Ishiguro, Masako; Ohjimi, Yuko; Fujita, Chikako; Yanai, Fumio; Nibu, Keiko; Mitsudome, Akihisa; Kaneko, Yasuhiko (September 2002). "एक उपन्यास मानव डिस्मोप्लास्टिक छोटे गोल सेल ट्यूमर सेल लाइनों की स्थापना और लक्षण वर्णन, IN-DSRCT-1". Laboratory Investigation; A Journal of Technical Methods and Pathology. 82 (9): 1175–1182. doi:10.1097/01.LAB.0000028059.92642.03. ISSN 0023-6837. PMID 12218078.
- ↑ "Jn-Dsrct-1".
- ↑ "St Jude Children's Research Hospital".
