राइबोन्यूक्लिएज: Difference between revisions
m (added Category:Vigyan Ready using HotCat) |
m (4 revisions imported from alpha:राइबोन्यूक्लिएज) |
(No difference)
| |
Revision as of 12:00, 4 July 2023
| ribonuclease | |||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|
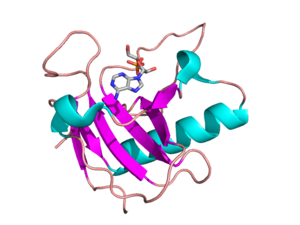 | |||||||||||
| Identifiers | |||||||||||
| Symbol | Ribonuclease | ||||||||||
| Pfam | PF00545 | ||||||||||
| InterPro | IPR000026 | ||||||||||
| SCOP2 | 1brn / SCOPe / SUPFAM | ||||||||||
| |||||||||||
राइबोन्यूक्लिज़ सामान्यतः संक्षिप्त आरएनएस प्रकार का ऐसा न्यूक्लियस है, जो छोटे-छोटे घटकों में आरएनए के क्षरण को उत्प्रेरित करने में सहायता प्रदान करता है। इस प्रकार राइबोन्यूक्लिएज को एंडोरिबोन्यूक्लिएज और एक्सोरिबोन्यूक्लीज़ में विभाजित किया जा सकता है, और ईसी 2.7 फॉस्फोरोलिटिक एंजाइमों के लिए और 3.1 हाइड्रोलाइटिक एंजाइमों के लिए इनके वर्गों के भीतर कई उप-वर्ग सम्मिलित कर देता हैं।
फलन
इस प्रकार अध्ययन किए गए सभी जीवों में दो अलग-अलग वर्गों के कई आरएनएस होते हैं, जो दिखाते हैं कि आरएनए गिरावट बहुत ही प्राचीन और महत्वपूर्ण प्रक्रिया है। साथ ही साथ सेलुलर आरएनए की समाशोधन जो अब आवश्यक नहीं है, आरएनएएस सभी आरएनए अणुओं की परिपक्वता में महत्वपूर्ण भूमिका निभाते हैं, दोनों मैसेंजर आरएनए जो प्रोटीन और गैर-कोडिंग आरएनए बनाने के लिए अनुवांशिक सामग्री लेते हैं जो विभिन्न सेलुलर प्रक्रियाओं में कार्य करते हैं। इसके अतिरिक्त, सक्रिय आरएनए गिरावट प्रणाली आरएनए वायरस के विरुद्ध पहली रक्षा है और आरएनएआई जैसी अधिक उन्नत सेलुलर प्रतिरक्षा रणनीतियों के लिए अंतर्निहित मशीनरी प्रदान करती है।
कुछ कोशिकाएं प्रचुर मात्रा में गैर-विशिष्ट आरएनएसs जैसे ए और टी1 का भी स्राव करती हैं। इसलिए, आरएनएसs अत्यंत सामान्य हैं, जिसके परिणामस्वरूप किसी भी आरएनए के लिए बहुत कम जीवनकाल होता है जो संरक्षित वातावरण में नहीं होता है। यह ध्यान देने योग्य है कि सभी अंतःकोशिकीय आरएनए आरएनएएस गतिविधि से 5' कैप या 5' एंड कैपिंग, 3' एंड पॉलीएडेनाइलेशन, आरएनए·आरएनए डुप्लेक्स के गठन, और आरएनए प्रोटीन कॉम्प्लेक्स ( राइबोन्यूक्लियोप्रोटीन ) के भीतर फोल्डिंग सहित कई रणनीतियों द्वारा सुरक्षित हैं।
इस प्रकार की सुरक्षा के लिए अन्य तंत्र जैसे राइबोन्यूक्लिज़ अवरोधक (आरआई) सहायक है, जिसमें कुछ प्रकार की कोशिकाओं में सेलुलर प्रोटीन (~0.1%) का अपेक्षाकृत बड़ा अंश सम्मिलित होता है, और जो किसी भी प्रोटीन-प्रोटीन इंटरेक्शन के उच्चतम संबंध के साथ कुछ राइबोन्यूक्लाइजेस को बांधता है; RI-आरएनएस A कॉम्प्लेक्स के लिए पृथक्करण स्थिरांक शारीरिक स्थितियों के तहत ~ 20 fM है। अधिकांश प्रयोगशालाओं में आरआई का उपयोग किया जाता है जो पर्यावरणीय आरएनएएस से गिरावट के विरुद्ध अपने प्रमाणों की रक्षा के लिए आरएनए का अध्ययन करते हैं।
इस प्रकार के प्रतिबंध एंजाइमों के समान, जो डबल-स्ट्रैंडेड डीएनए के अत्यधिक विशिष्ट अनुक्रमों को काटते हैं, विभिन्न प्रकार के एंडोरिबोन्यूक्लाइजेस जो सिंगल-स्ट्रैंडेड आरएनए के विशिष्ट अनुक्रमों को पहचानते हैं और अलग कर देते हैं, उन्हें वर्तमान समय में वर्गीकृत किया जा सकता है।
आरएनएस कई जैविक प्रक्रियाओं में महत्वपूर्ण भूमिका निभाते हैं, जिसमें फूलों के पौधों (एंजियोस्पर्म) में एंजियोजिनेसिस और स्व-असंगति सम्मिलित है।[2][3] प्रोकैरियोटिक विष-प्रतिविष प्रणाली के कई तनाव-प्रतिक्रिया विषाक्त पदार्थों को आरएनएस गतिविधि और समरूपता (जीव विज्ञान) के लिए दिखाया गया है।[4]
वर्गीकरण
प्रमुख प्रकार के एंडोरिबोन्यूक्लाइजेस
* EC 3.1.27.5: रिबोन्यूक्लिएज ए आरएनएएस है जो सामान्यतः अनुसंधान में प्रयोग किया जाता है। आरएनएस A (उदा., गोजातीय अग्नाशय राइबोन्यूक्लिएज ए: PDB: 2AAS) सामान्य प्रयोगशाला उपयोग में सबसे कठिन एंजाइमों में से है; इसे अलग करने की विधि कच्चे सेलुलर अर्क को तब तक उबालना है जब तक कि आरएनएस A के अतिरिक्त अन्य सभी एंजाइम विकृतीकरण (जैव रसायन) नहीं हो जाते। यह एकल-फंसे आरएनए के लिए विशिष्ट है। यह अयुग्मित सी और यू अवशेषों के 3'-छोर को काटता है, अंततः 2', 3'-चक्रीय मोनोफॉस्फेट मध्यवर्ती के माध्यम से 3'-फॉस्फोराइलेटेड उत्पाद बनाता है।[5] इसकी गतिविधि के लिए इसे किसी सहकारकों की आवश्यकता नहीं होती है [6]
- EC 3.1.26.4: आरएनएस H राइबोन्यूक्लिज़ है जो एसएस डीएनए का उत्पादन करने के लिए डीएनए/आरएनए द्वैध में आरएनए को विभाजित करता है। आरएनएस H गैर-विशिष्ट एंडोन्यूक्लिज़ है और हाइड्रोलाइटिक तंत्र के माध्यम से आरएनए के दरार को उत्प्रेरित करता है, जो एंजाइम-बाउंड डाइवलेंट धातु आयन द्वारा सहायता प्राप्त करता है। आरएनएस H 5'-फॉस्फोराइलेटेड उत्पाद छोड़ता है।[7]
- EC 3.1.26.3: आरएनएस III प्रकार का राइबोन्यूक्लिज़ है जो प्रोकैरियोट्स में लिखित पॉलीसिस्ट्रोनिक आरएनए ऑपेरॉन से आर-आरएनए (16s आर-आरएनए और 23s आर-आरएनए) को अलग करता है। यह आरएनएस के डबल-स्ट्रैंडेड आरएनए (डीएस आरएनए)-डाइसर परिवार को भी ग्रहण करके पचा देता है, विशिष्ट साइट पर प्री-एमआई-आरएनए 60-70bp लंबा होता हैं और इसे अलग कर देता है और इसे एमआई-आरएनए (22-30bp) में परिवर्तित करता है, जो कि प्रतिलेखन के नियमन में सक्रिय रूप से सम्मिलित रहता है, और एमआरएनए लाइफ-टाइम रहता हैं।
- एंजाइम आयोग संख्या 3.1.26.-??: आरएनएस L इंटरफेरॉन-प्रेरित न्यूक्लियस है, जो सक्रियण पर, कोशिका के भीतर सभी आरएनए को नष्ट कर देता है
- EC 3.1.26.5: आरएनएस P प्रकार का राइबोन्यूक्लिएज है जो इस आशय में अद्वितीय है कि यह राइबोजाइम है - आरएनए जो एंजाइम के समान उत्प्रेरक के रूप में कार्य करता है। इसके कार्यों में से फंसे हुए प्री-टीआरएनए के 5' छोर से नेता अनुक्रम को अलग करना है। आरएनएस P प्रकृति में दो ज्ञात मल्टीपल टर्नओवर राइबोजाइम में से है दूसरा राइबोसोम है। इस प्रकार बैक्टीरिया में आरएनएस P होलोनीजाइम की उत्प्रेरक गतिविधि के लिए भी जिम्मेदार होता है, जिसमें एपोएंजाइम होता है जो कोएंजाइम के साथ संयोजन द्वारा सक्रिय एंजाइम प्रणाली बनाता है और सब्सट्रेट के लिए इस प्रणाली की विशिष्टता निर्धारित करता है। आरएनएस P का रूप जो प्रोटीन है और इसमें आरएनए नहीं होता है, हाल ही में खोजा गया है।[8]
- एंजाइम कमीशन संख्या 3.1.??: आरएनएस PhyM एकल-स्ट्रैंडेड आरएनएएस के लिए अनुक्रम विशिष्ट है। यह अयुग्मित A और U अवशेषों के 3'-छोर को काटता है।
- EC 3.1.27.3: आरएनएस T1 एकल-फंसे हुए आरएनएएस के लिए अनुक्रम विशिष्ट है। यह अयुग्मित G अवशेषों के 3'-छोर को काटता है।
- EC 3.1.27.1: आरएनएस T2 एकल-फंसे हुए आरएनएएस के लिए अनुक्रम विशिष्ट है। यह सभी 4 अवशेषों के 3'-अंत को काटता है, अपितु अधिमानतः 3'-अंत के रूप में प्राप्त होता हैं।
- EC 3.1.27.4: आरएनएस U2 एकल-फंसे हुए आरएनएएस के लिए अनुक्रम विशिष्ट है। यह अयुग्मित A अवशेषों के 3'-छोर को काटता है।
- EC 3.1.27.8: आरएनएस V पॉलीएडेनाइन और पॉलीयूरिडीन आरएनए के लिए विशिष्ट है।
- EC 3.1.26.12: आरएनएस E पौधे की उत्पत्ति का राइबोन्यूक्लिज़ है, जो बैक्टीरिया में एसओएस प्रतिक्रियाओं को नियंत्रित करता है, रेक ए/लेक्स ए आश्रित सिग्नल ट्रांसडक्शन पाथवे द्वारा एसओएस तंत्र के सक्रियण द्वारा डीएनए क्षति के तनाव की प्रतिक्रिया के लिए जो ट्रांसक्रिप्शनल रूप से अग्रणी जीनों की बहुलता को कम करता है। इस प्रकार की कोशिकाओं के विभाजन की पारगमन अधिकृत करने के साथ-साथ डीएनए को सही करने का प्रारंभ हो जाता हैं। [9]
- EC 3.1.26.-: आरएनएस G यह 5s आर-आरएनए के 16'-अंत को संसाधित करने में सम्मिलित है। यह गुणसूत्र पृथक्करण और कोशिका विभाजन से संबंधित है। इसे साइटोप्लाज्मिक अक्षीय फिलामेंट बंडलों के घटकों में से माना जाता है। यह भी माना जाता है कि यह इस संरचना के गठन को नियंत्रित कर सकता है।[10]
प्रमुख प्रकार के एक्सोरिबोन्यूक्लाइजेस
- एंजाइम आयोग संख्या EC 2.7.7.8: पोलिन्यूक्लियोटाइड फॉस्फोरिलेज़ (पीएनपेस) एक्सोन्यूक्लिज़ के साथ-साथ न्यूक्लियोटिडिलट्रांसफेरेज़ के रूप में कार्य करता है।
- एंजाइम आयोग संख्या EC 2.7.7.56: आरएनएस पीएच एक्सोन्यूक्लिज़ के साथ-साथ न्यूक्लियोटिडाइलट्रांसफेरेज़ के रूप में कार्य करता है।
- एंजाइम कमीशन नंबर 3.1.??: आरएनएस R, आरएनएस II का समीपस्थ होमोलॉग है, अपितु यह आरएनएस II के विपरीत, गौण कारकों की सहायता के बिना माध्यमिक संरचनाओं के साथ आरएनए को नीचा दिखा सकता है।
- एंजाइम आयोग संख्या EC 3.1.13.5: आरएनएस डी प्री-ट्रांसफर आरएनए के 3'-टू-5' प्रोसेसिंग में सम्मिलित है।
- एंजाइम कमीशन संख्या 3.1.??: आरएनएस टी कई स्थिर आरएनएएस की 3'-to-5' परिपक्वता के लिए प्रमुख योगदानकर्ता है।
- EC 3.1.13.3: ओलिगोरिबोन्यूक्लिएज छोटे ऑलिगोन्यूक्लियोटाइड्स को मोनोन्यूक्लियोटाइड्स में डिग्रेड करता है।
- EC 3.1.11.1: एक्सोरिबोन्यूक्लिज़ I एकल-फंसे हुए आरएनए को 5'-टू-3' से नीचा दिखाता है, केवल यूकेरियोट्स में उपस्थित है।
- EC 3.1.13.1: एक्सोरिबोन्यूक्लिज़ II, एक्सोरिबोन्यूक्लिज़ I का समीपी होमोलॉग है।
आरएनएस विशिष्टता
सक्रिय स्थल पर उपस्थित दरार होने के कारण उक्त घाटी के समान दिखाई देता है, जहाँ सभी सक्रिय स्थल अवशेष घाटी की दीवार और तल बनाते हैं। दरार बहुत पतली है और छोटा सब्सट्रेट पूर्ण रूप से सक्रिय साइट के बीच में फिट बैठता है, जो अवशेषों के साथ सही बातचीत की अनुमति देता है। यह वास्तव में उस साइट के लिए थोड़ा वक्रता है जो सब्सट्रेट भी है। चूंकि सामान्यतः अधिकांश एक्सो- और एंडोरिबोन्यूक्लाइजेस अनुक्रम विशिष्ट नहीं होते हैं, हाल ही में सीआरआईएसपीआर/कैस सिस्टम मूल रूप से डीएनए को पहचानने और काटने के लिए अनुक्रम-विशिष्ट की विशेष विधि से एसएसआरएनए को साफ करने के लिए इंजीनियर किया गया था।[11]
आरएनएस संदूषण आरएनए निष्कर्षण के समय
आणविक जीव विज्ञान प्रयोगों में आरएनए निष्कर्षण सर्वव्यापी और हार्डी राइबोन्यूक्लाइजेस की उपस्थिति से बहुत जटिल है जो आरएनए प्रमाणों को नीचा दिखाते हैं। कुछ आरएनएसएस अत्यधिक कठोर हो सकते हैं और डीएनएसेस को अप्रभावित करने की तुलना में उन्हें निष्क्रिय करना कठिन हो जाता है। इस प्रकार से उत्पत्ति होने वाले सेलुलर आरएनएसs के अतिरिक्त, कई आरएनएसएस हैं जो पर्यावरण में उपस्थित हैं। आरएनएसs विभिन्न जीवों में कई बाह्य कार्य करने के लिए विकसित हुए हैं।[12][13][14] उदाहरण के लिए, आरएनएस ए सुपरफैमिली का सदस्य आरएनएस 7, मानव त्वचा द्वारा स्रावित होता है और शक्तिशाली एंटीपैथोजेन रक्षा के रूप में कार्य करता है।[15][16] इन स्रावित आरएनएसएस में, एंजाइमैटिक आरएनएस गतिविधि इसके नए, निर्वासन फ़ंक्शन के लिए आवश्यक भी नहीं हो सकती है। उदाहरण के लिए, प्रतिरक्षा आरएनएसएस जीवाणुओं की कोशिका झिल्लियों को अस्थिर करके कार्य करते हैं।[17][18]
संदर्भ
- ↑ Noguchi S (July 2010). "Isomerization mechanism of aspartate to isoaspartate implied by structures of Ustilago sphaerogena ribonuclease U2 complexed with adenosine 3'-monophosphate". Acta Crystallographica D. 66 (Pt 7): 843–9. doi:10.1107/S0907444910019621. PMID 20606265.
- ↑ Sporn MB, Roberts AB (6 December 2012). पेप्टाइड ग्रोथ फैक्टर और उनके रिसेप्टर्स II. Springer Science & Business Media. p. 556. ISBN 978-3-642-74781-6.
- ↑ Raghavan V (6 December 2012). फूलों के पौधों का विकासात्मक जीव विज्ञान. Springer Science & Business Media. p. 237. ISBN 978-1-4612-1234-8.
- ↑ Ramage HR, Connolly LE, Cox JS (December 2009). "Comprehensive functional analysis of Mycobacterium tuberculosis toxin-antitoxin systems: implications for pathogenesis, stress responses, and evolution". PLOS Genetics. 5 (12): e1000767. doi:10.1371/journal.pgen.1000767. PMC 2781298. PMID 20011113.
- ↑ Cuchillo CM, Nogués MV, Raines RT (September 2011). "Bovine pancreatic ribonuclease: fifty years of the first enzymatic reaction mechanism". Biochemistry. 50 (37): 7835–41. doi:10.1021/bi201075b. PMC 3172371. PMID 21838247.
- ↑ "Library Preparation Kits".
- ↑ Nowotny M (February 2009). "Retroviral integrase superfamily: the structural perspective". EMBO Reports. 10 (2): 144–51. doi:10.1038/embor.2008.256. PMC 2637324. PMID 19165139.
- ↑ Holzmann J, Frank P, Löffler E, Bennett KL, Gerner C, Rossmanith W (October 2008). "RNase P without RNA: identification and functional reconstitution of the human mitochondrial tRNA processing enzyme". Cell. 135 (3): 462–74. doi:10.1016/j.cell.2008.09.013. PMID 18984158.
- ↑ Shamsher S. Kanwar*, Puranjan Mishra, Khem Raj Meena, Shruti Gupta and Rakesh Kumar, Ribonucleases and their Applications, 2016, Journal of Advanced Biotechnology and Bioengineering
- ↑ Wachi M, Umitsuki G, Shimizu M, Takada A, Nagai K. Escherichia coli cafA gene encodes a novel RNase, designated as RNase G, involved in processing of the 5' end of 16S rRNA. Biochem Biophys Res Commun. 1999;259(2):483‐488. doi:10.1006/bbrc.1999.0806
- ↑ Tamulaitis G, Kazlauskiene M, Manakova E, Venclovas Č, Nwokeoji AO, Dickman MJ, Horvath P, Siksnys V (November 2014). "स्ट्रेप्टोकोकस थर्मोफिलस के III-A CRISPR-Cas सिस्टम द्वारा प्रोग्राम करने योग्य RNA श्रेडिंग". Molecular Cell. 56 (4): 506–17. doi:10.1016/j.molcel.2014.09.027. PMID 25458845.
- ↑ Rossier O, Dao J, Cianciotto NP (March 2009). "लेजिओनेला न्यूमोफिला के एक प्रकार II स्रावित RNase हार्टमैनेला वर्मीफोर्मिस के इष्टतम इंट्रासेल्युलर संक्रमण की सुविधा देता है". Microbiology. 155 (Pt 3): 882–90. doi:10.1099/mic.0.023218-0. PMC 2662391. PMID 19246759.
- ↑ Luhtala N, Parker R (May 2010). "T2 Family ribonucleases: ancient enzymes with diverse roles". Trends in Biochemical Sciences. 35 (5): 253–9. doi:10.1016/j.tibs.2010.02.002. PMC 2888479. PMID 20189811.
- ↑ Dyer KD, Rosenberg HF (November 2006). "The RNase a superfamily: generation of diversity and innate host defense". Molecular Diversity. 10 (4): 585–97. doi:10.1007/s11030-006-9028-2. PMID 16969722. S2CID 20922592.
- ↑ Harder J, Schroder JM (November 2002). "RNase 7, a novel innate immune defense antimicrobial protein of healthy human skin". The Journal of Biological Chemistry. 277 (48): 46779–84. doi:10.1074/jbc.M207587200. PMID 12244054.
- ↑ Köten B, Simanski M, Gläser R, Podschun R, Schröder JM, Harder J (July 2009). "RNase 7 contributes to the cutaneous defense against Enterococcus faecium". PLOS ONE. 4 (7): e6424. Bibcode:2009PLoSO...4.6424K. doi:10.1371/journal.pone.0006424. PMC 2712763. PMID 19641608.
- ↑ Huang YC, Lin YM, Chang TW, Wu SJ, Lee YS, Chang MD, Chen C, Wu SH, Liao YD (February 2007). "The flexible and clustered lysine residues of human ribonuclease 7 are critical for membrane permeability and antimicrobial activity". The Journal of Biological Chemistry. 282 (7): 4626–33. doi:10.1074/jbc.M607321200. PMID 17150966.
- ↑ Rosenberg HF (May 2008). "RNase A ribonucleases and host defense: an evolving story". Journal of Leukocyte Biology. 83 (5): 1079–87. doi:10.1189/jlb.1107725. PMC 2692241. PMID 18211964.
Ahmed TAE, Udenigwe CC, Gomaa A. Editorial: Biotechnology and Bioengineering Applications for Egg-Derived Biomaterials. Front Bioeng Biotechnol. 2021 Sep 20;9:756058
स्रोत
- डी अलेसियो जी और रिओर्डन जेएफ, एड। (1997) राइबोन्यूक्लाइजेस: स्ट्रक्चर्स एंड फंक्शंस, अकादमिक प्रेस।
- गेर्डेस के, क्रिस्टेंसन एसके और लोबनेर-ओलेसन ए (2005)। प्रोकैरियोटिक विष-एंटीटॉक्सिन तनाव प्रतिक्रिया लोकी। नट। रेव। माइक्रोबॉयल। (3) 371-382।
