बोल्ट्ज़मान वितरण: Difference between revisions
No edit summary |
No edit summary |
||
| Line 3: | Line 3: | ||
[[File:Exponential probability density.svg|upright=1.75|right|thumb|बोल्ट्ज़मैन का वितरण घातांकीय वितरण है।]] | [[File:Exponential probability density.svg|upright=1.75|right|thumb|बोल्ट्ज़मैन का वितरण घातांकीय वितरण है।]] | ||
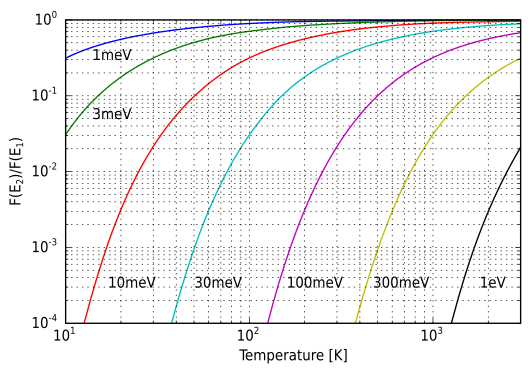
[[File:Boltzmann distribution graph.svg|upright=1.75|right|thumb|बोल्ट्ज़मान कारक {{tmath|\tfrac{p_i}{p_j} }} (ऊर्ध्वाधर अक्ष) तापमान के फलन के रूप में {{mvar|T}} कई ऊर्जा अंतरों के लिए {{math|''ε<sub>i</sub>'' − ''ε<sub>j</sub>''}}.]][[सांख्यिकीय यांत्रिकी]] और गणित में, '''बोल्ट्ज़मैन वितरण''' (जिसे गिब्स वितरण भी कहा जाता है<ref name ="landau">{{cite book | author=Landau, Lev Davidovich |author2=Lifshitz, Evgeny Mikhailovich |name-list-style=amp | title=सांख्यिकीय भौतिकी|volume=5 |series=Course of Theoretical Physics |edition=3 |orig-year=1976 |year=1980 |place=Oxford |publisher=Pergamon Press|isbn=0-7506-3372-7|author-link=Lev Landau |author2-link=Evgeny Lifshitz }} Translated by J.B. Sykes and M.J. Kearsley. See section 28</ref>) संभाव्यता वितरण या [[संभाव्यता माप]] होता है, जो | [[File:Boltzmann distribution graph.svg|upright=1.75|right|thumb|बोल्ट्ज़मान कारक {{tmath|\tfrac{p_i}{p_j} }} (ऊर्ध्वाधर अक्ष) तापमान के फलन के रूप में {{mvar|T}} कई ऊर्जा अंतरों के लिए {{math|''ε<sub>i</sub>'' − ''ε<sub>j</sub>''}}.]][[सांख्यिकीय यांत्रिकी]] और गणित में, '''बोल्ट्ज़मैन वितरण''' (जिसे गिब्स वितरण भी कहा जाता है<ref name ="landau">{{cite book | author=Landau, Lev Davidovich |author2=Lifshitz, Evgeny Mikhailovich |name-list-style=amp | title=सांख्यिकीय भौतिकी|volume=5 |series=Course of Theoretical Physics |edition=3 |orig-year=1976 |year=1980 |place=Oxford |publisher=Pergamon Press|isbn=0-7506-3372-7|author-link=Lev Landau |author2-link=Evgeny Lifshitz }} Translated by J.B. Sykes and M.J. Kearsley. See section 28</ref>) संभाव्यता वितरण या [[संभाव्यता माप]] होता है, जो सिद्धांत के अनुसार प्रदत्त स्थिति में प्रणाली के सिद्धांतिक ऊर्जा और प्रणाली के तापमान के रूप में स्थिति में प्रणाली की होने की प्रायिकता देता है। वितरण को निम्नलिखित रूप में व्यक्त किया जाता है: | ||
:<math>p_i \propto \exp\left(- \frac{\varepsilon_i}{kT} \right)</math> | :<math>p_i \propto \exp\left(- \frac{\varepsilon_i}{kT} \right)</math> | ||
यहाँ {{mvar|p<sub>i</sub>}} प्रणाली के स्थिति {{mvar|i}} में होने की प्रायिकता है, {{math|exp}} गणनात्मक | यहाँ {{mvar|p<sub>i</sub>}} प्रणाली के स्थिति {{mvar|i}} में होने की प्रायिकता है, {{math|exp}} गणनात्मक फलन है, {{mvar|ε<sub>i</sub>}} उस अवस्था की ऊर्जा है, और वितरण का स्थिरांक {{mvar|kT}} बोल्ट्जमान स्थिरांक {{mvar|k}} और [[थर्मोडायनामिक तापमान]] {{mvar|T}} का उत्पाद होता है। चिन्ह <math display="inline">\propto</math> [[आनुपातिकता (गणित)]] को दर्शाता है (इसके लिए {{section link||प्रमाणितता }} का वितरण देखें)। | ||
यहां संख्यात्मक यांत्रिकी का व्यापक अर्थ है; यह परमाणुओं की 'पर्याप्त संख्या' के संग्रह या एकल परमाणु तक हो सकता है{{r|landau}} [[प्राकृतिक गैस भंडारण]] जैसी स्थूल प्रणाली के लिए होता है । इसलिए, बोल्ट्जमान वितरण को विभिन्न प्रकार की समस्याओं का समाधान करने के लिए प्रयोग किया जा सकता है। यह वितरण दिखाता है कि कम ऊर्जा वाली स्थितियों को स्थान देने की प्रायिकता हमेशा अधिक होगी। | |||
दो स्थितियों की संभावनाओं के अनुपात को 'बोल्ट्ज़मैन | दो स्थितियों की संभावनाओं के अनुपात को 'बोल्ट्ज़मैन अनुपात' के रूप में जाना जाता है और यह विशेष रूप से केवल स्थितियों के ऊर्जा अंतर पर निर्भर करता है: | ||
:<math>\frac{p_i}{p_j} = \exp\left( \frac{\varepsilon_j - \varepsilon_i}{kT} \right)</math> | :<math>\frac{p_i}{p_j} = \exp\left( \frac{\varepsilon_j - \varepsilon_i}{kT} \right)</math> | ||
बोल्ट्ज़मैन वितरण का नाम [[लुडविग बोल्ट्ज़मान]] के नाम पर रखा गया है, जिन्होंने पहली बार 1868 में [[थर्मल संतुलन]] में गैसों के सांख्यिकीय यांत्रिकी के अध्ययन के समय इसे तैयार किया था।<ref>{{cite journal |last=Boltzmann |first=Ludwig |author-link=Ludwig Boltzmann | बोल्ट्ज़मैन वितरण का नाम [[लुडविग बोल्ट्ज़मान]] के नाम पर रखा गया है, जिन्होंने पहली बार इसे 1868 में [[थर्मल संतुलन]] में गैसों के सांख्यिकीय यांत्रिकी के अध्ययन के समय इसे तैयार किया था।<ref>{{cite journal |last=Boltzmann |first=Ludwig |author-link=Ludwig Boltzmann | ||
|year=1868 | |year=1868 | ||
|title=Studien über das Gleichgewicht der lebendigen Kraft zwischen bewegten materiellen Punkten | |title=Studien über das Gleichgewicht der lebendigen Kraft zwischen bewegten materiellen Punkten | ||
|trans-title=Studies on the balance of living force between moving material points | |trans-title=Studies on the balance of living force between moving material points | ||
|journal=Wiener Berichte |volume=58 |pages=517–560 | |journal=Wiener Berichte |volume=58 |pages=517–560 | ||
}}</ref> | }}</ref> बोल्ट्जमान के सांख्यिकीय कार्य को उनके लेख "तापीय संतुलन की सांख्यिकी तांत्रिकता के बारे में द्वितीय मूलभूत सिद्धांत और थर्मल संतुलन की स्थिति के लिए प्रायिकता गणनाओं के संबंध पर" में प्रमाणित किया गया था।<ref>{{Cite web |url=http://crystal.med.upenn.edu/sharp-lab-pdfs/2015SharpMatschinsky_Boltz1877_Entropy17.pdf |title=संग्रहीत प्रति|access-date=2017-05-11 |archive-date=2021-03-05 |archive-url=https://web.archive.org/web/20210305005604/http://crystal.med.upenn.edu/sharp-lab-pdfs/2015SharpMatschinsky_Boltz1877_Entropy17.pdf |url-status=dead }}</ref> इस वितरण की बाद में, 1902 में [[जोशिया विलार्ड गिब्स]] द्वारा उसके आधुनिक साधारित रूप में विशेष जांच की गई।<ref name="gibbs">{{cite book |last=Gibbs |first=Josiah Willard |author-link=Josiah Willard Gibbs |title=सांख्यिकीय यांत्रिकी में प्राथमिक सिद्धांत|year=1902 |publisher=[[Charles Scribner's Sons]] | ||
|location=New York|title-link=सांख्यिकीय यांत्रिकी में प्राथमिक सिद्धांत}}</ref> | |location=New York|title-link=सांख्यिकीय यांत्रिकी में प्राथमिक सिद्धांत}}</ref> | ||
बोल्ट्ज़मैन वितरण को मैक्सवेल-बोल्ट्ज़मैन वितरण या मैक्सवेल-बोल्ट्ज़मैन सांख्यिकी के साथ भ्रमित नहीं किया जाना चाहिए। | बोल्ट्ज़मैन वितरण को मैक्सवेल-बोल्ट्ज़मैन वितरण या मैक्सवेल-बोल्ट्ज़मैन सांख्यिकी के साथ भ्रमित नहीं किया जाना चाहिए। बोल्ट्जमान वितरण प्रणाली की प्रायिकता देता है जो उस स्थिति की ऊर्जा के रूप में होने की प्रायिकता देती है,<ref name="Atkins, P. W. 2010">Atkins, P. W. (2010) Quanta, W. H. Freeman and Company, New York</ref> जबकि मैक्सवेल-बोल्ट्जमान वितरण आदर्श गैसों में कणों की गति या ऊर्जाओं की प्रायिकता देता है। चूँकि , <em>एक-आयामी</em> गैस में ऊर्जा का वितरण बोल्ट्ज़मैन वितरण का पालन करता है। | ||
==वितरण== | ==वितरण== | ||
बोल्ट्जमान वितरण प्रायिकता वितरण है जो निश्चित स्थिति की प्रायिकता देता है और | बोल्ट्जमान वितरण प्रायिकता वितरण है जो निश्चित स्थिति की प्रायिकता देता है जिसकी स्थिति की ऊर्जा और उस [[प्रणाली]] के तापमान के रूप में व्यवहार की जाती है, जिस पर वितरण लागू होता है। इसे निम्नलिखित रूप में दिया जाता है:<ref name="McQuarrie, A. 2000">{{cite book |last=McQuarrie |first=A. |year=2000 |title=सांख्यिकीय यांत्रिकी|publisher=University Science Books |location=Sausalito, CA |isbn=1-891389-15-7 }}</ref> | ||
<math display="block"> | <math display="block"> | ||
p_i=\frac{1}{Q} \exp\left(- \frac{\varepsilon_i}{kT} \right) = \frac{ \exp\left(- \tfrac{\varepsilon_i}{kT} \right) }{ \displaystyle \sum_{j=1}^{M} \exp\left(- \tfrac{\varepsilon_j}{kT} \right) } | p_i=\frac{1}{Q} \exp\left(- \frac{\varepsilon_i}{kT} \right) = \frac{ \exp\left(- \tfrac{\varepsilon_i}{kT} \right) }{ \displaystyle \sum_{j=1}^{M} \exp\left(- \tfrac{\varepsilon_j}{kT} \right) } | ||
| Line 35: | Line 35: | ||
*{{mvar|k}} बोल्ट्ज़मैन स्थिरांक है, | *{{mvar|k}} बोल्ट्ज़मैन स्थिरांक है, | ||
*{{mvar|T}} प्रणाली का पूर्ण तापमान है, | *{{mvar|T}} प्रणाली का पूर्ण तापमान है, | ||
*{{mvar|M}} | *{{mvar|M}} स संबंधित प्रणाली के सभी स्थितियों की संख्या है,<ref name="McQuarrie, A. 2000"/><ref name="Atkins, P. W. 2010"/> | ||
*{{mvar|Q}} (कुछ लेखकों द्वारा | *{{mvar|Q}} (कुछ लेखकों द्वारा {{mvar|Z}} दर्शाया गया है ) सामान्यीकरण विभाजक है, जो [[विहित विभाजन फ़ंक्शन|विहित विभाजन फलन]] है<math display=block> | ||
Q = \sum_{j=1}^{M} \exp\left(- \tfrac{\varepsilon_j}{kT} \right) | Q = \sum_{j=1}^{M} \exp\left(- \tfrac{\varepsilon_j}{kT} \right) | ||
</math> यह | </math> यह प्राथमिकता देता है कि सभी संभव स्थितियों की प्रायिकताओं का योग 1 होना चाहिए। | ||
बोल्ट्ज़मैन वितरण वह वितरण है जो [[एन्ट्रापी]] को | बोल्ट्ज़मैन वितरण वह वितरण है जो अधिकतम [[एन्ट्रापी]] को अधिक्षेपित करता है | ||
<math display=block>S(p_1,p_2,\cdots,p_M) = -\sum_{i=1}^{M} p_i\log_2 p_i</math> | <math display=block>S(p_1,p_2,\cdots,p_M) = -\sum_{i=1}^{M} p_i\log_2 p_i</math> | ||
सामान्यता नियमितता और शरीरिक माध्यम की औसत ऊर्जा मान के समान होने की शर्त के साथ। यह [[लैग्रेंज गुणक]] का उपयोग करके सिद्ध किया जा सकता है। | सामान्यता नियमितता और शरीरिक माध्यम की औसत ऊर्जा मान के समान होने की शर्त के साथ। यह [[लैग्रेंज गुणक]] का उपयोग करके सिद्ध किया जा सकता है। | ||
यदि हमें | यदि हमें संबंधित प्रणाली की प्रायिकताओं के ऊर्जाओं के बारे में जानकारी हो, तो हम प्रतिष्ठानिक निर्णयक के रूप में गणना कर सकते हैं। परमाणु तत्वों के लिए प्रतिष्ठानिक निर्णयक मूल्यों को एनआईएसटी परमाणु विकिरण डेटाबेस में खोजा जा सकता है।<ref>[http://physics.nist.gov/PhysRefData/ASD/levels_form.html NIST Atomic Spectra Database Levels Form] at nist.gov</ref> | ||
वितरण दिखाता है कि कम | यह वितरण दिखाता है कि ऊर्जा कम वाली स्थितियों को हमेशा ऊर्जा अधिक वाली स्थितियों की तुलना में अधिक प्रायिकता होगी। इसके अलावा, यह हमें दो स्थितियों की प्रायिकताओं के माप्यांतर को भी दे सकता है। स्थिति {{mvar|i}} और {{mvar|j}} के लिए प्रायिकता के अनुपात को निम्न रूप में दिया जाता है: | ||
<math display="block">\frac{p_i}{p_j} = \exp\left( \frac{\varepsilon_j - \varepsilon_i}{kT} \right)</math> | <math display="block">\frac{p_i}{p_j} = \exp\left( \frac{\varepsilon_j - \varepsilon_i}{kT} \right)</math> | ||
यहाँ: | यहाँ: | ||
| Line 65: | Line 65: | ||
यह समीकरण [[स्पेक्ट्रोस्कोपी|वित्रोस्कोपी]] के लिए बहुत महत्वपूर्ण है। वित्रोस्कोपी में हम अणु या अणु के स्थिति से दूसरी स्थिति में संक्रमण करने वाली अणुओं की [[वर्णक्रमीय रेखा]] देखते हैं।<ref name="Atkins, P. W. 2010"/><ref>{{cite book |last1=Atkins |first1=P. W. |last2=de Paula |first2=J. |year=2009 |title=भौतिक रसायन|edition=9th |publisher=Oxford University Press |location=Oxford |isbn=978-0-19-954337-3 }}</ref> इसके लिए, पहली स्थिति में कुछ कण होना चाहिए जो संक्रमण करें। हम यह शर्त पूरी होने पर पाएंगे कि जो प्राथमिक स्थिति में कणों का अंश होना चाहिए। यदि यह उपयुक्त नहीं होता है, तो संक्रमण को संभावित रूप से तापमान के लिए गणना की गई है, वह रेखा अधिक संभावित रूप से देखी नहीं जाती है। सामान्यतः, प्राथमिक स्थिति में अधिकांश अणुओं का अंश दूसरी स्थिति में संक्रमणों की अधिक संख्या का कारण होता है।<ref>{{cite book |last1=Skoog |first1=D. A. |last2=Holler |first2=F. J. |last3=Crouch |first3=S. R. |year=2006 |title=वाद्य विश्लेषण के सिद्धांत|publisher=Brooks/Cole |location=Boston, MA |isbn=978-0-495-12570-9 }}</ref> इससे मजबूत वर्णक्रमीय रेखा मिलती है। चूँकि, अनुमत या [[निषिद्ध संक्रमण]] के रूप में क्या होने वाले संक्रमण की प्रभावशीलता पर भी अन्य कारक प्रभाव डालते हैं। | यह समीकरण [[स्पेक्ट्रोस्कोपी|वित्रोस्कोपी]] के लिए बहुत महत्वपूर्ण है। वित्रोस्कोपी में हम अणु या अणु के स्थिति से दूसरी स्थिति में संक्रमण करने वाली अणुओं की [[वर्णक्रमीय रेखा]] देखते हैं।<ref name="Atkins, P. W. 2010"/><ref>{{cite book |last1=Atkins |first1=P. W. |last2=de Paula |first2=J. |year=2009 |title=भौतिक रसायन|edition=9th |publisher=Oxford University Press |location=Oxford |isbn=978-0-19-954337-3 }}</ref> इसके लिए, पहली स्थिति में कुछ कण होना चाहिए जो संक्रमण करें। हम यह शर्त पूरी होने पर पाएंगे कि जो प्राथमिक स्थिति में कणों का अंश होना चाहिए। यदि यह उपयुक्त नहीं होता है, तो संक्रमण को संभावित रूप से तापमान के लिए गणना की गई है, वह रेखा अधिक संभावित रूप से देखी नहीं जाती है। सामान्यतः, प्राथमिक स्थिति में अधिकांश अणुओं का अंश दूसरी स्थिति में संक्रमणों की अधिक संख्या का कारण होता है।<ref>{{cite book |last1=Skoog |first1=D. A. |last2=Holler |first2=F. J. |last3=Crouch |first3=S. R. |year=2006 |title=वाद्य विश्लेषण के सिद्धांत|publisher=Brooks/Cole |location=Boston, MA |isbn=978-0-495-12570-9 }}</ref> इससे मजबूत वर्णक्रमीय रेखा मिलती है। चूँकि, अनुमत या [[निषिद्ध संक्रमण]] के रूप में क्या होने वाले संक्रमण की प्रभावशीलता पर भी अन्य कारक प्रभाव डालते हैं। | ||
मशीन लर्निंग में सामान्यतः उपयोग किया जाने वाला [[सॉफ्टमैक्स फ़ंक्शन|सामान्यीकृत घातीय | मशीन लर्निंग में सामान्यतः उपयोग किया जाने वाला [[सॉफ्टमैक्स फ़ंक्शन|सामान्यीकृत घातीय फलन]] बोल्ट्ज़मैन वितरण से संबंधित है: | ||
:<math> | :<math> | ||
| Line 112: | Line 112: | ||
*फ़र्मी-डिराक आँकड़े | *फ़र्मी-डिराक आँकड़े | ||
*[[नकारात्मक तापमान]] | *[[नकारात्मक तापमान]] | ||
*सामान्यीकृत घातीय | *सामान्यीकृत घातीय फलन | ||
== संदर्भ == | == संदर्भ == | ||
Revision as of 23:25, 19 July 2023
सांख्यिकीय यांत्रिकी और गणित में, बोल्ट्ज़मैन वितरण (जिसे गिब्स वितरण भी कहा जाता है[1]) संभाव्यता वितरण या संभाव्यता माप होता है, जो सिद्धांत के अनुसार प्रदत्त स्थिति में प्रणाली के सिद्धांतिक ऊर्जा और प्रणाली के तापमान के रूप में स्थिति में प्रणाली की होने की प्रायिकता देता है। वितरण को निम्नलिखित रूप में व्यक्त किया जाता है:
यहाँ pi प्रणाली के स्थिति i में होने की प्रायिकता है, exp गणनात्मक फलन है, εi उस अवस्था की ऊर्जा है, और वितरण का स्थिरांक kT बोल्ट्जमान स्थिरांक k और थर्मोडायनामिक तापमान T का उत्पाद होता है। चिन्ह आनुपातिकता (गणित) को दर्शाता है (इसके लिए § प्रमाणितता का वितरण देखें)।
यहां संख्यात्मक यांत्रिकी का व्यापक अर्थ है; यह परमाणुओं की 'पर्याप्त संख्या' के संग्रह या एकल परमाणु तक हो सकता है[1] प्राकृतिक गैस भंडारण जैसी स्थूल प्रणाली के लिए होता है । इसलिए, बोल्ट्जमान वितरण को विभिन्न प्रकार की समस्याओं का समाधान करने के लिए प्रयोग किया जा सकता है। यह वितरण दिखाता है कि कम ऊर्जा वाली स्थितियों को स्थान देने की प्रायिकता हमेशा अधिक होगी।
दो स्थितियों की संभावनाओं के अनुपात को 'बोल्ट्ज़मैन अनुपात' के रूप में जाना जाता है और यह विशेष रूप से केवल स्थितियों के ऊर्जा अंतर पर निर्भर करता है:
बोल्ट्ज़मैन वितरण का नाम लुडविग बोल्ट्ज़मान के नाम पर रखा गया है, जिन्होंने पहली बार इसे 1868 में थर्मल संतुलन में गैसों के सांख्यिकीय यांत्रिकी के अध्ययन के समय इसे तैयार किया था।[2] बोल्ट्जमान के सांख्यिकीय कार्य को उनके लेख "तापीय संतुलन की सांख्यिकी तांत्रिकता के बारे में द्वितीय मूलभूत सिद्धांत और थर्मल संतुलन की स्थिति के लिए प्रायिकता गणनाओं के संबंध पर" में प्रमाणित किया गया था।[3] इस वितरण की बाद में, 1902 में जोशिया विलार्ड गिब्स द्वारा उसके आधुनिक साधारित रूप में विशेष जांच की गई।[4]
बोल्ट्ज़मैन वितरण को मैक्सवेल-बोल्ट्ज़मैन वितरण या मैक्सवेल-बोल्ट्ज़मैन सांख्यिकी के साथ भ्रमित नहीं किया जाना चाहिए। बोल्ट्जमान वितरण प्रणाली की प्रायिकता देता है जो उस स्थिति की ऊर्जा के रूप में होने की प्रायिकता देती है,[5] जबकि मैक्सवेल-बोल्ट्जमान वितरण आदर्श गैसों में कणों की गति या ऊर्जाओं की प्रायिकता देता है। चूँकि , एक-आयामी गैस में ऊर्जा का वितरण बोल्ट्ज़मैन वितरण का पालन करता है।
वितरण
बोल्ट्जमान वितरण प्रायिकता वितरण है जो निश्चित स्थिति की प्रायिकता देता है जिसकी स्थिति की ऊर्जा और उस प्रणाली के तापमान के रूप में व्यवहार की जाती है, जिस पर वितरण लागू होता है। इसे निम्नलिखित रूप में दिया जाता है:[6]
- exp() गणितीय फलन है,
- pi स्थिति i की प्रायिकता है ,
- εi स्थिति i की ऊर्जा है ,
- k बोल्ट्ज़मैन स्थिरांक है,
- T प्रणाली का पूर्ण तापमान है,
- M स संबंधित प्रणाली के सभी स्थितियों की संख्या है,[6][5]
- Q (कुछ लेखकों द्वारा Z दर्शाया गया है ) सामान्यीकरण विभाजक है, जो विहित विभाजन फलन हैयह प्राथमिकता देता है कि सभी संभव स्थितियों की प्रायिकताओं का योग 1 होना चाहिए।
बोल्ट्ज़मैन वितरण वह वितरण है जो अधिकतम एन्ट्रापी को अधिक्षेपित करता है
यदि हमें संबंधित प्रणाली की प्रायिकताओं के ऊर्जाओं के बारे में जानकारी हो, तो हम प्रतिष्ठानिक निर्णयक के रूप में गणना कर सकते हैं। परमाणु तत्वों के लिए प्रतिष्ठानिक निर्णयक मूल्यों को एनआईएसटी परमाणु विकिरण डेटाबेस में खोजा जा सकता है।[7]
यह वितरण दिखाता है कि ऊर्जा कम वाली स्थितियों को हमेशा ऊर्जा अधिक वाली स्थितियों की तुलना में अधिक प्रायिकता होगी। इसके अलावा, यह हमें दो स्थितियों की प्रायिकताओं के माप्यांतर को भी दे सकता है। स्थिति i और j के लिए प्रायिकता के अनुपात को निम्न रूप में दिया जाता है:
- pi स्थिति i की संभावना है ,
- pj स्थिति j की संभावना ,
- εi स्थिति i की ऊर्जा है ,
- εj स्थिति j की ऊर्जा है .
ऊर्जा स्तरों की जनसंख्या का अनुपात भी उनकी अध:पतन (क्वांटम यांत्रिकी) को भी ध्यान में रखना जाता है ।
बोल्ट्जमान वितरण सामान्यतः कणों, जैसे अणु या अणुओं के वितरण को वर्णित करने के लिए उपयोग किया जाता है जो उनके लिए उपलब्ध बंधित स्थितियों पर होते हैं। यदि हमारे पास बहुत सारे कणों से मिलकर बनी प्रणाली है, तो कण i के स्थिति में कण की प्रायिकता वास्तव में यह प्रायिकता होती है कि हम उस प्रणाली से यादृच्छिक कण चुनते हैं और देखते हैं कि वह किस स्थिति में है। यह प्रायिकता स्थिति i में कणों की संख्या को प्रणाली में कुल कणों की संख्या से विभाजित करने के समान होती है, जो स्थिति i में निवास करने वाले कणों का अंश है।
यहाँ Ni अवस्था i में कणों की संख्या है और N प्रणाली में कुल कणों की संख्या है। हम इस संभाव्यता को खोजने के लिए बोल्ट्ज़मान वितरण का उपयोग कर सकते हैं, जो कि हमने देखा है, स्थिति i में निवास करने वाले कणों की प्रायिकता के समान होती है। इसलिए, स्थिति की ऊर्जा के आधार पर स्थिति में कणों का अंश देने वाला समीकरण है [5]
मशीन लर्निंग में सामान्यतः उपयोग किया जाने वाला सामान्यीकृत घातीय फलन बोल्ट्ज़मैन वितरण से संबंधित है:
सामान्यीकृत बोल्ट्ज़मैन वितरण
कुछ लेखकों द्वारा, निम्नलिखित रूप के वितरण को "सामान्य बोल्ट्जमान वितरण" कहा जाता है:[10]
बोल्ट्ज़मान वितरण सामान्यीकृत बोल्ट्ज़मान वितरण का विशेष स्थिति है। सामान्यीकृत बोल्ट्ज़मैन वितरण का उपयोग सांख्यिकीय यांत्रिकी में विहित समूह, भव्य विहित समूह और तापीय-बारीय समूह का वर्णन करने के लिए किया जाता है। सामान्य बोल्ट्जमान वितरण सामान्यतः अधिकतम अनुपात के सिद्धान्त से प्राप्त किया जाता है, लेकिन अन्य निर्धारण भी हो सकते हैं।[10][11]
सामान्य बोल्ट्जमान वितरण के निम्नलिखित गुण होते हैं:
- यह वितरण एकमात्र वितरण है जिसके लिए जिब्स एंट्रोपी सूत्र द्वारा परिभाषित एन्ट्रॉपी (शास्त्रीय थर्मोडायनामिक्स) में परिभाषित एन्ट्रॉपी से मेल खाती है।[10]
- यह वितरण एकमात्र वितरण है जो मानक थर्मोडायनामिक संबंध के अनुरूप है जहां स्थिति कार्यों को औसत द्वारा वर्णित किया जाता है।[11]
सांख्यिकीय यांत्रिकी में
बोल्ट्जमान वितरण सांख्यिकीय मेकेनिक्स में प्रकट होता है जब बंद आवयविता वाली निर्धारित संघों को विचार किया जाता है जो ऊर्जा विनिमय के संबंध में थर्मल संतुलन में होते हैं (ऊर्जा विनिमय के संबंध में संतुलन)। सबसे सामान्य स्थिति कैननिक समूह के लिए प्रायिकता वितरण है। कुछ विशेष स्थिति (कैननिक समूह से प्राप्त किए जाने योग्य) विभिन्न पहलुओं में बोल्ट्जमान वितरण दिखाते हैं:
- विहित समूह (सामान्य स्थिति )
- विहित समूह ऊष्मा स्नान के साथ तापीय संतुलन में, निश्चित आयतन की बंद प्रणाली की विभिन्न संभावित स्थितियों की संभावनाएँ देता है। विहित समूह में बोल्ट्ज़मैन फॉर्म के साथ स्थिति संभाव्यता वितरण होता है।
- उपप्रणालियों की स्थिति की सांख्यिकीय आवृत्तियाँ (गैर-अंतःक्रियात्मक संग्रह में)
- जब रुचि की प्रणाली छोटे उपप्रणाली की कई गैर-अंतःक्रियात्मक प्रतियों का संग्रह होती है, तो संग्रह के बीच किसी दिए गए उपप्रणाली स्थिति की सांख्यिकीय आवृत्ति का पता लगाना कभी-कभी उपयोगी होता है। ऐसे संग्रह पर लागू होने पर विहित समुच्चय में पृथक्करण की संपत्ति होती है: जब तक गैर-अंतःक्रियात्मक उपप्रणालियों की संरचना निश्चित होती है, तब तक प्रत्येक उपप्रणाली की स्थिति दूसरों से स्वतंत्र होती है और विहित समुच्चय की विशेषता भी होती है। परिणामस्वरूप, उपप्रणाली स्थितियों के अपेक्षित मूल्य सांख्यिकीय आवृत्ति वितरण में बोल्ट्ज़मैन रूप होता है।
- शास्त्रीय गैसों के मैक्सवेल-बोल्ट्ज़मैन आँकड़े (गैर-अंतःक्रियात्मक कणों की प्रणाली)
- कण प्रणालियों में, कई कण ही स्थान साझा करते हैं और नियमित रूप से दूसरे के साथ स्थान बदलते हैं; वे जिस एकल-कण अवस्था स्थान पर कब्जा करते हैं वह साझा स्थान है। मैक्सवेल-बोल्ट्ज़मैन आँकड़े संतुलन में गैर-अंतःक्रियात्मक कणों की शास्त्रीय यांत्रिकी गैस में दिए गए एकल-कण अवस्था में पाए जाने वाले कणों की अपेक्षित संख्या देते हैं। इस अपेक्षित संख्या वितरण में बोल्ट्ज़मैन फॉर्म है।
चूँकि इन स्थितियों में मजबूत समानताएँ हैं, किन्तु इन्हें अलग करना मददगार है क्योंकि जब महत्वपूर्ण धारणाएँ बदल जाती हैं तो वे अलग-अलग विधियों से सामान्यीकरण करते हैं:
- जब कोई प्रणाली ऊर्जा विनिमय और कण विनिमय दोनों के संबंध में थर्मोडायनामिक संतुलन में होती है, तो निश्चित संरचना की आवश्यकता में छूट दी जाती है और विहित समूह के अतिरिक्त भव्य विहित समूह प्राप्त होता है। दूसरी ओर, यदि संरचना और ऊर्जा दोनों निश्चित हैं, तो इसके स्थान पर माइक्रोकैनोनिकल समूह लागू होता है।
- यदि किसी संग्रह के भीतर उपप्रणालियाँ एक-दूसरे के साथ परस्पर क्रिया करती हैं, तो उपप्रणाली स्थितियों की अपेक्षित आवृत्तियाँ अब बोल्ट्ज़मान वितरण का पालन नहीं करती हैं, और यहां तक कि उनका कोई विश्लेषणात्मक समाधान भी नहीं हो सकता है।[12] चूँकि , विहित समूह अभी भी पूरे प्रणाली की सामूहिक अवस्थाओं पर लागू किया जा सकता है, बशर्ते कि पूर्ण प्रणाली थर्मल संतुलन में हो।
- संतुलन में गैर-अंतःक्रियात्मक कणों की क्वांटम यांत्रिकी गैसों के साथ, किसी दिए गए एकल-कण अवस्था में पाए जाने वाले कणों की संख्या मैक्सवेल-बोल्ट्ज़मैन आंकड़ों का पालन नहीं करती है, और विहित समूह में क्वांटम गैसों के लिए कोई सरल बंद रूप अभिव्यक्ति नहीं है। भव्य विहित समूह में क्वांटम गैसों के राज्य-भरण आँकड़ों का वर्णन फर्मी-डिराक आँकड़ों या बोस-आइंस्टीन आँकड़ों द्वारा किया जाता है, जो इस बात पर निर्भर करता है कि कण क्रमशः फर्मियन या बोसॉन हैं।
गणित में
अधिक सामान्य गणितीय सेटिंग्स में, बोल्ट्ज़मैन वितरण को गिब्स माप के रूप में भी जाना जाता है। सांख्यिकी और यंत्र अधिगम में, इसे लॉग-रैखिक मॉडल कहा जाता है। गहन शिक्षण में, बोल्ट्ज़मैन वितरण का उपयोग बोल्ट्ज़मान मशीन, प्रतिबंधित बोल्ट्ज़मैन मशीन, ऊर्जा आधारित मॉडल ऊर्जा-आधारित मॉडल और डीप बोल्ट्ज़मैन मशीन जैसे स्टोकेस्टिक तंत्रिका नेटवर्क के नमूना वितरण में किया जाता है। गहन शिक्षण में, बोल्ट्ज़मैन मशीन को बिना पर्यवेक्षित शिक्षण मॉडल में से माना जाता है। गहन शिक्षण में बोल्ट्ज़मैन मशीन के डिज़ाइन में, जैसे-जैसे नोड्स की संख्या बढ़ती है, वास्तविक समय अनुप्रयोगों में कार्यान्वयन की कठिनाई महत्वपूर्ण हो जाती है, इसलिए प्रतिबंधित बोल्ट्ज़मैन मशीन नामक अलग प्रकार की वास्तुकला प्रस्तुत की जाती है।
अर्थशास्त्र में
उत्सर्जन व्यापार में परमिट आवंटित करने के लिए बोल्ट्ज़मैन वितरण प्रारंभ किया जा सकता है।[13][14] बोल्ट्ज़मैन वितरण का उपयोग करने वाली नई आवंटन विधि कई देशों के बीच उत्सर्जन परमिट के सबसे संभावित, प्राकृतिक और निष्पक्ष वितरण का वर्णन कर सकती है।
बोल्ट्ज़मैन वितरण का रूप बहुराष्ट्रीय लॉजिस्टिक प्रतिगमन मॉडल के समान है। अलग विकल्प मॉडल के रूप में, यह अर्थशास्त्र में बहुत अच्छी प्रकार से जाना जाता है क्योंकि डेनियल मैकफैडेन ने यादृच्छिक उपयोगिता अधिकतमकरण से संबंध बनाया है।[15]
यह भी देखें
- बोस-आइंस्टीन आँकड़े
- फ़र्मी-डिराक आँकड़े
- नकारात्मक तापमान
- सामान्यीकृत घातीय फलन
संदर्भ
- ↑ 1.0 1.1 Landau, Lev Davidovich & Lifshitz, Evgeny Mikhailovich (1980) [1976]. सांख्यिकीय भौतिकी. Course of Theoretical Physics. Vol. 5 (3 ed.). Oxford: Pergamon Press. ISBN 0-7506-3372-7. Translated by J.B. Sykes and M.J. Kearsley. See section 28
- ↑ Boltzmann, Ludwig (1868). "Studien über das Gleichgewicht der lebendigen Kraft zwischen bewegten materiellen Punkten" [Studies on the balance of living force between moving material points]. Wiener Berichte. 58: 517–560.
- ↑ "संग्रहीत प्रति" (PDF). Archived from the original (PDF) on 2021-03-05. Retrieved 2017-05-11.
- ↑ Gibbs, Josiah Willard (1902). सांख्यिकीय यांत्रिकी में प्राथमिक सिद्धांत. New York: Charles Scribner's Sons.
- ↑ 5.0 5.1 5.2 5.3 Atkins, P. W. (2010) Quanta, W. H. Freeman and Company, New York
- ↑ 6.0 6.1 McQuarrie, A. (2000). सांख्यिकीय यांत्रिकी. Sausalito, CA: University Science Books. ISBN 1-891389-15-7.
- ↑ NIST Atomic Spectra Database Levels Form at nist.gov
- ↑ Atkins, P. W.; de Paula, J. (2009). भौतिक रसायन (9th ed.). Oxford: Oxford University Press. ISBN 978-0-19-954337-3.
- ↑ Skoog, D. A.; Holler, F. J.; Crouch, S. R. (2006). वाद्य विश्लेषण के सिद्धांत. Boston, MA: Brooks/Cole. ISBN 978-0-495-12570-9.
- ↑ 10.0 10.1 10.2 Gao, Xiang; Gallicchio, Emilio; Roitberg, Adrian (2019). "सामान्यीकृत बोल्ट्ज़मान वितरण एकमात्र वितरण है जिसमें गिब्स-शैनन एन्ट्रॉपी थर्मोडायनामिक एन्ट्रॉपी के बराबर होती है". The Journal of Chemical Physics. 151 (3): 034113. arXiv:1903.02121. Bibcode:2019JChPh.151c4113G. doi:10.1063/1.5111333. PMID 31325924. S2CID 118981017.
- ↑ 11.0 11.1 Gao, Xiang (March 2022). "एन्सेम्बल थ्योरी का गणित". Results in Physics. 34: 105230. Bibcode:2022ResPh..3405230G. doi:10.1016/j.rinp.2022.105230. S2CID 221978379.
- ↑ A classic example of this is magnetic ordering. Systems of non-interacting spins show paramagnetic behaviour that can be understood with a single-particle canonical ensemble (resulting in the Brillouin function). Systems of interacting spins can show much more complex behaviour such as ferromagnetism or antiferromagnetism.
- ↑ Park, J.-W., Kim, C. U. and Isard, W. (2012) Permit allocation in emissions trading using the Boltzmann distribution. Physica A 391: 4883–4890
- ↑ The Thorny Problem Of Fair Allocation. Technology Review blog. August 17, 2011. Cites and summarizes Park, Kim and Isard (2012).
- ↑ Amemiya, Takeshi (1985). "Multinomial Logit Model". उन्नत अर्थमिति. Oxford: Basil Blackwell. pp. 295–299. ISBN 0-631-13345-3.