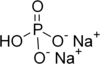सोडियम फॉस्फेट: Difference between revisions
No edit summary |
|||
| Line 2: | Line 2: | ||
[[File:monosodium phosphate.png|thumb|right|100px|[[ सोडियम डाइहाइड्रोजन फॉस्फेट ]]]] | [[File:monosodium phosphate.png|thumb|right|100px|[[ सोडियम डाइहाइड्रोजन फॉस्फेट ]]]] | ||
[[File:disodium hydrogen phosphate.png|thumb|100px|right|[[ सोडियम हाइड्रोजन फॉस्फेट ]]]] | [[File:disodium hydrogen phosphate.png|thumb|100px|right|[[ सोडियम हाइड्रोजन फॉस्फेट ]]]] | ||
[[File:trisodium phosphate.png|thumb|right|100px|[[ ट्राइसोडियम फॉस्फेट ]]]][[ सोडियम | सोडियम]] फॉस्फेट सोडियम (Na<sup>+</sup>) और [[ फास्फेट |फास्फेट]] (PO<sub>4</sub><sup>3−</sup>). फॉस्फेट डी-, ट्राई-, टेट्रा- और पॉलीफॉस्फेट सहित परिवारों या संघनित आयनों का भी निर्माण करता है। इनमें से अधिकांश लवण निर्जल (जल-मुक्त) और जलयोजित दोनों रूपों में जाने जाते हैं। निर्जल रूपों की तुलना में हाइड्रेट अधिक सामान्य हैं।<ref name=Ullmann>{{Ullmann|author1=Klaus Schrödter|author2=Gerhard Bettermann|author3=Thomas Staffel|author4=Friedrich Wahl|author5=Thomas Klein|author6=Thomas Hofmann|title=Phosphoric Acid and Phosphates|doi=10.1002/14356007.a19_465.pub3|year=2012}}</ref> | [[File:trisodium phosphate.png|thumb|right|100px|[[ ट्राइसोडियम फॉस्फेट ]]]]'''[[ सोडियम |सोडियम]] फॉस्फेट''' सोडियम (Na<sup>+</sup>) और [[ फास्फेट |फास्फेट]] (PO<sub>4</sub><sup>3−</sup>). फॉस्फेट डी-, ट्राई-, टेट्रा- और पॉलीफॉस्फेट सहित परिवारों या संघनित आयनों का भी निर्माण करता है। इनमें से अधिकांश लवण निर्जल (जल-मुक्त) और जलयोजित दोनों रूपों में जाने जाते हैं। निर्जल रूपों की तुलना में हाइड्रेट अधिक सामान्य हैं।<ref name=Ullmann>{{Ullmann|author1=Klaus Schrödter|author2=Gerhard Bettermann|author3=Thomas Staffel|author4=Friedrich Wahl|author5=Thomas Klein|author6=Thomas Hofmann|title=Phosphoric Acid and Phosphates|doi=10.1002/14356007.a19_465.pub3|year=2012}}</ref> | ||
== उपयोग करता है == | == उपयोग करता है == | ||
सोडियम फॉस्फेट के भोजन और जल उपचार में कई अनुप्रयोग हैं। उदाहरण के लिए, सोडियम फॉस्फेट प्रायः पायसीकारी के रूप में उपयोग किया जाता है (प्रसंस्कृत पनीर के रूप में),<ref>{{cite web |url=http://www.sodiumphosphateformula.com/tag/monosodium-phosphate |url-status=dead |archive-url=https://web.archive.org/web/20150402120338/http://www.sodiumphosphateformula.com/tag/monosodium-phosphate |archive-date=2015-04-02 |title=Monosodium Phosphate {{!}} Sodium Phosphate Formula}}</ref> पके हुए माल के लिए | सोडियम फॉस्फेट के भोजन और जल उपचार में कई अनुप्रयोग हैं। उदाहरण के लिए, सोडियम फॉस्फेट प्रायः पायसीकारी के रूप में उपयोग किया जाता है (प्रसंस्कृत पनीर के रूप में),<ref>{{cite web |url=http://www.sodiumphosphateformula.com/tag/monosodium-phosphate |url-status=dead |archive-url=https://web.archive.org/web/20150402120338/http://www.sodiumphosphateformula.com/tag/monosodium-phosphate |archive-date=2015-04-02 |title=Monosodium Phosphate {{!}} Sodium Phosphate Formula}}</ref> पके हुए माल के लिए गाढ़ा करने का पदार्थ और [[ उठना एजेंट |रिसाव एजेंट]] उनका उपयोग प्रसंस्कृत खाद्य पदार्थों के पीएच को नियंत्रित करने के लिए भी किया जाता है।<ref>{{cite journal | last1 = Lampila | first1 = Lucina E. | year = 2013 | title = Applications and functions of food-grade phosphates | journal = Ann. N.Y. Acad. Sci. | volume = 1301 | issue = 1| pages = 37–44 | doi = 10.1111/nyas.12230 | pmid = 24033359 | bibcode = 2013NYASA1301...37L | s2cid = 206223856 | doi-access = free }}</ref> उनका उपयोग [[ कब्ज |कब्ज]] के लिए दवा में और चिकित्सा प्रक्रियाओं के लिए आंत्र तैयार करने के लिए भी किया जाता है। इसके अतिरिक्त, वे पानी को नरम करने के लिए डिटर्जेंट में औरकुशल जंग रोधी समाधान के रूप में उपयोग किए जाते हैं। | ||
== प्रतिकूल प्रभाव == | == प्रतिकूल प्रभाव == | ||
| Line 109: | Line 109: | ||
|- | |- | ||
|} | |} | ||
डाइफॉस्फेट्स के अतिरिक्त, सोडियम लवणों को ट्राइफॉस्फेट्स के रूप में जाना जाता है, उदा. [[ सोडियम ट्राइफॉस्फेट |सोडियम ट्राइफॉस्फेट]] और | डाइफॉस्फेट्स के अतिरिक्त, सोडियम लवणों को ट्राइफॉस्फेट्स के रूप में जाना जाता है, उदा. [[ सोडियम ट्राइफॉस्फेट |सोडियम ट्राइफॉस्फेट]] और टेट्राफॉस्फेट है। चक्रीय पॉलीफॉस्फेट्स, जिन्हें मेटाफॉस्फेट कहा जाता है, ट्रिमर [[ सोडियम ट्राइमेटाफॉस्फेट |सोडियम ट्राइमेटाफॉस्फेट]] और टेट्रामर सम्मलित हैं, Na<sub>3</sub>P<sub>3</sub>O<sub>9</sub> और Na<sub>4</sub>P<sub>4</sub>O<sub>12</sub>, क्रमश। | ||
NaH<sub>2</sub>PO<sub>4</sub> के मिश्रण को गर्म करने पर पॉलिमरिक सोडियम फॉस्फेट बनते हैं और Na<sub>2</sub>HPO<sub>4</sub>, जो [[ संघनन प्रतिक्रिया |संघनन प्रतिक्रिया]] को प्रेरित करता है। उत्पन्न विशिष्ट पॉलीफॉस्फेट हीटिंग और एनीलिंग के विवरण पर निर्भर करता है। व्युत्पन्न [[ कांच |कांच]] (अर्थात, अनाकार) ग्राहम का नमक है। यह रैखिक पॉलीफॉस्फेट है जिसका औसत सूत्र NaO(NaPO<sub>3</sub>)Na<sub>2</sub> पहले से क्रिस्टलीय उच्च आणविक भार पॉलीफॉस्फेट में कुरोल का नमक और मैड्रेल का नमक (कैस 10361-03-2) सम्मलित हैं। इन प्रजातियों का सूत्र है [NaPO<sub>3</sub>]<sub>n</sub>[NaPO<sub>3</sub>(OH)]<sub>2</sub> जहाँ n 2000 जितना बड़ा हो सकता है। उनकी संरचना के संदर्भ में, इन पॉलिमर में PO<sub>3</sub><sup>−</sup> होता है मोनोमर्स, जंजीरों के साथ प्रोटोनेटेड फॉस्फेट द्वारा समाप्त होते हैं।<ref name=Ullmann/><ref name=G&E>{{Greenwood&Earnshaw2nd|page=530}}</ref> | NaH<sub>2</sub>PO<sub>4</sub> के मिश्रण को गर्म करने पर पॉलिमरिक सोडियम फॉस्फेट बनते हैं और Na<sub>2</sub>HPO<sub>4</sub>, जो [[ संघनन प्रतिक्रिया |संघनन प्रतिक्रिया]] को प्रेरित करता है। उत्पन्न विशिष्ट पॉलीफॉस्फेट हीटिंग और एनीलिंग के विवरण पर निर्भर करता है। व्युत्पन्न [[ कांच |कांच]] (अर्थात, अनाकार) ग्राहम का नमक है। यह रैखिक पॉलीफॉस्फेट है जिसका औसत सूत्र NaO(NaPO<sub>3</sub>)Na<sub>2</sub> पहले से क्रिस्टलीय उच्च आणविक भार पॉलीफॉस्फेट में कुरोल का नमक और मैड्रेल का नमक (कैस 10361-03-2) सम्मलित हैं। इन प्रजातियों का सूत्र है [NaPO<sub>3</sub>]<sub>n</sub>[NaPO<sub>3</sub>(OH)]<sub>2</sub> जहाँ n 2000 जितना बड़ा हो सकता है। उनकी संरचना के संदर्भ में, इन पॉलिमर में PO<sub>3</sub><sup>−</sup> होता है मोनोमर्स, जंजीरों के साथ प्रोटोनेटेड फॉस्फेट द्वारा समाप्त होते हैं।<ref name=Ullmann/><ref name=G&E>{{Greenwood&Earnshaw2nd|page=530}}</ref> | ||
Revision as of 18:04, 30 January 2023
सोडियम फॉस्फेट सोडियम (Na+) और फास्फेट (PO43−). फॉस्फेट डी-, ट्राई-, टेट्रा- और पॉलीफॉस्फेट सहित परिवारों या संघनित आयनों का भी निर्माण करता है। इनमें से अधिकांश लवण निर्जल (जल-मुक्त) और जलयोजित दोनों रूपों में जाने जाते हैं। निर्जल रूपों की तुलना में हाइड्रेट अधिक सामान्य हैं।[1]
उपयोग करता है
सोडियम फॉस्फेट के भोजन और जल उपचार में कई अनुप्रयोग हैं। उदाहरण के लिए, सोडियम फॉस्फेट प्रायः पायसीकारी के रूप में उपयोग किया जाता है (प्रसंस्कृत पनीर के रूप में),[2] पके हुए माल के लिए गाढ़ा करने का पदार्थ और रिसाव एजेंट उनका उपयोग प्रसंस्कृत खाद्य पदार्थों के पीएच को नियंत्रित करने के लिए भी किया जाता है।[3] उनका उपयोग कब्ज के लिए दवा में और चिकित्सा प्रक्रियाओं के लिए आंत्र तैयार करने के लिए भी किया जाता है। इसके अतिरिक्त, वे पानी को नरम करने के लिए डिटर्जेंट में औरकुशल जंग रोधी समाधान के रूप में उपयोग किए जाते हैं।
प्रतिकूल प्रभाव
सोडियम फॉस्फेट वाणिज्य में आंशिक रूप से लोकप्रिय हैं क्योंकि वे सस्ती हैं और क्योंकि वे खपत के सामान्य स्तर पर गैर-विषैले हैं।[4] चूंकि, मौखिक सोडियम फॉस्फेट जब कोलोनोस्कोपी के लिए आंत्र तैयारी के लिए उच्च खुराक पर लिया जाता है, तो कुछ व्यक्तियों में फॉस्फेट नेफ्रोपैथी के रूप में गुर्दे की चोट का खतरा हो सकता है। ऐसे कई ओरल फॉस्फेट फॉर्मूलेशन हैं जो तत्काल तैयार किए जाते हैं। संयुक्त राज्य अमेरिका में मौखिक फॉस्फेट प्रस्तुत करने वाली दवाओं को वापस ले लिया गया है, चूंकि कार्य-कारण का प्रमाण अस्पष्ट है।[5] चूंकि फॉस्फेट जुलाब के लिए सुरक्षित और प्रभावी प्रतिस्थापन उपलब्ध हैं, कई चिकित्सा अधिकारियों ने मौखिक फॉस्फेट के सामान्य अनुपयोग की सिफारिश की है।[6]
मोनोफॉस्फेट्स
सोडियम मोनोफॉस्फेट के तीन परिवार आम हैं, जो ऑर्थोफॉस्फेट (PO43−), हाइड्रोजन फॉस्फेट (HPO42−), और डायहाइड्रोजनफॉस्फेट (H2PO4−). तालिका में कुछ सबसे प्रसिद्ध लवण दिखाए गए हैं।
| नाम | सूत्र | सीएएस रजिस्ट्री संख्या |
|---|---|---|
| मोनोसोडियम फॉस्फेट (निर्जल) | NaH2PO4 | 7558-80-7 |
| मोनोसोडियम फॉस्फेट (मोनोहाइड्रेट) | NaH2PO4(H2O) | 10049-21-5 |
| मोनोसोडियम फॉस्फेट (डिहाइड्रेट) | NaH2PO4(H2O)2 | 13472-35-0 |
| सोडियम फास्फेट (निर्जल) | Na2HPO4 | 7558-79-4 |
| सोडियम फास्फेट (डिहाइड्रेट) | HNa2PO4(H2O)2 | 10028-24-7 |
| सोडियम फास्फेट (हेप्टाहाइड्रेट) | HNa2PO4(H2O)7 | 7782-85-6 |
| सोडियम फास्फेट (ऑक्टाहाइड्रेट) | HNa2PO4(H2O)8 | |
| सोडियम फास्फेट (डोडकाहाइड्रेट) | HNa2PO4(H2O)12 | 10039-32-4 |
| ट्राइसोडियम फॉस्फेट (निर्जल, हेक्सागोनल) | Na3PO4 | |
| ट्राइसोडियम फॉस्फेट (निर्जल, क्युबिक) | Na3PO4 | 7601-54-9 |
| ट्राइसोडियम फॉस्फेट (हेमिहाइड्रेट) | Na3PO4(H2O)0.5 | |
| ट्राइसोडियम फॉस्फेट (हेक्साहाइड्रेट) | Na3PO4(H2O)6 | |
| ट्राइसोडियम फॉस्फेट (ऑक्टाहाइड्रेट) | Na3PO4(H2O)8 | |
| ट्राइसोडियम फॉस्फेट (डोडकाहाइड्रेट) | Na3PO4(H2O)12 | 10101-89-0 |
डि- और पॉलीफॉस्फेट्स
इन फॉस्फेट के अतिरिक्त, सोडियम पाइरोफॉस्फेट (जिन्हें डाइफॉस्फेट भी कहा जाता है), ट्राइफॉस्फेट और उच्च पॉलिमर के साथ कई उपयोगी लवण बनाता है। इन लवणों में से, डाइफोस्फेट विशेष रूप से व्यावसायिक रूप से सामान्य हैं।
| नाम | सूत्र | कैस रजिस्ट्री संख्या |
|---|---|---|
| मोनोसोडियम डाइफॉस्फेट (निर्जल) | NaH3P2O7 | |
| डाइसोडियम डाइफॉस्फेट (निर्जल) | Na2H2P2O7 | 7758-16-9 |
| डाइसोडियम डाइफॉस्फेट (हेक्साहाइड्रेट) | Na2H2P2O7(H2O)6 | |
| ट्राइसोडियम डाइफॉस्फेट (निर्जल) | Na3HP2O7 | |
| ट्राइसोडियम डाइफॉस्फेट (मोनोहाइड्रेट) | Na3HP2O7(H2O) | |
| ट्राइसोडियम डाइफॉस्फेट (नोनाहाइड्रेट) | Na3HP2O7(H2O)9 | |
| टेट्रासोडियम डाइफोस्फेट (निर्जल) | Na4P2O7 | 7722-88-5 |
| टेट्रासोडियम डाइफोस्फेट (डेकाहाईड्रेट) | Na4P2O7(H2O)10 | 13472-36-1 |
डाइफॉस्फेट्स के अतिरिक्त, सोडियम लवणों को ट्राइफॉस्फेट्स के रूप में जाना जाता है, उदा. सोडियम ट्राइफॉस्फेट और टेट्राफॉस्फेट है। चक्रीय पॉलीफॉस्फेट्स, जिन्हें मेटाफॉस्फेट कहा जाता है, ट्रिमर सोडियम ट्राइमेटाफॉस्फेट और टेट्रामर सम्मलित हैं, Na3P3O9 और Na4P4O12, क्रमश।
NaH2PO4 के मिश्रण को गर्म करने पर पॉलिमरिक सोडियम फॉस्फेट बनते हैं और Na2HPO4, जो संघनन प्रतिक्रिया को प्रेरित करता है। उत्पन्न विशिष्ट पॉलीफॉस्फेट हीटिंग और एनीलिंग के विवरण पर निर्भर करता है। व्युत्पन्न कांच (अर्थात, अनाकार) ग्राहम का नमक है। यह रैखिक पॉलीफॉस्फेट है जिसका औसत सूत्र NaO(NaPO3)Na2 पहले से क्रिस्टलीय उच्च आणविक भार पॉलीफॉस्फेट में कुरोल का नमक और मैड्रेल का नमक (कैस 10361-03-2) सम्मलित हैं। इन प्रजातियों का सूत्र है [NaPO3]n[NaPO3(OH)]2 जहाँ n 2000 जितना बड़ा हो सकता है। उनकी संरचना के संदर्भ में, इन पॉलिमर में PO3− होता है मोनोमर्स, जंजीरों के साथ प्रोटोनेटेड फॉस्फेट द्वारा समाप्त होते हैं।[1][7]
संदर्भ
- ↑ 1.0 1.1 Klaus Schrödter; Gerhard Bettermann; Thomas Staffel; Friedrich Wahl; Thomas Klein; Thomas Hofmann (2012). "Phosphoric Acid and Phosphates". Ullmann's Encyclopedia of Industrial Chemistry. Weinheim: Wiley-VCH. doi:10.1002/14356007.a19_465.pub3.
- ↑ "Monosodium Phosphate | Sodium Phosphate Formula". Archived from the original on 2015-04-02.
- ↑ Lampila, Lucina E. (2013). "Applications and functions of food-grade phosphates". Ann. N.Y. Acad. Sci. 1301 (1): 37–44. Bibcode:2013NYASA1301...37L. doi:10.1111/nyas.12230. PMID 24033359. S2CID 206223856.
- ↑ Razzaque, M. S. (2011). "Phosphate toxicity: New insights into an old problem". Clinical Science. 120 (3): 91–97. doi:10.1042/CS20100377. PMC 3120105. PMID 20958267.
- ↑ Markawitz, GB; Parezelli, MA (Aug 12, 2007), "Acute Phosphate Nephropathyl", Kidney Int., vol. 76, no. 10, pp. 1027–34, doi:10.1038/ki.2009.308, PMID 19675530
- ↑ Mackey, AC; Breen, L; Amand, KS; Evigan, M (August 2007), "Sodium phosphate tablets and acute Phosphate Nephropathy", Am J Gastroenterol, vol. 104, no. 8, pp. 1903–6, doi:10.1038/ajg.2009.342, PMID 19661931, S2CID 12551005
- ↑ Greenwood, Norman N.; Earnshaw, Alan (1997). Chemistry of the Elements (2nd ed.). Butterworth-Heinemann. p. 530. ISBN 978-0-08-037941-8.
बाहरी कड़ियाँ
- Bell, Russel N (April 1973), "Sodium Aluminum Phosphate Cheese Emulsifying Agent", US Patent 3726960
- Lien, YH (16 July 2008), "Is bowel preparation before colonoscopy a risky business for the kidney?", Nature Clinical Practice Nephrology, 4 (11): 606–14, doi:10.1038/ncpneph0939, PMID 18797448, S2CID 340122