राइबोसोमल डीएनए
राइबोसोमल डीएनए (आरडीएनए) एक डीएनए अनुक्रम है, जो राइबोसोमल आरएनए के लिए कोड करते है। ये अनुक्रम प्रतिलेखन (आनुवांशिकी) प्रवर्तन और प्रवर्धन को विनियमित करते हैं, और इसमें अनुलेखित और गैर-प्रतिलेखित अन्तरालक खंड दोनों होते हैं।
मानव जीनोम में न्यूक्लियोलस आयोजक क्षेत्रों के साथ 5 गुणसूत्र होते हैं: अग्रकेंद्रिक गुणसूत्र 13 (आरएनआर1), 14( आरएनआर 2), 15 (आरएनआर3), 21 (आरएनआर 4) और 22 (आरएनआर 5)। आरआरएनए की विभिन्न उप-इकाइयों को संकेतीकरण करने के लिए उत्तरदायी वंशाणु, मनुष्यों में कई गुणसूत्रों में स्थित होते हैं। किन्तु वंशाणु जो आरआरएनए के लिए सांकेतिक शब्दों में बदला करते हैं, डोमेन में अत्यधिक संरक्षित होते हैं, प्रति प्रजातियों में अलग-अलग संख्या वाले जीनों के लिए केवल प्रतिलिपि संख्याएं सम्मलित होते हैं। [1] जीवाणु, आर्किया और क्लोरोप्लास्ट में आरआरएनए विभिन्न (छोटी) इकाइयों से बने होते है, 23S राइबोसोमल आरएनए, 16S राइबोसोमल आरएनए और 5एस आरआरएनए से बना होता है। 16एस आरआरएनए का व्यापक रूप से फाइलोजेनेटिक अध्ययन के लिए उपयोग किया जाता है।[2]
यूकेरियोट्स
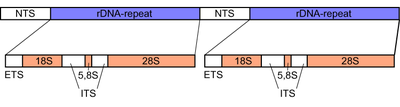
लगभग 600 आरडीएनए दोहराव से अनुलेखित आरआरएनए यूकेरियोट्स की कोशिकाओं में पाए जाने वाले आरएनए का सबसे प्रचुर खंड बनाता है।।[1] राइबोसोम प्रोटीन और आरआरएनए अणुओं की समन्वायोजन हैं, जो प्रोटीन का उत्पादन करने के लिए एमआरएनए अणुओं का अनुवाद (जीव विज्ञान) में करते हैं। जैसा कि चित्र में दिखाया गया है, यूकेरियोट्स के आरडीएनए में एनटीएस, ईटीएस, 18एस, आईटीएस1, 5.8 एस, आईटीएस 2, और 28एस ट्रैक्ट्स से बना एक इकाई खंड का अग्रानुक्रमित दोहराव होता है। आरडीएनए में एक और जीन होता है, जो 5S आरआरएनए के लिए संकेतबद्ध करता है, जो अधिकांश यूकेरियोट्स में जीनोम में स्थित होता है। [3] ड्रोसोफिला की तरह स्वतंत्र अग्रानुक्रम दोहराव में 5S आरडीएनए भी उपस्थित है।।[3] दोहराए जाने वाले डीएनए क्षेत्र अधिकांशतः पुनर्संयोजन की घटनाओं से निकलते हैं। आरडीएनए दोहराव में कई नियामक तंत्र होते हैं जो डीएनए को उत्परिवर्तन से बचाते हैं, इस प्रकार आरडीएनए को संरक्षित रखते हैं।[1]
नाभिक में, गुणसूत्र के आरडीएनए क्षेत्र को न्यूक्लियोलस के रूप में देखा जाता है जो आरडीएनए के साथ विस्तारित क्रोमोसोमल लूप बनाता है। आरआरएनए ट्रांसक्रिप्शनल इकाइयों को अग्रानुक्रम दोहराव में क्लस्टर किया जाता है। इन आरडीएनए क्षेत्रों को न्यूक्लियोलस आयोजक क्षेत्र भी कहा जाता है, क्योंकि वे न्यूक्लियोलस को जन्म देते हैं। आरडीएनए में, अग्रानुक्रम दोहराव ज्यादातर नाभिक में पाए जाते हैं; किन्तु हेटरोक्रोमैटिक आरडीएनए न्यूक्लियोलस के बाहर पाया जाता है। चूँकि, ट्रांसक्रिप्शनल रूप से सक्रिय आरडीएनए न्यूक्लियोलस के अंदर ही रहता है।[1]
अनुक्रम एकरूपता
बड़े आरडीएनए सरणी में, आरडीएनए दोहराने वाली इकाइयों के बीच बहुरूपता बहुत कम है यह दर्शाता है कि आरडीएनए अग्रानुक्रम सरणियाँ ठोस विकास के माध्यम से विकसित हो रही हैं।[3] चूँकि, ठोस विकास का तंत्र अपूर्ण है, जैसे कि एक व्यक्ति के भीतर दोहराए जाने वाले बहुरूपता महत्वपूर्ण स्तरों पर हो सकते हैं और बारीकी से संबंधित जीवों के लिए जातिवृत्तीय्स विश्लेषण को भ्रमित कर सकते हैं।Cite error: Closing </ref> missing for <ref> tag
कई ड्रोसोफिला में 5S अग्रानुक्रम दोहराव दृश्यों की एक दूसरे के साथ तुलना की गई; परिणाम से पता चला कि सम्मिलन (आनुवांशिकी) और विलोपन (आनुवांशिकी) प्रजातियों के बीच अधिकांशतः होता है और अधिकांशतः संरक्षित अनुक्रमों से घिरा होता है। [4] वे डीएनए प्रतिकृति या जीन रूपांतरण के दौरान नए संश्लेषित स्ट्रैंड के स्लिपेज द्वारा हो सकते हैं। [4]
अनुक्रम विचलन
आरडीएनए ट्रांसक्रिप्शन ट्रैक्ट्स में प्रजातियों के बीच जीन बहुरूपता की कम दर होती है, जो केवल कुछ नमूनों का उपयोग करके फ़िलेजेनेटिक संबंध को स्पष्ट करने के लिए प्रतिच्छेदन तुलना की अनुमति देता है। आरडीएनए के संकेतबद्ध क्षेत्र प्रजातियों के बीच अत्यधिक संरक्षित हैं लेकिन आईटीएस क्षेत्र सम्मिलन, विलोपन और बिंदु उत्परिवर्तन के कारण परिवर्तनशील हैं। दूरस्थ प्रजातियों के बीच मानव और मेंढक के रूप में ITS ट्रैक्ट्स में अनुक्रमों की तुलना उचित नहीं है।[5] आरडीएनए के संकेतबद्ध क्षेत्रों में संरक्षित अनुक्रम दूरस्थ प्रजातियों की तुलना करने की अनुमति देते हैं, यहां तक कि खमीर और मानव के बीच भी। मानव 5.8S आरआरएनए की खमीर 5.8S आरआरएनए के साथ 75% समरूपता है।[6] सहोदर प्रजातियों के स्थितियों में, प्रजातियों के बीच ITS ट्रैक्ट सहित आरडीएनए खंड की तुलना और वंशावली विश्लेषण संतोषजनक ढंग से किया जाता है। [7][8] आरडीएनए दोहराव के विभिन्न संकेतबद्ध क्षेत्र सामान्यतः अलग-अलग विकास दर दिखाते हैं। परिणाम स्वरुप,डीएनए व्यापक व्यवस्थित स्तरों से संबंधित प्रजातियों की जातिवृत्तीय जानकारी प्रदान कर सकता है।[9]
पुनर्संयोजन-उत्तेजक गतिविधि
खमीर आरडीएनए के एक टुकड़े में 5S जीन, गैर-प्रतिलेखित स्पेसर डीएनए, और 35S जीन का हिस्सा होता है, जिसमें सीआईएस-अभिनय माइटोटिक पुनर्संयोजन उत्तेजक गतिविधि होती है।[10] इस डीएनए टुकड़े में माइटोटिक पुनर्संयोजन हॉटस्पॉट होते है, जिसे हॉट1 कहा जाता है। हॉट1 पुनर्संयोजन-उत्तेजक गतिविधि को व्यक्त करता है जब इसे खमीर जीनोम में उपन्यास स्थानों में डाला जाता है। हॉट1 में एक आरएनए पोलीमरेज़ में (पोल) ट्रांसक्रिप्शन प्रमोटर (आनुवांशिकी) सम्मलित है, जो 35S राइबोसोमल आरएनए जीन ट्रांसक्रिप्शन को उत्प्रेरित करता है। एक पोल दोषपूर्ण उत्परिवर्ती में, हॉट1 हॉटस्पॉट पुनर्संयोजन-उत्तेजक गतिविधि को समाप्त कर दिया जाता है। हॉट1 में पोली प्रतिलेखन का स्तर आनुवंशिक पुनर्संयोजन के स्तर को निर्धारित करता प्रतीत होता है।[11]
नैदानिक महत्व
रोग डीएनए उत्परिवर्तन से जुड़े हो सकते हैं जहां डीएनए का विस्तार किया जा सकता है, जैसे हंटिंग्टन रोग, या विलोपन उत्परिवर्तन के कारण खो गया। आरडीएनए दोहराव में होने वाले उत्परिवर्तन के लिए भी यही सही; यह पाया गया है कि यदि राइबोसोम के संश्लेषण से जुड़े जीन बाधित या उत्परिवर्तित होते हैं, तो इसका परिणाम कंकाल या अस्थि मज्जा से जुड़े विभिन्न रोग हो सकते हैं। इसके अतिरिक्त, आरडीएनए के अग्रानुक्रम दोहराव की रक्षा करने वाले एंजाइमों में किसी भी तरह की क्षति या व्यवधान के परिणामस्वरूप राइबोसोम का संश्लेषण कम हो सकता है जिससे कोशिका में अन्य दोष भी हो सकते हैं। आरडीएनए अग्रानुक्रम दोहराव में उत्परिवर्तन से न्यूरोलॉजिकल रोग भी उत्पन्न हो सकते हैं, जैसे कि ब्लूम सिंड्रोम, जो तब होता है, जब अग्रानुक्रम दोहराव की संख्या सौ गुना करीब बढ़ जाती है; अग्रानुक्रम दोहराव की सामान्य संख्या की तुलना में। राइबोसोमल डीएनए में अग्रानुक्रम दोहराव के उत्परिवर्तन से विभिन्न प्रकार के कैंसर भी हो सकते हैं। अग्रानुक्रम दोहराव की पुनर्व्यवस्था, या आरडीएनए में दोहराव के विस्तार से कोशिका रेखाएँ घातक हो सकती हैं।[12]
संदर्भ
- ↑ 1.0 1.1 1.2 1.3 Warmerdam, Daniël O.; Wolthuis, Rob M. F. (2019-03-01). "Keeping ribosomal DNA intact: a repeating challenge". Chromosome Research (in English). 27 (1): 57–72. doi:10.1007/s10577-018-9594-z. ISSN 1573-6849. PMC 6394564. PMID 30556094.
- ↑ Weisburg WG, Barns SM, Pelletier DA, Lane DJ (January 1991). "16S ribosomal DNA amplification for phylogenetic study". Journal of Bacteriology. 173 (2): 697–703. doi:10.1128/jb.173.2.697-703.1991. PMC 207061. PMID 1987160.
- ↑ 3.0 3.1 3.2 Richard GF, Kerrest A, Dujon B (December 2008). "Comparative genomics and molecular dynamics of DNA repeats in eukaryotes". Microbiology and Molecular Biology Reviews. 72 (4): 686–727. doi:10.1128/MMBR.00011-08. PMC 2593564. PMID 19052325.
- ↑ 4.0 4.1 Päques F, Samson ML, Jordan P, Wegnez M (November 1995). "Structural evolution of the Drosophila 5S ribosomal genes". Journal of Molecular Evolution. 41 (5): 615–21. Bibcode:1995JMolE..41..615P. doi:10.1007/bf00175820. PMID 7490776.
- ↑ Sumida M, Kato Y, Kurabayashi A (April 2004). "Sequencing and analysis of the internal transcribed spacers (ITSs) and coding regions in the EcoR I fragment of the ribosomal DNA of the Japanese pond frog Rana nigromaculata". Genes & Genetic Systems. 79 (2): 105–18. doi:10.1266/ggs.79.105. PMID 15215676.
- ↑ Nazar RN, Sitz TO, Busch H (February 1976). "Sequence homologies in mammalian 5.8S ribosomal RNA". Biochemistry. 15 (3): 505–8. doi:10.1021/bi00648a008. PMID 1252408.
- ↑ Fengyi MY, Jiannong X, Zheming Z (1998). "Sequence differences of rDNA-ITS2 and species-diagnostic PCR assay of Anopheles sinensis and Anopheles anthropophagus from China" (PDF). J Med Coll PLA. 13: 123–128.
- ↑ Li, C; Lee, JS; Groebner, JL; Kim, HC; Klein, TA; O'Guinn, ML; Wilkerson, RC (2005). "A newly recognized species in the Anopheles hyrcanus group and molecular identification of related species from the Republic of South Korea (Diptera: Culicidae)" (PDF). Zootaxa. 939: 1–8. doi:10.11646/zootaxa.939.1.1. Archived from the original on October 1, 2012.
- ↑ Hillis DM, Dixon MT (December 1991). "Ribosomal DNA: molecular evolution and phylogenetic inference". The Quarterly Review of Biology. 66 (4): 411–53. doi:10.1086/417338. PMID 1784710.
- ↑ Keil RL, Roeder GS (December 1984). "Cis-acting, recombination-stimulating activity in a fragment of the ribosomal DNA of S. cerevisiae". Cell. 39 (2 Pt 1): 377–86. doi:10.1016/0092-8674(84)90016-3. PMID 6094015.
- ↑ Serizawa N, Horiuchi T, Kobayashi T (April 2004). "Transcription-mediated hyper-recombination in HOT1". Genes to Cells. 9 (4): 305–15. doi:10.1111/j.1356-9597.2004.00729.x. PMID 15066122.
- ↑ Warmerdam DO, Wolthuis RM (March 2019). "Keeping ribosomal DNA intact: a repeating challenge". Chromosome Research. 27 (1–2): 57–72. doi:10.1007/s10577-018-9594-z. PMC 6394564. PMID 30556094.
