यूक्रोमैटिन
यूक्रोमैटिन (जिसे "ओपन क्रोमैटिन" भी कहा जाता है) क्रोमेटिन (डीएनए, आरएनए और प्रोटीन) का हल्का पैक रूप है जो जीन में समृद्ध होता है, और सक्रिय प्रतिलेखन (आनुवांशिकी) के अनुसार अधिकांश (लेकिन सदैव नहीं) होता है। यूक्रोमैटिन हेट्रोक्रोमैटिन के विपरीत खड़ा है, जो कसकर पैक किया गया है और प्रतिलेखन के लिए कम सुलभ है। मानव जीनोम का 92% यूक्रोमैटिक है।[1]
यूकेरियोट् में, यूक्रोमैटिन में कोशिका नाभिक के अंदर जीनोम का सबसे सक्रिय भाग होता है। प्रोकैर्योसाइटों में, यूक्रोमैटिन उपस्थित क्रोमैटिन का एकमात्र रूप है; यह इंगित करता है कि हेटरोक्रोमैटिन संरचना कोशिका नाभिक के साथ बाद में विकसित हुई, संभवतः जीनोम के बढ़ते आकार को संभालने के लिए तंत्र के रूप में इंगित है।
संरचना
यूक्रोमैटिन न्यूक्लियोसोम के रूप में जानी जाने वाली दोहराई जाने वाली सबयूनिट से बना होता है, जो स्ट्रिंग पर मोतियों के खुले हुए सेट की याद दिलाता है, जो लगभग 11 nm व्यास का होता है।[2] इन न्यूक्लियोसोम के मूल में चार हिस्टोन प्रोटीन जोड़े का एक सेट होता है: मैं इंतजार करूंगा, हिस्टोन एच4, हिस्टोन H2A, और हिस्टोन H2B[2]प्रत्येक कोर हिस्टोन प्रोटीन में एक 'पूंछ' संरचना होती है, जो कई तरीकों से भिन्न हो सकती है; ऐसा माना जाता है कि ये विविधताएं विभिन्न मेथिलिकरण और एसिटिलिकेशन राज्यों के माध्यम से मास्टर कंट्रोल स्विच के रूप में कार्य करती हैं, जो क्रोमेटिन की समग्र व्यवस्था को निर्धारित करती हैं।[2]डीएनए के लगभग 147 आधार जोड़े हिस्टोन ऑक्टामर्स के चारों ओर लपेटे जाते हैं, या हेलिक्स के 2 घुमावों से थोड़ा कम होते हैं।[3] इन न्यूक्लियोसोम के मूल में चार हिस्टोन प्रोटीन जोड़े का सेट होता है: H3, H4, H2A, और H2B। प्रत्येक कोर हिस्टोन प्रोटीन में 'पूंछ' संरचना होती है, जो कई विधियों से भिन्न हो सकती है; ऐसा माना जाता है कि ये विविधताएं विभिन्न मेथिलिकरण और एसिटिलीकरण अवस्थाओं के माध्यम से "मास्टर कंट्रोल स्विच" के रूप में कार्य करती हैं, जो क्रोमैटिन की समग्र व्यवस्था को निर्धारित करती हैं। डीएनए के लगभग 147 आधार जोड़े हिस्टोन ऑक्टामर्स के चारों ओर लपेटे जाते हैं, या हेलिक्स के 2 घुमावों से थोड़ा कम होते हैं। स्ट्रैंड के साथ न्यूक्लियोसोम हिस्टोन, हिस्टोन H1 और खुले लिंकर डीएनए की छोटी जगह के माध्यम से लगभग 0-80 बेस पेयर से लेकर एक साथ जुड़े हुए हैं।[4] यूक्रोमैटिन और हेटरोक्रोमैटिन की संरचना के बीच मुख्य अंतर यह है कि यूक्रोमैटिन में न्यूक्लियोसोम बहुत अधिक व्यापक रूप से फैले हुए हैं, जो डीएनए स्ट्रैंड में विभिन्न प्रोटीन परिसरों की आसान पहुंच की अनुमति देता है और इस प्रकार जीन प्रतिलेखन में वृद्धि करता है।[2]
उपस्थिति
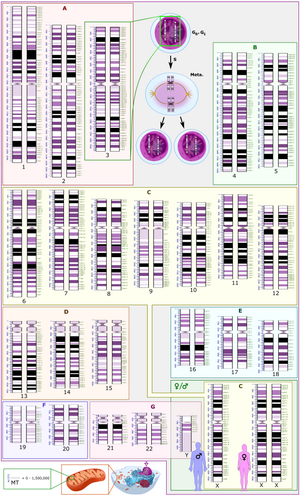
यूक्रोमैटिन बड़े आवर्धन पर स्ट्रिंग पर मोतियों के सेट जैसा दिखता है।[2]दूर से, यह उलझे हुए धागे की गेंद जैसा हो सकता है, जैसे कि कुछ सूक्ष्मछवि विज़ुअलाइज़ेशन में।[5] ऑप्टिकल और इलेक्ट्रॉन माइक्रोस्कोपिक विज़ुअलाइज़ेशन दोनों में, यूक्रोमैटिन हेटरोक्रोमैटिन की तुलना में कम सघन संरचना के कारण रंग में हल्का दिखाई देता है - जो कोशिका न्यूक्लियस में भी उपस्थित होता है और गहरा दिखाई देता है।[6][5] गुणसूत्रों की कल्पना करते समय, जैसे कि कार्यग्राम में, गुणसूत्रों को दागने के लिए साइटोजेनेटिक बैंडिंग का उपयोग किया जाता है। साइटोजेनेटिक बैंडिंग हमें यह देखने की अनुमति देती है कि क्रोमोसोमल उपखंडों, अनियमितताओं या पुनर्व्यवस्थाओं को अलग करने के लिए क्रोमोसोम के कौन से हिस्से यूक्रोमैटिन या हेटरोक्रोमैटिन से बने होते हैं।[7] ऐसा ही एक उदाहरण G बैंडिंग है, अन्यथा गिमेसा स्टेनिंग के रूप में जाना जाता है जहां यूक्रोमैटिन हेटरोक्रोमैटिन से हल्का दिखाई देता है।[8]
| गिमेसा (G-) बैंडिंग | उत्क्रम (R-) बैंडिंग | संवैधानिक हेटेरोक्रोमैटिन(C-) बैंडिंग | क्विनाक्राइन (Q-) बैंडिंग | टेलोमेरिक आर (T-) बैंडिंग | |
|---|---|---|---|---|---|
| यूक्रोमैटिन | हल्का | गहरा | हल्का | उदासीन | हल्का |
| हेट्रोक्रोमैटिन | गहरा | हल्का | गहरा | उज्ज्वल (फ्लोरोसेंट) | गहरा (बेहोश) |
कार्य
प्रतिलेखन
यूक्रोमैटिन डीएनए से एमआरएनए उत्पादों के सक्रिय प्रतिलेखन में भाग लेता है। प्रकट संरचना जीन विनियामक प्रोटीन और आरएनए पोलीमरेज़ कॉम्प्लेक्स को डीएनए अनुक्रम से बाँधने की अनुमति देती है, जो तब प्रतिलेखन प्रक्रिया प्रारंभ कर सकती है।[2] जबकि सभी यूक्रोमैटिन आवश्यक रूप से लिखित नहीं हैं, क्योंकि यूक्रोमैटिन को प्रतिलेखनल रूप से सक्रिय और निष्क्रिय डोमेन में विभाजित किया गया है,[13] यूक्रोमैटिन अभी भी सामान्यतः सक्रिय जीन प्रतिलेखन से जुड़ा हुआ है। इसलिए कोशिका कितनी सक्रिय रूप से उत्पादक है और इसके नाभिक में पाए जाने वाले यूक्रोमैटिन की मात्रा का सीधा संबंध है।
ऐसा माना जाता है कि कोशिका जीन अभिव्यक्ति और डीएनए प्रतिकृति को नियंत्रित करने की विधि के रूप में यूक्रोमैटिन से हेटरोक्रोमैटिन में परिवर्तन का उपयोग करती है, क्योंकि ऐसी प्रक्रियाएं घनी सघन क्रोमैटिन पर अलग-अलग व्यवहार करती हैं। इसे 'अभिगम्यता परिकल्पना' के रूप में जाना जाता है।[14] संवैधानिक यूक्रोमैटिन का एक उदाहरण जो 'सदैव प्रारंभ रहता है' हाउसकीपिंग जीन है, जो कोशिका अस्तित्व के मूलभूत कार्यों के लिए आवश्यक प्रोटीन के लिए कोड है।[15]
एपिजेनेटिक्स
एपिजेनेटिक्स में फेनोटाइप में परिवर्तन सम्मिलित हैं जिन्हें डीएनए अनुक्रम को बदले बिना विरासत में प्राप्त किया जा सकता है। यह कई प्रकार की पर्यावरणीय अंतःक्रियाओं के माध्यम से हो सकता है।[16] यूक्रोमैटिन के संबंध में, हिस्टोन के पोस्ट-ट्रांसलेशन संबंधी संशोधन क्रोमेटिन की संरचना को बदल सकते हैं, जिसके परिणामस्वरूप डीएनए को बदले बिना जीन की अभिव्यक्ति बदल जाती है।[17] इसके अतिरिक्त, हेटरोक्रोमैटिन की हानि और यूक्रोमैटिन में वृद्धि को त्वरित उम्र बढ़ने की प्रक्रिया के साथ सहसंबद्ध दिखाया गया है, विशेष रूप से उन रोगों में जिन्हें समय से पहले बूढ़ा होने के लिए जाना जाता है।[18] अनुसंधान ने कई अतिरिक्त रोगों के लिए हिस्टोन पर एपिजेनेटिक मार्कर दिखाए हैं।[19][20]
विनियमन
यूक्रोमैटिन मुख्य रूप से कई हिस्टोन-संशोधित एंजाइमों द्वारा संचालित अपने न्यूक्लियोसोम के हिस्टोन्स में अनुवाद के बाद के संशोधन द्वारा नियंत्रित किया जाता है। ये संशोधन हिस्टोन के N- टर्मिनस "पूंछ" पर होते हैं जो न्यूक्लियोसोम संरचना से फैलते हैं, और क्रोमैटिन को अपने खुले रूप में, यूक्रोमैटिन के रूप में, या इसके बंद रूप में, हेटरोक्रोमैटिन के रूप में रखने के लिए एंजाइमों की भर्ती करने के बारे में सोचा जाता है।Cite error: Closing </ref> missing for <ref> tag
- Epigenetic inheritance and the missing heritability – Trerotola M, Relli V, Simeone P, Alberti S (July 2015). "Epigenetic inheritance and the missing heritability". Human Genomics. 9 (1): 17. doi:10.1186/s40246-015-0041-3. PMC 4517414. PMID 26216216.</ref>
- Histone epigenetic marks in heterochromatin and euchromatin of the Chagas' disease vector, Triatoma infestans – Alvarenga EM, Rodrigues VL, Moraes AS, Naves LS, Mondin M, Felisbino MB, Mello ML (May 2016). "Histone epigenetic marks in heterochromatin and euchromatin of the Chagas' disease vector, Triatoma infestans". Acta Histochemica. 118 (4): 401–412. doi:10.1016/j.acthis.2016.04.002. PMID 27079857.
- ↑ International Human Genome Sequencing Consortium (October 2004). "Finishing the euchromatic sequence of the human genome". Nature. 431 (7011): 931–945. Bibcode:2004Natur.431..931H. doi:10.1038/nature03001. PMID 15496913. S2CID 186242248.
{{cite journal}}: CS1 maint: uses authors parameter (link) - ↑ 2.0 2.1 2.2 2.3 2.4 2.5 2.6 Babu A, Verma RS (January 1987). Bourne GH, Jeon KW, Friedlander M (eds.). "गुणसूत्र संरचना: यूक्रोमैटिन और हेटरोक्रोमैटिन". International Review of Cytology. Academic Press. 108: 1–60. doi:10.1016/s0074-7696(08)61435-7. ISBN 9780123645081. PMID 2822591.
- ↑ "Definition: nucleosome/nucleosomes". Scitable Nature Education (in English). Retrieved 2021-10-06.
- ↑ Mobley AS (January 2019). "Chapter 4 - Induced Pluripotent Stem Cells". In Mobley AS (ed.). Neural Stem Cells and Adult Neurogenesis (in English). Academic Press. pp. 67–94. ISBN 978-0-12-811014-0.
- ↑ 5.0 5.1 "The cell. 4. Nucleus. Chromatin. Atlas of plant and animal histology". mmegias.webs.uvigo.es. Retrieved 2021-12-02.
- ↑ Enukashvily NI (January 2013). "Chapter Two - Mammalian Satellite DNA: A Speaking Dumb". In Donev R, Ponomartsev NV (eds.). Advances in Protein Chemistry and Structural Biology. Organisation of Chromosomes (in English). Vol. 90. Academic Press. pp. 31–65. doi:10.1016/B978-0-12-410523-2.00002-X. ISBN 9780124105232. PMID 23582201.
- ↑ Shen CH (January 2019). "Chapter 13 - Molecular Diagnosis of Chromosomal Disorders". In Shen CH (ed.). Diagnostic Molecular Biology (in English). Academic Press. pp. 331–358. doi:10.1016/B978-0-12-802823-0.00013-4. ISBN 978-0-12-802823-0. S2CID 131915096.
- ↑ 8.0 8.1 "Giemsa banding". Biology Articles, Tutorials & Dictionary Online (in English). 2019-10-07. Retrieved 2021-12-02.
- ↑ "Reverse banding - Definition and Examples - Biology Online Dictionary". Biology Articles, Tutorials & Dictionary Online (in English). 2020-09-18. Retrieved 2021-12-02.
- ↑ "Constitutive heterochromatin banding". Biology Articles, Tutorials & Dictionary Online (in English). 2019-10-07. Retrieved 2021-12-02.
- ↑ "Quinacrine banding". Biology Articles, Tutorials & Dictionary Online (in English). 2019-10-07. Retrieved 2021-12-02.
- ↑ "T-banding". Biology Articles, Tutorials & Dictionary Online (in English). 2019-10-07. Retrieved 2021-12-02.
- ↑ Verschure PJ, van Der Kraan I, Manders EM, van Driel R (October 1999). "Spatial relationship between transcription sites and chromosome territories". The Journal of Cell Biology. 147 (1): 13–24. doi:10.1083/jcb.147.1.13. PMC 2164981. PMID 10508851.
- ↑ Muegge K (2003-04-01). "Modifications of histone cores and tails in V(D)J recombination". Genome Biology. 4 (4): 211. doi:10.1186/gb-2003-4-4-211. PMC 154571. PMID 12702201.
- ↑ Eisenberg E, Levanon EY (October 2013). "Human housekeeping genes, revisited". Trends in Genetics (in English). 29 (10): 569–574. doi:10.1016/j.tig.2013.05.010. PMID 23810203.
- ↑ Arney KL, Fisher AG (September 2004). "Epigenetic aspects of differentiation". Journal of Cell Science. 117 (Pt 19): 4355–4363. doi:10.1242/jcs.01390. PMID 15331660. S2CID 24376600.
- ↑ Singh NP, Madabhushi SR, Srivastava S, Senthilkumar R, Neeraja C, Khosla S, Mishra RK (May 2011). "Epigenetic profile of the euchromatic region of human Y chromosome". Nucleic Acids Research. 39 (9): 3594–3606. doi:10.1093/nar/gkq1342. PMC 3089472. PMID 21252296.
- ↑ Wang J, Jia ST, Jia S (May 2016). "New Insights into the Regulation of Heterochromatin". Trends in Genetics. 32 (5): 284–294. doi:10.1016/j.tig.2016.02.005. PMC 4842111. PMID 27005444.
- ↑ Simmons D (2008). "Epigenetic Influences and Disease". Nature Education. 1 (1): 6. Retrieved 2021-12-02.
- ↑ Alaskhar Alhamwe B, Khalaila R, Wolf J, von Bülow V, Harb H, Alhamdan F, et al. (2018-05-23). "Histone modifications and their role in epigenetics of atopy and allergic diseases". Allergy, Asthma, and Clinical Immunology. 14 (1): 39. doi:10.1186/s13223-018-0259-4. PMC 5966915. PMID 29796022.
