ऑर्थोसिलिकेट
रसायन शास्त्र में, ऑर्थोसिलिकेट आयन है SiO4−
4, या इसका कोई भी नमक (रसायन विज्ञान) और एस्टर। यह सिलिकेट आयनों में से एक है। इसे कभी-कभी सिलिकॉन टेट्रोक्साइड आयन या मोइटी (रसायन विज्ञान) कहा जाता है।[1]
ऑर्थोसिलिकेट लवण, जैसे सोडियम ऑर्थोसिलिकेट, स्थिर होते हैं, और प्रकृति में व्यापक रूप से सिलिकेट खनिजों के रूप में पाए जाते हैं, जो सिलिकेट खनिजों #Nesosilicates या orthosilicates की परिभाषित विशेषता है।[2] ओलीवाइन, एक मैग्नीशियम या आयरन (II) ऑर्थोसिलिकेट, ऊपरी मेंटल (पृथ्वी) में सबसे प्रचुर मात्रा में खनिज है।
ऑर्थोसिलिकेट आयन एक मजबूत आधार (रसायन) है, अत्यंत कमजोर सिलिकिक एसिड का संयुग्म आधार H
4SiO
4 (पकa2 = 13.2 25 डिग्री सेल्सियस पर)। इस संतुलन का अध्ययन करना मुश्किल है क्योंकि एसिड एक जलमिश्रित पत्थर कंडेनसेट में विघटित हो जाता है।[3]
संरचना
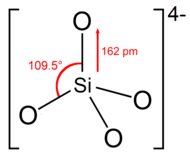
ऑर्थोसिलिकेट आयन या समूह में चतुर्पाश्वीय आकार होता है, जिसमें एक सिलिकॉन परमाणु चार ऑक्सीजन परमाणुओं से घिरा होता है।
आयनों में, प्रत्येक ऑक्सीजन में एक इकाई ऋणात्मक आवेश होता है।[4] Si–O बॉन्ड 162 pm लंबा है।[5] टेट्रामेथिल ऑर्थोसिलिकेट जैसे कार्बनिक यौगिकों में, प्रत्येक ऑक्सीजन औपचारिक रूप से तटस्थ होता है और शेष अणु से एक सहसंयोजक बंधन से जुड़ा होता है।
उपयोग करता है
यूरोपियम डोप्ड बेरियम ऑर्थोसिलिकेट (बीए2यह4) हरे प्रकाश उत्सर्जक डायोड (एलईडी) में इस्तेमाल होने वाला एक सामान्य भास्वर है। ब्लू एल ई डी के लिए फॉस्फर स्ट्रोंटियम डोप्ड बेरियम ऑर्थोसिलिकेट के साथ बनाया जा सकता है।[6] बेरियम ऑर्थोसिलिकेट वेक्यूम - ट्यूब ों में कैथोड विषाक्तता का एक प्रमुख कारण है।[7]
कार्बनिक रसायन
हालांकि अकार्बनिक रसायन विज्ञान और भू-रसायन में बहुत महत्वपूर्ण है, कार्बनिक रसायन विज्ञान में ऑर्थोसिलिकेट आयन शायद ही कभी देखा जाता है। हालाँकि, दो सिलिकेट यौगिकों का उपयोग कार्बनिक संश्लेषण में किया जाता है: टेट्राएथिल ओर्थोसिलिकेट या TEOS का उपयोग पॉलिमर को जोड़ने के लिए किया जाता है, और विशेष रूप से एरोगल्स के निर्माण में महत्वपूर्ण है। Tetramethyl orthosilicate या TMOS का उपयोग TEOS के विकल्प के रूप में किया जाता है, और इसमें अभिकर्मक के रूप में कई अन्य उपयोग भी होते हैं। टीईओएस को टीएमओएस से अधिक पसंद किया जाता है क्योंकि टीएमओएस जहरीले मेथनॉल की उच्च सांद्रता का उत्पादन करने के लिए विघटित होता है। टीएमओएस को सूंघने से फेफड़ों में सिलिका का विषैला निर्माण हो सकता है।
संदर्भ
- ↑ C. A. Kumins, and A. E. Gessler (1953), "Short-Cycle Syntheses of Ultramarine Blue". Indunstrial & Engineering Chemistry, volume 45, issue 3, pages 567–572. doi:10.1021/ie50519a031
- ↑ Western Oregon University
- ↑ Jurkić, Lela Munjas; Cepanec, Ivica; Pavelić, Sandra Kraljević; Pavelić, Krešimir (2013). "ऑर्थो-सिलिकिक एसिड और कुछ ऑर्थो-सिलिकिक एसिड-रिलीजिंग यौगिकों के जैविक और चिकित्सीय प्रभाव: चिकित्सा के लिए नए दृष्टिकोण". Nutrition & Metabolism. 10 (1): 2. doi:10.1186/1743-7075-10-2. ISSN 1743-7075. PMC 3546016.
- ↑ Balaram Sahoo; Nayak Nimai Charan; Samantaray Asutosh; Pujapanda Prafulla Kumar. अकार्बनिक रसायन शास्त्र. PHI Learning Pvt. Ltd. p. 306. ISBN 978-81-203-4308-5.
- ↑ Horacio E. Bergna; William O. Roberts (19 December 2005). Colloidal Silica: Fundamentals and Applications. CRC Press. p. 10. ISBN 978-1-4200-2870-6.
- ↑ Huayna Cerqueira Streit, Jennifer Kramer, Markus Suta, Claudia Wickleder, "Red, green, and blue photoluminescence of Ba₂SiO4:M (M = Eu3+, Eu2+, Sr2+) nanophosphors", Materials (Basel), vol. 6, iss. 8, pp. 3079–3093, 24 July 2013 doi:10.3390/ma6083079.
- ↑ Jones, Morgan (Electronics engineer) (2011). वाल्व एम्पलीफायरों (4th ed.). Oxford: Newnes. p. 301. ISBN 978-0-08-096640-3. OCLC 760157359.