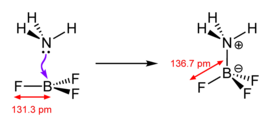लुईस अम्ल और क्षार
एक लुईस अम्ल (अमेरिकी भौतिक रसायनज्ञ गिल्बर्ट एन लुईस के नाम पर रखा गया है) एक रासायनिक प्रजाति है, जिसमें एक खाली कक्षा होती है जो एक लुईस क्षार से एक इलेक्ट्रॉन जोड़ी को स्वीकार करने में सक्षम होती है ताकि लुईस योगोत्पाद बनाया जा सके। एक लुईस क्षार, फिर, कोई भी प्रजाति है जिसमें एक इलेक्ट्रॉन जोड़ी युक्त एक भरी हुआ कक्षा होती है जो सहसंयोजक बंध में सम्मिलित नहीं होती है लेकिन एक लुईस अम्ल के साथ एक दाता बंध बना सकती है। उदाहरण के लिए, अमोनिया NH3लुईस क्षार है, क्योंकि यह इलेक्ट्रॉनों की एक जोड़ी दान कर सकता है। ट्राइमिथाइलबोरेन (Me3B) एक लुईस अम्ल है क्योंकि यह एक जोड़ी इलेक्ट्रॉन को स्वीकार करने में सक्षम है। एक लुईस जोड़े में, लुईस अम्ल और क्षार एक इलेक्ट्रॉन जोड़ी साझा करते हैं जो लुईस क्षार द्वारा प्रस्तुत किया जाता है, जो एक दाता बंध बनाता है।[1] NH3 और Me3B के बीच एक विशिष्ट रासायनिक अभिक्रिया के संदर्भ में NH3 से एक अकेली जोड़ी Me3B के खाली कक्षीय के साथ एक यौगिक NH3•BMe3 बनाने के लिए एक दाता बंध बनाएगी।यह शब्दावली गिल्बर्ट एन लुईस के योगदान को संदर्भित करती है।[2] न्यूक्लियोफाइल और इलेक्ट्रोफाइल शब्द क्रमशः लुईस क्षार और लुईस अम्ल के साथ विनिमेय हैं। सामान्यता, ये शब्द, विशेष रूप से उनके अमूर्त संज्ञा न्यूक्लियोफिलिसिटी और इलेक्ट्रोफिलिसिटी बनाते हैं, अभिक्रियाशीलता के गतिज ऊर्जा पहलू पर जोर देते हैं, जबकि लुईस क्षारता और लुईस अम्लता,लुईस व्यसन के ऊष्मागतिकी पहलू पर जोर देते हैं
व्यसनों का चित्रण
कई मामलों में, एक जटिल में लुईस क्षार और लुईस अम्ल के बीच की बातचीत को एक तीर द्वारा इंगित किया जाता है जो लुईस क्षार के इलेक्ट्रॉनों को लुईस अम्ल की ओर एक दाता बंध के चिन्हांकन का उपयोग करते हुए दर्शाता है - उदाहरण के लिए, Me3B←NH3. कुछ स्रोत लुईस क्षार को बिन्दुओ की एक जोड़ी (स्पष्ट इलेक्ट्रॉनों का दान किया जा रहा है) के साथ इंगित करते हैं, जो क्षार से ही अम्ल के साथ जटिल में संक्रमण के लगातार प्रतिनिधित्व की अनुमति देता है:
- Me3B + :NH3 → Me3B:NH3
लुईस व्यसन का प्रतिनिधित्व करने के लिए एक केंद्र बिंदु का भी उपयोग किया जा सकता है, जैसे Me3B·NH3. एक अन्य उदाहरण बोरोन ट्राइफ्लोराइड डायथाइल ईथेरेट है, BF3·Et2O. थोड़ा अलग उपयोग में, केंद्र बिंदु का उपयोग विभिन्न क्रिस्टल में क्रिस्टलीकरण के पानी का प्रतिनिधित्व करने के लिए भी किया जाता है, जैसे कि MgSO4·7H2O : जलयोजित मैग्नीशियम सल्फेट के लिए, भले ही पानी धातु के साथ एक दाता बंध बनाता हो।
यद्यपि गैर-दाता सहसंयोजक बंधों से दाता बंध को अलग करने के लिए संगणनात्मक, और प्रायोगिक ऊर्जावान मानदंड का उपयोग करने का प्रयास किया गया है,[3] अधिकांश भाग के लिए,मुख्यता केवल इलेक्ट्रॉन जोड़ी के स्रोत पर ध्यान देता है, और दाता बंध एक बार बनने के बाद अन्य सहसंयोजक बन्धो के रूप में व्यवहार करते हैं,सामान्यता उनके पास पर काफी ध्रुवीय चरित्र होता है। इसके अलावा, कुछ मामलों में (जैसे, सल्फॉक्साइड्स और अमीन ऑक्साइड्स R2S → O और R3N → O), औपचारिक शुल्कों के आरेखण से बचने के लिए दाता बंध तीर का उपयोग सिर्फ एक सांकेतिक सुविधा है। सामान्य तौर पर,यद्पि, दाता-स्वीकर्ता बंधन को आदर्श सहसंयोजक बंधन और आयनिक बंधन के बीच एक निरंतरता के रूप में देखा जाता है।[4]
लुईस अम्ल
लुईस अम्ल विविध हैं और इस शब्द का प्रयोग शिथिल रूप से किया जाता है। सबसे सरल वे हैं जो लुईस क्षार के साथ सीधे अभिक्रिया करते हैं, जैसे कि बोरॉन ट्राइहैलाइड्स और फॉस्फोरस, आर्सेनिक और एंटीमनी के पेंटाहैलाइड्स।
इसी क्रम में CH3+ को मेथिलिकरण अभिक्रियाओं में लुईस अम्ल माना जा सकता है। तथापि, संघनित चरण में मिथाइल धनायन कभी भी एक मुक्त प्रजाति के रूप में नहीं होता है, और CH3I जैसे अभिकर्मकों द्वारा मेथिलिकरण अभिक्रियाएं 3 नाभिकरागी से कार्बन तक एक बंधन के एक साथ गठन के माध्यम से और कार्बन और आयोडीन के बीच बंधन की विदलन (SN2 प्रतिक्रिया) से होती है। पाठ्यपुस्तकें इस बिंदु पर असहमत हैं: कुछ का कहना है कि एल्काइल हलाइड्स इलेक्ट्रॉनरागी हैं लेकिन लुईस अम्ल नहीं हैं,[5] जबकि अन्य अल्काइल हलाइड्स का वर्णन करते हैं (उदाहरण के लिए CH3Br) लुईस अम्ल के एक प्रकार के रूप में।[6] IUPAC गोल्ड बुक में कहा गया है कि लुईस अम्ल और लुईस क्षार अभिक्रिया करके लुईस व्यसन बनाते हैं,[1]और इलेक्ट्रॉनरागी को लुईस अम्ल के रूप में परिभाषित करते है।[7]
सरल लुईस अम्ल
इस तरह के लुईस अम्ल के कुछ सबसे अधिक अध्ययन किए गए उदाहरण बोरॉन ट्राइहैलाइड्स और ओर्गेनोबोरेनस हैं:[8]
- BF3 + F− → BF4−
इस जोड़ में, सभी चार फ्लोराइड केंद्र (या अधिक सटीक रूप से, लिगेंड) समतुल्य हैं।
- BF3 + OMe2 → BF3OMe2
दोनों BF4− और BF3OMe2 बोरॉन ट्राइफ्लोराइड के लुईस क्षार व्यसन हैं।
कई व्यसन ऑक्टेट नियम का उल्लंघन करते हैं, जैसे ट्रायोड्स का ऋणायन
- I2 + I− → I3−
आयोडीन विलयन,के रंगों की परिवर्तनशीलता लुईस अम्ल I2के साथ व्यसनों को बनाने के लिए विलायक की परिवर्तनशील क्षमताओं को दर्शाती है.
कुछ लुईस अम्ल दो लुईस क्षारों को बांधते हैं, एक प्रसिद्ध उदाहरण hexafluorosilicate का निर्माण होता है:
- सिफ4 + 2 एफ− → SiF62−
जटिल लुईस अम्ल
लुईस अम्ल माने जाने वाले अधिकांश यौगिकों को लुईस क्षार के साथ जोड़ के गठन से पहले एक सक्रियण चरण की आवश्यकता होती है। एथिलेलुमिनियम सेस्क्यूक्लोराइड Et3Al2Cl3और एल्यूमीनियम क्लोराइड AlCl3 जैसे जटिल यौगिकों को ट्राइगोनल प्लानर लुईस अम्ल के रूप में माना जाता है ये लेकिन समुच्चय और बहुलक के रूप में मौजूद होते है जिसे लुईस क्षार द्वारा अवक्रमित किया जाना चाहिए।[9] एक सरल मामला बोरेन के व्यसनों का निर्माण है। मोनोमेरिक BH3 पर्याप्त रूप से मौजूद नहीं है, इसलिए डाईबोरेन के क्षरण से बोरेन के योग उत्पन्न होते हैं:
- B2H6 + 2 H− → 2 BH4−
इस मामले में, एक मध्यवर्ती B2H7− अलग किया जा सकता है।
कई धातु परिसर लुईस अम्ल के रूप में काम करते हैं, लेकिन आमतौर पर केवल अधिक कमजोर रूप से बंधे लुईस क्षार को अलग करने के बाद, अक्सर पानी।
- [Mg(H2O)6]2+ + 6 NH3 → [Mg(NH3)6]2+ + 6 H2O
H+ लुईस अम्ल के रूप में
प्रोटॉन (H+)[10]सबसे मजबूत में से एक है, लेकिन सबसे जटिल लुईस अम्ल में से भी एक है। इस तथ्य को अनदेखा करने के लिए चलन है कि एक प्रोटॉन भारी विलायक (विलायक के लिए बाध्य) है। इस सरलीकरण को ध्यान में रखते हुए, अम्ल-क्षार अभिक्रियाओं को व्यसनों के निर्माण के रूप में देखा जा सकता है
- H+ + NH3 → NH4+
- H+ + OH− → H2O
लुईस अम्ल के अनुप्रयोग
कार्रवाई में लुईस अम्ल का एक विशिष्ट उदाहरण फ्रीडेल-क्राफ्ट्स एल्केलाइजेशन रिएक्शन में है।[4]मुख्य कदम है AlCl3 द्वारा एक क्लोराइड आयन अयुग्मित युग्म की स्वीकृति जिससे AlCl4 का निर्माण होता है और अत्यधिक अम्लीय, यानी इलेक्ट्रोफिलिक, कार्बोनियम आयन का निर्माण होता है।
- RCl +AlCl3 → R+ + AlCl4−
लुईस क्षार
एक लुईस क्षार एक परमाणु या आणविक प्रजाति है जहां सबसे अधिक व्याप्त आणविक कक्षीय (HOMO) अत्यधिक स्थानीयकृत है। विशिष्ट लुईस क्षार अमोनिया और एल्काइल एमाइन जैसे पारंपरिक अमाइन हैं। अन्य आम लुईस क्षारों में पिरिडीन और इसके व्युत्पन्न शामिल हैं। लुईस क्षार के कुछ मुख्य वर्ग हैं
- सूत्र NH3 की अमीन्स NH3−xRx जहाँ R = ऐल्किल या ऐरिल। इनसे संबंधित पिरिडीन और इसके व्युत्पन्न हैं।
- फॉर्मूला पीआर के फॉस्फीन PR3−xAx, जहाँ R =एल्काइल, A= एरील।
- O, S, Se और Te के यौगिक ऑक्सीकरण अवस्था -2 में, जिनमें पानी, ईथर, कीटोन्स शामिल हैं
सबसे आम लुईस क्षार ऋणायन हैं। लुईस क्षारकता की ताकत मूल अम्ल pKa के साथ संबंध रखती है उच्च pKa अम्ल अच्छे लुईस क्षार देते हैं। हमेशा की तरह, एक कमजोर अम्ल का एक मजबूत संयुग्म क्षार होता है।
- इलेक्ट्रॉन जोड़ी दाता की सामान्य परिभाषा के क्षार पर लुईस क्षारों के उदाहरणों में शामिल हैं:
लुईस क्षार की ताकत का मूल्यांकन विभिन्न लुईस अम्ल के लिए किया गया है, जैसे I2, एसबीसीएल5, और बीएफ3.[11]
| Lewis base | Donor atom | Enthalpy of complexation (kJ/mol) |
|---|---|---|
| quinuclidine | N | 150 |
| Et3N | N | 135 |
| pyridine | N | 128 |
| Acetonitrile | N | 60 |
| DMA | O | 112 |
| DMSO | O | 105 |
| THF | O | 90.4 |
| Et2O | O | 78.8 |
| acetone | O | 76.0 |
| EtOAc | O | 75.5 |
| Trimethylphosphine | P | 97.3 |
| Tetrahydrothiophene | S | 51.6 |
लुईस क्षारों के अनुप्रयोग
लगभग सभी इलेक्ट्रॉन युग्म दाता जो बाध्यकारी संक्रमण तत्वों द्वारा यौगिकों का निर्माण करते हैं, उन्हें लुईस क्षार-या लिगैंड्स के संग्रह के रूप में देखा जा सकता है। इस प्रकार लुईस क्षार का एक बड़ा अनुप्रयोग धातु उत्प्रेरक की गतिविधि और चयनात्मकता को संशोधित करना है। चिराल लुईस क्षार इस प्रकार एक उत्प्रेरक पर चिरालिटी (रसायन विज्ञान) प्रदान करते हैं, असममित कटैलिसीस को सक्षम करते हैं, जो दवा्स के उत्पादन के लिए उपयोगी है।
कई लेविस क्षार मल्टीडेंटेट हैं, यानी वे लुईस अम्ल के लिए कई बंधन बना सकते हैं। इन बहुदंतुक लुईस क्षारों को कीलेटिंग एजेंट कहा जाता है।
हार्ड और सॉफ्ट वर्गीकरण
लुईस अम्ल और क्षार को आमतौर पर उनकी कठोरता या कोमलता के अनुसार वर्गीकृत किया जाता है। इस संदर्भ में कठिन का तात्पर्य छोटे और गैर-ध्रुवीय और नरम से है जो बड़े परमाणुओं को इंगित करता है जो अधिक ध्रुवीकरण योग्य हैं।
- ठेठ हार्ड अम्ल: एच+, क्षार/क्षारीय मृदा धातु धनायन, बोरेन, Zn2+
- ठेठ सॉफ्ट अम्ल: Ag+, मो(0), नी(0), पं2+
- विशिष्ट कठोर क्षार: अमोनिया और एमाइन, पानी, कार्बोक्सिलेट्स, फ्लोराइड और क्लोराइड
- ठेठ नरम क्षार: ऑर्गनोफॉस्फिन्स, थियोईथर, कार्बन मोनोऑक्साइड, आयोडाइड
उदाहरण के लिए, एक अमाइन अम्ल बीएफ के साथ फॉस्फीन को एडिक्ट से विस्थापित कर देगा3. इसी प्रकार क्षारों का वर्गीकरण किया जा सकता है। उदाहरण के लिए, ऑक्सीजन परमाणु से एक अकेला जोड़ा दान करने वाले क्षार नाइट्रोजन परमाणु के माध्यम से दान करने वाले क्षारों की तुलना में कठिन होते हैं। हालांकि वर्गीकरण को कभी भी परिमाणित नहीं किया गया था, यह प्रमुख अवधारणाओं का उपयोग करते हुए, कठोर अम्ल-हार्ड क्षार और सॉफ्ट अम्ल-सॉफ्ट क्षार इंटरैक्शन हार्ड अम्ल-सॉफ्ट क्षार या सॉफ्ट अम्ल-हार्ड से अधिक मजबूत होते हैं, यह व्यसन गठन की ताकत का अनुमान लगाने में बहुत उपयोगी साबित हुआ। क्षार इंटरैक्शन। बाद में बातचीत के ऊष्मप्रवैगिकी की जांच ने सुझाव दिया कि कठिन-कठोर अंतःक्रियाएं उत्साहजनक हैं, जबकि नरम-मुलायम एन्ट्रापी के पक्षधर हैं।
लुईस अम्लता की मात्रा निर्धारित करना
लुईस अम्लता का मूल्यांकन और भविष्यवाणी करने के लिए कई तरीके तैयार किए गए हैं। कई स्पेक्ट्रोस्कोपिक हस्ताक्षरों पर क्षारित होते हैं जैसे शिफ्ट एनएमआर सिग्नल या आईआर बैंड उदा। गुटमैन-बेकेट विधि और चिल्ड्स[12] तरीका।
ECW मॉडल एक मात्रात्मक मॉडल है जो लुईस अम्ल क्षार इंटरैक्शन -ΔH की ताकत का वर्णन और भविष्यवाणी करता है। मॉडल ने कई लुईस अम्ल और क्षार को ई और सी पैरामीटर दिए। प्रत्येक अम्ल की विशेषता एक ई हैA और एक सीA. इसी तरह प्रत्येक क्षार की अपनी ई द्वारा विशेषता हैB और सीB. ई और सी पैरामीटर क्रमशः इलेक्ट्रोस्टैटिक और सहसंयोजक योगदान को संदर्भित करते हैं जो बांड की ताकत में अम्ल और क्षार बनेंगे। समीकरण है
- −ΔH = ईAEB + सीACB + डब्ल्यू
डब्ल्यू टर्म अम्ल-क्षार रिएक्शन के लिए निरंतर ऊर्जा योगदान का प्रतिनिधित्व करता है जैसे डिमेरिक अम्ल या क्षार की दरार। समीकरण अम्ल और क्षार स्ट्रेंथ के उलट होने की भविष्यवाणी करता है। समीकरण की चित्रमय प्रस्तुतियों से पता चलता है कि लुईस क्षार स्ट्रेंथ या लुईस अम्ल स्ट्रेंथ का एक ही क्रम नहीं है।[13][14] और वह एकल संपत्ति पैमाने अम्ल या क्षार की एक छोटी श्रेणी तक सीमित हैं।
इतिहास

अवधारणा की उत्पत्ति गिल्बर्ट एन. लुईस से हुई जिन्होंने रासायनिक बंधन का अध्ययन किया। 1923 में, लुईस ने लिखा था कि एक अम्ल पदार्थ वह है जो अपने स्वयं के परमाणुओं में से एक के स्थिर समूह को पूरा करने के लिए दूसरे अणु से एक इलेक्ट्रॉन अकेला जोड़ा नियोजित कर सकता है।[2]Cite error: Closing </ref> missing for <ref> tag जब प्रत्येक परमाणु ने बंधन में एक इलेक्ट्रॉन का योगदान दिया, तो इसे सहसंयोजक बंधन कहा जाता था। जब दोनों इलेक्ट्रॉन एक परमाणु से आते हैं, तो इसे मूल सहसंयोजक बंधन या समन्वय बंधन कहा जाता है। भेद बहुत स्पष्ट नहीं है। उदाहरण के लिए, अमोनिया और हाइड्रोजन से अमोनियम आयन के निर्माण में अमोनिया अणु हाइड्रोन (रसायन) को इलेक्ट्रॉनों की एक जोड़ी दान करता है;[10] बनने वाले अमोनियम आयन में इलेक्ट्रॉनों की पहचान खो जाती है। फिर भी, लुईस ने सुझाव दिया कि एक इलेक्ट्रॉन-जोड़ी दाता को क्षार के रूप में वर्गीकृत किया जाना चाहिए और एक इलेक्ट्रॉन-जोड़ी स्वीकर्ता को अम्ल के रूप में वर्गीकृत किया जाना चाहिए।
लुईस अम्ल की एक और अधिक आधुनिक परिभाषा एक परमाणु या आणविक प्रजाति है जो कम ऊर्जा के स्थानीय खाली परमाणु कक्षीय या आणविक कक्षीय कक्षीय है। यह निम्नतम-ऊर्जा आणविक कक्षीय (LUMO) इलेक्ट्रॉनों की एक जोड़ी को समायोजित कर सकता है।
ब्रोंस्टेड-लोरी सिद्धांत के साथ तुलना
एक लुईस क्षार अक्सर ब्रोंस्टेड-लोरी क्षार होता है क्योंकि यह एच को इलेक्ट्रॉनों की एक जोड़ी दान कर सकता है+;[10]प्रोटॉन एक लुईस अम्ल है क्योंकि यह इलेक्ट्रॉनों की एक जोड़ी को स्वीकार कर सकता है। ब्रोंस्टेड-लोरी अम्ल का संयुग्म क्षार भी डीप्रोटोनेशन के रूप में लुईस क्षार है। एच की हानि+ अम्ल से उन इलेक्ट्रॉनों को छोड़ देता है जो संयुग्म क्षार पर एक अकेले जोड़े के रूप में ए-एच बंधन के लिए उपयोग किए जाते थे। हालांकि, एक लुईस क्षार प्रोटोनेशन के लिए बहुत मुश्किल हो सकता है, फिर भी लुईस अम्ल के साथ अभिक्रिया करता है। उदाहरण के लिए, कार्बन मोनोआक्साइड एक बहुत कमजोर ब्रोंस्टेड-लोरी क्षार है लेकिन यह बीएफ के साथ एक मजबूत जोड़ बनाता है।3.
ब्राउन और कनेर द्वारा लुईस और ब्रोंस्टेड-लोरी अम्लता की एक और तुलना में,[15] 2,6-di-t-butylpyridine HCl के साथ हाइड्रोक्लोराइड नमक बनाने के लिए अभिक्रिया करता है लेकिन BF के साथ अभिक्रिया नहीं करता है3. यह उदाहरण दर्शाता है कि स्टायरिक कारक, इलेक्ट्रॉन विन्यास कारकों के अलावा, भारी di-t-butylpyridine और छोटे प्रोटॉन के बीच बातचीत की ताकत का निर्धारण करने में एक भूमिका निभाते हैं।
यह भी देखें
- अम्ल
- क्षार (रसायन विज्ञान)
- अम्ल-क्षार अभिक्रिया
- ब्रोंस्टेड-लोरी अम्ल-क्षार सिद्धांत
- चिरल लुईस अम्ल
- निराश लुईस जोड़ी
- गुटमैन-बेकेट विधि
- ईसीडब्ल्यू मॉडल
संदर्भ
- ↑ 1.0 1.1 IUPAC, Compendium of Chemical Terminology, 2nd ed. (the "Gold Book") (1997). Online corrected version: (2006–) "Lewis acid". doi:10.1351/goldbook.L03508
- ↑ 2.0 2.1 Lewis, Gilbert Newton (1923). Valence and the Structure of Atoms and Molecules. American chemical society. Monograph series. New York, New York, U.S.A.: Chemical Catalog Company. p. 142. ISBN 9780598985408. From p. 142: "We are inclined to think of substances as possessing acid or basic properties, without having a particular solvent in mind. It seems to me that with complete generality we may say that a basic substance is one which has a lone pair of electrons which may be used to complete the stable group of another atom, and that an acid substance is one which can employ a lone pair from another molecule in completing the stable group of one of its own atoms. In other words, the basic substance furnishes a pair of electrons for a chemical bond, the acid substance accepts such a pair."
- ↑ Lepetit, Christine; Maraval, Valérie; Canac, Yves; Chauvin, Remi (2016). "On the Nature of the Dative Bond: Coordination to Metals and Beyond. The Carbon Case". Coordination Chemistry Reviews. 308: 59–75. doi:10.1016/j.ccr.2015.07.018.
- ↑ 4.0 4.1 March, J. “Advanced Organic Chemistry” 4th Ed. J. Wiley and Sons, 1992: New York. ISBN 0-471-60180-2.[page needed]
- ↑ Vollhardt, K. Peter C. (2018). Organic chemistry : structure and function. Neil Eric Schore (8th ed.). New York. p. 73. ISBN 978-1-319-07945-1. OCLC 1007924903.
{{cite book}}: CS1 maint: location missing publisher (link) - ↑ Carey, Francis A. (2003). Organic chemistry (5th ed.). Boston: McGraw-Hill. p. 46. ISBN 0-07-242458-3. OCLC 48850987.
- ↑ IUPAC, Compendium of Chemical Terminology, 2nd ed. (the "Gold Book") (1997). Online corrected version: (2006–) "Electrophile (Electrophilic)". doi:10.1351/goldbook.E02020
- ↑ Rowsell, Bryan D.; Gillespie, Ronald J.; Heard, George L. (1999). "Ligand Close-Packing and the Lewis Acidity of BF3 and BCl3". Inorganic Chemistry. 38 (21): 4659–4662. doi:10.1021/ic990713m. PMID 11671188.
- ↑ Greenwood, N. N.; & Earnshaw, A. (1997). Chemistry of the Elements (2nd Edn.), Oxford:Butterworth-Heinemann. ISBN 0-7506-3365-4.[page needed]
- ↑ 10.0 10.1 10.2 Traditionally, but not precisely, H+ ions are referred as "protons". See IUPAC, Compendium of Chemical Terminology, 2nd ed. (the "Gold Book") (1997). Online corrected version: (2006–) "hydron". doi:10.1351/goldbook.H02904
- ↑ Christian Laurence and Jean-François Gal "Lewis Basicity and Affinity Scales : Data and Measurement" Wiley, 2009. ISBN 978-0-470-74957-9.[page needed]
- ↑ Childs, R.F; Mulholland, D.L; Nixon, A. (1982). "Lewis acid adducts of α,β-unsaturated carbonyl and nitrile compounds. A nuclear magnetic resonance study". Can. J. Chem. 60 (6): 801–808. doi:10.1139/v82-117.
- ↑ Vogel, Glenn C.; Drago, Russell S. (1996). "The ECW Model". Journal of Chemical Education. 73 (8): 701. Bibcode:1996JChEd..73..701V. doi:10.1021/ed073p701.
- ↑ Cramer, Roger E.; Bopp, Thomas T. (1977). "Great e and C plot. Graphical display of the enthalpies of adduct formation for Lewis acids and bases". Journal of Chemical Education. 54 (10): 612. Bibcode:1977JChEd..54..612C. doi:10.1021/ed054p612.
- ↑ Brown, Herbert C.; Kanner, Bernard (1966). "Preparation and Reactions of 2,6-Di-t-butylpyridine and Related Hindered Bases. A Case of Steric Hindrance toward the Proton". Journal of the American Chemical Society. 88 (5): 986–992. doi:10.1021/ja00957a023.
अग्रिम पठन
- Jensen, W.B. (1980). The Lewis acid-base concepts : an overview. New York: Wiley. ISBN 0-471-03902-0.
- Yamamoto, Hisashi (1999). Lewis acid reagents : a practical approach. New York: Oxford University Press. ISBN 0-19-850099-8.