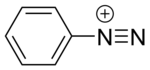
डायज़ोनियम यौगिक
डायज़ोनियम यौगिक या डायज़ोनियम लवण सामान्य कार्यात्मक समूह [R−N+≡N]X− को को विभक्त करने वाले कार्बनिक यौगिकों का समूह है जहां R कोई भी कार्बनिक समूह हो सकता है, जैसे कि एल्काइल या एरील, और X अकार्बनिक या कार्बनिक आयन है, जैसे हलाइड है।
सामान्य गुण और प्रतिक्रियाशीलता
एरेनेडियाज़ोनियम के धनायन और संबंधित प्रजातियाँ
एक्स- रे क्रिस्टलोग्राफी के अनुसार C−N+≡N लिंकेज विशिष्ट डायज़ोनियम लवण में रैखिक है। बेंजीनडायजोनियम टेट्राफ्लोरोबोरेट में N+≡N बांड की दूरी 1.083(3) Å है,[1] जो डाइनाइट्रोजन अणु (N≡N) के लिए लगभग समान है।
रैखिक मुक्त ऊर्जा स्थिरांक σm और σp प्रदर्शित करते हैं कि डायज़ोनियम समूह दृढ़ता से इलेक्ट्रॉन-निकासी है। इस प्रकार, डायज़ोनियो-प्रतिस्थापित फिनोल और बेंजोइक एसिड ने गैर-प्रतिस्थापित समकक्षों की तुलना में pKa मूल्यों को अधिक कम कर दिया है। 4-हाइड्रॉक्सीबेंजेडायजोनियम के फेनोलिक प्रोटॉन का pKa 3.4 है,[2] 9.9 फिनोल के लिए दूसरे शब्दों में, डायज़ोनियम समूह pKa (अम्लता को बढ़ाता है) को एक लाख गुना कम करता है।
एरेनेडियाज़ोनियम लवण की स्थिरता काउंटरियन के प्रति अत्यधिक संवेदनशील है। फेनिलडायज़ोनियम क्लोराइड खतरनाक रूप से विस्फोटक है, किंतु बेंजीनडायज़ोनियम टेट्राफ्लोरोबोरेट को बेंच पर सरलता से नियंत्रित किया जाता है।
SN1 और SN2 अभिक्रिया नहीं होती है।
एरेनेडियाज़ोनियम लवण बहुमुखी अभिकर्मक हैं जैसा कि अग्र अनुभागों में बताया गया है[3] इलेक्ट्रोफिलिक सुगंधित प्रतिस्थापन के पश्चात, सुगंधित यौगिकों को तैयार करने के लिए डायज़ोनियम रसायन सबसे अधिक बार प्रारम्भ की जाने वाली रणनीति है।
अल्केन डायज़ोनियम केशन और संबंधित प्रजातियाँ
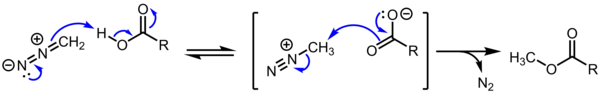
SN2/SN1/E1 प्रतिस्थापन के प्रति उनकी शीर्ष और अनियंत्रित प्रतिक्रियाशीलता के कारण अल्केनेडायज़ोनियम लवण कृत्रिम रूप से महत्वहीन हैं चूँकि ये उद्धरण सैद्धांतिक रुचि के हैं। इसके अलावा, मिथाइलडायज़ोनियम कार्बोक्सिलेट को डायज़ोमेथेन द्वारा कार्बोक्जिलिक एसिड के मिथाइलेशन में मध्यवर्ती माना जाता है, जो सामान्य परिवर्तन है।[4][5]
N2 की हानि एन्थैल्पिक और एंट्रोपिक रूप से अनुकूल दोनों है:
- [CH3N2]+ → [CH3]+ + N2, ΔH = −43 किलो कैलोरी/मोल
- [CH3CH2N2]+ → [CH3CH2]+ + N2, ΔH = -11 किलो कैलोरी/मोल
द्वितीयक और तृतीयक एल्केनेडियाज़ोनियम प्रजातियों के लिए, एन्थैल्पिक परिवर्तन की गणना शून्य या नकारात्मक के निकट होने के लिए की जाती है, न्यूनतम सक्रियण बाधा के साथ इसलिए, द्वितीयक और (विशेष रूप से) तृतीयक अल्केनेडियाज़ोनियम प्रजातियाँ या तो अबाधित हैं, कोई भी प्रजातियाँ नहीं हैं या, सबसे उत्तम रूप में, अत्यंत क्षणभंगुर मध्यवर्ती हैं[6]
मेथेनेडायज़ोनियम ([CH3N2]+) का जलीय pKa <10 होने का अनुमान है।[7]
तैयारी
डायज़ोनियम यौगिक बनाने की प्रक्रिया को डायज़ोटेशन, डायज़ोनेशन या डायज़ोटाइज़ेशन कहा जाता है। प्रतिक्रिया प्रथम बार 1858 में पीटर ग्रिस द्वारा रिपोर्ट की गई थी, जिन्होंने पश्चात में यौगिकों के इस नए वर्ग की कई प्रतिक्रियाओं का परीक्षण किया। सामान्यतः, नाइट्रस एसिड और अतिरिक्त एसिड के साथ सुगंधित अमाइन के प्रतिक्रिया से डायज़ोनियम लवण तैयार किए जाते हैं। सामान्यतः नाइट्रस एसिड सोडियम नाइट्राइट और अतिरिक्त खनिज एसिड (सामान्यतः जलीय HCl, H2SO4, p-H3CC6H4SO3H, या H[BF4]) से उत्पन्न होता है:
- ArNH2 + HNO2 + HX → [ArN2]+X− + 2 H2O
डायज़ोनियम केशन के क्लोराइड लवण, पारंपरिक रूप से एनिलिन, सोडियम नाइट्राइट और हाइड्रोक्लोरिक एसिड से तैयार किए जाते हैं, कक्ष के तापमान पर अस्थिर होते हैं और शास्त्रीय रूप से 0 - 5 डिग्री सेल्सियस पर तैयार किए जाते हैं। चूँकि, डायज़ोनियम यौगिकों को टेट्राफ्लोरोबोरेट या टॉयसिलेट लवण के रूप में भिन्न किया जा सकता है,[8] जो कक्ष के तापमान पर स्थिर ठोस होते हैं।[9] यह प्रायः लोकप्रिय होता है कि डायज़ोनियम नमक विलायक में रहता है, किंतु वे अतिसंतृप्ति होते हैं। नमक के अप्रत्याशित क्रिस्टलीकरण के पश्चात इसके विस्फोट से संचालक घायल हो गए या यहां तक कि मारे गए। रेफरी नाम = सुपरसेट>"यूके सीआरएचएफ घटना रिपोर्ट - सुपरसैचुरेटेड डायज़ोनियम नमक घातकता का कारण बनता है". UK Chemical Reaction Hazards Forum. Archived from the original on 6 October 2018. Retrieved 13 May 2010.</ref>
इन आशंका के कारण, डायज़ोनियम यौगिक प्रायः पृथक नहीं होते हैं। इसके अतिरिक्त उनका उपयोग सीटू में किया जाता है। इस दृष्टिकोण को एरेनसल्फोनील यौगिक की तैयारी में चित्रित किया गया है:
रेफरी>R. V. Hoffman (1981). "m-Trifluoromethylbenzenesulfonyl Chloride". Org. Synth. 60: 121. doi:10.15227/orgsyn.060.0121.</ref>
डायज़ो युग्मन प्रतिक्रियाएँ
डायज़ोनियम लवण का प्रथम उपयोग डायज़ोनियम यौगिक के जलीय घोल में कपड़े को डुबो कर जल-तेज़ रंगे कपड़े का उत्पादन करना था, इसके पश्चात कपलर (इलेक्ट्रॉन-समृद्ध रिंग जो इलेक्ट्रोफिलिक प्रतिस्थापन से निकलती है) के विलायक में विसर्जन होता है। डायज़ोनियम यौगिकों के प्रमुख अनुप्रयोग डाई और पिगमेंट उद्योग में बने हुए हैं।[10]
डायज़ोनियम लवण की सबसे व्यापक रूप से प्रचलित प्रतिक्रिया एज़ो युग्मन बनी हुई है, जिसका उपयोग एज़ो डाई के उत्पादन में किया जाता है।[11] इस प्रक्रिया में, डायज़ोनियम यौगिक पर वार किया जाता है, अर्थात, युग्मित, इलेक्ट्रॉन-समृद्ध सब्सट्रेट जब युग्मन भागीदार एनीलाइन और फिनोल जैसे एरेन होते हैं, तो यह प्रक्रिया इलेक्ट्रोफिलिक सुगन्धित प्रतिस्थापन का उदाहरण है:
- [ArN2]+ + Ar'H → ArN2Ar' + H+

- युग्मन भागीदारों का अन्य व्यावसायिक रूप से महत्वपूर्ण वर्ग एसीटोएसिटिक एमाइड्स है, जैसा कि पिगमेंट येलो 12, डायरलाइड वर्णक की तैयारी द्वारा चित्रित किया गया है।[12]
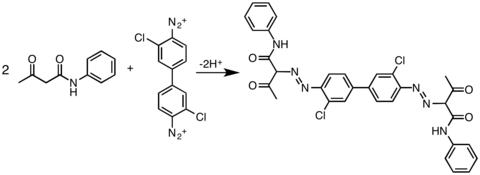
- परिणामी एज़ो यौगिक प्रायः उपयोगी रंजक होते हैं और वास्तव में एज़ो रंजक कहलाते हैं।[10]रंगों के गहरे रंग उनकी विस्तारित संयुग्मित प्रणाली को दर्शाते हैं। उदाहरण के लिए, एनिलिन येलो नामक डाई एनिलिन और डायज़ोनियम नमक के ठंडे घोल को मिलाकर और फिर इसे जोर से हिलाकर बनाई जाती है। अनिलिन येलो को पीले ठोस के रूप में प्राप्त किया जाता है।[13]इसी प्रकार, नेफ़थलेन-2-ऑल (बीटा-नेफ़थोल) का ठंडा मूल विलयन तीव्र नारंगी-लाल अवक्षेप देता है।[14] मिथाइल नारंगी एज़ो डाई का उदाहरण है जिसका प्रयोग प्रयोगशाला में पीएच संकेतक के रूप में किया जाता है।
N2 समूह का विस्थापन
एरेनेडियाज़ोनियम के धनायन कई प्रतिक्रियाओं से निकलते हैं जिनमें N2 समूह को दूसरे समूह या आयन द्वारा प्रतिस्थापित किया जाता है। इनमें से कुछ प्रमुख निम्नलिखित हैं।[15][16]
बायरिल युग्मन
डायज़ोनियम धनायनों की जोड़ी को बायरिल्स देने के लिए युग्मित किया जा सकता है। इस रूपांतरण को एंथ्रानिलिक एसिड से प्राप्त डायज़ोनियम नमक के युग्मन द्वारा डाइफेनिक एसिड (C6H4CO2H)2 देने के लिए चित्रित किया गया है, [17] संबंधित प्रतिक्रिया में, वही डायज़ोनियम नमक बेंजीन देने के लिए N2 और CO2 की हानि से निकलता है।[18]
हैलाइड्स द्वारा प्रतिस्थापन
सैंडमेयर प्रतिक्रिया
बेंजीनडायज़ोनियम क्लोराइड को क्यूप्रस क्लोराइड या क्यूप्रस ब्रोमाइड के साथ गर्म करने पर क्रमशः HCl या HBr में घुलने पर क्रमशः क्लोरोबेंजीन या ब्रोमोबेंजीन प्राप्त होता है।
- [C6H5N2]+ + CuCl → C6H5Cl + N2 + Cu+
गैटरमैन प्रतिक्रिया
गैटरमैन प्रतिक्रिया में, बेंजीनडायज़ोनियम क्लोराइड को क्रमशः क्लोरोबेंजीन और ब्रोमोबेंजीन का उत्पादन करने के लिए तांबे के पाउडर और HCl या HBr के साथ गर्म किया जाता है। इसका नाम जर्मन रसायनज्ञ लुडविग गैटरमैन के नाम पर रखा गया है।[19]
- 2 Cu + 2 [C6H5N2]+ → 2 Cu+ + (C6H5)2 + 2 N2 (initiation)
- [C6H5N2]+ + HX → C6H5X + N2 + H+ (Cu+ catalysis)
आयोडाइड द्वारा प्रतिस्थापन
एरिल आयोडाइड देने के लिए एरेनेडियाज़ोनियम केशन पोटेशियम आयोडाइड के साथ प्रतिक्रिया करते हैं:[20]
- [C6H5N2]+ + KI → C6H5I + K+ + N2
फ्लोराइड द्वारा प्रतिस्थापन
फ्लोरोबेंजीन बेंज़ेनडायज़ोनियम टेट्रफ्लुओरोबोरेट के थर्मल अपघटन द्वारा निर्मित होता है। रूपांतरण को बाल्ज़-शिमेन प्रतिक्रिया कहा जाता है।[21]
- [C6H5N2]+[BF4]− → C6H5F + BF3 + N2
पारंपरिक बल्ज़-शिमेन प्रतिक्रिया कई प्रेरणाओं का विषय रही है, उदा: हेक्साफ्लोरोफॉस्फेट (V) ([PF6]−) और हेक्साफ्लोरोएंटीमोनेट (V) ([SbF6]−) टेट्राफ्लोरोबोरेट के स्थान पर ([BF4]−) का उपयोग करना। डायज़ोटाइजेशन को नाइट्रोसोनियम लवण जैसे नाइट्रोसोनियम हेक्साफ्लोरोएंटीमोनेट (V) [NO]+[SbF6]− के साथ प्रभावित किया जा सकता है।[22]
विविध प्रतिस्थापन
हाइड्रोजन द्वारा प्रतिस्थापन
हाइपोफॉस्फोरस एसिड द्वारा इथेनॉल, सोडियम स्टैनाइट या क्षारीय सोडियम थायोसल्फेट द्वारा कम किए गए एरेनेडियाज़ोनियम केशन बेंजीन देता है:[23] ,[24] [25] [26]
- [C6H5N2]+Cl− + H3PO2 + H2O → C6H6 + N2 + H3PO3 + HCl
- [C6H5N2]+Cl− + CH3CH2OH → C6H6 + N2 + CH3CHO + HCl
- [C6H5N2]+Cl− + NaOH + Na2SnO2 → C6H6 + N2 + Na2SnO3 + NaCl
बायर और फिट्ज़िंगर द्वारा सुझाया गया वैकल्पिक विधि डायज़ो समूह को H के साथ परिवर्तित करना है: सबसे पहले इसे SnCl2 से प्रतिक्रिया करके हाइड्राज़ीन में परिवर्तित करना और फिर क्यूप्रिक सल्फेट घोल के साथ उबालकर इसे हाइड्रोकार्बन में ऑक्सीकृत करना।[27]
हाइड्रॉक्सिल समूह द्वारा प्रतिस्थापन
एरेनेडायज़ोनियम लवण के जलीय घोल को गर्म करके फेनॉल्स का उत्पादन किया जाता है:[28][29][30][31]
- [C6H5N2]+ + H2O → C6H5OH + N2 + H+
यह प्रतिक्रिया जर्मन नाम फेनोल्वरकोचुंग (फिनोल उत्पन्न करने के लिए नीचे खाना पकाने) द्वारा चला जाता है। गठित फिनोल डायज़ोनियम नमक के साथ प्रतिक्रिया कर सकता है और इसलिए प्रतिक्रिया एसिड की उपस्थिति में की जाती है जो इस आगे की प्रतिक्रिया को दबा देती है।[32] पानी में Cu2O और Cu2+ का उपयोग करके सैंडमेयर-प्रकार का हाइड्रॉक्सिलेशन भी संभव है।
नाइट्रो समूह द्वारा प्रतिस्थापन
तांबे की उपस्थिति में सोडियम नाइट्राइट के साथ बेंजीनडायजोनियम फ्लोरोबोरेट की प्रतिक्रिया करके नाइट्रोबेंजीन प्राप्त किया जा सकता है। वैकल्पिक रूप से, एनिलिन का डायज़ोटाइजेशन क्यूप्रस ऑक्साइड की उपस्थिति में किया जा सकता है, जो सीटू में क्यूप्रस नाइट्राइट उत्पन्न करता है:
- [C6H5N2]+ + CuNO2 → C6H5NO2 + N2 + Cu+
साइनो समूह द्वारा प्रतिस्थापन
सायनो समूह को सामान्यतः हैलोएरीन के न्यूक्लियोफिलिक प्रतिस्थापन द्वारा प्रस्तुत नहीं किया जा सकता है, किंतु ऐसे यौगिकों को डायज़ोनियम लवण से सरलता से तैयार किया जा सकता है। अभिकारक क्यूप्रस साइनाइड का उपयोग करके बेंज़ोनाइट्राइल की तैयारी निदर्शी है:
- [C6H5N2]+ + CuCN → C6H5CN + Cu+ + N2
यह अभिक्रिया विशेष प्रकार की सैंडमेयर अभिक्रिया है।
ट्राइफ्लोरोमेथाइल समूह द्वारा प्रतिस्थापन
दो अनुसंधान समूहों ने 2013 में डायज़ोनियम लवणों के ट्राइफ्लोरोमेथाइलेशन की सूचना दी। गूसेन ने CuSCN, TMSCF3 और Cs2CO3 से CuCF3 परिसर की तैयारी की सूचना दी। इसके विपरीत, फू ने उमेमोटो के अभिकर्मक (एस-ट्राइफ्लोरोमेथिल्डी बेंज़ोथियोफेनियम टेट्रफ्लुओरोबोरेट) और Cu पाउडर (गैटरमैन-प्रकार की स्थिति) का उपयोग करके ट्राइफ्लोरोमेथाइलेशन की सूचना दी। उन्हें निम्नलिखित समीकरण द्वारा वर्णित किया जा सकता है:
- [C6H5N2]+ + [CuCF3] → C6H5CF3 + [Cu]+ + N2
ब्रैकेट प्रदर्शित करता है कि तांबे पर अन्य लिगेंड उपस्तिथ होने की संभावना है किंतु त्याग दिए गए हैं।
थायोल समूह द्वारा प्रतिस्थापन
डायज़ोनियम लवण को दो-चरणीय प्रक्रिया में थिओल्स में परिवर्तित किया जा सकता है। बेंजीनडायज़ोनियम क्लोराइड का पोटेशियम एथिलक्सैंथेट के साथ प्रतिक्रिया के पश्चात मध्यवर्ती एक्स एंथे
एस्टर के हाइड्रोलिसिस के पश्चात थियोफेनोल देता है:
- [C6H5N2]+ + C2H5OCS−2 → C6H5SC(S)OC2H5 + N2
- C6H5SC(S)OC2H5 + H2O → C6H5SH + HOC(S)OC2H5
आर्यल समूह द्वारा प्रतिस्थापन
एरील समूह को एरेनेडायज़ोनियम लवण का उपयोग करके दूसरे से जोड़ा जा सकता है। उदाहरण के लिए, सोडियम हाइड्रॉक्साइड की उपस्थिति में बेंजीन (सुगंधित यौगिक) के साथ बेंजीनडायजोनियम क्लोराइड की प्रतिक्रिया डाइफिनाइल देता है:
- [C6H5N2]+Cl− + C6H6 → (C6H5)2 + N2 + HCl
इस प्रतिक्रिया को गोमबर्ग-बचमन प्रतिक्रिया के रूप में जाना जाता है। इथेनॉल और तांबे के पाउडर के साथ बेंजीनडायज़ोनियम क्लोराइड की प्रतिक्रिया करके भी इसी प्रकार का रूपांतरण प्राप्त किया जाता है।
बोरोनेट एस्टर समूह द्वारा प्रतिस्थापन
सुजुकी-मियौरा युग्मन प्रतिक्रियाओं में उपयोग के लिए बीपिन (पाइनकोलेटोबोरोन) सर्जक के रूप में बेंज़ोयल पेरोक्साइड (2 mol%) की उपस्थिति में बीआईएस (पाइनकोलेटो) डिबोरॉन के साथ डायज़ोनियम नमक की प्रतिक्रिया द्वारा स्थापित की जा सकती हैं।[33] वैकल्पिक रूप से इसी प्रकार के बोरिलीकरण को संक्रमण धातु कार्बोनिल कॉम्प्लेक्स का उपयोग करके प्राप्त किया जा सकता है, जिसमें डायमैंगनीज डेकाकार्बोनिल भी सम्मिलित है।[34]
- [C6H5N2]+X− + pinB−Bpin → C6H5Bpin + X−Bpin + N2
फॉर्मिल समूह द्वारा प्रतिस्थापन
एरील डायज़ोनियम नमक को फॉर्मलडॉक्सिम (H2C=NOH), इसके पश्चात एरियल एल्डिहाइड देने के लिए एरील एल्डोक्साइम का जल-अपघटन होता है।[35] इस प्रतिक्रिया को मध्य प्रतिक्रिया के रूप में जाना जाता है।[36]
अन्य डीडियाज़ोटाइजेशन
- इलेक्ट्रोसिंथेसिस पर जैविक कमी से
- एस्कॉर्बिक अम्ल (विटामिन सी) जैसे हल्के कम करने वाले एजेंटों द्वारा[37]
- पानी में उत्पन्न सॉल्वेटेड इलेक्ट्रॉनों से गामा विकिरण द्वारा
- प्रकाश रसायन इलेक्ट्रॉन ट्रांसफर
- मेटल केशन द्वारा कमी, सामान्यतः कपनुमा नमक।
- ऋणायन-प्रेरित डीडायज़ोनेशन: आयोडीन जैसे प्रतिरूप आर्य रेडिकल और आयोडीन रेडिकल बनाने वाले डायज़ोनियम केशन को इलेक्ट्रॉन हस्तांतरण देता है
- इलेक्ट्रॉन दाता के रूप में सेवा करने वाले विलायक के साथ विलायक-प्रेरित विचलन
मीरवीन प्रतिक्रिया
बेंजीनडायजोनियम क्लोराइड सक्रिय डबल बॉन्ड वाले यौगिकों के साथ प्रतिक्रिया करके फिनाइलेटेड उत्पादों का उत्पादन करता है। प्रतिक्रिया को मीरवीन आर्यलेशन कहा जाता है:
- [C6H5N2]+Cl− + ArCH=CH−COOH → ArCH=CH−C6H5 + N2 + CO2 + HCl
धातु परिसरों
धातु परिसरों के साथ उनकी प्रतिक्रियाओं में, डायज़ोनियम केशन समान व्यवहार करते हैं NO+. उदाहरण के लिए, कम-वैलेंट मेटल कॉम्प्लेक्स डायज़ोनियम लवण के साथ जोड़ते हैं। उदाहरणात्मक परिसर हैं [Fe(CO)2(PPh3)2(N2Ph)]+ और चिरल-एट-मेटल कॉम्प्लेक्स Fe(CO)(NO)(PPh3)(N2Ph).[38]
ग्राफ्टिंग प्रतिक्रियाएँ
नैनोटेक्नोलॉजी में संभावित अनुप्रयोग में, डायज़ोनियम लवण 4-क्लोरोबेंजेनडायज़ोनियम टेट्राफ्लोरोबोरेट बहुत कुशलता से कार्बन नैनोट्यूब को कार्यात्मक बनाता है।[39] नैनोट्यूब को एक्सफोलिएशन (भौतिक विज्ञान) करने के लिए, उन्हें मोर्टार और मूसल में आयनिक तरल के साथ मिलाया जाता है। डायज़ोनियम नमक को पोटेशियम कार्बोनेट के साथ जोड़ा जाता है, और कक्ष के तापमान पर मिश्रण को पीसने के पश्चात नैनोट्यूब की सतह को 44 कार्बन परमाणुओं में 1 की दक्षता के साथ क्लोरोफेनिल समूहों से ढक दिया जाता है। ये अतिरिक्त प्रतिस्थापी ट्यूबों को उनके मध्य बड़ी संसंजक शक्तियों के कारण घनिष्ठ बंडल बनाने से रोकते हैं, जो नैनोट्यूब प्रौद्योगिकी में आवर्ती समस्या है।
एरील मोनोलेयर बनाने वाले डायज़ोनियम लवण के साथ सिलिकॉन बिस्किट ्स को कार्यात्मक बनाना भी संभव है। अध्ययन में, सिलिकॉन की सतह को अमोनियम हाइड्रोजन फ्लोराइड से धोया जाता है और इसे सिलिकॉन-हाइड्रोजन बांड (हाइड्राइड पैसिवेशन) के साथ कवर किया जाता है।[40] अंधेरे में 2 घंटे के लिए acetonitrile में डायज़ोनियम नमक के घोल के साथ सतह की प्रतिक्रिया मुक्त कट्टरपंथी प्रतिक्रिया तंत्र के माध्यम से सहज प्रक्रिया है:[41]
अब तक लोहे, कोबाल्ट, निकल, प्लैटिनम , दुर्ग , जस्ता, तांबे और सोने की सतहों पर धातुओं पर डायज़ोनियम लवण की ग्राफ्टिंग की जा चुकी है।[42] साथ ही हीरे की सतहों पर ग्राफ्टिंग की सूचना मिली है।[43] उठाया गया दिलचस्प सवाल सतह पर एरियल समूह की वास्तविक स्थिति है। एन सिलिको में स्टडी [44] प्रदर्शित करता है कि टाइटेनियम से तांबे तक 4 तत्वों की अवधि में बाध्यकारी ऊर्जा बाएं से दाएं घट जाती है क्योंकि डी-इलेक्ट्रॉनों की संख्या बढ़ जाती है। लोहे के बायीं ओर की धातुएं सतह पर झुकी हुई या समतल होती हैं, जो धातु को कार्बन पाई बांड बनाने के पक्ष में होती हैं और लोहे के दायीं ओर की धातुएं कार्बन सिग्मा बंधन के गठन के लिए धातु के पक्ष में सीधी स्थिति में स्थित होती हैं। यह यह भी बताता है कि आवर्त सारणी में लोहे के अधिकार के लिए उन धातुओं के साथ अब तक डायज़ोनियम नमक ग्राफ्टिंग क्यों संभव है।
हाइड्राज़ीन समूह में कमी
डायज़ोनियम लवण को स्टैनस क्लोराइड से कम किया जा सकता है (SnCl2) संबंधित हाइड्राज़ीन डेरिवेटिव के लिए। यह प्रतिक्रिया ट्रिप्टान यौगिकों और इंडोमिथैसिन के फिशर इण्डोल संश्लेषण में विशेष रूप से उपयोगी है। सोडियम डाइथियोनाइट का उपयोग स्टैनस क्लोराइड पर सुधार है क्योंकि यह कम पर्यावरणीय समस्याओं के साथ सस्ता कम करने वाला एजेंट है।
जैव रसायन
Alkanediazonium आयन, अन्यथा शायद ही कभी कार्बनिक रसायन विज्ञान में पाए जाते हैं, कार्सिनोजेन्स में प्रेरक एजेंटों के रूप में निहित होते हैं। विशेष रूप से, ऐसा माना जाता है कि nitrosamines अल्केनेडियाज़ोनियम प्रजातियों का उत्पादन करने के लिए चयापचय सक्रियण से गुजरते हैं।

सुरक्षा
ठोस डायज़ोनियम हलाइड्स प्रायः खतरनाक रूप से विस्फोटक होते हैं, और मौत और चोटों की सूचना मिली है।[46]
ऋणायनों की प्रकृति लवण की स्थिरता को प्रभावित करती है। एरेनेडियाज़ोनियम पर्क्लोरेट्स, जैसे कि नाइट्रोबेंजेनेडायज़ोनियम परक्लोरेट, का उपयोग विस्फोटकों को शुरू करने के लिए किया गया है।
यह भी देखें
- डायज़ो
- व्हाइटप्रिंट # डायज़ो प्रिंटिंग प्रक्रिया
- बेंज़ेनडायज़ोनियम क्लोराइड
- ट्रायज़ीन दरार
- डाइनाइट्रोजन कॉम्प्लेक्स
संदर्भ
- ↑ Cygler, Miroslaw; Przybylska, Maria; Elofson, Richard Macleod (1982). "The Crystal Structure of Benzenediazonium Tetrafluoroborate, C6H5N2+•BF4−1". Canadian Journal of Chemistry. 60 (22): 2852–2855. doi:10.1139/v82-407.
- ↑ D. Bravo-Díaz, Carlos (2010-10-15), "Diazohydroxides, Diazoethers and Related Species", in Rappoport, Zvi (ed.), PATai's Chemistry of Functional Groups (in English), John Wiley & Sons, Ltd, doi:10.1002/9780470682531.pat0511, ISBN 9780470682531
- ↑ Norman, R. O. C. (Richard Oswald Chandler) (2017). कार्बनिक संश्लेषण के सिद्धांत (3rd ed.). CRC Press. ISBN 9780203742068. OCLC 1032029494.
- ↑ Streitwieser, Andrew; Schaeffer, William D. (June 1957). "प्राथमिक कार्बन की त्रिविम रसायन। छठी। नाइट्रस एसिड के साथ वैकल्पिक रूप से सक्रिय 1-एमिनोब्यूटेन-1-डी की प्रतिक्रिया। अमाइन-नाइट्रस एसिड रिएक्शन का तंत्र1". Journal of the American Chemical Society. 79 (11): 2888–2893. doi:10.1021/ja01568a054.
- ↑ Friedman, Lester; Jurewicz, Anthony T.; Bayless, John H. (March 1969). "अमीन डीमिनेशन में डायज़ोल्केन-अल्केनेडायज़ोनियम आयन संतुलन पर विलायक का प्रभाव". Journal of the American Chemical Society. 91 (7): 1795–1799. doi:10.1021/ja01035a032.
- ↑ Carey, Francis A. (2007). उन्नत कार्बनिक रसायन. Sundberg, Richard J. (5th ed.). New York: Springer. ISBN 9780387448978. OCLC 154040953.
- ↑ Fei, Na; Sauter, Basilius; Gillingham, Dennis (2016). "The pK a of Brønsted acids controls their reactivity with diazo compounds". Chemical Communications (in English). 52 (47): 7501–7504. doi:10.1039/C6CC03561B. PMID 27212133.
- ↑ Filimonov, Victor D.; Trusova, Marina; Postnikov, Pavel; Krasnokutskaya, Elena A.; Lee, Young Min; Hwang, Ho Yun; Kim, Hyunuk; Chi, Ki-Whan (2008-09-18). "Unusually Stable, Versatile, and Pure Arenediazonium Tosylates: Their Preparation, Structures, and Synthetic Applicability". Organic Letters (in English). 10 (18): 3961–3964. doi:10.1021/ol8013528. ISSN 1523-7060. PMID 18722457.
- ↑ {{cite journal | author1=Mihelač, M. |author2=Siljanovska, A. |author3=Košmrlj, J. |title=एरेनेडियाज़ोनियम टॉसिलेट्स के लिए एक सुविधाजनक दृष्टिकोण|journal=Dyes Pigm. |year=2021 |volume=184 |pages=108726 |doi=10.1016/j.dyepig.2020.108726 |doi-access=free}
- ↑ 10.0 10.1 Klaus Hunger, Peter Mischke, Wolfgang Rieper, et al. "Azo Dyes" in Ullmann’s Encyclopedia of Industrial Chemistry, 2005, Wiley-VCH, Weinheim. doi:10.1002/14356007.a03_245.
- ↑ Chemistry of the Diazonium and Diazo Groups: Part 1. S. Patai, Ed. 1978 Wiley-Blackwell. ISBN 0-471-99492-8. Chemistry of the Diazonium and Diazo Groups: Part 2. S. Patai, Ed. 1978 Wiley-Blackwell. ISBN 0-471-99493-6.
- ↑ K. Hunger. W. Herbst "Pigments, Organic" in Ullmann's Encyclopedia of Industrial Chemistry, Wiley-VCH, Weinheim, 2012. doi:10.1002/14356007.a20_371
- ↑ Cite error: Invalid
<ref>tag; no text was provided for refs namedchemguide - ↑ Clark, Jim. "केमगाइड". Retrieved 28 September 2011.
- ↑ March, J. “Advanced Organic Chemistry” 4th Ed. J. Wiley and Sons, 1992: New York. ISBN 978-0-471-60180-7.
- ↑ Marye Anne Fox; James K. Whitesell (2004). कार्बनिक रसायन विज्ञान (3, illustrated ed.). Jones & Bartlett Learning. pp. 535–538. ISBN 978-0-7637-2197-8.
- ↑ Atkinson, E. R.; Lawler, H. J. (1927). "डाइफेनिक एसिड". Org. Synth. 7: 30. doi:10.15227/orgsyn.007.0030.
- ↑ Logullo, F. M.; Seitz, A. H.; Friedman, L. (1968). "Benzenediazonium-2-carboxy- and Biphenylene". Org. Synth. 48: 12. doi:10.15227/orgsyn.048.0012.
- ↑ L. Gattermann (1894). "Untersuchungen über Diazoverbindungen". Berichte der Deutschen Chemischen Gesellschaft. 23 (1): 1218–1228. doi:10.1002/cber.189002301199.
- ↑ Lucas, H. J.; Kennedy, E. R. (1939). "आयोडोबेंजीन". Org. Synth. 19: 55. doi:10.15227/orgsyn.019.0055.
- ↑ Flood, D. T. (1933). "फ्लोरोबेंजीन". Org. Synth. 13: 46. doi:10.15227/orgsyn.013.0046..
- ↑ Furuya, Takeru; Klein, Johannes E. M. N.; Ritter, Tobias (2010). "C–F Bond Formation for the Synthesis of Aryl Fluorides". Synthesis. 2010 (11): 1804–1821. doi:10.1055/s-0029-1218742. PMC 2953275. PMID 20953341.
- ↑ Reinhard Bruckner, ed. Michael Harmata; Organic Mechanisms Reactions, Stereochemistry and Synthesis 3rd Ed, p.246, ISBN 978-3-8274-1579-0
- ↑ DeTarr, D.F.; Kosuge, T. (1958). "Mechanisms of Diazonium Salt Reactions. VI. The Reactions of Diazonium Salts with Alcohols under Acidic Conditions; Evidence for Hydride Transfer1". Journal of the American Chemical Society. 80 (22): 6072–6077. doi:10.1021/ja01555a044.
- ↑ Friedlander, Ber., 1889, 587, 22
- ↑ Grandmougin, Ber., 1907, 40, 858
- ↑ Baeyer & Pfitzinger, Ber., 1885, 18, 90, 786
- ↑ H. E. Ungnade, E. F. Orwoll (1943). "3-Bromo-4-hydroxytoluene". Org. Synth. 23: 11. doi:10.15227/orgsyn.023.0011.
- ↑ Kazem-Rostami, Masoud (2017). "फिनोल की आसान तैयारी". Synlett. 28 (13): 1641–1645. doi:10.1055/s-0036-1588180.
- ↑ Carey, F. A.; Sundberg, R. J. (2007). उन्नत कार्बनिक रसायन. Vol. B, Chapter 11: Springer. pp. 1028.
{{cite book}}: CS1 maint: location (link) - ↑ Khazaei, Ardeshir; Kazem-Rostami, Masoud; Zare, Abdolkarim; Moosavi-Zare, Ahmad Reza; Sadeghpour, Mahdieh; Afkhami, Abbas (2013). "एक डाई अधिशोषक के रूप में ट्राईजेन-आधारित पॉलीसल्फोन का संश्लेषण, लक्षण वर्णन और अनुप्रयोग". Journal of Applied Polymer Science. 129 (6): 3439–3446. doi:10.1002/app.39069.
- ↑ R. H. F. Manske (1928). "म-नाइट्रोफीनॉल". Org. Synth. 8: 80. doi:10.15227/orgsyn.008.0080.
- ↑ Wu, Jie; Gao, Yueqiu; Qiu, Guanyinsheng; He, Linman (2014-08-20). "डायज़ोनियम नमक-आधारित प्रतिक्रियाओं के माध्यम से एनिलिन से अमीनो समूहों को हटाना". Organic & Biomolecular Chemistry (in English). 12 (36): 6965–6971. doi:10.1039/C4OB01286K. ISSN 1477-0539. PMID 25093920.
- ↑ Fairlamb, Ian; Firth, James D.; Hammarback, L. Anders; Burden, Thomas J.; Eastwood, Jonathan B.; Donald, James R.; Horbaczewskyj, Chris S.; McRobie, Matthew T.; Tramaseur, Adam; Clark, Ian P.; Towrie, Michael; Robinson, Alan; Krieger, Jean-Philippe; Lynam, Jason M. (2020). "Light‐ and Manganese‐Initiated Borylation of Aryl Diazonium Salts: Mechanistic Insight on the Ultrafast Time‐Scale Revealed by Time‐Resolved Spectroscopic Analysis". Chemistry – A European Journal. 27 (12): 3979–3985. doi:10.1002/chem.202004568. PMID 33135818. S2CID 226232322.
- ↑ "कार्बनिक संश्लेषण प्रक्रिया". 2-bromo-4-methylbenzaldehyde (in English). Archived from the original on 2013-12-20. Retrieved 2021-05-04.
- ↑ Beech, W. F. (1954-01-01). "डायज़ोनियम लवण से सुगंधित एल्डिहाइड और कीटोन तैयार करना". Journal of the Chemical Society (Resumed) (in English): 1297–1302. doi:10.1039/JR9540001297. ISSN 0368-1769.
- ↑ Pinacho Crisóstomo Fernando (2014). "एस्कॉर्बिक एसिड (हेटेरो) के प्रत्यक्ष सी-एच आर्यलेशन के लिए एक पहल के रूप में सीटू में अनिलिन नाइट्रोसेट के साथ एरेन्स". Angewandte Chemie International Edition. 53 (8): 2181–2185. doi:10.1002/anie.201309761. PMID 24453180.
- ↑ Sutton, D (1993). "ऑर्गेनोमेटेलिक डायज़ो यौगिक". Chem. Rev. 93 (3): 905–1022. doi:10.1021/cr00019a008.
- ↑ Price, B. Katherine (2005). "आयनिक तरल पदार्थों में एकल-दीवार वाले कार्बन नैनोट्यूब का हरित रासायनिक क्रियाशीलता". Journal of the American Chemical Society. 127 (42): 14867–14870. doi:10.1021/ja053998c. PMID 16231941.
- ↑ Michael P. Stewart; Francisco Maya; Dmitry V. Kosynkin; et al. (2004). "एरेनेडियाज़ोनियम साल्ट से Si, GaAs और Pd सतहों पर संयुग्मित अणुओं का प्रत्यक्ष सहसंयोजक ग्राफ्टिंग". J. Am. Chem. Soc. 126 (1): 370–8. doi:10.1021/ja0383120. PMID 14709104.
- ↑ Reaction sequence: silicon surface reaction with ammonium hydrogen fluoride creates hydride layer. An electron is transferred from the silicon surface to the diazonium salt in an open circuit potential reduction leaving a silicon radical cation and a diazonium radical. In the next step a proton and a nitrogen molecule are expelled and the two radical residues recombine creating a surface silicon to carbon bond.
- ↑ Bélanger, Daniel; Pinson, Jean (2011). "Electrografting: a powerful method for surface modification". Chemical Society Reviews (in English). 40 (7): 3995–4048. doi:10.1039/c0cs00149j. ISSN 0306-0012. PMID 21503288.
- ↑ S.Q. Lud; M. Steenackers; P. Bruno; et al. (2006). "अल्ट्रानैनोक्रिस्टलाइन डायमंड पर बाइफिनाइल सेल्फ-असेंबल मोनोलेयर्स का केमिकल ग्राफ्टिंग". J. Am. Chem. Soc. 128 (51): 16884–91. doi:10.1021/ja0657049. PMID 17177439.
- ↑ De-en Jiang; Bobby G. Sumpter; Sheng Dai (2006). "आर्यल समूह और धातु की सतहों के बीच संरचना और संबंध". J. Am. Chem. Soc. 128 (18): 6030–1. doi:10.1021/ja061439f. PMID 16669660. S2CID 41590197.
- ↑ Tricker, A.R.; Preussmann, R. (1991). "Carcinogenic N-Nitrosamines in the Diet: Occurrence, Formation, Mechanisms and Carcinogenic Potential". Mutation Research/Genetic Toxicology. 259 (3–4): 277–289. doi:10.1016/0165-1218(91)90123-4. PMID 2017213.
- ↑ Cite error: Invalid
<ref>tag; no text was provided for refs namedsupersat
बाहरी संबंध
- W. Reusch. "Reactions of Amines". VirtualText of Organic Chemistry. Michigan State University. Archived from the original on 2012-12-12.