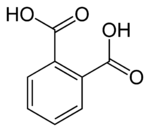
थैलिक एसिड
| |
| |
| Names | |
|---|---|
| Preferred IUPAC name
Benzene-1,2-dicarboxylic acid | |
| Other names
1,2-Benzenedioic acid
Phthalic acid Benzene-1,2-dioic acid ortho-Phthalic acid Dicarboxylbenzene Carboxylbenzoic acid 1,2-Phenylenedicarboxylic acid Phenylene-1,2-dicarboxylic acid | |
| Identifiers | |
3D model (JSmol)
|
|
| ChEBI | |
| ChemSpider | |
| EC Number |
|
PubChem CID
|
|
| UNII | |
| |
| |
| Properties | |
| C8H6O4 | |
| Molar mass | 166.132 g/mol |
| Appearance | white solid |
| Density | 1.593 g/cm3, solid |
| Melting point | 207 °C (405 °F; 480 K)[3] |
| 0.6 g / 100 mL [1] | |
| Acidity (pKa) | 2.89, 5.51[2] |
| -83.61·10−6 cm3/mol | |
| Hazards | |
| NFPA 704 (fire diamond) | |
| Related compounds | |
Related carboxylic acids
|
Isophthalic acid Terephthalic acid |
Related compounds
|
Phthalic anhydride Phthalimide Phthalhydrazide Phthaloyl chloride Benzene-1,2- dicarboxaldehyde |
Except where otherwise noted, data are given for materials in their standard state (at 25 °C [77 °F], 100 kPa).
| |
थैलिक एसिड एक सुगंधित डाइकारबॉक्सिलिक एसिड है, जिसका सूत्र C6H4(CO2H)2 है हालांकि थैलिक एसिड साधारण व्यावसायिक महत्व का, निकट से संबंधित डेरिवेटिव फ्थेलिक एनहाइड्राइड बड़े पैमाने पर उत्पादित एक वस्तु रसायन है।[4] थैलिक एसिड बेंजीनाइकारबॉक्सिलिक एसिड के तीन आइसोमर्स में से एक है, अन्य आइसोफथलिक एसिड और टेरेफ्थेलिक एसिड हैं।
उत्पादन
थैलिक एसिड नेफ़थलीन या ऑर्थो-ज़ाइलिन | ऑर्थो-ज़ाइलीन के उत्प्रेरक ऑक्सीकरण द्वारा सीधे फ़ाथलिक एनहाइड्राइड और एनहाइड्राइड के बाद के हाइड्रोलिसिस द्वारा निर्मित होता है।[4]
थैलिक एसिड पहली बार 1836 में फ्रांस के रसायनज्ञ अगस्त लौरेंत द्वारा ऑक्सीकरण नेफ़थलीन टेट्राक्लोराइड द्वारा प्राप्त किया गया था।[5] परिणामी पदार्थ को नेफ़थलीन व्युत्पन्न मानते हुए, उन्होंने इसे नेफ़थलिक एसिड नाम दिया।[5][6][7] स्विट्ज़रलैंड के रसायनज्ञ जीन-चार्ल्स गैलिसार्ड डी मरिग्नाक ने इसका सही सूत्र निर्धारित करने के बाद,[8] लॉरेंट ने इसे अपना वर्तमान नाम दिया।[5][9][10] उन्नीसवीं शताब्दी में विनिर्माण विधियों में नाइट्रिक एसिड के साथ नेफ़थलीन टेट्राक्लोराइड का ऑक्सीकरण शामिल था, या बेहतर, सल्फ्यूरिक एसिड के साथ हाइड्रोकार्बन का ऑक्सीकरण, एक उत्प्रेरक के रूप में पारा या पारा (II) सल्फेट का उपयोग करना।[5]
संश्लेषण
नेफ़थलीन पोटेशियम परमैंगनेट या पोटेशियम डाइक्रोमेट के साथ ऑक्सीकरण पर थैलिक एसिड देता है।[citation needed]
प्रतिक्रियाएं और उपयोग
यह पीके के साथ एक डिबासिक एसिड हैa2.89 और 5.51 के एस। विश्लेषणात्मक रसायन विज्ञान में मोनोपोटेशियम नमक, पोटेशियम हाइड्रोजन थैलेट एक मानक एसिड है। आमतौर पर थैलेट एस्टर व्यापक रूप से उपलब्ध थैलिक एनहाइड्राइड से तैयार किए जाते हैं। पानी की उपस्थिति में सोडियम अमलगम के साथ थैलिक एसिड की कमी से 1,3-साइक्लोहेक्साडीन व्युत्पन्न होता है।[11]
सुरक्षा
थैलिक एसिड की विषाक्तता मध्यम है LD50 (माउस) 550 मिलीग्राम/किग्रा।
बायोडिग्रेडेशन
बैक्टीरिया स्यूडोमोनास सपा। P1 थैलिक एसिड को नीचा दिखाता है।[12]
यह भी देखें
- आइसोफैलिक एसिड
- थैलेट
- फ्थेलिक एनहाइड्राइड
- पोटेशियम हाइड्रोजन थैलेट, अम्ल-क्षार अनुमापन के लिए एक प्राथमिक मानक
- टेरेफ्थलिक एसिड
संदर्भ
- ↑ "PHTHALIC ACID". hazard.com.
- ↑ Brown, H.C., et al., in Baude, E.A. and Nachod, F.C., Determination of Organic Structures by Physical Methods, Academic Press, New York, 1955.
- ↑ Several melting points are reported, for example: (i) 480. K (NIST website), (ii) 210−211 °C with decomposition (Sigma-Aldrich on-line), (iii) 191 °C in a sealed tube (Ullmann's Encyclopedia of Industrial Chemistry), (iv) 230 °C with conversion to phthalic anhydride and water (J.T.Baker MSDS).
- ↑ 4.0 4.1 Lorz, Peter M.; Towae, Friedrich K.; Enke, Walter; et al. (2007). "Phthalic Acid and Derivatives". Ullmann's Encyclopedia of Industrial Chemistry. Weinheim: Wiley-VCH. doi:10.1002/14356007.a20_181.pub2.
- ↑ 5.0 5.1 5.2 5.3 Chisholm, Hugh, ed. (1911). . Encyclopædia Britannica (in English). Vol. 21 (11th ed.). Cambridge University Press. pp. 545–546.
- ↑ Auguste Laurent (1836) "Sur l'acide naphtalique et ses combinaisons" (On naphthalic acid and its compounds), Annales de Chimie et de Physique, 61 : 113-125. (Note: The empirical formulae of the compounds that were analyzed in this article are incorrect, in part because, during this period, chemists used incorrect atomic masses for carbon (6 instead of 12) and other elements.)
- ↑ Reprinted in German as: Auguste Laurent (1836) "Ueber Naphthalinsäure und ihre Verbindungen" (On naphthalenic acid and its compounds), Annalen der Pharmacie, 19 (1) : 38-50; for the preparation of phthalic acid, see page 41.
- ↑ C. de Marignac (1841) "Ueber die Naphtalinsäure und ein bei ihrer Darstellung entstehendes flüchtiges Produkt" ("On naphthalinic acid and a volatile product that arises during its preparation"), Annalen der Chemie und Pharmacie, 38 (1) : 13-20. (Note: Again, Marignac's empirical formulae are wrong because chemists at this time used incorrect atomic masses.)
- ↑ Auguste Laurent (1841) "Sur de nouvelles combinaisons nitrogénées de la naphtaline et sur les acides phtalique et nitrophtalique" (On new nitrogenous compounds of naphthalene, and on phthalic acid and nitrophthalic acid), Revue Scientifique et Industrielle, 6 : 76-99; on page 92, Laurent coins the name "acide phtalique" (phthalic acid) and admits that his earlier empirical formula for phthalic acid was wrong.
- ↑ Reprinted in German as: Auguste Laurent (1842) "Ueber neue stickstoffhaltige Verbindungen des Naphtalins, über Phtalinsäure und Nitrophtalinsäure" (On new nitrogenous compounds of naphthalene, on phthalic acid and nitrophthalic acid), Annalen der Chemie und Pharmacie, 41 (1) : 98-114; on page 108, Laurent coins the name "Phtalinsäure" (phthalic acid).
- ↑ Richard N. McDonald and Charles E. Reineke (1988). "trans-1,2-Dihydrophthalic Acid". Organic Syntheses.; Collective Volume, vol. 6, p. 461
- ↑ Ishtiaq Ali, Muhammad (2011). पॉलीविनाइल क्लोराइड प्लास्टिक का माइक्रोबियल डिग्रेडेशन (PDF) (Ph.D.). Quaid-i-Azam University. p. 47.
- Merck Index, 9th ed, #7178

