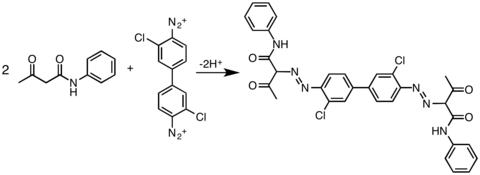
एज़ो युग्मन
कार्बनिक रसायन विज्ञान में, एज़ो युग्मन डायज़ोनियम यौगिक के बीच कार्बनिक प्रतिक्रिया (R−N≡N+) है। और अन्य सुगंधित यौगिक जो एज़ो यौगिक उत्पन्न करता है (R−N=N−R’) इस इलेक्ट्रोफिलिक सुगंधित प्रतिस्थापन प्रतिक्रिया में, एरिल्डियाज़ोनियम धनायन इलेक्ट्रोफाइल है। और सक्रिय समूह कार्बन (सामान्यतः एरेने से जिसे युग्मन प्रतिनिधि कहा जाता है।) न्यूक्लियोफाइल के रूप में कार्य करता है।[1] अधिकांश स्थितियों में, नीचे दिए गए उदाहरणों सहित, डायज़ोनियम यौगिक भी सुगंधित होता है।
डायज़ोटाइजेशन
प्राथमिक ऐरोमैटिक ऐमीन को उसके डायज़ोनियम नमक में बदलने की प्रक्रिया को डायज़ोटाइज़ेशन कहा जाता है। डायज़ोनियम लवण महत्वपूर्ण सिंथेटिक मध्यवर्ती हैं। जो कार्यात्मक समूह को प्रस्तुत करने के लिए एज़ो डाई और इलेक्ट्रोफिलिक प्रतिस्थापन प्रतिक्रियाओं को बनाने के लिए युग्मन प्रतिक्रियाओं से निकल सकते हैं।
प्रतिक्रिया का उपयोग
विस्तारित संयुग्मित प्रणालियों के कारण सुगंधित एज़ो यौगिक चमकीले रंग के होते हैं। कई का उपयोग रंगों के रूप में किया जाता है (अज़ो एज़ो देखें)।[2] महत्वपूर्ण एज़ो रंगों में मिथाइल लाल और वर्णक लाल 170 सम्मिलित हैं। एज़ो प्रिंटिंग इस प्रतिक्रिया का भी लाभ उठाती है। इस स्थितियों में, डायज़ोनियम आयन प्रकाश द्वारा अवक्रमित हो जाता है, जिससे अपघटित डायज़ोनियम नमक में अव्यक्त छवि निकल जाती है। जिसे फिनोल के साथ प्रतिक्रिया करने के लिए बनाया जाता है, जिससे रंगीन छवि बनती है: ब्लूप्रिंट[3] प्रोंटोसिल,पहली सल्फा दवा, एक बार एज़ो कपलिंग द्वारा निर्मित की गई थी। एज़ो कंपाउंड प्रोड्रग है। जो सुफानिलमाइड का उत्पादन करने के लिए इन-विवो सक्रिय होता है, जो सक्रिय है।
प्रतिक्रिया का उपयोग प्रोटीन में टायरोसिन या हिस्टिडीन अवशेषों का पता लगाने के लिए पॉली प्रतिक्रिया परीक्षण में भी किया जाता है।
एज़ो C-युग्मन प्रतिक्रियाओं के उदाहरण
कई प्रक्रियाओं का वर्णन किया गया है, जो पुनः.[4][5] फिनोल बेंज़ेनेडियाज़ोनियम क्लोराइड के साथ प्रतिक्रिया करके विलायक पीला 7, पीला-नारंगी एज़ो यौगिक देता है। उच्च pH पर प्रतिक्रिया तेज़ होती है।[2]
 एनिलिन पीला नामक संबंधित डाई एनिलिन और डायज़ोनियम नमक की प्रतिक्रिया से उत्पन्न होती है। इस स्थितियों में C- और N-युग्मन प्रतिस्पर्धा करते हैं।[2] जब पैरा स्थिति को ओरिएंटिंग समूह (सुगंधित इलेक्ट्रोफिलिक प्रतिस्थापन के लिए) में प्रतिस्थापित किया जाता है, तो युग्मन ऑर्थो स्थिति में होता है, यद्यपि धीमी गति हो।
एनिलिन पीला नामक संबंधित डाई एनिलिन और डायज़ोनियम नमक की प्रतिक्रिया से उत्पन्न होती है। इस स्थितियों में C- और N-युग्मन प्रतिस्पर्धा करते हैं।[2] जब पैरा स्थिति को ओरिएंटिंग समूह (सुगंधित इलेक्ट्रोफिलिक प्रतिस्थापन के लिए) में प्रतिस्थापित किया जाता है, तो युग्मन ऑर्थो स्थिति में होता है, यद्यपि धीमी गति हो।
नेफ़थोल लोकप्रिय युग्मन प्रतिनिधि हैं। उदाहरण रंगों का रासायनिक आधार और 1-नेफ़थॉल से डाई ऑर्गेनॉल ब्राउन का संश्लेषण है:
 इसी तरह β-नैफ्थॉल फेनिलडायज़ोनियम इलेक्ट्रोफाइल के साथ जुड़कर तीव्र नारंगी-लाल रंग का उत्पादन करता है।
इसी तरह β-नैफ्थॉल फेनिलडायज़ोनियम इलेक्ट्रोफाइल के साथ जुड़कर तीव्र नारंगी-लाल रंग का उत्पादन करता है।
सुगंधित छल्लों में सक्रिय कार्बन के अतिरिक्त, अन्य न्यूक्लियोफिलिक कार्बन को भी डायज़ोनियम नमक के साथ जोड़ा जा सकता है:
एज़ो N-युग्मन प्रतिक्रियाओं के उदाहरण
क्षारीय मीडिया में, डायज़ोनियम नमक अधिकांश प्राथमिक और द्वितीयक एमाइन के साथ प्रतिक्रिया कर सकता है। जो मुक्त आधार के रूप में उपस्थित होते हैं। और ट्राईज़ीन का उत्पादन करते हैं।[6] इस रासायनिक प्रतिक्रिया को एज़ो N-कपलिंग कहा जाता है।[7] या एज़ोमाइन का संश्लेषण कहा जाता है।[8]
संदर्भ
- ↑ Smith, Michael B.; March, Jerry (2007), Advanced Organic Chemistry: Reactions, Mechanisms, and Structure (6th ed.), New York: Wiley-Interscience, ISBN 978-0-471-72091-1
- ↑ 2.0 2.1 2.2 Klaus Hunger; Peter Mischke; Wolfgang Rieper; Roderich Raue; Klaus Kunde; Aloys Engel (2005). Ullmann's Encyclopedia of Industrial Chemistry. Weinheim: Wiley-VCH. doi:10.1002/14356007.a03_245.
- ↑ Pai, Damodar M.; Melnyk, Andrew R.; Weiss, David S.; Hann, Richard; Crooks, Walter; Pennington, Keith S.; Lee, Francis C.; Jaeger, C. Wayne; Titterington. "Imaging Technology, 2. Copying and Nonimpact Printing Processes". Ullmann's Encyclopedia of Industrial Chemistry. Weinheim: Wiley-VCH. pp. 1–53. doi:10.1002/14356007.o13_o08.pub2.
- ↑ J. L. Hartwell and Louis F. Fieser. "Coupling of o-tolidine and Chicago acid". Organic Syntheses.; Collective Volume, vol. 2, p. 145
- ↑ H. T. Clarke and W. R. Kirner. "Methyl red". Organic Syntheses.; Collective Volume, vol. 1, p. 374
- ↑ Khazaei; et al. (2012). "एज़ो अमीन युग्मन से ट्राइजेन मिलता है, और ट्राइजीन का अपघटन डायज़ोनियम नमक देता है". Synlett. 23 (13): 1893–1896. doi:10.1055/s-0032-1316557.
- ↑ Wiley Subscription Services (2013). "ट्राइजीन-बेस पॉलिमर का संश्लेषण, लक्षण वर्णन और अनुप्रयोग". Journal of Applied Polymer Science. 129 (6): 3439–3446. doi:10.1002/app.39069.
- ↑ Serge Ratton, Bernard Botannet (1981). "Preparation of aromatic azoamines by diazotization/coupling/rearrangement of aromatic amines". US Patent 4275003A.