स्राव
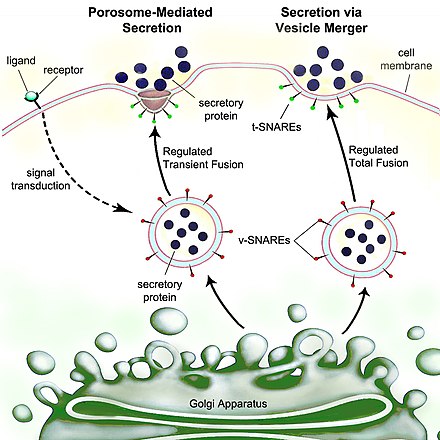
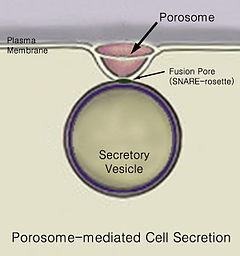
स्राव पदार्थ का पहले बिंदु से दूसरे बिंदु तक संचलन है, जैसे किसी कोशिका (जीव विज्ञान) या ग्रंथि से स्रावित रासायनिक पदार्थ आदि। इसके विपरीत, उत्सर्जन किसी कोशिका या जीव से कुछ पदार्थों या अपशिष्ट उत्पादों को निकालना है। कोशिका स्राव का मौलिक प्रक्रिया कोशिका मेम्ब्रेन में स्रावी पोर्टलों के माध्यम से होता है जिन्हें पोरोसोम्स कहा जाता है।[1] पोरोसोम कोशिका मेम्ब्रेन में अंतर्निहित स्थायी कप के आकार की लिपोप्रोटीन संरचनाएं हैं, जहां स्रावी वेसिकलएं क्षणिक रूप से जुड़ती हैं और कोशिका से इंट्रा-वेसिकुलर सामग्री को मुक्त करने के लिए फ्यूज हो जाती हैं।
जीवाणु स्राव प्रणाली का अर्थ है प्रभावकारी अणुओं का परिवहन या स्थानान्तरण, उदाहरण के लिए: प्रोटीन, एंजाइमों या विषाक्त पदार्थ (जैसे रोगजनक जीवाणु में हैजा विष जैसे विब्रियो हैजा ) जीवाणु कोशिका के आंतरिक ( कोशिका द्रव्य या साइटोसोल) से उसके बाहरी भाग तक अनुकूलन और अस्तित्व के लिए उनके प्राकृतिक आसपास के वातावरण में बैक्टीरिया के कार्य और संचालन में स्राव बहुत ही महत्वपूर्ण प्रक्रिया है।
यूकैरियोटिक कोशिकाओं में
मैकेनिज्म
मानव कोशिकाओं सहित यूकेरियोट कोशिका (जीव विज्ञान) में स्राव की अत्यधिक विकास प्रक्रिया होती है। प्रोटीन बाहर के लिए लक्षित प्रोटीन रफ अन्तः प्रदव्ययी जलिका (ईआर) से जुड़े राइबोसोम द्वारा प्रोटीन संश्लेषण है। जैसे ही उनका संश्लेषण होता है, यह प्रोटीन ईआर लुमेन (शरीर रचना) में स्थानांतरित हो जाते हैं, जहां वह ग्लाइकोसिलेशन होते हैं और जहां आणविक चैपरोन (प्रोटीन) प्रोटीन को मोड़ने में सहायता करते हैं। वंहा गलत विधि से मुड़े हुए प्रोटीन की पहचान सामान्यतः यहां की जाती है और एंडोप्लाज्मिक-रेटिकुलम-संबद्ध प्रोटीन निम्नीकरण द्वारा रेट्रोट्रांसलेट किया जाता है। साइटोसोल में ईआर-संबद्ध निम्नीकरण, जहां वह एंटीबॉडी द्वारा अपमानित होते हैं। तथा जहाँ उचित रूप से मुड़े हुए प्रोटीन युक्त वेसिकल (जीव विज्ञान) फिर गोल्गी एप्रेट्स में प्रवेश करती है।
गोल्गी एप्रेट्स में, प्रोटीन के ग्लाइकोसिलेशन को संशोधित किया जाता है और दरार और क्रियाशीलता सहित आगे के पश्चात के अनुवाद संबंधी संशोधन हो सकते हैं। फिर प्रोटीन को स्रावी वेसिक्लए में ले जाया जाता है जो साइटोस्केलेटन के साथ कोशिका के किनारे तक यात्रा करते हैं। स्रावी वेसिक्लए में अधिक संशोधन हो सकता है (उदाहरण के लिए स्रावी वेसिक्लए में इंसुलिन को प्रोइंसुलिन से पृथक किया जाता है)।
अंततः, एक्सोसाइटोसिस नामक प्रक्रिया द्वारा पोरोसोम में कोशिका मेम्ब्रेन के साथ वेसिकल का संलयन होता है, जिससे इसकी सामग्री कोशिका के वातावरण से बाहर निकल जाती है।[2]
pH ग्रेडिएंट के उपयोग से इस अनुक्रम पर सख्त जैव रासायनिक नियंत्रण बनाए रखा जाता है: साइटोसोल का pH 7.4 है, ER का pH 7.0 है, और सीस-गोल्गी का pH 6.5 है। स्रावी वेसिक्लए का pH 5.0 और 6.0 के मध्य होता है; तथा जहाँ कुछ स्रावी वेसिकल लाइसोसोम में विकसित होती हैं, जिनका pH 4.8 होता है।
अमौलिक स्राव
FGF1 (aFGF), FGF2 (bFGF), इंटरल्युकिन 1 (IL1) आदि जैसे बहुत से प्रोटीन हैं जिनमें सिग्नल अनुक्रम नहीं होता है। वह मौलिक ईआर-गोल्गी मार्ग का उपयोग नहीं करते हैं। इन्हें विभिन्न गैर-मौलिक मार्गों के माध्यम से स्रावित किया जाता है।
कम से कम चार गैर-मौलिक (अपरंपरागत) प्रोटीन स्राव मार्गों का वर्णन किया गया है।[3] वह सम्मिलित करते हैं:
- मेम्ब्रेन ट्रांसपोर्ट प्रोटीन के माध्यम से संभवतः प्लाज्मा मेम्ब्रेन में प्रोटीन का प्रत्यक्ष स्थानांतरण
- ब्लेब (कोशिका जीव विज्ञान)
- लाइसोसोमल स्राव
- बहुकोशिकीय निकायों से प्राप्त एक्सोसोम के माध्यम से रिलीज
इसके अतिरिक्त, प्रोटीन कोशिकाओं से यांत्रिक या शारीरिक घावों द्वारा प्रयुक्त किया जा सकता है [4] और सीरम-मुक्त मीडिया या बफ़र्स के साथ कोशिकाओं को धोने से प्रेरित प्लाज्मा मेम्ब्रेन में गैर-घातक, क्षणिक ऑन्कोटिक दबाव के माध्यम से भी प्रयुक्त किया जा सकता है।[5]
मानव ऊतकों में
ऐसे बहुत से मानव कोशिका प्रकारों में स्रावी कोशिकाएँ बनने की क्षमता होती है। इस कार्य को पूरा करने के लिए उनके पास अच्छी तरह से विकसित एंडोप्लाज्मिक रेटिकुलम और गोल्गी एप्रेट्स है। ऊतक (जीव विज्ञान) जो स्राव उत्पन्न करते हैं उनमें जठरांत्र संबंधी मार्ग सम्मिलित है जो पाचन एंजाइमों और गैस्ट्रिक अम्ल को स्रावित करता है, फेफड़े जो सर्फेकेंट्स का स्राव करते हैं, और वसामय ग्रंथियां जो त्वचा और बालों को स्मूथ करने के लिए सीबम का स्राव करते हैं। पलक में मेइबोमियन ग्रंथियां आंख को स्मूथ करने और उसकी सुरक्षा करने के लिए मैबम का स्राव करती हैं।
ग्राम-नेगेटिव बैक्टीरिया में
इस प्रकार स्राव यूकेरियोट्स के लिए अद्वितीय नहीं है - यह बैक्टीरिया और आर्किया में भी उपस्तिथ है। एटीपी बाइंडिंग कैसेट (एबीसी) प्रकार के ट्रांसपोर्टर जीवन के तीन क्षेत्रों के लिए सामान्य हैं। कुछ स्रावित प्रोटीनों को दो ट्रांसलोकेशन प्रणालियों में से एक, सेकवाईईजी अनुवाद द्वारा साइटोप्लाज्मिक मेम्ब्रेन में स्थानांतरित किया जाता है, जिसके लिए स्रावित प्रोटीन पर एन-टर्मिनल सिग्नल पेप्टाइड की उपस्थिति की आवश्यकता होती है। अन्य को ट्विन-आर्जिनिन ट्रांसलोकेशन मार्ग (टाट) द्वारा साइटोप्लाज्मिक मेम्ब्रेन में स्थानांतरित किया जाता है। ग्राम-नकारात्मक बैक्टीरिया में दो झिल्लियाँ होती हैं, जिससे स्राव स्थैतिक रूप से अधिक सम्मिश्र हो जाता है। ग्राम-नेगेटिव बैक्टीरिया में कम से कम छह विशेष स्राव प्रणालियाँ होती हैं। बहुत से स्रावित प्रोटीन जीवाणु रोगजनन में विशेष रूप से महत्वपूर्ण हैं।[6]
टाइप I स्राव प्रणाली (T1SS या TOSS)
टाइप I स्राव चैपरोन आश्रित स्राव प्रणाली है जो हेली और टोल जीन समूहों को नियोजित करती है। यह प्रक्रिया स्रावित होने वाले प्रोटीन पर लीडर अनुक्रम के रूप में प्रारंभ होती है जिसे HlyA द्वारा पहचाना जाता है और HlyB को मेम्ब्रेन पर बांधता है। यह सिग्नल अनुक्रम एबीसी ट्रांसपोर्टर के लिए असिमित विशिष्ट है। HlyAB कॉम्प्लेक्स HlyD को उत्तेजित करता है जो खोलना प्रारंभ कर देता है और बाहरी मेम्ब्रेन तक पहुंचता है जहां TolC HlyD पर टर्मिनल अणु या सिग्नल को पहचानता है। HlyD TolC को आंतरिक मेम्ब्रेन में भर्ती करता है और HlyA लंबी-सुरंग प्रोटीन चैनल के माध्यम से बाहरी मेम्ब्रेन के बाहर उत्सर्जित होता है।
टाइप I स्राव प्रणाली विभिन्न अणुओं को आयनों, दवाओं से लेकर विभिन्न आकारों (20 - 900 केडीए) के प्रोटीन तक पहुंचाती है। स्रावित अणुओं का आकार छोटे इशरीकिया कोली पेप्टाइड कोलिसिन वी, (10 केडीए) से लेकर 520 केडीए के स्यूडोमोनास फ्लोरेसेंस सेल आसंजन प्रोटीन लैपा तक भिन्न होता है।[7] सबसे अच्छी विशेषता आरटीएक्स टॉक्सिन्स और लाइपेज हैं। टाइप I स्राव चक्रीय β-ग्लूकेन्स और पॉलीसेकेराइड जैसे गैर-प्रोटीनसियस सब्सट्रेट्स के निर्यात में भी सम्मिलित है।
टाइप II स्राव प्रणाली (T2SS)
टाइप II प्रणाली, या सामान्य स्रावी मार्ग की मुख्य टर्मिनल शाखा के माध्यम से स्रावित प्रोटीन, पेरीप्लाज्म में प्रारंभिक परिवहन के लिए सेक या टैट प्रणाली पर निर्भर करते हैं। इस प्रकार वहां, वह स्रावी प्रोटीन बनाने वाले छिद्रों के मल्टीमेरिक (12-14 सबयूनिट) कॉम्प्लेक्स के माध्यम से बाहरी मेम्ब्रेन से निकलते हैं। सेक्रेटिन प्रोटीन के अतिरिक्त, 10-15 अन्य आंतरिक और बाहरी मेम्ब्रेन प्रोटीन पूर्ण स्राव प्रक्रिया की रचना करते हैं, जिनमें से बहुत से अभी तक अज्ञात कार्य करते हैं। ग्राम-नेगेटिव पिलस टाइप IV पिली अपने जैवजनन के लिए टाइप II प्रणाली के संशोधित संस्करण का उपयोग करते हैं, और कुछ स्तिथियों में कुछ प्रोटीन ही जीवाणु प्रजाति के अंदर पाइलस कॉम्प्लेक्स और टाइप II प्रणाली के मध्य साझा किए जाते हैं।
प्रकार III स्राव प्रणाली (T3SS या TTSS)
यह बैक्टीरियल फ्लैगेल्ला में बेसल शरीर के अनुरूप है। यह आणविक श्रेणी की तरह है जिसके माध्यम से जीवाणु (उदाहरण के लिए कुछ प्रकार के साल्मोनेला, शिगेला, यर्सिनिया,, विब्रियो) प्रोटीन को यूकेरियोटिक कोशिकाओं में इंजेक्ट कर सकता है। साइटोसोल से कम Ca2+ की एकाग्रता उस द्वार को खोलती है जो T3SS को नियंत्रित करता है। कम कैल्शियम सांद्रता का पता लगाने के लिए ऐसा प्रक्रिया येर्सिनिया पेस्टिस द्वारा उपयोग किए गए एलसीआरवी (लो कैल्शियम रिस्पांस) एंटीजन द्वारा चित्रित किया गया है, जिसका उपयोग कम कैल्शियम सांद्रता का पता लगाने और T3SS लगाव प्राप्त करने के लिए किया जाता है। पादप रोगज़नक़ों में एचआरपी प्रणाली समान प्रक्रिया के माध्यम से हार्पिन और रोगज़नक़ प्रभावक प्रोटीन को पौधों में इंजेक्ट करती है। इस स्राव प्रणाली को पहली बार यर्सिनिया पेस्टिस में खोजा गया था और दिखाया गया था कि विषाक्त पदार्थों को जीवाणु साइटोप्लाज्म से सीधे इसके होस्ट की कोशिकाओं के साइटोप्लाज्म में इंजेक्ट किया जा सकता है, न कि केवल बाह्य माध्यम में स्रावित किया जा सकता है।[8]
टाइप IV स्राव प्रणाली (T4SS या TFSS)
| T4SS | |||||||||
|---|---|---|---|---|---|---|---|---|---|
 टाइप IV स्राव प्रणाली | |||||||||
| Identifiers | |||||||||
| Symbol | T4SS | ||||||||
| Pfam | PF07996 | ||||||||
| InterPro | आईपीआर012991 | ||||||||
| SCOP2 | 1gl7 / SCOPe / SUPFAM | ||||||||
| TCDB | 3.A.7 | ||||||||
| OPM superfamily | 215 | ||||||||
| OPM protein | 3jqo | ||||||||
| |||||||||
यह जीवाणुओं की जीवाणु संयुग्मन मशीनरी, संयुग्मी पिली के अनुरूप है। यह डीएनए और प्रोटीन दोनों का परिवहन करने में सक्षम है। इसकी खोज एग्रोबैक्टीरियम ट्यूमेफैसिएन्स में की गई थी, जो इस प्रणाली का उपयोग टीआई प्लास्मिड के टी-डीएनए भाग को प्लांट होस्ट में प्रस्तुत करने के लिए करता है, जिसके परिणामस्वरूप प्रभावित क्षेत्र क्राउन पित्त (ट्यूमर) में विकसित होता है। हैलीकॉप्टर पायलॉरी गैस्ट्रिक उपकला कोशिकाओं में CagA पहुंचाने के लिए प्रकार IV स्राव प्रणाली का उपयोग करता है, जो गैस्ट्रिक कार्सिनोजेनेसिस से जुड़ा होता है।[9] बोर्डेटेला पर्टुसिस, काली खांसी का प्रेरक एजेंट, पर्टुसिस विष को आंशिक रूप से टाइप IV प्रणाली के माध्यम से स्रावित करता है। लीजियोनेला न्यूमोफिला, लीजियोनेलोसिस (लीजियोनेरेस रोग) का कारक एजेंट, प्रकार के IV B स्राव प्रणाली का उपयोग करता है, जिसे आईसीएम/डॉट ('अंतःकोशिकीय गुणन/ऑर्गेनेल में दोष) के रूप में जाना जाता है। टी'रैफिकिंग जीन) प्रणाली, बहुत से जीवाणु प्रभावक प्रोटीन को उसके यूकेरियोटिक होस्ट में स्थानांतरित करने के लिए।[10] प्रोटोटाइपिक प्रकार IV A स्राव प्रणाली एग्रोबैक्टीरियम टूमफेशियन्स का VirB कॉम्प्लेक्स है।[11]
इस वर्ग के प्रोटीन सदस्य प्रकार IV स्राव प्रणाली के कॉम्पोनेन्ट हैं। वह परमाणु रिसेप्टर या क्रिया के प्रक्रिया के माध्यम से मैक्रोमोलेक्युलस के अंतःकोशिकीय स्थानांतरण में मध्यस्थता करते हैं, जो पैतृक रूप से जीवाणु संयुग्मन मशीनरी से संबंधित है।[12][13]
फ़ंक्शन
संक्षेप में, टाइप IV स्राव प्रणाली (T4SS), वह सामान्य प्रक्रिया है जिसके द्वारा जीवाणु कोशिकाएँ मैक्रोमोलेक्यूल्स का स्राव करती हैं या ग्रहण करती हैं। उनका स्पष्ट प्रक्रिया अज्ञात रहता है। T4SS ग्राम नकारात्मक बैक्टीरिया पर एन्कोड किया गया है। बैक्टीरिया में ग्राम-नकारात्मक संयुग्मी तत्व। T4SS कोशिका आवरण-फैले हुए कॉम्प्लेक्स हैं या दूसरे शब्दों में 11-13 कोर प्रोटीन हैं जो चैनल बनाते हैं जिसके माध्यम से डीएनए और प्रोटीन दाता कोशिका के साइटोप्लाज्म से यात्रा कर सकते हैं। प्राप्तकर्ता कोशिका के साइटोप्लाज्म में। इसके अतिरिक्त, T4SS प्राकृतिक परिवर्तन (बैक्टीरिया) के दौरान माध्यम से डीएनए लेने के साथ-साथ सीधे होस्ट कोशिकाओं में विषाणु कारक प्रोटीन का स्राव भी करता है, जो इस मैक्रोमोलेक्युलर स्राव प्रक्रिया की बहुमुखी प्रतिभा को दर्शाता है।[14]
संरचना
जैसा कि उपरोक्त चित्र में दिखाया गया है, विशेष रूप से ट्रैसी में तीन हेलिक्स बंडल और लूज़ गोलाकार उपांग होता है।[13]
इंटरैक्शन
T4SS में दो प्रभावकारी प्रोटीन होते हैं: पहला, ATS-1, जो एनाप्लाज्मा ट्रांसलोकेटेड सब्सट्रेट 1 के लिए है, और दूसरा अंकिरिन रिपीट, जो अंकिरिन दोहराएँ डोमेन-युक्त प्रोटीन A के लिए है। इसके अतिरिक्त, T4SS कपलिंग प्रोटीन VirD4 हैं, जो VirE2 से बंधते हैं।[15]
प्रकार V स्राव प्रणाली (T5SS)
इसे ऑटोट्रांसपोर्टर प्रणाली भी कहा जाता है,[16] इस प्रकार V स्राव में आंतरिक मेम्ब्रेन को पार करने के लिए Sec प्रणाली का उपयोग सम्मिलित होता है। जो प्रोटीन इस मार्ग का उपयोग करते हैं उनमें अपने C-टर्मिनस के साथ बीटा-बैरल बनाने की क्षमता होती है जो कि बाहरी मेम्ब्रेन में प्रवेश करती है, जिससे शेष पेप्टाइड (यात्री डोमेन) को कोशिका के बाहर तक पहुंचने की अनुमति मिलती है। अधिकांशतः, ऑटोट्रांसपोर्टर्स को साफ़ कर दिया जाता है, जिससे बीटा-बैरल डोमेन बाहरी मेम्ब्रेन में रह जाता है और यात्री डोमेन मुक्त हो जाता है। कुछ शोधकर्ताओं का मानना है कि ऑटोट्रांसपोर्टर्स के अवशेषों ने पोरिन (प्रोटीन) को जन्म दिया जो समान बीटा-बैरल संरचनाएं बनाते हैं। इस स्राव प्रणाली का उपयोग करने वाले ऑटोट्रांसपोर्टर का सामान्य उदाहरण ट्रिमेरिक ऑटोट्रांसपोर्टर एडेसिन्स (टीएए)टीएए) है।[17]
टाइप VI स्राव प्रणाली (T6SS)
टाइप VI स्राव प्रणालियों की पहचान मूल रूप से 2006 में हार्वर्ड मेडिकल स्कूल (बोस्टन, यूएसए) में जॉन मेकलानोस के समूह द्वारा दो जीवाणु रोगजनकों, विब्रियो कॉलेरी और स्यूडोमोनास एरुगिनोसा में की गई थी।[18][19] इनकी पहचान तब की गई जब विब्रियो कॉलेरी में एचसीपी और वीआरजीजी जीन में उत्परिवर्तन के कारण विषाणु और रोगजनकता में कमी आई। तब से, टाइप VI स्राव प्रणालियाँ सभी प्रोटीओबैक्टीरियल जीनोम के चौथाई में पाई गई हैं, जिनमें जानवर, पौधे, मानव रोगजनकों के साथ-साथ मिट्टी, पर्यावरण या समुद्री बैक्टीरिया भी सम्मिलित हैं।[20][21] जबकि टाइप VI स्राव के अधिकांश प्रारंभिक अध्ययन उच्च जीवों के रोगजनन में इसकी भूमिका पर केंद्रित थे, वर्तमान के अध्ययनों ने सरल यूकेरियोटिक शिकारियों के खिलाफ रक्षा में व्यापक शारीरिक भूमिका और अंतर-बैक्टीरिया इंटरैक्शन में इसकी भूमिका का सुझाव दिया है।[22][23] टाइप VI स्राव प्रणाली जीन समूहों में 15 से लेकर 20 से अधिक जीन होते हैं, जिनमें से दो, एचसीपी और वीजीआरजी, को प्रणाली के लगभग सार्वभौमिक रूप से स्रावित सब्सट्रेट के रूप में दिखाया गया है। इस प्रणाली में इन और अन्य प्रोटीनों का संरचनात्मक विश्लेषण टी4 फ़ेज़ के टेल स्पाइक से उल्लेखनीय समानता रखता है, और प्रणाली की गतिविधि को कार्यात्मक रूप से फ़ेज़ संक्रमण के समान माना जाता है।[24]
बाहरी मेम्ब्रेन वेसिक्लए का निकलना
ऊपर सूचीबद्ध मल्टीप्रोटीन कॉम्प्लेक्स के उपयोग के अतिरिक्त, ग्राम-नेगेटिव बैक्टीरिया के पास सामग्री प्रयुक्त करने की और विधि होती है: बैक्टीरिया की बाहरी मेम्ब्रेन वेसिक्लए का निर्माण।[25] बाहरी मेम्ब्रेन के भाग चुटकी बजाते हैं, जिससे लिपोपॉलीसेकेराइड-समृद्ध लिपिड बाइलेयर से बनी नैनो-स्केल गोलाकार संरचनाएं बनती हैं, जो पेरिप्लास्मिक सामग्रियों को घेरती हैं, और पर्यावरण में हेरफेर करने या होस्ट-रोगज़नक़ इंटरफ़ेस पर आक्रमण करने के लिए मेम्ब्रेन वेसिकल तस्करी के लिए तैनात की जाती हैं। बहुत से जीवाणु प्रजातियों के वेसिक्लए में विषाणु कारक पाए गए हैं, कुछ में इम्यूनोमॉड्यूलेटरी प्रभाव होते हैं, और कुछ सीधे होस्ट कोशिकाओं से चिपक सकते हैं और उन्हें नशीला बना सकते हैं। वेसिक्लए की रिहाई को तनाव की स्थिति के लिए सामान्य प्रतिक्रिया के रूप में प्रदर्शित किया गया है, कार्गो प्रोटीन लोड करने की प्रक्रिया चयनात्मक प्रतीत होती है।[26]
ग्राम-पॉजिटिव बैक्टीरिया में
कुछ स्टैफिलोकोकस और स्ट्रेप्टोकोकस प्रजातियों में, सहायक स्रावी प्रणाली अत्यधिक दोहराव वाले आसंजन ग्लाइकोप्रोटीन के निर्यात को संभालती है।
यह भी देखें
- जीवाणु प्रभावकारक प्रोटीन
- जीवाणु बाहरी मेम्ब्रेन वेसिकल
- होस्ट-रोगज़नक़ इंटरफ़ेस
- मेम्ब्रेन वेसिकल की तस्करी
- रहस्यवाद
- सेक्रेट्री प्रोटीन
- सेक्रेटर स्टेटस
संदर्भ
- ↑ Lee JS, Jeremic A, Shin L, Cho WJ, Chen X, Jena BP (July 2012). "Neuronal porosome proteome: Molecular dynamics and architecture". Journal of Proteomics. 75 (13): 3952–62. doi:10.1016/j.jprot.2012.05.017. PMC 4580231. PMID 22659300.
- ↑ Anderson LL (2006). "Discovery of the 'porosome'; the universal secretory machinery in cells". Journal of Cellular and Molecular Medicine. 10 (1): 126–31. doi:10.1111/j.1582-4934.2006.tb00294.x. PMC 3933105. PMID 16563225.
- ↑ Nickel W, Seedorf M (2008). "यूकेरियोटिक कोशिकाओं की कोशिका सतह तक प्रोटीन परिवहन के अपरंपरागत तंत्र". Annual Review of Cell and Developmental Biology. 24: 287–308. doi:10.1146/annurev.cellbio.24.110707.175320. PMID 18590485.
- ↑ McNeil PL, Steinhardt RA (2003). "Plasma membrane disruption: repair, prevention, adaptation". Annual Review of Cell and Developmental Biology. 19: 697–731. doi:10.1146/annurev.cellbio.19.111301.140101. PMID 14570587.
- ↑ Chirico WJ (October 2011). "एक वैकल्पिक गैर-शास्त्रीय स्रावी मार्ग के रूप में गैर-घातक ऑन्कोटिक छिद्रों के माध्यम से प्रोटीन जारी होता है". BMC Cell Biology. 12: 46. doi:10.1186/1471-2121-12-46. PMC 3217904. PMID 22008609.
- ↑ Wooldridge, K, ed. (2009). Bacterial Secreted Proteins: Secretory Mechanisms and Role in Pathogenesis. Caister Academic Press. ISBN 978-1-904455-42-4.[page needed]
- ↑ Boyd CD, Smith TJ, El-Kirat-Chatel S, Newell PD, Dufrêne YF, O'Toole GA (August 2014). "लैपजी-निर्भर दरार, बायोफिल्म निर्माण और कोशिका सतह स्थानीयकरण के लिए आवश्यक स्यूडोमोनस फ्लोरेसेंस बायोफिल्म चिपकने वाला लैपा की संरचनात्मक विशेषताएं". Journal of Bacteriology. 196 (15): 2775–88. doi:10.1128/JB.01629-14. PMC 4135675. PMID 24837291.
- ↑ Salyers, A. A. & Whitt, D. D. (2002). Bacterial Pathogenesis: A Molecular Approach, 2nd ed., Washington, D.C.: ASM Press. ISBN 1-55581-171-X[page needed]
- ↑ Hatakeyama M, Higashi H (December 2005). "Helicobacter pylori CagA: a new paradigm for bacterial carcinogenesis". Cancer Science. 96 (12): 835–43. doi:10.1111/j.1349-7006.2005.00130.x. PMID 16367902. S2CID 5721063.
- ↑ Cascales E, Christie PJ (November 2003). "बहुमुखी जीवाणु प्रकार IV स्राव प्रणाली". Nature Reviews. Microbiology. 1 (2): 137–49. doi:10.1038/nrmicro753. PMC 3873781. PMID 15035043.
- ↑ Christie PJ, Atmakuri K, Krishnamoorthy V, Jakubowski S, Cascales E (2005). "जीवाणु प्रकार IV स्राव प्रणालियों की जैवजनन, वास्तुकला और कार्य". Annual Review of Microbiology. 59: 451–85. doi:10.1146/annurev.micro.58.030603.123630. PMC 3872966. PMID 16153176.
- ↑ Christie PJ (November 2004). "Type IV secretion: the Agrobacterium VirB/D4 and related conjugation systems". Biochimica et Biophysica Acta (BBA) - Molecular Cell Research. 1694 (1–3): 219–34. doi:10.1016/j.bbamcr.2004.02.013. PMC 4845649. PMID 15546668.
- ↑ 13.0 13.1 Yeo HJ, Yuan Q, Beck MR, Baron C, Waksman G (December 2003). "Structural and functional characterization of the VirB5 protein from the type IV secretion system encoded by the conjugative plasmid pKM101". Proceedings of the National Academy of Sciences of the United States of America. 100 (26): 15947–52. Bibcode:2003PNAS..10015947Y. doi:10.1073/pnas.2535211100. JSTOR 3149111. PMC 307673. PMID 14673074.
- ↑ Lawley TD, Klimke WA, Gubbins MJ, Frost LS (July 2003). "एफ कारक संयुग्मन एक वास्तविक प्रकार IV स्राव प्रणाली है". FEMS Microbiology Letters. 224 (1): 1–15. doi:10.1016/S0378-1097(03)00430-0. PMID 12855161.
- ↑ Rikihisa Y, Lin M, Niu H (September 2010). "अनिवार्य इंट्रासेल्युलर जीवाणु एनाप्लाज्मा फागोसाइटोफिलम में टाइप IV स्राव". Cellular Microbiology. 12 (9): 1213–21. doi:10.1111/j.1462-5822.2010.01500.x. PMC 3598623. PMID 20670295.
- ↑ Thanassi DG, Stathopoulos C, Karkal A, Li H (2005). "Protein secretion in the absence of ATP: the autotransporter, two-partner secretion and chaperone/usher pathways of gram-negative bacteria (review)". Molecular Membrane Biology. 22 (1–2): 63–72. doi:10.1080/09687860500063290. PMID 16092525. S2CID 2708575.
- ↑ Gerlach RG, Hensel M (October 2007). "Protein secretion systems and adhesins: the molecular armory of Gram-negative pathogens". International Journal of Medical Microbiology. 297 (6): 401–15. doi:10.1016/j.ijmm.2007.03.017. PMID 17482513.
- ↑ Pukatzki S, Ma AT, Sturtevant D, Krastins B, Sarracino D, Nelson WC, Heidelberg JF, Mekalanos JJ (January 2006). "डिक्टियोस्टेलियम होस्ट मॉडल सिस्टम का उपयोग करके विब्रियो कॉलेरी में एक संरक्षित जीवाणु प्रोटीन स्राव प्रणाली की पहचान". Proceedings of the National Academy of Sciences of the United States of America. 103 (5): 1528–33. Bibcode:2006PNAS..103.1528P. doi:10.1073/pnas.0510322103. JSTOR 30048406. PMC 1345711. PMID 16432199.
- ↑ Mougous JD, Cuff ME, Raunser S, Shen A, Zhou M, Gifford CA, Goodman AL, Joachimiak G, Ordoñez CL, Lory S, Walz T, Joachimiak A, Mekalanos JJ (June 2006). "स्यूडोमोनास एरुगिनोसा का विषाणु स्थान एक प्रोटीन स्राव तंत्र को कूटबद्ध करता है". Science. 312 (5779): 1526–30. Bibcode:2006Sci...312.1526M. doi:10.1126/science.1128393. PMC 2800167. PMID 16763151.
- ↑ Bingle LE, Bailey CM, Pallen MJ (February 2008). "Type VI secretion: a beginner's guide" (PDF). Current Opinion in Microbiology. 11 (1): 3–8. doi:10.1016/j.mib.2008.01.006. PMID 18289922.
- ↑ Cascales E (August 2008). "प्रकार VI स्राव टूलकिट". EMBO Reports. 9 (8): 735–41. doi:10.1038/embor.2008.131. PMC 2515208. PMID 18617888.
- ↑ Schwarz S, Hood RD, Mougous JD (December 2010). "What is type VI secretion doing in all those bugs?". Trends in Microbiology. 18 (12): 531–7. doi:10.1016/j.tim.2010.09.001. PMC 2991376. PMID 20961764.
- ↑ Coulthurst SJ (2013). "टाइप VI स्राव प्रणाली - एक व्यापक और बहुमुखी कोशिका लक्ष्यीकरण प्रणाली". Research in Microbiology. 164 (6): 640–54. doi:10.1016/j.resmic.2013.03.017. PMID 23542428.
- ↑ Silverman JM, Brunet YR, Cascales E, Mougous JD (2012). "प्रकार VI स्राव प्रणाली की संरचना और विनियमन". Annual Review of Microbiology. 66: 453–72. doi:10.1146/annurev-micro-121809-151619. PMC 3595004. PMID 22746332.
- ↑ Kuehn MJ, Kesty NC (November 2005). "जीवाणु बाहरी झिल्ली पुटिकाएं और मेजबान-रोगज़नक़ बातचीत". Genes & Development. 19 (22): 2645–55. doi:10.1101/gad.1299905. PMID 16291643.
- ↑ McBroom AJ, Kuehn MJ (January 2007). "ग्राम-नेगेटिव बैक्टीरिया द्वारा बाहरी झिल्ली पुटिकाओं का निकलना एक नवीन आवरण तनाव प्रतिक्रिया है". Molecular Microbiology. 63 (2): 545–58. doi:10.1111/j.1365-2958.2006.05522.x. PMC 1868505. PMID 17163978.
- ↑ Z. Esna Ashari, N. Dasgupta, K. Brayton & S. Broschat, “An optimal set of features for predicting type IV secretion system effector proteins for a subset of species based on a multi-level feature selection approach”, PLOS ONE Journal, 2018, 13, e0197041. (doi.org/10.1371/journal.pone.0197041.)
अग्रिम पठन
- Alberts B, Johnson A, Lewis J, Raff M, Roberts K, Walter P, eds. (2002). "Search: Secretion". Molecular Biology of the Cell (4th ed.). New York: Garland Science. ISBN 978-0-8153-3218-3.
- White D (2000). The Physiology and Biochemistry of Prokaryotes (2nd ed.). Oxford University Press. ISBN 978-0-19-512579-5.
- Avon D. "Home page". Cells alive!.
बाहरी संबंध
- Secretions at the US National Library of Medicine Medical Subject Headings (MeSH)
- T5SS / Autotransporter illustration at Uni Münster