द्विध्रुवी विद्युत् रसायन
द्विध्रुवी इलेक्ट्रोकैमिस्ट्री इलेक्ट्रोकैमिस्ट्री में विद्युत क्षेत्रों में विद्युत चालन वस्तुओं के ढांकता हुआ ध्रुवीकरण पर आधारित एक घटना है। दरअसल, यह ध्रुवीकरण सब्सट्रेट के दो छोरों के बीच एक संभावित अंतर उत्पन्न करता है जो वस्तु के आयाम से गुणा किए गए विद्युत क्षेत्र मान के बराबर होता है। यदि यह संभावित अंतर पर्याप्त महत्वपूर्ण है, तो वस्तु के छोर पर रेडॉक्स प्रतिक्रियाएं उत्पन्न हो सकती हैं, एक छोर पर ऑक्सीकरण दूसरे छोर पर कटौती के साथ-साथ होगा।[1][2] पीएच सूचक समाधान वाली वजन नाव में प्लैटिनम तार से युक्त एक सरल प्रयोगात्मक सेटअप में, दो इलेक्ट्रोडों में 30 वी वोल्टेज तार के एक छोर (कैथोड) पर पानी की कमी और पीएच वृद्धि (ओएच) का कारण बनेगा।−गठन) और एनोडिक सिरे पर पानी का ऑक्सीकरण और पीएच में कमी। द्विध्रुवी इलेक्ट्रोड के ध्रुव भी स्वयं को लागू विद्युत क्षेत्र के साथ संरेखित करते हैं।[3]
बुनियादी बातें
जब एक विद्युत प्रवाहकीय इलेक्ट्रोड को सीधे कनेक्शन के बिना, एक ही इलेक्ट्रोलाइट में, एक इलेक्ट्रोकैमिस्ट्री सेल में एनोड और कैथोड के बीच पर्याप्त वोल्टेज के साथ रखा जाता है; इलेक्ट्रोड दोनों चरम पर एक साथ कैथोडिक और एनोडिक प्रतिक्रिया का अनुभव करेगा। इसका मतलब है, प्रवाहकीय इलेक्ट्रोड द्विध्रुवी इलेक्ट्रोड (बीपीई) बन जाएगा; आयनिक चालकता (ठोस अवस्था) इलेक्ट्रोलाइट के संपर्क में एक विद्युत प्रवाहकीय सामग्री जिसका बिजली आपूर्ति के साथ कोई सीधा इलेक्ट्रॉनिक संबंध नहीं है, जो इसके दोनों सिरों (ध्रुवों) पर इलेक्ट्रोकेमिकल (कमी और ऑक्सीकरण) प्रतिक्रियाओं को बढ़ावा देता है; जिसका अर्थ है कि यह एक ही समय में कैथोड और एनोड है।[4][5] ऐसा इसके कारण होता है:
केस (ए)
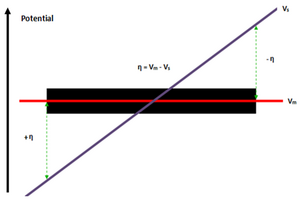
विद्युत प्रवाहकीय इलेक्ट्रोड (V) के बीच संभावित अंतर (η)।m) और इलेक्ट्रोलाइट (वीs) एक संभावित ग्रेडिएंट का कारण बनता है जो बीपीई-इलेक्ट्रोलाइट इंटरफ़ेस में बाद में वितरित होता है, जिसमें एक चरम में उच्चतम क्षमता (एनोड +η) होती है और दूसरे चरम में सबसे कम क्षमता (कैथोड -η) होती है।[5]इलेक्ट्रोलाइट क्षमता की तुलना (वीs) ढाल/बूंद; इलेक्ट्रोड क्षमता (वीm) बीपीई ध्रुवों के बीच नहीं बदलता है, यह इलेक्ट्रोड की उच्च चालकता के कारण होता है जो 10 से अधिक हैअधिकांश स्टील मिश्रधातुओं के लिए 6S/m, जल आयनाइज़र के लिए 5.5 μS/m और समुद्री जल के लिए 5 S/m की सीमा में समाधान चालकता की तुलना में।[5]
केस (बी)
बीपीई में करंट प्रवाहित होता है क्योंकि यह इलेक्ट्रोलाइट की तुलना में कम प्रतिरोधी करंट पथ प्रदान करता है। जैसा कि चित्र में दिखाया गया है; एनोड से धारा (डी/ब्लू) में प्रवेश करने के परिणामस्वरूप, पक्ष डी कैथोडिक रूप से ध्रुवीकृत हो जाएगा (संभावना अधिक नकारात्मक हो जाएगी)। दूसरी ओर, जिस तरफ (बी/रेड) से करंट निकल रहा है, वह एनोडिक रूप से ध्रुवीकृत हो जाएगा (क्षमता अधिक सकारात्मक हो जाएगी) और संक्षारित हो जाएगी। यह ध्रुवीकरण के कारण होता है जो वर्तमान दिशा के विपरीत होता है।[6] यह सिद्धांत लगभग सभी क्लासिकों में स्वीकृत है [7] और हाल की कैथोडिक सुरक्षा पुस्तकें,[8] और सामग्री संरक्षण और प्रदर्शन प्रकाशन और मानकों के लिए एसोसिएशन,[9] पाइपलाइनों और विभिन्न संरचनाओं (जैसे कैथोडिक रूप से संरक्षित या असुरक्षित संरचनाएं, रेलवे और उच्च वोल्टेज प्रत्यक्ष धारा) के बीच प्रत्यक्ष वर्तमान हस्तक्षेप के कारण होने वाले क्षरण और कोटिंग विघटन की व्याख्या के रूप में। ऐसा इसलिए क्योंकि यह अत्यधिक प्रतिरोधी, विषम वातावरण में बड़े पैमाने की संरचनाओं के लिए अधिक उपयुक्त है जहां समाधान क्षमता (वीs) कम महत्वपूर्ण भूमिका निभाता है और प्रतिक्रियाएँ मुख्य रूप से केवल ध्रुवों (जहाँ से धारा प्रवेश करती है और निकलती है) पर केंद्रित होती है।[7]
केस (सी)
बीपीई के प्रत्येक ध्रुव पर संभावित अंतर (जो विद्युत रासायनिक प्रतिक्रियाओं के लिए पर्याप्त हो भी सकता है और नहीं भी)।[4]
ध्यान दें कि समाधान क्षमता सीधे किसी शक्ति स्रोत (जैसे पोटेंशियोस्टैट्स) द्वारा नियंत्रित नहीं होती है क्योंकि यह समाधान संरचना पर भी निर्भर करती है। इसलिए, समाधान में प्रजातियों को कम करने के लिए इलेक्ट्रॉनों को स्थानांतरित करने के लिए, कार्यशील इलेक्ट्रोड की क्षमता को समाधान में एक इलेक्ट्रोएक्टिव अणु की तुलना में अधिक नकारात्मक मूल्य पर सेट करने की आवश्यकता होती है, और फिर - कैनेटीक्स के आधार पर - इलेक्ट्रॉन स्थानांतरित हो सकते हैं। इसी तरह, ऑक्सीकरण प्रतिक्रियाएं होती हैं।[4]साथ ही, ओम के नियम|ओम के नियम के अनुसार, विद्युत क्षेत्र और समाधान क्षमता (Vs) बढ़ते समाधान प्रतिरोधकता और बाहरी सर्किट पर लागू धारा के साथ बढ़ेगा।[6] [[File:Bipolar electrochemistry, 420 SS BPE in 0.1M NaCl Solution.mpg|center|thumb|464x464px|420 Satinless Steel sample in bipolar setup in 0.1M NaCl Solution. See [[:File:Bipolar Cell, Side.png and [[:File:Bipolar Cell, top.pngसेटअप की ड्राइंग के लिए[6]]]
उपयोग
द्विध्रुवी इलेक्ट्रोकैमिस्ट्री की घटना 1970 के दशक से ज्ञात है[10] और उद्योग में कुछ इलेक्ट्रोलाइटिक रिएक्टरों में उपयोग किया जाता है। इस अवधारणा के प्रति वैज्ञानिक समुदाय की रुचि बहुत अधिक बढ़ गई है क्योंकि मार्टिन फ्लेशमैन और सहकर्मियों ने प्रदर्शित किया है कि माइक्रोमीटर आकार के द्विध्रुवी इलेक्ट्रोड का उपयोग करके पानी का विभाजन संभव है।[11] हाल ही में, असममित सूक्ष्म और नैनो-संरचनाओं के संश्लेषण जैसे डोमेन में कई अनुप्रयोग सामने आए हैं[12][13] विश्लेषणात्मक रसायनशास्त्र[14][15][16] भौतिक विज्ञान,[17][18] माइक्रोइलेक्ट्रॉनिक्स [19] और सूक्ष्म वस्तु प्रणोदन[20][21] विकसित किया गया है।
संदर्भ
- ↑ G. Loget; A. Kuhn (2011). "द्विध्रुवी इलेक्ट्रोकैमिस्ट्री का उपयोग करके सूक्ष्म और नैनोवर्ल्ड को आकार देना और उसकी खोज करना". Analytical and Bioanalytical Chemistry. 400 (6): 1691–704. doi:10.1007/s00216-011-4862-1. PMID 21455656. S2CID 44000438.
- ↑ F. Mavré; R. K. Anand; D. R. Laws; K.-F. Chow; B.-Y. Chang; J. A. Crooks; R. M. Crooks (2010). "Feature Bipolar Electrodes: A Useful Tool for Concentration, Separation, and Detection of Analytes in Microelectrochemical Systems". Anal. Chem. 82 (21): 8766–74. doi:10.1021/ac101262v. PMID 20815405.
- ↑ Fosdick, S. E.; Knust, K. N.; Scida, K.; Crooks, R. M. (2013). "द्विध्रुवी इलेक्ट्रोकैमिस्ट्री". Angew. Chem. Int. Ed. 52 (40): 10438–10456. doi:10.1002/anie.201300947. PMID 23843205.
- ↑ 4.0 4.1 4.2 Mavré, François; Anand, Robbyn K.; Laws, Derek R.; Chow, Kwok-Fan; Chang, Byoung-Yong; Crooks, John A.; Crooks, Richard M. (2010-09-03). "Bipolar Electrodes: A Useful Tool for Concentration, Separation, and Detection of Analytes in Microelectrochemical Systems". Analytical Chemistry. 82 (21): 8766–8774. doi:10.1021/ac101262v. ISSN 0003-2700.
- ↑ 5.0 5.1 5.2 Ulrich, Christian; Andersson, Olof; Nyholm, Leif; Björefors, Fredrik (2008-04-07). "द्विध्रुवी इलेक्ट्रोड पर आणविक ग्रेडियेंट का गठन". Angewandte Chemie. 120 (16): 3076–3078. doi:10.1002/ange.200705824. ISSN 0044-8249.
- ↑ 6.0 6.1 6.2 Abdalrhaman Saeed (2017). "Application of Bipolar Electrochemistry for Corrosion Screening of Type 420 Stainless Steel in Sodium Chloride Solution" (in English). doi:10.13140/RG.2.2.31999.71845.
{{cite journal}}: Cite journal requires|journal=(help) - ↑ 7.0 7.1 Bohnes, H.; Richter, B. (1997), "Cathodic Protection of Ships", Handbook of Cathodic Corrosion Protection, Elsevier, pp. 391–414, retrieved 2023-02-12
- ↑ Ahmad, Zaki (2006), "CORROSION PREVENTION BY DESIGN", Principles of Corrosion Engineering and Corrosion Control, Elsevier, pp. 438–478, retrieved 2023-02-12
- ↑ Winston., Revie, R. (2011). उहलिग की संक्षारण पुस्तिका।. Wiley. ISBN 978-1-118-11003-4. OCLC 927504000.
{{cite book}}: CS1 maint: multiple names: authors list (link) - ↑ Goodridge, F.; King, C. J. H.; Wright, A. R. (1977-04-01). "द्विध्रुवी पैक-बेड इलेक्ट्रोड का व्यवहार". Electrochimica Acta (in English). 22 (4): 347–352. doi:10.1016/0013-4686(77)85085-8. ISSN 0013-4686.
- ↑ M. Fleischmann; J. Ghoroghchian; D. Rolison; S. Pons (1986). "गोलाकार अल्ट्रामाइक्रोइलेक्ट्रोड के फैलाव का विद्युत रासायनिक व्यवहार". J. Phys. Chem. 90 (23): 6392. doi:10.1021/j100281a065. Archived from the original on September 23, 2017.
- ↑ G. Loget; V. Lapeyre; P. Garrigue; C. Warakulwit; J. Limtrakul; M.-H. Delville; A. Kuhn (2011). "जानूस-प्रकार की कार्बन ट्यूबों के संश्लेषण के लिए बहुमुखी प्रक्रिया". Chem. Mater. 23 (10): 2595. doi:10.1021/cm2001573.
- ↑ C. Warakulwit; T. Nguyen; J. Majimel; M.-H. Delville; V. Lapeyre; P. Garrigue; V.Ravaine; J. Limtrakul; A. Kuhn (2008). "द्विध्रुवी इलेक्ट्रोकैमिस्ट्री द्वारा असममित कार्बन नैनोट्यूब". Nano Lett. 8 (2): 500–4. Bibcode:2008NanoL...8..500W. doi:10.1021/nl072652s. PMID 18189438.
- ↑ K.-F. Chow; B.-Y. Chang; B. A. Zaccheo; F. Mavré; R. M. Crooks (2010). "एजी बाइपोलर इलेक्ट्रोड के इलेक्ट्रोडिसोल्यूशन पर आधारित एक सेंसिंग प्लेटफॉर्म". J. Am. Chem. Soc. 132 (27): 9228. doi:10.1021/ja103715u. PMID 20557051.
- ↑ Hlushkou D, Perdue RK, Dhopeshwarkar R, Crooks RM, Tallarek U (2009). "एम्बेडेड द्विध्रुवी इलेक्ट्रोड के साथ माइक्रोचैनल में ध्यान केंद्रित करने वाला विद्युत क्षेत्र ढाल". Lab Chip. 9 (13): 1903. doi:10.1039/b822404h. PMID 19532966.
- ↑ Ulrich C, Andersson O, Nyholm L, Björefors F (2009). "द्विध्रुवी पैटर्निंग के लिए इच्छित इलेक्ट्रोड पर संभावित और वर्तमान घनत्व वितरण". Anal. Chem. 81 (1): 453–459. doi:10.1021/ac801871c. PMID 19125451.
- ↑ Ramakrishnan S, Shannon C (2010). "द्विध्रुवी इलेक्ट्रोकैमिस्ट्री का उपयोग करके ठोस-अवस्था सामग्री का प्रदर्शन". Langmuir. 26 (7): 4602–4606. doi:10.1021/la100292u. PMID 20229995.
- ↑ Abdalrhaman Saeed (2017). "Application of Bipolar Electrochemistry for Corrosion Screening of Type 420 Stainless Steel in Sodium Chloride Solution" (in English). doi:10.13140/RG.2.2.31999.71845.
{{cite journal}}: Cite journal requires|journal=(help) - ↑ J. C. Bradley; H. M. Chen; J. Crawford; J. Eckert; K. Ernazarova; T. Kurzeja; M. Lin; M. McGee; W. Nadler; S. G. Stephens (1997). "निर्देशित विद्युत रासायनिक वृद्धि का उपयोग करके धातु के कणों के बीच विद्युत संपर्क बनाना". Nature. 389 (6648): 268. Bibcode:1997Natur.389..268B. doi:10.1038/38464. S2CID 4329476.
- ↑ G. Loget; A. Kuhn (2010). "गतिशील द्विध्रुवी स्व-पुनर्जनन द्वारा सूक्ष्म वस्तुओं का प्रणोदन". J. Am. Chem. Soc. 132 (45): 15918–9. doi:10.1021/ja107644x. PMID 20964295.
- ↑ G. Loget; A. Kuhn (2011). "संचालन करने वाली वस्तुओं की विद्युत क्षेत्र-प्रेरित रासायनिक गति". Nature Communications. 2 (11): 535. Bibcode:2011NatCo...2E.535L. doi:10.1038/ncomms1550. PMID 22086336.