क्लॉस्ट्रिडिओइड्स डिफिसाइल
| colspan=2 style="text-align: center; background-color: rgb(220,235,245)" | क्लॉस्ट्रिडिओइड्स डिफिसाइल | |
|---|---|

| |
| C. difficile colonies on a blood agar plate | |
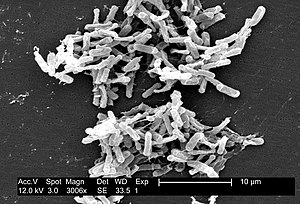
| |
| Electron micrograph of the bacterium | |
| colspan=2 style="min-width:15em; text-align: center; background-color: rgb(220,235,245)" | Scientific classification | |
| Domain: | Bacteria |
| Phylum: | Bacillota |
| Class: | Clostridia |
| Order: | Eubacteriales |
| Family: | Peptostreptococcaceae |
| Genus: | Clostridioides |
| Species: | C. difficile
|
| colspan=2 style="text-align: center; background-color: rgb(220,235,245)" | Binomial name | |
| Clostridioides difficile (Hall & O'Toole, 1935) Lawson & Rainey, 2016
| |
| colspan=2 style="text-align: center; background-color: rgb(220,235,245)" | Synonyms | |
क्लोस्ट्रीडियोइड्स डिफिसाइल जिसका पर्यायवाची टैक्सोनॉमी हैं, क्लोस्ट्रीडियम डिफिसाइल एक प्रकार का जीवाणु होता है जो गंभीर डायरिया संक्रमण उत्पन्न करने के लिए जाना जाता है, और इसकी अधिकता कोलन कैंसर का कारण भी बन सकता है।[4][5] इसे सी डिफिसाइल या सी. अंतर के नाम से भी जाना जाता है।[6]
क्लॉस्ट्रिडिओइड्स डिफिसाइल वर्तमान समय में एक महत्वपूर्ण व उभरता हुआ मानव रोगज़नक़ है, मुख्य रूप से रोग नियंत्रण और रोकथाम केंद्रों के अनुसार, 2017 में संयुक्त राज्य अमेरिका में अस्पताल में भर्ती मरीजों के 223,900 मामले और 12,800 मौतें हुई थी।[7] चूंकि सी डिफिसाइल को सामान्य रूप से अस्पताल और एंटीबायोटिक से जुड़े रोगज़नक़ के रूप में जाना जाता है, इसके अधिक से अधिक एक तिहाई संक्रमणों का पता अस्पतालों में संक्रमित व्यक्ति से संचरण के कारण लगाया जा सकता है, [8] और केवल कुछ ही एंटीबायोटिक्स क्लॉस्ट्रिडिओइड्स डिफिसाइल संक्रमण के विकास के बढ़ते जोखिम से सीधे तौर पर जुड़े हुए हैं। सी डिफिसाइल संक्रमण (सीडीआई), अर्थात् क्लिंडामाइसिन , फ़्लुओरोक़ुइनोलोनेस और सेफैलोस्पोरिन [9][10] अधिकांश संक्रमण अस्पतालों के बाहर से होते हैं, और अधिकांश एंटीबायोटिक दवाओं में संक्रमण का खतरा कई गैर-एंटीबायोटिक खतरों के कारकों के समान होता है, जैसे कि रेचक का उपयोग करना और एनीमा प्राप्त करना इसके प्रमुख उदाहरण हैं।[11]
क्लॉस्ट्रिडिओइड्स डिफिसाइल रोग उत्पन्न किए बिना भी मानव की बड़ी आंत में स्थापित हो सकता है।[12] चूंकि प्रारंभिक अनुमानों से संकेत मिलता है कि सी डिफिसाइल 2-5% वयस्क आबादी में उपस्थित था,[13] वर्तमान समय में कई शोधों के अंतर्गत यह संकेत मिला है कि उपनिवेशीकरण असंबद्ध डायरिया संबंधी बीमारियों के इतिहास से निकटता से जुड़ा हुआ है, जैसे कि खाद्य विषाक्तता या रेचक दुरुपयोग इसका प्रमुख उदाहरण हैं।[14] जिन व्यक्तियों में गैस्ट्रोइंटेस्टाइनल गड़बड़ी का कोई इतिहास नहीं है, उनके स्पर्शोन्मुख वाहक बनने की संभावना नहीं है। इन वाहकों को संक्रमण का एक प्रमुख भंडार माना जाता है।[15]
वर्गीकरण
इस प्रजाति को 2016 में जीनस क्लोस्ट्रीडियम से क्लॉस्ट्रिडिओइड्स में स्थानांतरित किया गया था, इस प्रकार इसे द्विपद क्लोस्ट्रीडियोइड्स डिफिसाइल दिया गया।[16][17][18] यह नया नाम इस प्रजाति और क्लोस्ट्रीडियम जीनस के सदस्यों के बीच वर्गीकरण संबंधी अंतर को दर्शाता है, जबकि सामान्य नाम को सी. डिफ के रूप में बनाए रखा गया है।[19] इस नए जीनस में एकमात्र अन्य प्रजाति क्लॉस्ट्रिडिओइड्स मैंजेनोटी (जिसे पहले क्लोस्ट्रीडियम मैंजेनोटी के नाम से जाना जाता था) है।[20]
मानव रोगज़नक़
रोगजनक सी डिफिसाइल उपभेद कई विषाक्त पदार्थों का उत्पादन करते हैं।[21] सबसे अच्छे लक्षण आंत्रजीवविष (क्लोस्ट्रीडियम डिफिसाइल टॉक्सिन ए या सी डिफिसाइल टॉक्सिन ए) और साइटोटोक्सिन (क्लोस्ट्रीडियम डिफिसाइल टॉक्सिन बी या सी डिफिसाइल टॉक्सिन बी) हैं, जो दोनों संक्रमित रोगियों में दस्त और [[सूजन]] (क्लोस्ट्रीडियम डिफिसाइल कोलाइटिस या सी डिफिसाइल कोलाइटिस) उत्पन्न कर सकते हैं। चूंकि उनके सापेक्ष योगदान पर वाद-विवाद हुआ है। इसके दस्त के कुछ दिनों के आंतों के तरल पदार्थ के हानि से लेकर जीवन-घातक स्यूडोमेम्ब्रानस कोलाइटिस तक हो सकता है, जो बृहदान्त्र की तीव्र सूजन और आंतों की श्लैष्मिक सतह पर स्यूडोमेम्ब्रेन के गठन से जुड़ा होता है।[13] इस कारण टॉक्सिन ए और बी ग्लूकोसिलट्रांसफेरेज़ हैं जो जीटीपेज़ के आरएचओ परिवार को लक्षित और निष्क्रिय करते हैं। इस प्रकार टॉक्सिन बी (साइटोटॉक्सिन) कम आणविक द्रव्यमान जीटीपी-बाइंडिंग आरएचओ प्रोटीन के एडीपी-राइबोसाइलेशन में कमी के साथ सहसंबद्ध तंत्र द्वारा एक्टिन डीपोलीमराइजेशन को प्रेरित करता है।[22] इसके कारण छिद्र बनाने वाला विष बाइनरी टॉक्सिन (एबी विष) भी है, किंतु बीमारी में इसकी भूमिका पूर्ण रूप से समझ में नहीं आती है।[23]
इसके अतिरिक्त विषाणु कारकों में एक आसंजन कारक सम्मिलित होता है जो मानव कोलोनिक कोशिकाओं और एक हाइलूरोनिडेज़ के बंधन में मध्यस्थता करता है।[24] जीवाणु रासायनिक पैरा-क्रेसोल भी उत्पन्न करता है, जो इसके आसपास के क्षेत्र में अन्य रोगाणुओं के विकास को रोकता है और इसे सामान्य मानव आंत वनस्पतियों से आगे निकलने की अनुमति देता है।[25]
सी डिफ संक्रमण का एंटीबायोटिक दवाओं उपचार कठिन हो सकता है, एंटीबायोटिक प्रतिरोध और जीवाणु के शारीरिक कारकों (बीजाणु निर्माण, स्यूडोमेम्ब्रेन के सुरक्षात्मक प्रभाव) दोनों के कारण होता हैं।[13] इसके आधार पर सिप्रोफ्लोक्सासिं और लिवोफ़्लॉक्सासिन जैसे फ़्लोरोक्विनोलोन एंटीबायोटिक दवाओं के प्रति प्रतिरोधी सी डिफिसाइल के एक नए, अत्यधिक जहरीले तनाव के उद्भव की सूचना 2005 में दी गई थी, जिसके बारे में कहा जाता है कि यह उत्तरी अमेरिका में भौगोलिक रूप से फैले हुए प्रकोप का कारण बन रहा है।[26] अटलांटा में अमेरिकी रोग नियंत्रण केंद्र ने बढ़ी हुई विषाक्तता, एंटीबायोटिक प्रतिरोध या दोनों के साथ एक महामारी तनाव के उद्भव की चेतावनी दी है।[27] इस प्रकार सीडीआई का उपचार करते समय रोगाणुरोधी दवा की पहली पसंद मेट्रोनिडाजोल जैसे अन्य एंटीबायोटिक दवाओं के प्रति प्रतिरोध 12% क्लिनिकल आइसोलेट्स में देखा गया है, इसलिए जैसे-जैसे विभिन्न एंटीबायोटिक दवाओं के साथ उपचार जारी रहेगा, अधिक विविध और मजबूत प्रतिरोध निरंतर रहेगा। इस प्रकार सी डिफिसाइल आबादी में विकसित होना, प्रभावी उपचार के प्रयासों को और अधिक जटिल बना रहा है। [28]
संचरण
क्लॉस्ट्रिडिओइड्स डिफिसाइल मौखिक मार्ग से मल के माध्यम से एक व्यक्ति या जानवर से दूसरे व्यक्ति में फैलता है। इस प्रकार जीव गर्मी-प्रतिरोधी बीजाणु बनाता है जो अल्कोहल-आधारित हाथ क्लीनर या नियमित सतह की सफाई से नहीं मरते हैं, इस प्रकार, ये बीजाणु लंबे समय तक नैदानिक वातावरण में जीवित रहते हैं। किसी भी सतह, उपकरण या सामग्री (जैसे, शौचालय, स्नान टब और इलेक्ट्रॉनिक रेक्टल थर्मामीटर) जो मल से दूषित हो जाती है, सी डिफिसाइल बीजाणुओं के लिए भंडार के रूप में कार्य कर सकती है, और सी डिफिसाइल बीजाणु लंबे समय तक जीवित रह सकते हैं। निम्न सतहों[29] के कारण जीवाणु को लगभग किसी भी सतह से संवर्धित किया जा सकता है। यहा पर एक बार जब बीजाणु अंतर्ग्रहण हो जाते हैं, तो उनका एसिड प्रतिरोध उन्हें बिना किसी हानि के पेट से गुजरने की अनुमति देता है। पित्त अम्लों के संपर्क में आने पर वे बृहदान्त्र में अंकुरित होते हैं और वनस्पति कोशिकाओं में विकसित होते हैं। परिणामस्वरूप विश्व स्वास्थ्य संगठन बीजाणुओं के प्रसार को सीमित करने के लिए अल्कोहल समाधान के अतिरिक्त साबुन के उपयोग की वकालत करता है।[30] सी डिफिसाइल के डीएनए मिथाइलट्रांसफेरेज़ कैमा के निष्क्रिय होने के पश्चात स्पोरुलेशन में काफी कमी देखी गई हैं,[31] यह ऐसी दवा विकसित करने की संभावना बढ़ाना जो इस जीवाणु को एक विशिष्ट तरीकों से रोक सके।
ऐसा प्रतीत होता है कि उपनिवेशीकरण की संवेदनशीलता डायरिया संबंधी बीमारियों से उत्पन्न होती है, जैसे कि खाद्य-विषाक्तता या रेचक दुरुपयोग, जिन लोगों में डायरिया संबंधी बीमारियों का इतिहास नहीं है, जो सी डिफिसाइल बीजाणुओं के संपर्क में हैं, यह आवश्यक नहीं हैं कि वे इसके वाहक बनें।[14] एक बार जब लोग सी डिफिसाइल द्वारा उपनिवेशित हो जाते हैं, तो वे साल भर के समय के पैमाने पर वाहक बने रहते हैं, किंतु सी डिफिसाइल की दिन-प्रतिदिन प्रचुरता में काफी उतार-चढ़ाव होता है - इसका पता लगाने की सीमा से नीचे होने से लेकर एक दिन से उच्च स्तर के बहाव तक उतार-चढ़ाव होता है। इसपर वाहकों में जठरांत्र संबंधी रोग के कारण स्राव में वृद्धि की अवधि प्रारंभ हो जाती है जो संचरण के लिए महत्वपूर्ण कारक हो सकता है।
होस्ट रेंज
क्लॉस्ट्रिडिओइड्स डिफिसाइल सूअरों, बछड़ों और मनुष्यों को संक्रमित करता है, और मिट्टी, घरेलू जानवरों और मनुष्यों के मल, मल, मानव आंत्र पथ और खुदरा मांस के प्राकृतिक भंडार में रहता है।[32]
2015 के सीडीसी अध्ययन में अनुमान लगाया गया है कि सी. ने लगभग आधे मिलियन अमेरिकियों को पीड़ित किया और 2011 में 29,000 लोगों की मौत हुई। अध्ययन का अनुमान है कि 40% मामले नर्सिंग होम या सामुदायिक स्वास्थ्य देखभाल सेटिंग्स में प्रारंभ हुए, जबकि 24% अस्पतालों में हुए।[33]
क्लोस्ट्रीडियोइड्स डिफिसाइल मानव पाचन तंत्र में आम है। चूंकि, यह एक ख़राब प्रतियोगी है, और अक्सर पाचन तंत्र में अन्य जीवाणुओं द्वारा पोषक तत्वों की स्थिति में मात खा जाता है। परिणामस्वरूप, सी डिफिसाइल को एक प्रबंधनीय संख्या में रखा जाता है। यदि एंटीबायोटिक का अचानक परिचय माइक्रोबायोम को बाधित करता है, तो सी डिफिसाइल अपने कई प्रतिस्पर्धियों के मारे जाने के परिणामस्वरूप बढ़ने में सक्षम हो सकता है। ऊष्मायन अवधि 5-10 दिन है, जिसमें एंटीबायोटिक से जुड़े दस्त के लिए एंटीबायोटिक उपचार के बाद 1 दिन से लेकर सप्ताह तक का समय होता है। इसके अतिरिक्त, उच्च स्तर के विषाक्त पदार्थों के साथ सी डिफिसाइल का संचरण छोटे बच्चों में आम है, जबकि बीमारी दुर्लभ है। लक्षण उत्पन्न करने के लिए एक या दोनों विषाक्त पदार्थों का उत्पादन सदैव पर्याप्त नहीं होता है।[34]
संकेत और लक्षण
सी डिफिसाइल संक्रमण के लक्षणों में सम्मिलित हैं: दस्त (जो कि दिन में कम से कम तीन बार मल त्यागना), निर्जलीकरण, पेट में दर्द जो गंभीर हो सकता है, भूख न लगना और मतली इत्यादि हो सकती हैं।[35]
प्रतिरक्षा प्रतिक्रिया
सी डिफिसाइल स्रावित विषाक्त पदार्थ ए (टीसीडीए) और बी (टीसीडीबी) में इम्युनोजेनिक एंटीजन होते हैं जिन्हें एंटीबॉडी और टी कोशिकाओं द्वारा पहचाना जाता है। चूंकि, एंटी-टीसीडीए और -टीसीडीबी आईजीजी एंटीबॉडी का स्तर स्वस्थ व्यक्तियों को सी डिफिसाइल संक्रमण वाले रोगियों से अलग करने में सक्षम नहीं है, जिसका अर्थ है कि उनका नैदानिक उपयोग सीमित है।[36][37] वर्तमान समय के कार्य से पता चला है कि इन विषाक्त पदार्थों को सहायक Cd4+ टी कोशिकाओं द्वारा भी पहचाना जाता है, मुख्य रूप से टी हेल्पर 17 कोशिका या टीh द्वारा की जाती हैं। इस प्रकार17 सहायक कोशिकाएँ, जो आंत के स्वस्थ वातावरण को बनाए रखने में महत्वपूर्ण हैं, चूंकि गंभीर संक्रमण वाले रोगियों में ये कोशिकाएँ क्षीण हो जाती हैं।[38] यहाँ पर रोचक बात यह है कि गंभीर सी डिफिसाइल संक्रमण वाले व्यक्तियों में हल्के संक्रमण वाले लोगों की तुलना में अत्यधिक विष-विशिष्ट टी कोशिकाएं थीं, जो दर्शाता है कि टी कोशिकाएं इस संक्रमण से लड़ने में महत्वपूर्ण भूमिका निभा रही हैं। यह प्रतिरक्षा प्रतिक्रिया माइक्रो आरएनए अभिव्यक्ति को और अधिक ख़राब कर सकती है।[39] गंभीर बीमारी वाले रोगियों के फेकल माइक्रोबायोटा प्रत्यारोपण के बाद विष-विशिष्ट Th17 कोशिकाओं और माइक्रोआरएनए अभिव्यक्ति की पुनर्प्राप्ति से इसका प्रमाण मिलता है।[39][40]
उपचार
इस कारण किसी प्रकार के लक्षण प्रारंभ होने पर एंटीबायोटिक दवाओं से उपचार करा रहे मरीजों को यदि संभव हो तो उन्हें लेना बंद कर देना चाहिए। एंटीबायोटिक थेरेपी में यह रुकावट कभी-कभी लक्षणों के सहज समाधान का कारण बन सकती है। जिन मरीजों पर ब्रॉड-स्पेक्ट्रम एंटीबायोटिक दवाओं के बंद होने पर कोई प्रतिक्रिया नहीं होती है, उन्हें सी डिफिसाइल बीजाणुओं को मारने में सक्षम एंटीबायोटिक दवाओं से उपचार करने की आवश्यकता होगी। इसके आधार पर प्राथमिक संक्रमणों का उपचार सामान्य रूप से वैनकोमाइसिन से किया जाता है, जिसकी सामान्य खुराक हर 6 घंटे में 125 मिलीग्राम होती है।[41] वैनकॉमायसिन आहार ने अपनी अधिक प्रभावकारिता, सुरक्षा प्रोफ़ाइल और कम पुनरावृत्ति दर के कारण मेट्रोनाइडाजोल के पारंपरिक उपयोग को प्रतिस्थापित कर दिया है। उन रोगियों में जो वैनकोमाइसिन को सहन नहीं कर सकते हैं, फ़िडाक्सोमिसिन समान प्रभावकारिता और वैनकोमाइसिन की तुलना में कम पुनरावृत्ति दर के साथ एक स्वीकार्य विकल्प है।[42] फुलमिनेंट सीडीआई के मामलों में, पैरेंट्रल मेट्रोनिडाजोल प्लस ओरल वैनकोमाइसिन या फिडाक्सोमिसिन के साथ सहायक चिकित्सा का सुझाव दिया जाता है।[43]
लगभग 20% मरीज़ जो मेट्रोनिडाज़ोल या वैनकोमाइसिन के साथ प्राथमिक संक्रमण का उपचार सफलतापूर्वक पूरा करते हैं, उन्हें दोबारा संक्रमण का अनुभव होगा। उन रोगियों का एक भाग क्रमशः संक्रमण की पुनरावृत्ति का अनुभव करेगा। सी डिफिसाइल की पहली पुनरावृत्ति का उपचार सामान्य रूप से उसी एंटीबायोटिक से किया जाता है जिसका उपयोग प्राथमिक संक्रमण के उपचार के लिए किया जाता है। इसके बाद के किसी भी संक्रमण का उपचार मेट्रोनिडाजोल से नहीं किया जाना चाहिए। कभी-कभी, मौखिक वैनकोमाइसिन का मानक 10-दिवसीय कोर्स कार्य नहीं करेगा। इन स्थितियों में, वैनकोमाइसिन टेपर पसंदीदा उपचार है। संक्रमण की गंभीरता के आधार पर, मरीज़ 3 महीने तक की अवधि में वैनकोमाइसिन की घटती खुराक लेते हैं।[35]
सी डिफिसाइल की प्रत्येक बाद की पुनरावृत्ति पिछले संक्रमणों की तुलना में अधिक गंभीर होती है। प्रोबायोटिक्स, विशेष रूप से सैक्रोमाइसेस बौलार्डी के साथ पूरक वैनकोमाइसिन टेपर के साथ दीर्घकालिक उपचार, सफलता की उच्च दर के साथ जुड़ा हुआ है।[44]
तीन पुनरावृत्तियों के बाद, रोगियों को मौखिक फ़िडाक्सोमिसिन, एक संकीर्ण-स्पेक्ट्रम एंटीबायोटिक, के साथ उपचार किया जा सकता है। सामान्य खुराक 10 दिनों के लिए दिन में दो बार मौखिक रूप से 200 मिलीग्राम है। इसके कारण गंभीर सीडीआई के लिए फिडाक्सोमिसिन को वैनकोमाइसिन से उत्तम माना जाता है।[45] फ़िडाक्सोमिसिन से उपचार का प्रमुख नकारात्मक पक्ष दवा की लागत है। 10-दिवसीय पाठ्यक्रम की लागत US$3500 तक हो सकती है।
जिन मरीजों पर पारंपरिक एंटीबायोटिक थेरेपी का असर नहीं होता, वे फेकल माइक्रोबायोटा ट्रांसप्लांट (एफएमटी) के लिए पात्र हो सकते हैं। इस प्रकार की स्वास्थ्य सेवा प्रदाता बार-बार सीडीआई वाले रोगी के मल को एक स्वस्थ व्यक्ति से रोगी के बृहदान्त्र में स्थानांतरित कर सकते हैं। यह प्रक्रिया लगभग 93% उपचार दर के साथ गंभीर सीडीआई के लिए सबसे सफल उपचार है। एफएमटी से उपचारित रोगियों में सीडीआई की पुनरावृत्ति दर आम तौर पर कम, लगभग 19% होती है, जो इसे पुराने सीडीआई स्थितियों के उपचार में बहुत प्रभावी बनाती है। चूंकि, कुछ स्थितियों में, सूजन आंत्र रोग की भड़कना उपचार का एक संभावित दुष्प्रभाव है।[46] एफएमटी के दीर्घकालिक प्रभाव अज्ञात हैं, क्योंकि प्रक्रिया को 2011 से केवल एफडीए-अनुमोदित किया गया है और अपेक्षाकृत कुछ प्रक्रियाएं निष्पादित की गई हैं। यदि प्रत्यारोपण कोई विकल्प नहीं है, तो बृहदान्त्र के संक्रमित हिस्से को हटाने से सीडीआई ठीक हो सकता है।[45][35]
उपभेद
2005 में, आणविक विश्लेषण से सी डिफिसाइल स्ट्रेन प्रकार की पहचान हुई, जिसे प्रतिबंध एंजाइम विश्लेषण द्वारा समूह बीआई के रूप में जाना जाता है।, स्पंदित-क्षेत्र जेल वैद्युतकणसंचलन द्वारा उत्तरी अमेरिकी पल्स-फील्ड-प्रकार एनएपी1 के रूप में और रिबोटाइपिंग 027 के रूप में, अलग-अलग शब्दावली महामारी विज्ञान टाइपिंग के लिए उपयोग की जाने वाली प्रमुख तकनीकों को दर्शाती है। इस स्ट्रेन को सी डिफिसाइल बीआई/एनएपी1/027 कहा जाता है।[47]
2016 तक, ब्रिटिश कोलंबिया के कुछ क्षेत्रों में एनएपी1 स्ट्रेन को नए स्ट्रेन से बदल दिया गया है। इन नवीन उपभेदों में एनएपी2 और एनएपी4 सम्मिलित हैं, और कुछ उपभेदों में एनएपी पदनाम नहीं है। इस प्रकार अध्ययन किए गए एक क्षेत्र में इन नए उपभेदों की आवृत्ति 2008 से 2013 तक बढ़ गई, जिससे मूल रूप से अधिक सामान्य और पहचाने जाने योग्य एनएपी1 बैक्टीरिया विस्थापित हो गए थे।[48]
दो उपभेद, राइबोटाइप आरटी078 और आरटी027, चीनी ट्रीहाल्सो की कम सांद्रता पर जीवित रह सकते हैं, 2000 के दशक के प्रारंभ में ट्रेहलोज़ को खाद्य योज्य के रूप में प्रस्तुत किए जाने के पश्चात दोनों उपभेद अधिक आम हो गए, जिससे आहार में ट्रेहलोज़ का सेवन बढ़ गया। [49]
जीनोम
Template:Infobox genome सी डिफिसाइल स्ट्रेन का पहला पूर्ण जीनोम अनुक्रम 2005 में यूके में सेंगर संस्थान द्वारा प्रकाशित किया गया था। इस प्रकार यह दबाव 630 का था, जो 1982 में स्विट्ज़रलैंड में अलग किया गया एक विषैला और कई दवा-प्रतिरोधी स्ट्रेन था। इस प्रकार सेंगर इंस्टीट्यूट के वैज्ञानिकों ने 454 लाइफ साइंसेज और इलुमिना (कंपनी) की अगली पीढ़ी की अनुक्रमण प्रौद्योगिकियों का उपयोग करके लगभग 30 सी डिफिसाइल आइसोलेट्स के जीनोम को अनुक्रमित किया है।[50]
मॉन्ट्रियल में मैकगिल विश्वविद्यालय के शोधकर्ताओं ने अल्ट्रा-हाई थ्रूपुट अनुक्रमण तकनीक का उपयोग करके 2005 में सी डिफिसाइल के अत्यधिक विषैले क्यूबेक तनाव के जीनोम को अनुक्रमित किया गया था। इस प्रकार परीक्षणों में जीवाणु के जीनोम की 400,000 डीएनए समानांतर-अनुक्रमण प्रतिक्रियाएं करना सम्मिलित था, जिन्हें अनुक्रमण के लिए खंडित किया गया था। इस प्रकार संपूर्ण जीनोम अनुक्रम बनाने के लिए इन अनुक्रमों को कम्प्यूटेशनल रूप से एकत्रित किये गये थे।[26][51]
2012 में, ऑक्सफ़ोर्ड विश्वविद्यालय के वैज्ञानिकों ने इलुमिना की अगली पीढ़ी की अनुक्रमण प्रौद्योगिकियों का उपयोग करके ऑक्सफ़ोर्डशायर में चार वर्षों में उत्पन्न हुए 486 स्थितियों से सी डिफिसाइल जीनोम का अनुक्रमित किया गया था।[52]
एपिजेनोम
क्लॉस्ट्रिडिओइड्स डिफिसाइल में अत्यधिक विविध एपिजेनोम है, जिसमें अब तक 17 उच्च-गुणवत्ता वाले मेथिलिकरण रूपांकनों की सूचना दी गई है, जिनमें से अधिकांश 6मिलीएम्पियर प्रकार से संबंधित हैं। इन रूपांकनों में से एक - सीएएएएए, पर मिथाइलेशन को स्पोरुलेशन पर प्रभाव डालने के लिए दिखाया गया था, जो सी डिफिसाइल रोग संचरण में महत्वपूर्ण कदम है, इसके साथ ही कोशिका की लंबाई, बायोफिल्म निर्माण और मेजबान उपनिवेशण भी है।[31]
जीवाणुभोजी
कम से कम आठ मुख्य रूप से शीतोष्णता (वायरोलॉजी) बैक्टीरियोफेज को सी डिफिसाइल से अलग किया गया है, जिनका जीनोम आकार लगभग 30 से लेकर लगभग 60 बेस पेयर तक है।[53] पर्यावरण और चिकित्सकीय रूप से व्युत्पन्न सी डिफिसाइल उपभेदों में विविध और प्रचलित प्रसार का समूह होता है।[53]
व्युत्पत्ति और उच्चारण
संदर्भ
- ↑ Hall, Ivan C.; O'Toole, Elizabeth (1935). "Intestinal flora in new-born infants: with a description of a new pathogenic anaerobe, Bacillus difficilis". American Journal of Diseases of Children. 49 (2): 390–402. doi:10.1001/archpedi.1935.01970020105010.
- ↑ Prévot, A.-R. (1938). "Études de systématique bactérienne. IV. Critique de la conception actuelle du genre Clostridium". Annales de l'Institut Pasteur. 61 (1): 84.
- ↑ Page Species: Clostridioides difficile on "LPSN - List of Prokaryotic names with Standing in Nomenclature". Deutsche Sammlung von Mikroorganismen und Zellkulturen. Retrieved 2022-11-08.
- ↑ Drewes, Julia L.; et al. (5 August 2022). "मानव बृहदान्त्र कैंसर-व्युत्पन्न क्लोस्ट्रीडियोइड्स डिफिसाइल स्ट्रेन चूहों में बृहदान्त्र ट्यूमरजनन को प्रेरित करता है". Cancer Discovery. 12 (8): 1873–1885. doi:10.1158/2159-8290.CD-21-1273. PMC 9357196. PMID 35678528.
- ↑ "जॉन्स हॉपकिन्स डॉक्टरों ने पाया कि एक सामान्य संक्रमण कैंसर का कारण बन सकता है". 24 August 2022.
- ↑ (/siː dɪf/), और [[जीवाणु बीजाणु]] बनाने वाले जीवाणुओं की एक ग्राम पॉजिटिव प्रजाति है।<संदर्भ नाम = मोरेनो - जून 2013 >Moreno MA, Furtner F, Rivara FP (June 2013). "क्लोस्ट्रीडियम डिफिसाइल: बच्चों में दस्त का एक कारण". JAMA Pediatrics. 167 (6): 592. doi:10.1001/jamapediatrics.2013.2551. PMID 23733223.क्लॉस्ट्रिडिओइड्स एसपीपी। अवायवीय जीव, गतिशीलता बैक्टीरिया, प्रकृति में सर्वव्यापी और विशेष रूप से मिट्टी में प्रचलित हैं। इसकी कायिक कोशिकाएँ छड़ के आकार की, प्लियोमोर्फिज्म (सूक्ष्मजीवविज्ञान) होती हैं, और जोड़े या छोटी श्रृंखलाओं में होती हैं। माइक्रोस्कोप के तहत, वे लंबी, अनियमित (अक्सर ड्रमस्टिक- या स्पिंडल के आकार की) कोशिकाओं के रूप में दिखाई देते हैं जिनके अंतिम छोर पर एक उभार होता है (सबटर्मिनल बीजाणु बनता है)। ग्राम स्टेनिंग के तहत, सी. डिफिसाइल कोशिकाएं ग्राम-पॉजिटिव होती हैं और ऑक्सीजन की अनुपस्थिति में मानव शरीर के तापमान पर रक्त एगर पर इष्टतम वृद्धि दिखाती हैं। सी. डिफिसाइल केटालेज़ - और सुपरऑक्साइड डिसम्यूटेज़ है, और तीन प्रकार के विषाक्त पदार्थों का उत्पादन करता है: क्लॉस्ट्रिडियम डिफिसाइल टॉक्सिन ए, [[क्लोस्ट्रीडियम डिफिसाइल टॉक्सिन ए]] और क्लोस्ट्रीडियोइड्स डिफिसाइल ट्रांसफरेज (सीडीटी)।Kordus, Shannon L.; Thomas, Audrey K.; Lacy, D. Borden (2021-11-26). "क्लॉस्ट्रिडिओइड्स डिफिसाइल टॉक्सिन्स: क्रिया के तंत्र और एंटीटॉक्सिन उपचार". Nature Reviews Microbiology (in English). 20 (5): 285–298. doi:10.1038/s41579-021-00660-2. ISSN 1740-1534. PMC 9018519. PMID 34837014.तनाव की स्थिति में, बैक्टीरिया बैक्टीरिया बीजाणु उत्पन्न करते हैं जो चरम स्थितियों को सहन करने में सक्षम होते हैं जिन्हें सक्रिय बैक्टीरिया बर्दाश्त नहीं कर सकते हैं।Ryan KJ, Ray CG, eds. (2004). शेरिस मेडिकल माइक्रोबायोलॉजी (4th ed.). McGraw Hill. pp. 322–4. ISBN 978-0-8385-8529-0.
- ↑ "क्लॉस्ट्रिडिओइड्स डिफिसाइल संक्रमण | एचएआई | सीडीसी". www.cdc.gov (in English). 2020-01-02. Retrieved 2020-03-10.
- ↑ Eyre, David W.; Cule, Madeleine L.; Wilson, Daniel J.; Griffiths, David; Vaughan, Alison; O'Connor, Lily; Ip, Camilla L.C.; Golubchik, Tanya; Batty, Elizabeth M.; Finney, John M.; Wyllie, David H. (2013-09-26). "संपूर्ण-जीनोम अनुक्रमण पर सी. डिफिसाइल संक्रमण के विविध स्रोतों की पहचान की गई". New England Journal of Medicine. 369 (13): 1195–1205. doi:10.1056/NEJMoa1216064. ISSN 0028-4793. PMC 3868928. PMID 24066741.
- ↑ Guh, Alice Y.; Adkins, Susan Hocevar; Li, Qunna; Bulens, Sandra N.; Farley, Monica M.; Smith, Zirka; Holzbauer, Stacy M.; Whitten, Tory; Phipps, Erin C.; Hancock, Emily B.; Dumyati, Ghinwa (2017-10-01). "वयस्कों में समुदाय से जुड़े क्लोस्ट्रीडियम डिफिसाइल संक्रमण के जोखिम कारक: एक केस-नियंत्रण अध्ययन". Open Forum Infectious Diseases (in English). 4 (4): ofx171. doi:10.1093/ofid/ofx171. PMC 5903408. PMID 29732377.
- ↑ Brown, Kevin A.; Khanafer, Nagham; Daneman, Nick; Fisman, David N. (2013). "एंटीबायोटिक दवाओं का मेटा-विश्लेषण और समुदाय से जुड़े क्लोस्ट्रीडियम डिफिसाइल संक्रमण का जोखिम". Antimicrobial Agents and Chemotherapy (in English). 57 (5): 2326–2332. doi:10.1128/AAC.02176-12. ISSN 0066-4804. PMC 3632900. PMID 23478961.
- ↑ McFarland, Lynne V.; Surawicz, Christina M.; Stamm, Walter E. (1990-09-01). "अस्पताल में भर्ती मरीजों के एक समूह में क्लॉस्ट्रिडियम डिफिसाइल कैरिज और सी. डिफिसाइल-एसोसिएटेड डायरिया के जोखिम कारक". The Journal of Infectious Diseases (in English). 162 (3): 678–684. doi:10.1093/infdis/162.3.678. ISSN 0022-1899. PMID 2387993.
- ↑ McFarland, Lynne V.; Mulligan, Maury E.; Kwok, Richard Y.Y.; Stamm, Walter E. (1989-01-26). "क्लोस्ट्रीडियम डिफिसाइल संक्रमण का नोसोकोमियल अधिग्रहण". New England Journal of Medicine (in English). 320 (4): 204–210. doi:10.1056/NEJM198901263200402. ISSN 0028-4793. PMID 2911306.
- ↑ 13.0 13.1 13.2 Cite error: Invalid
<ref>tag; no text was provided for refs namedSherris - ↑ 14.0 14.1 VanInsberghe, David; Elsherbini, Joseph A.; Varian, Bernard; Poutahidis, Theofilos; Erdman, Susan; Polz, Martin F. (2020-02-10). "डायरिया की घटनाएं बार-बार खिलने के साथ दीर्घकालिक क्लोस्ट्रीडियम डिफिसाइल उपनिवेशण को ट्रिगर कर सकती हैं". Nature Microbiology (in English). 5 (4): 642–650. doi:10.1038/s41564-020-0668-2. ISSN 2058-5276. PMID 32042128. S2CID 211074075.
- ↑ Eyre, David W.; Griffiths, David; Vaughan, Alison; Golubchik, Tanya; Acharya, Milind; O’Connor, Lily; Crook, Derrick W.; Walker, A. Sarah; Peto, Tim E. A. (2013-11-12). Chang, Yung-Fu (ed.). "स्पर्शोन्मुख क्लोस्ट्रीडियम डिफिसाइल औपनिवेशीकरण और आगे का संचरण". PLOS ONE (in English). 8 (11): e78445. Bibcode:2013PLoSO...878445E. doi:10.1371/journal.pone.0078445. ISSN 1932-6203. PMC 3827041. PMID 24265690.
- ↑ Oren, Aharon; Garrity, George M. (2017). "नए नामों और नए संयोजनों की सूची पहले प्रभावी रूप से, लेकिन वैध रूप से प्रकाशित नहीं हुई". International Journal of Systematic and Evolutionary Microbiology. 67 (9): 3140–3143. doi:10.1099/ijsem.0.002278. PMC 5817221. PMID 28891789.
- ↑ Lawson, Paul A.; Citron, Diane M.; Tyrrell, Kerin L.; Finegold, Sydney M. (August 2016). "Reclassification of Clostridium difficile as Clostridioides difficile (Hall and O'Toole 1935) Prévot 1938". Anaerobe. 40: 95–99. doi:10.1016/j.anaerobe.2016.06.008. ISSN 1095-8274. PMID 27370902.
- ↑ Zhu, Duolong; Sorg, Joseph A.; Sun, Xingmin (2018). "Clostridioides difficile Biology: Sporulation, Germination, and Corresponding Therapies for C. difficile Infection". Frontiers in Cellular and Infection Microbiology (in English). 8: 29. doi:10.3389/fcimb.2018.00029. ISSN 2235-2988. PMC 5809512. PMID 29473021.
- ↑ Lawson, Paul A.; Citron, Diane M.; Tyrrell, Kerin L.; Finegold, Sydney M. (August 2016). "Reclassification of Clostridium difficile as Clostridioides difficile (Hall and O'Toole 1935) Prévot 1938". Anaerobe. 40: 95–99. doi:10.1016/j.anaerobe.2016.06.008. ISSN 1075-9964. PMID 27370902.
- ↑ Galperin, Michael Y.; Brover, Vyacheslav; Tolstoy, Igor; Yutin, Natalya (2016). "Phylogenomic analysis of the family Peptostreptococcaceae (Clostridium cluster XI) and proposal for reclassification of Clostridium litorale (Fendrich et al. 1991) and Eubacterium acidaminophilum (Zindel et al. 1989) as Peptoclostridium litorale gen. nov. comb. nov. and Peptoclostridium acidaminophilum comb. nov". International Journal of Systematic and Evolutionary Microbiology. 66 (12): 5506–5513. doi:10.1099/ijsem.0.001548. PMC 5244501. PMID 27902180.
- ↑ Di Bella, Stefano; Ascenzi, Paolo; Siarakas, Steven; Petrosillo, Nicola; di Masi, Alessandra (2016-01-01). "Clostridium difficile Toxins A and B: Insights into Pathogenic Properties and Extraintestinal Effects". Toxins. 8 (5): 134. doi:10.3390/toxins8050134. ISSN 2072-6651. PMC 4885049. PMID 27153087.
- ↑ Just I, Selzer J, von Eichel-Streiber C, Aktories K (1995). "कम आणविक भार वाला GTP-बाध्यकारी प्रोटीन Rh क्लोस्ट्रीडियम डिफिसाइल के विष से प्रभावित होता है।". The Journal of Clinical Investigation. 95 (3): 1026–31. doi:10.1172/JCI117747. PMC 441436. PMID 7883950.
- ↑ Barth H, Aktories K, Popoff MR, Stiles BG (2004). "Binary Bacterial Toxins: Biochemistry, Biology, and Applications of Common Clostridium and Bacillus Proteins". Microbiology and Molecular Biology Reviews. 68 (3): 373–402, table of contents. doi:10.1128/MMBR.68.3.373-402.2004. PMC 515256. PMID 15353562.
- ↑ [Medical Micriobiology, Fifth Edition, Patrick Murray, Elsevier Mosby, 2005, page 412]
- ↑ "वह रासायनिक हथियार जो बैक्टीरिया को आंत में कहर बरपाने में मदद करता है". Nature. 561 (7723): 288. 14 September 2018. Bibcode:2018Natur.561S.288.. doi:10.1038/d41586-018-06650-4. S2CID 52297840. Retrieved 8 October 2018.
{{cite journal}}: zero width space character in|title=at position 56 (help) - ↑ 26.0 26.1 Loo VG, Poirier L, Miller MA, Oughton M, Libman MD, Michaud S, Bourgault AM, Nguyen T, Frenette C, Kelly M, Vibien A, Brassard P, Fenn S, Dewar K, Hudson TJ, Horn R, René P, Monczak Y, Dascal A (December 2005). "उच्च रुग्णता और मृत्यु दर के साथ क्लोस्ट्रीडियम डिफिसाइल से जुड़े डायरिया का मुख्य रूप से क्लोनल बहु-संस्थागत प्रकोप". The New England Journal of Medicine. 353 (23): 2442–9. doi:10.1056/NEJMoa051639. PMID 16322602. S2CID 14818750.
- ↑ McDonald LC (August 2005). "क्लोस्ट्रीडियम डिफिसाइल: पुराने दुश्मन से नए खतरे का जवाब देना" (PDF). Infection Control and Hospital Epidemiology. 26 (8): 672–5. doi:10.1086/502600. PMID 16156321.
- ↑ Saeed S. Banawas (21 February 2018). "क्लोस्ट्रीडियम डिफिसाइल संक्रमण: दवा संवेदनशीलता और प्रतिरोध तंत्र का एक वैश्विक अवलोकन". BioMed Research International. 2018: 8414257. doi:10.1155/2018/8414257. PMC 5841113. PMID 29682562.
- ↑ "Clostridium difficile Infection Information for Patients | HAI | CDC". www.cdc.gov. Retrieved 22 May 2017.
- ↑ "WHO Guidelines on Hand Hygiene in Health Care: a Summary" (PDF). World Health Organization. 2009. p. 31. Retrieved June 18, 2018.
- ↑ 31.0 31.1 Oliveira, Pedro H.; Ribis, John W.; Garrett, Elizabeth M.; Trzilova, Dominika; Kim, Alex; Sekulovic, Ognjen; Mead, Edward A.; Pak, Theodore; Zhu, Shijia; Deikus, Gintaras; Touchon, Marie (2020). "क्लॉस्ट्रिडिओइड्स डिफिसाइल के एपिजेनोमिक लक्षण वर्णन में एक संरक्षित डीएनए मिथाइलट्रांसफेरेज़ पाया जाता है जो स्पोरुलेशन और रोगजनन में मध्यस्थता करता है". Nature Microbiology (in English). 5 (1): 166–180. doi:10.1038/s41564-019-0613-4. ISSN 2058-5276. PMC 6925328. PMID 31768029.
- ↑ Gould, L. Hannah; Limbago, Brandi (2010). "Clostridium difficile in Food and Domestic Animals: A New Foodborne Pathogen?". Clinical Infectious Diseases. 51 (5): 577–82. doi:10.1086/655692. PMID 20642351.
- ↑ Belluck, Pam (February 25, 2015). "सी. डिफिसाइल से मरने वालों की संख्या बढ़ी". The New York Times. Retrieved 25 February 2015.
- ↑ [Medical Microbiology, Fifth Edition, Patrick Murray, Elsevier Mosby, 2005, page 412]
- ↑ 35.0 35.1 35.2 "Could you have deadly diarrhea (C. Diff)?". 2019-01-04.
- ↑ Monaghan, Tanya M; Negm, Ola H; MacKenzie, Brendon; Hamed, Mohamed R; Shone, Clifford C; Humphreys, David P; Acharya, K Ravi; Wilcox, Mark H (July 2017). "High prevalence of subclass-specific binding and neutralizing antibodies against Clostridium difficile toxins in adult cystic fibrosis sera: possible mode of immunoprotection against symptomatic C. difficile infection". Clinical and Experimental Gastroenterology. 10: 169–175. doi:10.2147/CEG.S133939. PMC 5525456. PMID 28765714.
- ↑ Wullt, M.; Norén, T.; Ljungh, Å.; Åkerlund, T. (September 2012). "क्लोस्ट्रीडियम डिफिसाइल संक्रमण वाले मरीजों में विषाक्त पदार्थों ए और बी के प्रति आईजीजी एंटीबॉडी प्रतिक्रिया". Clinical and Vaccine Immunology. 19 (9): 1552–1554. doi:10.1128/CVI.00210-12. PMC 3428380. PMID 22787196.
- ↑ Cook, Laura; Rees, William D.; Wong, May Q.; Kwok, William W.; Levings, Megan K.; Steiner, Theodore S. (March 2021). "Recurrent Clostridioides difficile Infection Is Associated With Impaired T Helper Type 17 Immunity to C difficile Toxin B". Gastroenterology. 160 (4): 1410–1413.e4. doi:10.1053/J.GASTRO.2020.11.043. PMID 33253683.
- ↑ 39.0 39.1 Bocchetti, Marco; Ferraro, Maria Grazia; Melisi, Federica; Grisolia, Piera; Scrima, Marianna; Cossu, Alessia Maria; Yau, Tung On (2023-06-14). "क्लॉस्ट्रिडिओइड्स डिफिसाइल संक्रमण स्क्रीनिंग में वर्तमान पता लगाने के तरीकों और माइक्रोआरएनए क्षमता का अवलोकन". World Journal of Gastroenterology (in English). 29 (22): 3385–3399. doi:10.3748/wjg.v29.i22.3385. PMC 10303512.
- ↑ Cook, Laura; Rees, William D.; Wong, May Q.; Peters, Hannah; Levings, Megan K.; Steiner, Theodore S. (May 2021). "बार-बार होने वाले क्लॉस्ट्रिडिओइड्स डिफिसाइल संक्रमण के लिए फेकल माइक्रोबायोटा प्रत्यारोपण सी डिफिसाइल टॉक्सिन बी के प्रति अनुकूली प्रतिरक्षा को बढ़ाता है". Gastroenterology. 160 (6): 2155–2158.e4. doi:10.1053/J.GASTRO.2021.01.009. hdl:11343/289863. PMID 33444574. S2CID 231611318.
- ↑ "Clinical Practice Guidelines for Clostridium difficile Infection in Adults and Children: 2017 Update by the Infectious Diseases Society of America (IDSA) and Society for Healthcare Epidemiology of America (SHEA)". Clinical Infectious Diseases. 66 (7): e1–e48. 2018-03-19. doi:10.1093/cid/cix1085. ISSN 1537-6591. PMC 6018983. PMID 29462280.
- ↑ Mullane, Kathleen M.; Miller, Mark A.; Weiss, Karl; Lentnek, Arnold; Golan, Yoav; Sears, Pamela S.; Shue, Youe-Kong; Louie, Thomas J.; Gorbach, Sherwood L. (September 2011). "अन्य समवर्ती संक्रमणों के लिए सहवर्ती एंटीबायोटिक लेने वाले व्यक्तियों में क्लोस्ट्रीडियम डिफिसाइल संक्रमण के उपचार के रूप में फिडाक्सोमिसिन बनाम वैनकोमाइसिन की प्रभावकारिता". Clinical Infectious Diseases. 53 (5): 440–447. doi:10.1093/cid/cir404. ISSN 1537-6591. PMC 3156139. PMID 21844027.
- ↑ Shane, Andi L.; Mody, Rajal K.; Crump, John A.; Tarr, Phillip I.; Steiner, Theodore S.; Kotloff, Karen; Langley, Joanne M.; Wanke, Christine; Warren, Cirle Alcantara (2017-11-29). "2017 Infectious Diseases Society of America Clinical Practice Guidelines for the Diagnosis and Management of Infectious Diarrhea". Clinical Infectious Diseases. 65 (12): e45–e80. doi:10.1093/cid/cix669. ISSN 1537-6591. PMC 5850553. PMID 29053792.
- ↑ "वैनकोमाइसिन और सैक्रोमाइसेस बौलार्डी के साथ आवर्तक क्लोस्ट्रीडियम डिफिसाइल कोलाइटिस का उपचार" (PDF). The American Journal of Gastroenterology.
- ↑ 45.0 45.1 Surawicz, Christina M; Brandt, Lawrence J; Binion, David G; Ananthakrishnan, Ashwin N; Curry, Scott R; Gilligan, Peter H; McFarland, Lynne V; Mellow, Mark; Zuckerbraun, Brian S (2013-02-26). "क्लोस्ट्रीडियम डिफिसाइल संक्रमण के निदान, उपचार और रोकथाम के लिए दिशानिर्देश". The American Journal of Gastroenterology. 108 (4): 478–498. doi:10.1038/ajg.2013.4. ISSN 0002-9270. PMID 23439232. S2CID 54629762.
- ↑ Chen, Yu-Gen; Zheng, Xiao; Zhou, Jin-Yong; Wu, Jing; Jiang, Feng; Zhang, Dan; Zhou, Qun; Chen, Tuo (2018-05-25). "Effect of Faecal Microbiota Transplantation for Treatment of Clostridium difficile Infection in Patients With Inflammatory Bowel Disease: A Systematic Review and Meta-Analysis of Cohort Studies". Journal of Crohn's and Colitis. 12 (6): 710–717. doi:10.1093/ecco-jcc/jjy031. ISSN 1873-9946. PMID 29528385. S2CID 3841585.
- ↑ Rupnik M, Wilcox MH, Gerding DN (July 2009). "क्लोस्ट्रीडियम डिफिसाइल संक्रमण: महामारी विज्ञान और रोगजनन में नए विकास". Nature Reviews. Microbiology. 7 (7): 526–36. doi:10.1038/nrmicro2164. PMID 19528959. S2CID 23376891.
- ↑ Jassem, Agatha; Prystajecky, Natalie; Marra, Fawziah; Kibsey, Pamela; Tan, Kennard; Umlandt, Patricia; Janz, Loretta; Champagne, Sylvie; Gamage, Bruce; Golding, George; Mulvey, Michael; Henry, Bonnie; Hoang, Linda (29 Mar 2016). "ब्रिटिश कोलंबिया, कनाडा में क्लॉस्ट्रिडियम डिफिसाइल उपभेदों की विशेषता: एक क्षेत्र में एनएपी1 बहुमत (2008) से नवीन तनाव प्रकार (2013) में बदलाव।". Canadian Journal of Infectious Diseases and Medical Microbiology. 2016: 8207418. doi:10.1155/2016/8207418. PMC 4904575. PMID 27366181.
- ↑ Collins, J.; Robinson, C.; Danhof, H.; Knetsch, C. W.; van Leeuwen, H. C.; Lawley, T. D.; Auchtung, J. M.; Britton, R. A. (2018). "आहार ट्रेहलोज़ महामारी क्लॉस्ट्रिडियम डिफिसाइल के विषाणु को बढ़ाता है". Nature. 553 (7688): 291–294. Bibcode:2018Natur.553..291C. doi:10.1038/nature25178. ISSN 0028-0836. PMC 5984069. PMID 29310122.
- ↑ He M, Sebaihia M, Lawley TD, Stabler RA, Dawson LF, Martin MJ, Holt KE, Seth-Smith HM, Quail MA, Rance R, Brooks K, Churcher C, Harris D, Bentley SD, Burrows C, Clark L, Corton C, Murray V, Rose G, Thurston S, van Tonder A, Walker D, Wren BW, Dougan G, Parkhill J (April 2010). "छोटे और लंबे समय के पैमाने पर क्लोस्ट्रीडियम डिफिसाइल की विकासवादी गतिशीलता". Proceedings of the National Academy of Sciences of the United States of America. 107 (16): 7527–32. Bibcode:2010PNAS..107.7527H. doi:10.1073/pnas.0914322107. PMC 2867753. PMID 20368420.
- ↑ Scientists map C. difficile strain – Institute of Public Affairs, Montreal
- ↑ Didelot X, Eyre DW, Cule M, Ip CL, Ansari MA, Griffiths D, Vaughan A, O'Connor L, Golubchik T, Batty EM, Piazza P, Wilson DJ, Bowden R, Donnelly PJ, Dingle KE, Wilcox M, Walker AS, Crook DW, A Peto TE, Harding RM (December 2012). "संचरण की जांच के लिए क्लोस्ट्रीडियम डिफिसाइल जीनोम का सूक्ष्मविकासवादी विश्लेषण" (PDF). Genome Biology. 13 (12): R118. doi:10.1186/gb-2012-13-12-r118. PMC 4056369. PMID 23259504. Archived from the original (PDF) on 2013-09-21. Retrieved 2014-08-30.
- ↑ 53.0 53.1 Hargreaves KR, Clokie MR (2014). "Clostridium difficile phages: Still difficult?". Frontiers in Microbiology. 5: 184. doi:10.3389/fmicb.2014.00184. PMC 4009436. PMID 24808893.
बाहरी संबंध
- Pathogen Safety Data Sheets: Infectious Substances – Clostridium Difficile[permanent dead link], Public Health Agency, Canada, 10 September 2014.
- Type strain of Clostridium difficile, BacDive - the Bacterial Diversity Metadatabase.