नियॉन
रसायन विज्ञान में, नियॉन एकरासायनिक तत्व है जिसका प्रतीक Ne है और परमाणु संख्या 10 है। यह एक उत्कृष्ट गैस है[1] जोतापमान और दबाव के लिए मानक स्थिति यों के अन्तर्गत एक रंगहीन, गंधहीन, अक्रिय एकपरमाणुक गैस है, जिसमें हवा का घनत्व लगभग दो-तिहाई है। 1898 में नाइट्रोजन , ऑक्सीजन , आर्गन और कार्बन डाइआक्साइड को हटा दिए जाने के बाद शुष्क हवा में शेष तीन दुर्लभ दुर्लभ अक्रिय तत्वों में से एक के रूप में (क्रीप्टोण और क्सीनन के साथ) इसकी खोज की गई थी। खोजी जाने वाली इन तीन दुर्लभ गैसों में नियॉन दूसरा था और इसके चमकीले लाल उत्सर्जन स्पेक्ट्रम से तुरंत एक नए तत्व के रूप में पहचाना गया। नियॉन नाम ग्रीक शब्द से लिया गया है, νέον, का नपुंसक एकवचन रूप νέος (neos), जिसका अर्थ है 'नया'। नियॉन रासायनिक रूप से अक्रिय गैस है, और कोई अनावेशित नियॉन यौगिक ज्ञात नहीं है। वर्तमान में ज्ञात नियॉन यौगिकों में आयनिक अणु, वैन डेर वाल्स बलों और clathrates द्वारा एक साथ रखे गए अणु शामिल हैं।
तत्वों के कॉस्मिक न्यूक्लियोजेनेसिस के दौरान, सितारों में अल्फा-कैप्चर फ्यूजन प्रक्रिया से बड़ी मात्रा में नियॉन का निर्माण होता है। हालांकि नियॉन ब्रह्मांड और सौर मंडल में एक बहुत ही सामान्य तत्व है (यह हाइड्रोजन , हीलियम , ऑक्सीजन और कार्बन के बाद लौकिक बहुतायत में पांचवें स्थान पर है), यह पृथ्वी पर दुर्लभ है। यह आयतन के अनुसार लगभग 18.2 पीपीएम वायु (यह लगभग आणविक या मोल अंश के समान है) और पृथ्वी की पपड़ी में एक छोटा अंश बनाता है। पृथ्वी और स्थलीय ग्रह |आंतरिक (स्थलीय) ग्रहों पर नियॉन की आपेक्षिक कमी का कारण यह है कि नियॉन अत्यधिक वाष्पशील (रसायन) है और इसे ठोस पदार्थों में स्थिर करने के लिए कोई यौगिक नहीं बनाता है। नतीजतन, यह शुरुआती सौर मंडल में नव प्रज्वलित सूर्य की गर्मी के तहत ग्रहों से बच निकला। यहां तक कि बृहस्पति का बाहरी वातावरण भी कुछ हद तक नियॉन से रहित है, हालांकि एक अलग कारण से।[2] जब लो-वाल्ट ेज नियॉन लैंप , हाई-वोल्टेज गीस्लर ट्यूब और नियॉन साइन में इस्तेमाल किया जाता है तो नियॉन एक अलग लाल-नारंगी चमक देता है।[3][4] नियॉन से निकलने वाली लाल उत्सर्जन रेखा हीलियम-नियॉन लेसरों के प्रसिद्ध लाल प्रकाश का कारण भी बनती है। कुछ प्लाज्मा ट्यूब और रेफ्रिजरेंट अनुप्रयोगों में नियॉन का उपयोग किया जाता है लेकिन इसके कुछ अन्य व्यावसायिक उपयोग हैं। यह तरल हवा के आंशिक आसवन द्वारा व्यावसायिक रूप से निकाला जाता है। चूंकि हवा ही एकमात्र स्रोत है, यह हीलियम से काफी अधिक महंगा है।
इतिहास

नियॉन की खोज 1898 में ब्रिटिश रसायनज्ञ सर विलियम रामसे (1852-1916) और मॉरिस ट्रैवर्स (1872-1961) ने लंदन में की थी।[5] नियॉन की खोज तब हुई जब रामसे ने हवा के एक नमूने को तब तक ठंडा किया जब तक कि वह तरल नहीं हो गया, फिर तरल को गर्म किया और उबालने पर गैसों को पकड़ लिया। गैसों नाइट्रोजन, ऑक्सीजन और आर्गन की पहचान की गई थी, लेकिन शेष गैसों को मोटे तौर पर बहुतायत के क्रम में अलग किया गया था, मई 1898 के अंत से शुरू होने वाले छह सप्ताह की अवधि में। सबसे पहले क्रिप्टन की पहचान की गई थी। अगला, क्रिप्टन को हटा दिए जाने के बाद, एक गैस थी जिसने स्पेक्ट्रोस्कोपिक डिस्चार्ज के तहत एक शानदार लाल बत्ती दी। जून में पहचानी गई इस गैस को नियॉन नाम दिया गया था, जो लैटिन नोवम ('नया') का ग्रीक एनालॉग है।[6] रामसे के बेटे द्वारा सुझाया गया। विद्युतीय रूप से उत्तेजित होने पर गैसीय नियॉन द्वारा उत्सर्जित विशिष्ट शानदार लाल-नारंगी रंग तुरंत नोट किया गया। ट्रैवर्स ने बाद में लिखा: ट्यूब से क्रिमसन लाइट की ज्वाला ने अपनी कहानी बताई और यह एक ऐसा दृश्य था जिस पर ध्यान दिया जाना चाहिए और कभी नहीं भूलना चाहिए।[7]
नियॉन के साथ एक दूसरी गैस की भी सूचना मिली थी, जिसका घनत्व लगभग आर्गन के समान था लेकिन एक अलग स्पेक्ट्रम के साथ - रामसे और ट्रैवर्स ने इसे मेटार्गन नाम दिया।[8][9] हालांकि, बाद के स्पेक्ट्रोस्कोपिक विश्लेषण से पता चला कि यह कार्बन मोनोआक्साइड से दूषित आर्गन है। अंत में, उसी टीम ने सितंबर 1898 में उसी प्रक्रिया से क्सीनन की खोज की।[8]
नियॉन की कमी ने मूर ट्यूब ों की तर्ज पर प्रकाश व्यवस्था के लिए इसके शीघ्र आवेदन को रोक दिया, जो नाइट्रोजन का उपयोग करते थे और जिनका 1900 के दशक की शुरुआत में व्यावसायीकरण किया गया था। 1902 के बाद, जॉर्ज क्लाउड की कंपनी तरल वायु ने उनके वायु-द्रवीकरण व्यवसाय के उपोत्पाद के रूप में नियॉन की औद्योगिक मात्रा का उत्पादन किया। दिसंबर 1910 में क्लाउड ने नियॉन की सीलबंद ट्यूब पर आधारित आधुनिक नियॉन लाइटिंग का प्रदर्शन किया। क्लाउड ने अपनी तीव्रता के कारण इनडोर घरेलू प्रकाश व्यवस्था के लिए नियॉन ट्यूबों को बेचने की संक्षिप्त कोशिश की, लेकिन बाजार विफल रहा क्योंकि घर के मालिकों ने रंग पर आपत्ति जताई थी। 1912 में, क्लाउड के सहयोगी ने नियॉन डिस्चार्ज ट्यूब को आकर्षक नियॉन साइन के रूप में बेचना शुरू किया और तुरंत अधिक सफल रहा। नियॉन ट्यूबों को 1923 में लॉस एंजिल्स पैकार्ड कार डीलरशिप द्वारा खरीदे गए दो बड़े नियॉन संकेतों के साथ यू.एस. में पेश किया गया था। चमक और आकर्षक लाल रंग ने नियॉन विज्ञापन को प्रतियोगिता से बिल्कुल अलग बना दिया।[10] नियॉन का तीव्र रंग और जीवंतता उस समय अमेरिकी समाज के बराबर थी, जो प्रगति की एक सदी का सुझाव दे रही थी और शहरों को सनसनीखेज नए वातावरण में बदल रही थी, जो विकीर्ण विज्ञापनों और इलेक्ट्रो-ग्राफिक वास्तुकला से भरा था।[11][12] नियॉन ने 1913 में परमाणु ओं की प्रकृति की बुनियादी समझ में एक भूमिका निभाई, जब जे जे थॉमसन ने नहर की किरणों की संरचना में अपने अन्वेषण के हिस्से के रूप में, एक चुंबकीय और एक विद्युत क्षेत्र के माध्यम से नियॉन आयनों की धाराओं को चैनल किया और विक्षेपण को मापा। एक फोटोग्राफिक प्लेट के साथ धाराएँ। थॉमसन ने फोटोग्राफिक प्लेट पर प्रकाश के दो अलग-अलग पैच देखे (छवि देखें), जिसने विक्षेपण के दो अलग-अलग परवलयों का सुझाव दिया। थॉमसन ने अंततः निष्कर्ष निकाला कि नियॉन गैस में कुछ परमाणु बाकी की तुलना में अधिक द्रव्यमान के थे। हालांकि उस समय थॉमसन द्वारा नहीं समझा गया था, यह [[ स्थिर आइसोटोप ]] परमाणुओं के समस्थानिकों की पहली खोज थी। थॉमसन का उपकरण उस उपकरण का एक कच्चा संस्करण था जिसे अब हम मास स्पेक्ट्रोमीटर कहते हैं।
समस्थानिक
नियॉन में तीन स्थिर समस्थानिक होते हैं: 20नहीं (90.48%), 21ने (0.27%) और 22नहीं (9.25%)।
21ने और 22Ne आंशिक रूप से मौलिक समस्थानिक और आंशिक रूप से न्यूक्लियोजेनिक (अर्थात पर्यावरण में न्यूट्रॉन या अन्य कणों के साथ अन्य न्यूक्लाइड्स की परमाणु प्रतिक्रियाओं द्वारा निर्मित) और प्राकृतिक प्रचुरता में उनकी विविधताओं को अच्छी तरह से समझा जाता है। इसके विपरीत, 20Ne (तारकीय न्यूक्लियोसिंथेसिस में बने प्रमुख प्राइमर्डियल आइसोटोप) को न्यूक्लियोजेनिक या रेडियम-धर्मी नहीं माना जाता है। की भिन्नता के कारण 20ने पृथ्वी में इस प्रकार गर्मागर्म बहस हुई है।[13][14]
न्यूक्लियोजेनिक नियॉन आइसोटोप उत्पन्न करने वाली प्रमुख परमाणु प्रतिक्रिया एँ कहाँ से शुरू होती हैं? 24मिलीग्राम और 25मिलीग्राम, जो उत्पादन करते हैं 21ने और 22Ne क्रमशः, न्यूट्रॉन पर कब्जा करने और एक अल्फा कण के तत्काल उत्सर्जन के बाद। प्रतिक्रियाओं का उत्पादन करने वाले न्यूट्रॉन ज्यादातर अल्फा कणों से द्वितीयक स्पैलेशन प्रतिक्रियाओं द्वारा उत्पादित होते हैं, बदले में यूरेनियम -श्रृंखला क्षय श्रृंखला से प्राप्त होते हैं। शुद्ध परिणाम निम्न की ओर एक प्रवृत्ति पैदा करता है 20नहीं/22ने और उच्चतर 21नहीं/22 </supNe अनुपात ग्रेनाइट जैसे यूरेनियम युक्त चट्टानों में देखा गया।[14] इसके अलावा, उजागर स्थलीय चट्टानों के समस्थानिक विश्लेषण ने ब्रह्मांडीय (ब्रह्मांडीय किरण) उत्पादन का प्रदर्शन किया है 21नहीं। यह आइसोटोप मैग्नीशियम , सोडियम , सिलिकॉन और अल्युमीनियम पर स्पेलेशन प्रतिक्रियाओं द्वारा उत्पन्न होता है। तीनों समस्थानिकों का विश्लेषण करके, मैग्मैटिक नियॉन और न्यूक्लियोजेनिक नियॉन से कॉस्मोजेनिक घटक को हल किया जा सकता है। इससे पता चलता है कि नियॉन सतह की चट्टानों और उल्कापिंडों की ब्रह्मांडीय जोखिम आयु निर्धारित करने में एक उपयोगी उपकरण होगा।[15] सौर पवन में नियॉन का अनुपात अधिक होता है 20न्यूक्लियोजेनिक और कॉस्मोजेनिक स्रोतों की तुलना में Ne।[14]ज्वालामुखी गैसों और हीरे के नमूनों में देखी गई नियॉन सामग्री भी समृद्ध होती है 20नहीं, एक आदिम, संभवतः सौर उत्पत्ति का सुझाव दे रहा है।[16]
विशेषताएं
हीलियम के बाद नियॉन दूसरी सबसे हल्की नोबल गैस है। यह डिस्चार्ज ट्यूब में लाल-नारंगी चमकता है। इसमें लिक्विड हीलियम की रेफ्रिजरेटिंग क्षमता (प्रति यूनिट वॉल्यूम) से 40 गुना और लिक्विड हाइड्रोजन से तीन गुना ज्यादा है।[17]अधिकांश अनुप्रयोगों में यह हीलियम की तुलना में कम खर्चीला प्रशीतक है।[18][19]
नियॉन प्लाज्मा में सामान्य वोल्टेज और सभी महान गैसों की धाराओं में सबसे तीव्र प्रकाश निर्वहन होता है। इस सीमा में कई रेखाओं के कारण इस प्रकाश का औसत रंग मानव आँख के लिए लाल-नारंगी है; इसमें एक मजबूत हरी रेखा भी शामिल है, जो छिपी हुई है, जब तक कि दृश्य घटकों को स्पेक्ट्रोस्कोप द्वारा फैलाया नहीं जाता।[20]
नियॉन प्रकाश के दो बिल्कुल भिन्न प्रकार आम उपयोग में हैं। नियॉन लैंप आम तौर पर छोटे होते हैं, जिनमें अधिकांश 100 और 250 वोल्ट के बीच काम करते हैं।[21] उनका व्यापक रूप से पावर-ऑन संकेतक और सर्किट-परीक्षण उपकरण के रूप में उपयोग किया गया है, लेकिन प्रकाश उत्सर्जक डायोड (एल ई डी) अब उन अनुप्रयोगों में हावी हैं। ये साधारण नियॉन डिवाइस प्लाज्मा प्रदर्शन के अग्रदूत थे।[22][23] नियॉन संकेत आमतौर पर बहुत अधिक वोल्टेज (2-15 किलोवोल्ट ) पर काम करते हैं, और चमकदार ट्यूब आमतौर पर मीटर लंबी होती हैं।[24] ग्लास टयूबिंग अक्सर साइनेज के आकार और अक्षरों के साथ-साथ वास्तुशिल्प और कलात्मक अनुप्रयोगों में बनाई जाती है।
घटना
नियॉन के स्थिर समस्थानिक तारों में उत्पन्न होते हैं। नियॉन का सबसे प्रचुर मात्रा में आइसोटोप 20Ne (90.48%) तारकीय न्यूक्लियोसिंथेसिस की कार्बन जलाने की प्रक्रिया में कार्बन और कार्बन के परमाणु संलयन द्वारा निर्मित होता है। इसके लिए 500 मेगाकेल्विन से ऊपर के तापमान की आवश्यकता होती है, जो 8 से अधिक सौर द्रव्यमान वाले तारों के कोर में होता है।[25][26]
नियॉन सार्वभौमिक पैमाने पर प्रचुर मात्रा में है; यह हाइड्रोजन, हीलियम, ऑक्सीजन और कार्बन (रासायनिक तत्व देखें) के बाद ब्रह्मांड में द्रव्यमान द्वारा रासायनिक तत्वों की प्रचुरता है।[27] पृथ्वी पर इसकी सापेक्ष दुर्लभता, हीलियम की तरह, इसकी सापेक्ष लपट, बहुत कम तापमान पर उच्च वाष्प दबाव, और रासायनिक जड़ता के कारण है, सभी गुण जो इसे संघनक गैस और धूल के बादलों में फंसने से रोकते हैं, जो इसे बनाते हैं। पृथ्वी जैसे छोटे और गर्म ठोस ग्रह। नियॉन मोनोएटोमिक है, जो इसे डायटोमिक नाइट्रोजन और ऑक्सीजन के अणुओं से हल्का बनाता है जो पृथ्वी के वायुमंडल का बड़ा हिस्सा बनाते हैं; नीयन से भरा एक गुब्बारा हवा में ऊपर उठेगा, यद्यपि हीलियम के गुब्बारे की तुलना में अधिक धीरे-धीरे।[28] ब्रह्मांड में नियॉन की बहुतायत 750 में लगभग 1 भाग है; सूर्य में और संभवतः प्रोटो-सोलर सिस्टम नेबुला में, 600 में लगभग 1 भाग। गैलीलियो अंतरिक्ष यान वायुमंडलीय प्रवेश जांच में पाया गया कि बृहस्पति के ऊपरी वातावरण में भी, नियॉन की प्रचुरता लगभग 10 के एक कारक से कम (घट गई) है। , द्रव्यमान द्वारा 6,000 में 1 भाग के स्तर तक। यह संकेत दे सकता है कि यहां तक कि बर्फ-ग्रह, जो बाहरी सौर मंडल से नियॉन को बृहस्पति में लाए थे, एक ऐसे क्षेत्र में बने जो नियॉन वायुमंडलीय घटक को बनाए रखने के लिए बहुत गर्म था (बृहस्पति पर भारी अक्रिय गैसों की प्रचुरता कई गुना अधिक है जो बृहस्पति में पाए जाते हैं) रवि)।[29] नियॉन में पृथ्वी के वायुमंडल में 55,000 में 1 भाग, या मात्रा के अनुसार 18.2 पीपीएम (यह लगभग अणु या मोल अंश के समान है), या द्रव्यमान द्वारा 79,000 वायु में 1 भाग शामिल है। इसमें क्रस्ट में एक छोटा अंश शामिल है। यह तरलीकृत हवा के क्रायोजेनिक भिन्नात्मक आसवन द्वारा औद्योगिक रूप से निर्मित होता है।[17]
17 अगस्त 2015 को, चंद्र वायुमंडल और धूल पर्यावरण एक्सप्लोरर (एलएडीईई) अंतरिक्ष यान के साथ अध्ययन के आधार पर, नासा के वैज्ञानिकों ने चंद्रमा के बहिर्मंडल में नियॉन का पता लगाने की सूचना दी।[30]
रसायन विज्ञान
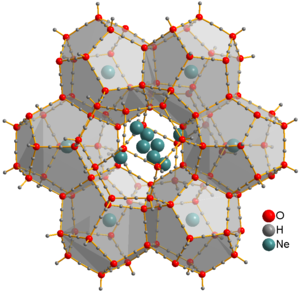
नियॉन पहला पी-ब्लॉक नोबल गैस है, और इलेक्ट्रॉनों का एक सच्चा ऑक्टेट वाला पहला तत्व है। यह रासायनिक रूप से निष्क्रिय है: जैसा कि इसके हल्के एनालॉग, हीलियम के मामले में है, कोई दृढ़ता से बाध्य तटस्थ नियॉन यौगिकों की पहचान नहीं की गई है। आयन [निकटवर्ती]+, [Nehydrogen]+, और [हेने]+ ऑप्टिकल और जन स्पेक्ट्रोमेट्री अध्ययनों से देखा गया है।[17]सॉलिड नियॉन क्लैथ्रेट हाइड्रेट को पानी की बर्फ और नियॉन गैस से 350-480 एमपीए के दबाव और लगभग -30 डिग्री सेल्सियस के तापमान पर तैयार किया गया था।[32] Ne परमाणु पानी से बंधे नहीं हैं और इस सामग्री के माध्यम से स्वतंत्र रूप से आगे बढ़ सकते हैं। क्लैथ्रेट को कई दिनों तक निर्वात कक्ष में रखकर निकाला जा सकता है, जिससे बर्फ XVI , पानी का सबसे कम घना क्रिस्टलीय रूप प्राप्त होता है।[31] परिचित इलेक्ट्रोनगेटिविटी #पॉलिंग इलेक्ट्रोनगेटिविटी रासायनिक बंधन ऊर्जा पर निर्भर करती है, लेकिन ऐसे मूल्यों को स्पष्ट रूप से निष्क्रिय हीलियम और नियॉन के लिए नहीं मापा गया है। इलेक्ट्रोनगेटिविटी # एलन इलेक्ट्रोनगेटिविटी, जो केवल (मापने योग्य) परमाणु ऊर्जा पर निर्भर करती है, नियॉन को सबसे अधिक विद्युतीय तत्व के रूप में पहचानती है, जिसके बाद फ्लोरीन और हीलियम का स्थान आता है।
नियॉन का त्रिगुण बिंदु तापमान (24.5561 K) 1990 के अंतर्राष्ट्रीय तापमान पैमाने में एक परिभाषित निश्चित बिंदु है।[33]
उत्पादन
क्रायोजेनिक वायु पृथक्करण | एयर-सेपरेशन प्लांट्स में हवा से नियॉन का उत्पादन होता है। मुख्य रूप से नाइट्रोजन, नियॉन और हीलियम का एक गैस-चरण मिश्रण उच्च दबाव वायु-पृथक्करण कॉलम के शीर्ष पर मुख्य कंडेनसर से वापस ले लिया जाता है और नियॉन के आसवन के लिए एक साइड कॉलम के नीचे खिलाया जाता है।[34] इसके बाद इसे हीलियम से और शुद्ध किया जा सकता है।
यूक्रेन में लगभग 70% वैश्विक नियॉन आपूर्ति का उत्पादन होता है[35] रूस में इस्पात उत्पादन के उप-उत्पाद के रूप में।[36] As of 2020[update], कंपनी Iceblick , ओडेसा और मास्को में संयंत्रों के साथ, नियॉन के दुनिया के उत्पादन का 65 प्रतिशत, साथ ही क्रिप्टन और क्सीनन के 15% की आपूर्ति करती है।[37][38]
2022 की कमी
क्रीमिया के 2014 के रूसी कब्जे के बाद वैश्विक नियॉन की कीमतों में लगभग 600% की वृद्धि हुई,[39]कुछ चिप निर्माताओं को रूसी और यूक्रेनी आपूर्तिकर्ताओं से दूर जाने के लिए प्रेरित करना[40] और चीन में आपूर्तिकर्ताओं की ओर।[38]2022 में यूक्रेन पर रूसी आक्रमण ने भी यूक्रेन में दो कंपनियों को बंद कर दिया: एलएलसी «क्रायोइन इंजीनियरिंग» (Ukrainian: ТОВ «Кріоін Інжинірінг») और एलएलसी «इन्हाज» (Ukrainian: ТОВ «ІНГАЗ») क्रमशः ओडेसा और मारियुपोल में स्थित है; जिसने वैश्विक आपूर्ति का लगभग आधा उत्पादन किया।[39][41] बंद होने की संभावना 2020-वर्तमान वैश्विक चिप की कमी को तेज करने की भविष्यवाणी की गई थी | COVID-19 चिप की कमी,[38][37]जो आगे नियॉन उत्पादन को चीन में स्थानांतरित कर सकता है।[40]
आवेदन
नियॉन अक्सर नियॉन साइन में प्रयोग किया जाता है और एक अचूक चमकदार लाल-नारंगी रोशनी पैदा करता है। हालांकि अन्य रंगों के साथ ट्यूब लाइट को अक्सर नियॉन कहा जाता है, वे विभिन्न महान गैसों या फ्लोरोसेंट बल्ब प्रकाश के विभिन्न रंगों का उपयोग करते हैं।
नियॉन का उपयोग वेक्यूम - ट्यूब , हाई-वोल्टेज इंडिकेटर्स, तड़ित पकड़क , वेवमीटर ट्यूब, टेलीविजन ट्यूब और हीलियम-नियॉन लेजर में किया जाता है। तरलीकृत नियॉन व्यावसायिक रूप से क्रायोजेनिक रेफ्रिजरेंट के रूप में उन अनुप्रयोगों में उपयोग किया जाता है जिन्हें अधिक चरम तरल-हीलियम प्रशीतन के साथ प्राप्य कम तापमान सीमा की आवश्यकता नहीं होती है।
नियॉन, तरल या गैस के रूप में, अपेक्षाकृत महंगा है - छोटी मात्रा के लिए, तरल नियॉन की कीमत तरल हीलियम के 55 गुना से अधिक हो सकती है। नियॉन का खर्च चलाना नियॉन की दुर्लभता है, जो हीलियम के विपरीत, इसे वातावरण से छानकर केवल प्रयोग करने योग्य मात्रा में प्राप्त किया जा सकता है।
सेमीकंडक्टर उद्योग
As of 2022[update] गैस मिश्रण जिसमें नियॉन शामिल है, का उपयोग अत्यधिक पराबैंगनी लिथोग्राफी के लिए लेज़रों को शक्ति प्रदान करने के लिए किया जाता है।[39]
यह भी देखें
- विस्तार अनुपात
- शिथिराति चिन्ह
- नियॉन लैंप
संदर्भ
- ↑ Group 18 refers to the modern numbering of the periodic table. Older numberings described the rare gases as Group 0 or Group VIIIA (sometimes shortened to 8). See also Group (periodic table).
- ↑ Wilson, Hugh F.; Militzer, Burkhard (March 2010), "Sequestration of Noble Gases in Giant Planet Interiors", Physical Review Letters, 104 (12): 121101, arXiv:1003.5940, Bibcode:2010PhRvL.104l1101W, doi:10.1103/PhysRevLett.104.121101, PMID 20366523, S2CID 9850759, 121101.
- ↑ Coyle, Harold P. (2001). प्रोजेक्ट स्टार: द यूनिवर्स इन योर हैंड्स. Kendall Hunt. p. 464. ISBN 978-0-7872-6763-6.
- ↑ Kohmoto, Kohtaro (1999). "Phosphors for lamps". In Shionoya, Shigeo; Yen, William M. (eds.). फॉस्फर हैंडबुक. CRC Press. p. 940. ISBN 978-0-8493-7560-6.
- ↑ Ramsay, William, Travers, Morris W. (1898). "आर्गन के साथियों पर". Proceedings of the Royal Society of London. 63 (1): 437–440. doi:10.1098/rspl.1898.0057. S2CID 98818445.
{{cite journal}}: CS1 maint: multiple names: authors list (link) - ↑ "नियॉन: इतिहास". Softciências. Archived from the original on 2007-03-14. Retrieved 2007-02-27.
- ↑ Weeks, Mary Elvira (2003). तत्वों की खोज: तीसरा संस्करण (पुनर्मुद्रण). Kessinger Publishing. p. 287. ISBN 978-0-7661-3872-8. Archived from the original on 2015-03-22.
- ↑ 8.0 8.1 Ramsay, Sir William (December 12, 1904). "Nobel Lecture – The Rare Gases of the Atmosphere". nobelprize.org. Nobel Media AB. Archived from the original on 13 November 2015. Retrieved 15 November 2015.
- ↑ Ramsay, William; Travers, Morris W. (1898). "आर्गन के साथियों पर". Proceedings of the Royal Society of London. 63 (1): 437–440. doi:10.1098/rspl.1898.0057. ISSN 0370-1662. S2CID 98818445.
- ↑ Mangum, Aja (December 8, 2007). "Neon: A Brief History". New York Magazine. Archived from the original on April 15, 2008. Retrieved 2008-05-20.
- ↑ Golec, Michael J. (2010). "लोगो/स्थानीय तीव्रता: लैकन, द डिस्कोर्स ऑफ़ द अदर, एंड द सॉलिसिटेशन टू "एंज़ॉय"". Design and Culture. 2 (2): 167–181. doi:10.2752/175470710X12696138525622. S2CID 144257608.
- ↑ Wolfe, Tom (October 1968). "इलेक्ट्रो-ग्राफिक आर्किटेक्चर". Architecture Canada.
- ↑ Dickin, Alan P (2005). "Neon". रेडियोजेनिक आइसोटोप भूविज्ञान. p. 303. ISBN 978-0-521-82316-6.
- ↑ 14.0 14.1 14.2 Resources on Isotopes Periodic Table--Neon at the U.S. Geological Survey, by Eric Caldwell, posted January 2004, retrieved February 10, 2011
- ↑ "नियॉन: आइसोटोप". Softciências. Archived from the original on 2012-11-15. Retrieved 2007-02-27.
- ↑ Anderson, Don L. "हीलियम, नियॉन और आर्गन". Mantleplumes.org. Archived from the original on 2006-05-28. Retrieved 2006-07-02.
- ↑ 17.0 17.1 17.2 Cite error: Invalid
<ref>tag; no text was provided for refs namedCRC - ↑ "NASSMC: समाचार बुलेटिन". December 30, 2005. Archived from the original on February 13, 2007. Retrieved 2007-03-05.
- ↑ Mukhopadhyay, Mamata (2012). क्रायोजेनिक इंजीनियरिंग के मूल सिद्धांत. p. 195. ISBN 9788120330573. Archived from the original on 2017-11-16.
- ↑ "प्लाज्मा". Archived from the original on 2007-03-07. Retrieved 2007-03-05.
- ↑ Baumann, Edward (1966). नियॉन लैंप और गैस डिस्चार्ज ट्यूब के अनुप्रयोग. Carlton Press.
- ↑ Myers, Robert L. (2002). प्रदर्शन इंटरफेस: बुनियादी बातें और मानक. John Wiley and Sons. pp. 69–71. ISBN 978-0-471-49946-6. Archived from the original on 2016-06-29.
प्लाज्मा डिस्प्ले साधारण नियॉन लैंप से निकटता से संबंधित हैं।
- ↑ Weber, Larry F. (April 2006). "प्लाज्मा डिस्प्ले पैनल का इतिहास". IEEE Transactions on Plasma Science. 34 (2): 268–278. Bibcode:2006ITPS...34..268W. doi:10.1109/TPS.2006.872440. S2CID 20290119. Paid access.
- ↑ "एएनएसआई चमकदार ट्यूब फुटेज चार्ट" (PDF). American National Standards Institute (ANSI). Archived (PDF) from the original on 2011-02-06. Retrieved 2010-12-10. Reproduction of a chart in the catalog of a lighting company in Toronto; the original ANSI specification is not given.
- ↑ Clayton, Donald (2003). ब्रह्मांड में आइसोटोप की हैंडबुक: हाइड्रोजन से गैलियम. Cambridge University Press. pp. 106–107. ISBN 978-0521823814.
- ↑ Ryan, Sean G.; Norton, Andrew J. (2010). तारकीय विकास और न्यूक्लियोसिंथेसिस. Cambridge University Press. p. 135. ISBN 978-0-521-13320-3.
- ↑ Asplund, Martin; Grevesse, Nicolas; Sauval, A. Jacques; Scott, Pat (2009). "सूर्य की रासायनिक संरचना". Annual Review of Astronomy and Astrophysics. 47 (1): 481–522. arXiv:0909.0948. Bibcode:2009ARA&A..47..481A. doi:10.1146/annurev.astro.46.060407.145222. S2CID 17921922.
- ↑ Gallagher, R.; Ingram, P. (2001-07-19). हायर टीयर के लिए केमिस्ट्री. University Press. p. 282. ISBN 978-0-19-914817-2.
- ↑ Morse, David (January 26, 1996). "गैलीलियो जांच विज्ञान परिणाम". Galileo Project. Archived from the original on February 24, 2007. Retrieved 2007-02-27.
- ↑ Steigerwald, William (17 August 2015). "NASA के LADEE अंतरिक्ष यान ने चंद्र वातावरण में नियॉन खोजा". NASA. Archived from the original on 19 August 2015. Retrieved 18 August 2015.
- ↑ 31.0 31.1 Falenty, Andrzej; Hansen, Thomas C.; Kuhs, Werner F. (2014). "प्रकार sII क्लैथ्रेट हाइड्रेट को खाली करने से प्राप्त बर्फ XVI का गठन और गुण". Nature. 516 (7530): 231–3. Bibcode:2014Natur.516..231F. doi:10.1038/nature14014. PMID 25503235. S2CID 4464711.
- ↑ Yu, X.; Zhu, J.; Du, S.; Xu, H.; Vogel, S. C.; Han, J.; Germann, T. C.; Zhang, J.; Jin, C.; Francisco, J. S.; Zhao, Y. (2014). "बर्फ II-संरचित नियॉन हाइड्रेट की क्रिस्टल संरचना और एनकैप्सुलेशन गतिकी". Proceedings of the National Academy of Sciences of the United States of America. 111 (29): 10456–61. Bibcode:2014PNAS..11110456Y. doi:10.1073/pnas.1410690111. PMC 4115495. PMID 25002464.
- ↑ "1990 के अंतर्राष्ट्रीय तापमान पैमाने के लिए इंटरनेट संसाधन". Archived from the original on 2009-08-15. Retrieved 2009-07-07.
- ↑ R. Norris Shreve; Joseph Brink (1977). रासायनिक प्रक्रिया उद्योग (4th ed.). p. 113. ISBN 0-07-057145-7.
- ↑ "समझाया: क्यों रूस-यूक्रेन संकट अर्धचालकों में कमी का कारण बन सकता है". MSN (in English). The Indian Express.
- ↑ Alper, Alexandra (2022-03-11). "विशेष: यूक्रेन पर रूस के हमले ने चिप्स के लिए दुनिया के आधे नियॉन उत्पादन को रोक दिया". Reuters (in English). Retrieved 2022-03-16.
- ↑ 37.0 37.1 "दुर्लभ गैस आपूर्तिकर्ता नवाचार के लिए जाने जाते हैं". The European Times. 2020.
- ↑ 38.0 38.1 38.2 यूक्रेन युद्ध में चिप्स के लिए नीयन चेतावनी रोशनी चमकती है, रायटर, 2022-02-25
- ↑ 39.0 39.1 39.2 Times, Financial (4 March 2022). "गैस पर कम: यूक्रेन के आक्रमण ने चिपमेकिंग के लिए आवश्यक नियॉन की आपूर्ति को रोक दिया". Ars Technica (in English). Retrieved 13 March 2022.
- ↑ 40.0 40.1 "चिप निर्माता अब सीमित प्रभाव देखते हैं, क्योंकि रूस यूक्रेन पर आक्रमण करता है". CNBC (in English). 24 February 2022.
- ↑ "रूस और यूक्रेन ने माइक्रोसर्किट के विश्व उत्पादन को नीचे लाया". CNews.ru (in русский). March 11, 2022. Retrieved 2022-04-17.
बाहरी संबंध
- Neon at The Periodic Table of Videos (University of Nottingham)
- WebElements.com – Neon.
- It's Elemental – Neon
- USGS Periodic Table – Neon
- Atomic Spectrum of Neon
- Neon Museum, Las Vegas