ऑर्गनोसेलेनियम रसायन विज्ञान
ऑर्गोसेलेनियम यौगिक (या सेलेनो-ऑर्गेनिक) रासायनिक यौगिक हैं जिनमें कार्बन -से-सेलेनियम तक रासायनिक बंधन होते हैं। ऑर्गनोसेलेनियम रसायन विज्ञान उनके गुणों और प्रतिक्रियाशीलता की खोज करने वाला संबंधित विज्ञान है।[1][2][3] सेलेनियम ऑक्सीजन और सल्फर के साथ समूह 16 तत्वो या काल्कोजन से संबंधित है, और रसायन विज्ञान में समानता की उम्मीद की जा सकती है। ऑर्गोसेलेनियम यौगिक परिवेशी जल, मिट्टी और तलछट में अनुरेखन स्तर पर पाए जाते हैं।[4] सेलेनियम ऑक्सीकरण अवस्था -2, +2, +4, +6 के साथ मौजूद हो सकता है। Se (द्वितीय) ऑर्गोसेलेनियम रसायन विज्ञान में प्रमुख रूप है। समूह 16 कॉलम के नीचे, बॉन्ड की ताकत तेजी से कम हो जाती है (C-Se बॉन्ड के लिए 234 किलोजूल सल (यूनिट) और इस बॉन्ड के लिए 272 Kj/मोल) और बॉन्ड की लंबाई लंबी हो जाती है (C-Se 198 pm, C-S 181pm और C-O 141pm। सेलेनियम यौगिक संबंधित गन्धक यौगिकों की तुलना में अधिक नाभिकरागी होते हैं और अधिक अम्लीय भी होते हैं। pka के मान XH2 ऑक्सीजन के लिए 16, गंधक के लिए 7 और सेलेनियम के लिए 3.8 हैं। सल्फ़ोक्साइड के विपरीत, संबंधित सेलेनॉक्साइड बीटा-प्रोटॉन की उपस्थिति में अस्थिर होते हैं और इस संपत्ति का उपयोग सेलेनियम की कई कार्बनिक प्रतिक्रियाओं में किया जाता है, विशेष रूप से सेलेनॉक्साइड ऑक्सीकरण और सेलेनॉक्साइड निष्कासन में है।
पृथक होने वाला पहला ऑर्गोसेलेनियम यौगिक 1836 में डायथाइल सेलेनाइड था।[5][6]
ऑर्गोसेलेनियम यौगिकों का संरचनात्मक वर्गीकरण
* Selenol s(RSeH) मद्यसार (रसायन विज्ञान) और थियोल के सेलेनियम समकक्ष हैं। ये यौगिक अपेक्षाकृत अस्थिर हैं और सामान्यतः एक अप्रिय गंध है। बेंजीनसेलेनोल (जिसे सेलेनाफेनॉल या PhSeh भी कहा जाता है) अधिक अम्लीय (Pka 5.9) है थियोफेनॉल (pKa 6.5) की तुलना में है।
और डाइफेनिलडिसेलेनाइड के लिए अधिक आसानी से ऑक्सीकरण करता है। सेलेनाफेनॉल डिफेनिलडिसेलेनाइड की कमी से तैयार किया जाता है।[7]
- डिसेलेनाइड्स (R−Se−Se−R) रसायनिक और डाइसल्फ़ाइड के सेलेनियम समकक्ष हैं। वे अधिक प्रतिक्रियाशील ऑर्गोसेलेनियम अभिकर्मकों जैसे सेलेनॉल्स और सेलेनाइल हैलाइड्स के लिए उपयोगी निधानी-स्थिर अग्रदूत हैं। कार्बनिक रसायन विज्ञान में सबसे अच्छी तरह से जाना जाने वाला डाइफेनिलडिसेलेनाइड है, जिसे फेनिलमैग्नेशियम पिष्टोक्ति और सेलेनियम से तैयार किया जाता है, जिसके बाद उत्पाद PhSeMgBr का ऑक्सीकरण होता है।[8]
- सेलेनाइल हैलाइड (R−Se−Cl, R−Se−Br) डिसेलेनाइड्स के हैलोजनीकरण द्वारा तैयार किए जाते हैं। डाइफेनिलडिसेलेनाइड का ब्रोमिनेशन फेनिलसेलेनाइल पिष्टोक्ति (PhSeBr) देता है। ये यौगिक PhSe+ के स्रोत हैं
- सेलेनाइड्स (R−Se−R), जिन्हें सेलेनोएथर भी कहा जाता है, व्योम और सल्फाइड (कार्बनिक) के सेलेनियम समकक्ष हैं। एक उदाहरण डाइमिथाइलसेलेनाइड है ((CH3)2Se)। ये सबसे प्रचलित ऑर्गोसेलेनियम यौगिक हैं। सममित सेलेनाइड सामान्यतः क्षार धातु सेलेनाइड लवण के क्षारीकरण द्वारा तैयार किए जाते हैं, उदा। सोडियम सेलेनाइड । असममित सेलेनाइड्स सेलेनोएट्स के क्षारीकरण द्वारा तैयार किए जाते हैं। ये यौगिक आमतौर पर नाभिकरागी के रूप में प्रतिक्रिया करते हैं, उदा। सेलेनियम लवण R'RRSe+X- देने के लिए एल्काइल हैलाईड (R'−X) के साथ द्विसंयोजक सेलेनियम उच्चसंयोजी सेलेनियम केंद्र बनाने के लिए नरम हेटेरोएटम के साथ भी परस्पर प्रभाव डाल सकता है।[6] वे कुछ परिस्थितियों में वैद्युतकणसंचलन के रूप में भी प्रतिक्रिया करते हैं, उदा। ऑर्गेनोलिथियम अभिकर्मकों (R'Li) के साथ जटिल R'RRSe_Li+.
- सेलेनॉक्साइड्स (R−Se(O)−R) सल्फोक्साइड के सेलेनियम मकक्ष हैं। उन्हें आगे सेलेनोन R−Se(O) 2R, सल्फोन के सेलेनियम सादृश्य में ऑक्सीकृत किया जा सकता है
- सेलेनेनिक अम्ल (RSe−OH) सेलेनॉल के ऑक्सीकरण में मध्यवर्ती हैं। वे कुछ सेलेनोएंजाइम में होते हैं, जैसे ग्लुटेथियॉन पेरोक्सिडेस
- सेलेनिक अम्ल (RSe(O)OH) सल्फिनिक अम्ल के अनुरूप हैं।
- सेलेनोनिक अम्ल (RSe(O)2OH) सल्फोनिक अम्ल के अनुरूप हैं।
- पेरोक्सीसेलेनिक अम्ल (RSe(O)OOH) एपॉक्सीडेशन प्रतिक्रियाओं और बेयर-विलीगर ऑक्सीकरण को उत्प्रेरित करता है।
- सेलेनुरेन्स अति संयोजकता ऑर्गोसेलेनियम यौगिक हैं, जो औपचारिक रूप से टेट्राहैलाइड्स जैसे कि SeCl4 से प्राप्त होते हैं उदाहरण ArSeCl3 प्रकार के हैं[9] विरंजक सेलेनियम ऑक्सीडिक्लोराइड के क्लोरीनीकरण द्वारा प्राप्त किए जाते हैं।
- सेलेनिरेन तीन सदस्यीय वलय हैं (जनक: C2H4Se) थाइइरेन वर्ग से संबंधित है, लेकिन, थिइरान्स के विपरीत, सेलेनिरेन गतिज रूप से अस्थिर हैं, सेलेनियम को सीधे (ऑक्सीकरण के बिना) बाहर निकालकर हाइड्रोकार्बन बनाते हैं। इस संपत्ति का उपयोग सिंथेटिक कार्बनिक रसायन विज्ञान में किया गया है।[10]
- सेलोंस (R2C=Se) कीटोन्स के सेलेनियम एनालॉग्स हैं। ऑलिगोमेराइज़ करने की उनकी प्रवृत्ति के कारण वे दुर्लभ हैं।[11] डिसेलेनोबेंजोक्विनोन एक धातु परिसर के रूप में स्थिर है।[12] सेलेनोरिया एक स्थिर यौगिक का एक उदाहरण है जिसमें C=Se बंध होता है।
प्रकृति में ऑर्गेनोसेलेनियम यौगिक
सेलेनियम, ऑर्गोसेलेनियम यौगिकों के रूप में, एक आवश्यक सूक्ष्म पोषक तत्व है जिसकी आहार से अनुपस्थिति हृदय की मांसपेशियों और कंकाल की शिथिलता का कारण बनती है। ऑक्सीकर क्षति के खिलाफ कोशिकीय रक्षा और प्रतिरक्षा प्रणाली के सही कामकाज के लिए ऑर्गेनोसेलेनियम यौगिकों की आवश्यकता होती है। वे समय से पहले बुढ़ापा और कैंसर की रोकथाम में भी भूमिका निभा सकते हैं। जैवसंश्लेषण में प्रयुक्त Se का स्रोत सेलेनोफॉस्फेट सिंथेटेस है।
ग्लूटाथियोन ऑक्सीडेज एक किण्वक है जिसके सक्रिय स्थल पर सेलेनॉल होता है। उच्च पौधों में ऑर्गेनोसेलेनियम यौगिक पाए गए हैं। उदाहरण के लिए, विवेचनात्मक रूप से संयोजित प्लाविका द्रव्यमान स्पेक्ट्रोमेट्री (HPLC-ICP-MS) के साथ संयुक्त उच्च-प्रदर्शन तरल क्रोमैटोग्राफी की तकनीक का उपयोग करके लहसुन के विश्लेषण पर, यह पाया गया कि γ-ग्लूटामाइल-Se-मिथाइलसेलेनोसिस्टीन प्रमुख Se-युक्त घटक था, Se-मिथाइलसेलेनोसिस्टीन व Se-मिथाइलसेलेनोसिस्टीन की कम मात्रा के साथ। कच्चा लहसुन खाने के बाद मानव सांस में डाइमिथाइल सेलेनाइड और एलिल मिथाइल सेलेनाइड की अनुरेख मात्रा पाई जाती है।[13]
सेलेनोसिस्टीन और सेलेनोमेथियोनिन
सेलेनोसिस्टीन, जिसे इक्कीसवां अमीनो अम्ल कहा जाता है, कुछ जीवों में राइबोसोम-निर्देशित प्रोटीन संश्लेषण के लिए आवश्यक है।[14] 25 से अधिक सेलेनियम युक्त प्रोटीन (सेलेनोप्रोटीन) अब ज्ञात हैं।[15] अधिकांश सेलेनियम-निर्भर किण्वक में सेलेनो सिस्टीन होता है, जो सिस्टीन समधर्मी से संबंधित होता है लेकिन सेलेनियम के साथ गंधक की जगह लेता है। यह एमिनो अम्ल DNA द्वारा एक विशेष तरीके से आनुवंशिक संहिता है। सेलेनोसल्फाइड्स को जैव रासायनिक मध्यवर्ती के रूप में भी प्रस्तावित किया जाता है।
सेलेनोमेथियोनिन एक सेलेनाइड युक्त अमीनो अम्ल है जो स्वाभाविक रूप से भी होता है, लेकिन पोस्ट-ट्रांसक्रिप्शनल संशोधन द्वारा उत्पन्न होता है।
कार्बनिक संश्लेषण में ऑर्गेनोसेलेनियम रसायन
ऑर्गेनोसेलेनियम यौगिक कार्बनिक संश्लेषण में अभिकर्मकों के विशिष्ट लेकिन उपयोगी संग्रह हैं, प्रायः उन्हें सामान्यतः नियामक संतति के कारण औषधीयों के लिए उपयोगी प्रक्रियाओं से बाहर रखा गया है। उनकी उपयोगिता कुछ विशेषताओं पर निर्भर करती है, जिसमें (i) C-Se बॉन्ड की कमजोरी और (ii) द्विसंयोजक सेलेनियम यौगिक का आसान ऑक्सीकरण शामिल है।
विनाइलिक सेलेनाइड्स
विनाइलिक सेलेनाइड्स ऑर्गोसेलेनियम यौगिक हैं जो कार्बनिक संश्लेषण में एक भूमिका निभाते हैं, विशेष रूप से कार्यात्मक एल्केनेस के लिए सुविधाजनक त्रिविम वरणात्मक मार्गों के विकास में।[16] यद्यपि विनाइलिक सेलेनाइड्स की तैयारी के लिए विभिन्न मार्गों का उल्लेख किया गया है, एक अधिक उपयोगी प्रक्रिया न्यूक्लियोफिलिक या इलेक्ट्रॉनरागी ऑर्गोसेलेनियम के अलावा टर्मिनल या आंतरिक एल्काइनेस पर केंद्रित है।[17][18][19][20] उदाहरण के लिए, एल्केनेस के लिए सेलेनोफेनॉल का न्यूक्लियोफिलिक जोड़ , अधिमानतः, कमरे के तापमान पर लंबे समय तक प्रतिक्रिया समय के बाद Z-विनाइलिक सेलेनाइड्स देता है। उच्च तापमान पर प्रतिक्रिया तेज होती है; हालाँकि, Z- और E-विनाइलिक सेलेनाइड्स का मिश्रण लगभग 1:1 के अनुपात में प्राप्त किया गया था।[21] दूसरी ओर, व्यसन त्रिगुण आबंध पर प्रतिस्थापन की प्रकृति पर निर्भर करते हैं। इसके विपरीत, विनाइलिक सेलेनाइड्स को दुर्ग-उत्प्रेरित हाइड्रोसेलेनेशन ऑफ अल्काइन्स द्वारा तैयार किया जा सकता है ताकि मार्कोवनिकोव की अच्छी पैदावार हो सके। ऊपर सचित्र विनाइलिक सेलेनाइड्स तैयार करने के तरीकों से जुड़ी कुछ सीमाएँ हैं; वर्णित प्रक्रियाएं डायऑर्गनॉयल डिसेलेनाइड्स या सेलेनोफेनॉल को शुरुआती सामग्री के रूप में नियोजित करती हैं, जो अस्थिर और अस्थिर होती हैं और एक अप्रिय गंध होती है। साथ ही, इन यौगिकों की तैयारी जटिल है।
सेलेनॉक्साइड ऑक्सीकरण
सेलेनियम डाइऑक्साइड कार्बनिक ऑक्सीकरण में उपयोगी है। विशेष रूप से, C2 एक एलिलिक मेथिलीन समूह को संबंधित एलिल अल्कोहल में बदल देगा। कई अन्य अभिकर्मक इस प्रतिक्रिया के बारे में बताते हैं।
प्रतिक्रिया तंत्र के संदर्भ में, SeO2 और एलिलिक क्रियाधार एक एनी प्रतिक्रिया से शुरू होने वाली पेरीसाइक्लिक प्रक्रिया के माध्यम से प्रतिक्रिया करता है जो C-H अनुबंध को सक्रिय करता है। दूसरा चरण एक [2,3] सिग्मैट्रोपिक प्रतिक्रिया है। सेलेनियम डाइऑक्साइड से जुड़े ऑक्सीकरण प्रायः सेलेनियम यौगिक की उत्प्रेरक मात्रा के साथ और हाइड्रोजन रसायनिक जैसे एक बलिदान उत्प्रेरक या सह-अपचायक की उपस्थिति में किए जाते हैं।
SeO2-आधारित ऑक्सीकरण कभी-कभी कार्बोनिल यौगिकों जैसे किटोन्स को वहन करते हैं,[22] β पाइनीन [23] और cyclohexanone ऑक्सीकरण 1,2-साइक्लोहेक्सानेडियोन के लिए।[24] α-मेथिलीन समूह वाले कीटोन्स का ऑक्सीकरण डाइकेटोन प्रदान करता है। सेलेनियम ऑक्साइड के साथ इस प्रकार के ऑक्सीकरण को रिले ऑक्सीकरण कहा जाता है।[25]
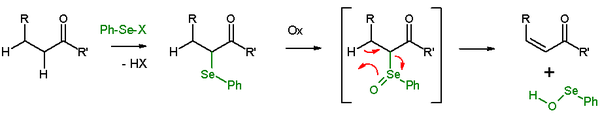
सेलेनॉक्साइड उन्मूलन
β-हाइड्रोजन की उपस्थिति में, सेलेनाइड ऑक्सीकरण के बाद एक उन्मूलन प्रतिक्रिया देगा, एक एल्केन और एक SeO-सेलेनोपरोक्सोल |SeO-सेलेनोपरोक्सोल को पीछे छोड़ देगा। SeO-सेलेनोपरोक्सोल अत्यधिक प्रतिक्रियाशील है और इस तरह पृथक नहीं है। उन्मूलन प्रतिक्रिया में, सभी पांच भाग लेने वाले प्रतिक्रिया केंद्र समतल हैं और इसलिए, प्रतिक्रिया त्रिविम सिंक उन्मूलन है। उपयोग किए जाने वाले ऑक्सीकरण एजेंट हाइड्रोजन पेरोक्साइड, ओजोन या MCPBA हैं। इस प्रतिक्रिया प्रकार का उपयोग अक्सर कीटोन्स के साथ किया जाता है जिससे एनोन होता है। एक उदाहरण बेंजीनसेलेनिलक्लोराइड और सोडियम हाइड्राइड के साथ एसिटाइलसाइक्लोहेक्सानोन उन्मूलन है।[26]
ग्रिको उन्मूलन O-नाइट्रोफेनिलसेलेनोसाइनेट और ट्रिब्यूटिलफॉस्फीन का उपयोग करके H2O के तत्वों के उन्मूलन का कारण बनने वाला एक समान सेलेनॉक्साइड उन्मूलन है।
संदर्भ
- ↑ A. Krief, L. Hevesi, Organoselenium Chemistry I. Functional Group Transformations., Springer, Berlin, 1988 ISBN 3-540-18629-8
- ↑ S. Patai, Z. Rappoport (Eds.), The Chemistry of Organic Selenium and Tellurium Compounds, John. Wiley and Sons, Chichester, Vol. 1, 1986 ISBN 0-471-90425-2
- ↑ Paulmier, C. Selenium Reagents and Intermediates in Organic Synthesis; Baldwin, J. E., Ed.; Pergamon Books Ltd.: New York, 1986 ISBN 0-08-032484-3
- ↑ Wallschläger, D.; Feldmann, F. (2010). पर्यावरण में Organoselenium और Organotellurium यौगिकों का निर्माण, घटना, महत्व और विश्लेषण. Metal Ions in Life Sciences. Vol. 7, Organometallics in Environment and Toxicology. RSC Publishing. pp. 319–364. ISBN 978-1-84755-177-1.
- ↑ Löwig, C. J. (1836). "हाइड्रोजन सल्फाइड और हाइड्रोजन सेलेनियम ईथर पर" [About hydrogen sulfide and selenium hydrogen ether]. Annalen der Physik. 37 (3): 550–553. Bibcode:1836AnP...113..550L. doi:10.1002/andp.18361130315.
- ↑ 6.0 6.1 Mukherjee, Anna J.; Zade, Sanjio S.; Singh, Harkesh B.; Sunoj, Raghavan B. (2010). "ऑर्गेनोसेलेनियम रसायन विज्ञान: इंट्रामोल्युलर इंटरैक्शन की भूमिका". Chemical Reviews. 110 (7): 4357–4416. doi:10.1021/cr900352j. PMID 20384363.
- ↑ Organic Syntheses, Coll. Vol. 3, p. 771 (1955); Vol. 24, p. 89 (1944) Online Article.
- ↑ Organic Syntheses, Coll. Vol. 6, p. 533 (1988); Vol. 59, p. 141 (1979) Article
- ↑ Chemistry of hypervalent compounds (1999) Kin-ya Akiba ISBN 978-0-471-24019-8
- ↑ Link Developments in the chemistry of selenaheterocyclic compounds of practical importance in synthesis and medicinal biology Arkivoc 2006 (JE-1901MR) Jacek Młochowski, Krystian Kloc, Rafał Lisiak, Piotr Potaczek, and Halina Wójtowicz
- ↑ Okazaki, R.; Tokitoh, N. (2000). "भारी कीटोन, एक कीटोन के भारी तत्व जन्मदाता". Accounts of Chemical Research. 33 (9): 625–630. doi:10.1021/ar980073b. PMID 10995200.
- ↑ Amouri, H.; Moussa, J.; Renfrew, A. K.; Dyson, P. J.; Rager, M. N.; Chamoreau, L.-M. (2010). "डिसेलेनोबेंजोक्विनोन के एक इरिडियम कॉम्प्लेक्स की खोज, संरचना और कैंसर विरोधी गतिविधि". Angewandte Chemie International Edition. 49 (41): 7530–7533. doi:10.1002/anie.201002532. PMID 20602399.
- ↑ Block, E. (2010). लहसुन और अन्य एलियम: विद्या और विज्ञान. Royal Society of Chemistry. ISBN 978-0-85404-190-9.
- ↑ Axley, M.J.; Böck, A.; Stadtman, T.C. (1991). "एस्चेरिचिया कोलाई के उत्प्रेरक गुण डिहाइड्रोजनेज उत्परिवर्ती बनाते हैं जिसमें सल्फर सेलेनियम की जगह लेता है". Proc. Natl. Acad. Sci. U.S.A. 88 (19): 8450–8454. Bibcode:1991PNAS...88.8450A. doi:10.1073/pnas.88.19.8450. PMC 52526. PMID 1924303.
- ↑ Papp, L.V.; Lu, J.; Holmgren, A.; Khanna, K.K. (2007). "सेलेनियम से सेलेनोप्रोटीन तक: संश्लेषण, पहचान, और मानव स्वास्थ्य में उनकी भूमिका". Antioxidants & Redox Signaling. 9 (7): 775–806. doi:10.1089/ars.2007.1528. PMID 17508906.
- ↑ Comasseto, João Valdir; Ling, Lo Wai; Petragnani, Nicola; Stefani, Helio Alexandre (1997). "विनाइलिक सेलेनाइड्स और टेलुराइड्स - तैयारी, प्रतिक्रियाशीलता और सिंथेटिक अनुप्रयोग". Synthesis. 1997 (4): 373. doi:10.1055/s-1997-1210.
- ↑ Comasseto, J (1983). "विनाइलिक सेलेनाइड्स". Journal of Organometallic Chemistry. 253 (2): 131–181. doi:10.1016/0022-328X(83)80118-1.
- ↑ Zeni, Gilson; Stracke, Marcelo P.; Nogueira, Cristina W.; Braga, Antonio L.; Menezes, Paulo H.; Stefani, Helio A. (2004). "लिथियम ब्यूटाइलसेलेनोलेट द्वारा एल्केनेस का हाइड्रोसेलेनेशन: विनाइलिक सेलेनाइड्स के संश्लेषण में एक दृष्टिकोण". Organic Letters. 6 (7): 1135–8. doi:10.1021/ol0498904. PMID 15040741.
- ↑ Dabdoub, M (2001). "(Z)-1-फेनिलसेलेनो-1,4-डायऑर्गेनिल-1-ब्यूटेन-3-येन्स का संश्लेषण: सममित और असममितीय 1,4-डायऑर्गेनिल-1,3-ब्यूटाडायनेस का हाइड्रोसेलेनेशन". Tetrahedron. 57 (20): 4271–4276. doi:10.1016/S0040-4020(01)00337-4.
- ↑ Doregobarros, O; Lang, E; Deoliveira, C; Peppe, C; Zeni, G (2002). "ईण्डीयुम (I) आयोडाइड-मध्यस्थता केमियो-, रेजियो-, और 2-एल्किन-1-ओएल डेरिवेटिव के स्टीरियोसेक्लेक्टिव हाइड्रोसेलेनेशन". Tetrahedron Letters. 43 (44): 7921. doi:10.1016/S0040-4039(02)01904-4.
- ↑ Comasseto, J (1981). "विनाइलिक सेलेनाइड्स का स्टीरियोसेलेक्टिव संश्लेषण". Journal of Organometallic Chemistry. 216 (3): 287–294. doi:10.1016/S0022-328X(00)85812-X.
- ↑ Organic Syntheses Coll. Vol. 9, p. 396 (1998); Vol. 71, p. 181 (1993) Online article Archived 2005-10-24 at the Wayback Machine
- ↑ Organic Syntheses Coll. Vol. 6, p. 946 (1988); Vol. 56, p. 25 (1977). Online article Archived 2005-11-01 at the Wayback Machine
- ↑ Organic Syntheses, Coll. Vol. 4, p. 229 (1963); Vol. 32, p. 35 (1952). Online article Archived 2005-11-27 at the Wayback Machine
- ↑ Riley, Harry Lister; Morley, John Frederick; Friend, Norman Alfred Child (1932). "255. सेलेनियम डाइऑक्साइड, एक नया ऑक्सीकरण एजेंट। भाग I। एल्डिहाइड और कीटोन्स के साथ इसकी प्रतिक्रिया". Journal of the Chemical Society (Resumed): 1875. doi:10.1039/JR9320001875.
- ↑ Organic Syntheses Coll. Vol. 6, p. 23 (1988); Vol. 59, p. 58 (1979) Online Article