झिल्ली विभव: Difference between revisions
No edit summary |
No edit summary |
||
| Line 2: | Line 2: | ||
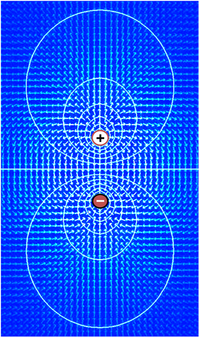
[[File:Basis of Membrane Potential2.png|thumb|right|350px|[[प्लाज्मा झिल्ली]] के विपरीत पक्षों पर [[आयन]]ों की सांद्रता में अंतर [[वोल्टेज]] की ओर ले जाता है जिसे झिल्ली क्षमता कहा जाता है। | [[File:Basis of Membrane Potential2.png|thumb|right|350px|[[प्लाज्मा झिल्ली]] के विपरीत पक्षों पर [[आयन]]ों की सांद्रता में अंतर [[वोल्टेज]] की ओर ले जाता है जिसे झिल्ली क्षमता कहा जाता है। | ||
झिल्ली क्षमता के विशिष्ट मूल्य -70 एमवी से -40 एमवी की सीमा में हैं। अनेक आयनों में झिल्ली के पार सांद्रता प्रवणता होती है, जिसमें [[पोटैशियम]] (K<sup>+</sup>), जो अंदर उच्च सांद्रता पर है और झिल्ली के बाहर | झिल्ली क्षमता के विशिष्ट मूल्य -70 एमवी से -40 एमवी की सीमा में हैं। अनेक आयनों में झिल्ली के पार सांद्रता प्रवणता होती है, जिसमें [[पोटैशियम]] (K<sup>+</sup>), जो अंदर उच्च सांद्रता पर है और झिल्ली के बाहर अल्प सांद्रता है। [[सोडियम]] (ना<sup>+</sup>) और [[क्लोराइड]] (Cl<sup>−</sup>) आयन बाह्य[[कोशिकी]]य क्षेत्र में उच्च सांद्रता में हैं, और अंतःकोशिकीय क्षेत्रों में अल्प सांद्रता में हैं। ये सघनता प्रवणता झिल्ली क्षमता के निर्माण को चलाने के लिए [[संभावित ऊर्जा]] प्रदान करते हैं। यह वोल्टेज तब स्थापित होता है जब झिल्ली में या अधिक आयनों के लिए पारगम्यता होती है। | ||
सबसे सरल स्थिति में, यहां सचित्र, यदि झिल्ली पोटेशियम के लिए चुनिंदा रूप से पारगम्य है, तो ये सकारात्मक रूप से आवेशित आयन कोशिका के बाहर की ओर सांद्रता प्रवणता को फैला सकते हैं, बिना किसी ऋणात्मक आवेश को पीछे छोड़ सकते हैं। आवेशों का यह पृथक्करण ही झिल्ली क्षमता का कारण बनता है। समग्र रूप से प्रणाली विद्युत-तटस्थ है। कोशिका के बाहर अप्रतिपूरक धनात्मक आवेश, और कोशिका के भीतर अप्रतिपूरक ऋणात्मक आवेश भौतिक रूप से झिल्ली की सतह पर पंक्तिबद्ध होते हैं और लिपिड द्विपरत में दूसरे को आकर्षित करते हैं। इस प्रकार, झिल्ली क्षमता भौतिक रूप से झिल्ली के तत्काल आसपास के क्षेत्र में ही स्थित है। यह झिल्ली भर में इन आवेशों का पृथक्करण है जो झिल्ली वोल्टेज का आधार है। | सबसे सरल स्थिति में, यहां सचित्र, यदि झिल्ली पोटेशियम के लिए चुनिंदा रूप से पारगम्य है, तो ये सकारात्मक रूप से आवेशित आयन कोशिका के बाहर की ओर सांद्रता प्रवणता को फैला सकते हैं, बिना किसी ऋणात्मक आवेश को पीछे छोड़ सकते हैं। आवेशों का यह पृथक्करण ही झिल्ली क्षमता का कारण बनता है। समग्र रूप से प्रणाली विद्युत-तटस्थ है। कोशिका के बाहर अप्रतिपूरक धनात्मक आवेश, और कोशिका के भीतर अप्रतिपूरक ऋणात्मक आवेश भौतिक रूप से झिल्ली की सतह पर पंक्तिबद्ध होते हैं और लिपिड द्विपरत में दूसरे को आकर्षित करते हैं। इस प्रकार, झिल्ली क्षमता भौतिक रूप से झिल्ली के तत्काल आसपास के क्षेत्र में ही स्थित है। यह झिल्ली भर में इन आवेशों का पृथक्करण है जो झिल्ली वोल्टेज का आधार है। | ||
| Line 14: | Line 14: | ||
लगभग सभी प्लाज्मा झिल्लियों में विद्युत क्षमता होती है, जिसके अंदर सामान्यतः बाहर के संबंध में नकारात्मक होता है।<ref>{{Cite book|title=Molecular biology of the cell|last=Bruce|first=Alberts|isbn=9780815344322|edition=Sixth|location=New York, NY|oclc=887605755|date = 2014-11-18}}</ref> झिल्ली क्षमता के दो वास्तविक कार्य हैं। सबसे पहले, यह सेल को बैटरी के रूप में कार्य करने की अनुमति देता है, झिल्ली में एम्बेडेड विभिन्न प्रकार के "आणविक उपकरणों" को संचालित करने की शक्ति प्रदान करता है।<ref>{{Cite journal|last1=Abdul Kadir|first1=Lina|last2=Stacey|first2=Michael|last3=Barrett-Jolley|first3=Richard|date=2018|title=Emerging Roles of the Membrane Potential: Action Beyond the Action Potential|journal=Frontiers in Physiology|language=English|volume=9|page=1661 |doi=10.3389/fphys.2018.01661|pmid=30519193|pmc=6258788 |issn=1664-042X|doi-access=free}}</ref> दूसरा, विद्युत रूप से उत्तेजनीय कोशिकाओं जैसे [[न्यूरॉन|न्यूरॉन्स]] और [[मायोसाइट|पेशी कोशिकाओं]] में, इसका उपयोग कोशिका के विभिन्न भागों के मध्य संकेतों को प्रसारित करने के लिए किया जाता है। झिल्ली में बिंदु पर आयन चैनलों को खोलने या बंद करने से सिग्नल उत्पन्न होते हैं, जिससे झिल्ली क्षमता में स्थानीय परिवर्तन होता है। विद्युत क्षेत्र में इस परिवर्तन को झिल्ली में आसन्न या अधिक दूर के आयन चैनलों द्वारा शीघ्रता से अनुभूत किया जा सकता है। वे आयन चैनल सिग्नल को पुन: उत्पन्न करने वाले संभावित परिवर्तन के परिणामस्वरूप खुल या बंद हो सकते हैं। | लगभग सभी प्लाज्मा झिल्लियों में विद्युत क्षमता होती है, जिसके अंदर सामान्यतः बाहर के संबंध में नकारात्मक होता है।<ref>{{Cite book|title=Molecular biology of the cell|last=Bruce|first=Alberts|isbn=9780815344322|edition=Sixth|location=New York, NY|oclc=887605755|date = 2014-11-18}}</ref> झिल्ली क्षमता के दो वास्तविक कार्य हैं। सबसे पहले, यह सेल को बैटरी के रूप में कार्य करने की अनुमति देता है, झिल्ली में एम्बेडेड विभिन्न प्रकार के "आणविक उपकरणों" को संचालित करने की शक्ति प्रदान करता है।<ref>{{Cite journal|last1=Abdul Kadir|first1=Lina|last2=Stacey|first2=Michael|last3=Barrett-Jolley|first3=Richard|date=2018|title=Emerging Roles of the Membrane Potential: Action Beyond the Action Potential|journal=Frontiers in Physiology|language=English|volume=9|page=1661 |doi=10.3389/fphys.2018.01661|pmid=30519193|pmc=6258788 |issn=1664-042X|doi-access=free}}</ref> दूसरा, विद्युत रूप से उत्तेजनीय कोशिकाओं जैसे [[न्यूरॉन|न्यूरॉन्स]] और [[मायोसाइट|पेशी कोशिकाओं]] में, इसका उपयोग कोशिका के विभिन्न भागों के मध्य संकेतों को प्रसारित करने के लिए किया जाता है। झिल्ली में बिंदु पर आयन चैनलों को खोलने या बंद करने से सिग्नल उत्पन्न होते हैं, जिससे झिल्ली क्षमता में स्थानीय परिवर्तन होता है। विद्युत क्षेत्र में इस परिवर्तन को झिल्ली में आसन्न या अधिक दूर के आयन चैनलों द्वारा शीघ्रता से अनुभूत किया जा सकता है। वे आयन चैनल सिग्नल को पुन: उत्पन्न करने वाले संभावित परिवर्तन के परिणामस्वरूप खुल या बंद हो सकते हैं। | ||
अन्य -उत्तेजक कोशिकाओं में, और उनके आधारभूत राज्यों में उत्तेजनीय कोशिकाओं में, झिल्ली क्षमता अपेक्षाकृत स्थिर मूल्य पर होती है, जिसे विश्राम क्षमता कहा जाता है। न्यूरॉन्स के लिए, विश्राम क्षमता को -80 से -70 मिलीवोल्ट तक के रूप में परिभाषित किया गया है; अर्थात्, सेल के आंतरिक भाग में वोल्ट के दसवें भाग से थोड़ा अल्प ऋणात्मक आधारभूत वोल्टेज होता है। आयन चैनलों के खुलने और बंद होने से विश्राम क्षमता से प्रस्थान हो सकता है। इसे [[विध्रुवण]] कहा जाता है यदि आंतरिक वोल्टेज अल्प ऋणात्मक हो जाता है (जैसे -70 mV से -60 mV), या [[अतिध्रुवीकरण (जीव विज्ञान)]]जीवविज्ञान) यदि आंतरिक वोल्टेज अधिक ऋणात्मक हो जाता है (-70 mV से -80 mV तक)। उत्तेजनीय कोशिकाओं में, पर्याप्त रूप से बड़ा विध्रुवण ऐक्शन पोटेंशिअल उत्पन्न कर सकता है, जिसमें झिल्ली क्षमता थोड़े समय के लिए (1 से 100 मिलीसेकंड के क्रम में) तेजी से और महत्वपूर्ण रूप से बदलती है, प्रायः इसकी ध्रुवीयता को उलट देती है। [[संभावित कार्रवाई]] कुछ [[वोल्टेज-गेटेड आयन चैनल]]ों की सक्रियता से उत्पन्न होते हैं। | |||
न्यूरॉन्स में, झिल्ली क्षमता को प्रभावित करने वाले कारक विविध होते हैं। उनमें अनेक प्रकार के आयन चैनल सम्मिलित हैं, जिनमें से कुछ रासायनिक रूप से गेटेड हैं और कुछ वोल्टेज-गेटेड हैं। क्योंकि वोल्टेज-गेटेड आयन चैनल झिल्ली क्षमता द्वारा नियंत्रित होते हैं, जबकि झिल्ली क्षमता स्वयं इन्हीं आयन चैनलों से प्रभावित होती है, फीडबैक लूप जो जटिल लौकिक गतिकी की अनुमति देते हैं, जिसमें दोलन और पुनर्योजी घटनाएं जैसे क्रिया क्षमता सम्मिलित हैं। | न्यूरॉन्स में, झिल्ली क्षमता को प्रभावित करने वाले कारक विविध होते हैं। उनमें अनेक प्रकार के आयन चैनल सम्मिलित हैं, जिनमें से कुछ रासायनिक रूप से गेटेड हैं और कुछ वोल्टेज-गेटेड हैं। क्योंकि वोल्टेज-गेटेड आयन चैनल झिल्ली क्षमता द्वारा नियंत्रित होते हैं, जबकि झिल्ली क्षमता स्वयं इन्हीं आयन चैनलों से प्रभावित होती है, फीडबैक लूप जो जटिल लौकिक गतिकी की अनुमति देते हैं, जिसमें दोलन और पुनर्योजी घटनाएं जैसे क्रिया क्षमता सम्मिलित हैं। | ||
== भौतिक आधार == | == भौतिक आधार == | ||
कोशिका में झिल्ली क्षमता अंततः दो कारकों से उत्पन्न होती है: विद्युत बल और प्रसार। विद्युत बल विपरीत विद्युत आवेशों (सकारात्मक और ऋणात्मक) वाले कणों के मध्य परस्पर आकर्षण और ही प्रकार के आवेश वाले कणों के मध्य पारस्परिक प्रतिकर्षण (धनात्मक या दोनों ऋणात्मक) से उत्पन्न होता है। कणों की सांख्यिकीय प्रवृत्ति से प्रसार उन क्षेत्रों से पुनर्वितरण के लिए उत्पन्न होता है जहां वे उन क्षेत्रों में अत्यधिक केंद्रित होते हैं जहां एकाग्रता | कोशिका में झिल्ली क्षमता अंततः दो कारकों से उत्पन्न होती है: विद्युत बल और प्रसार। विद्युत बल विपरीत विद्युत आवेशों (सकारात्मक और ऋणात्मक) वाले कणों के मध्य परस्पर आकर्षण और ही प्रकार के आवेश वाले कणों के मध्य पारस्परिक प्रतिकर्षण (धनात्मक या दोनों ऋणात्मक) से उत्पन्न होता है। कणों की सांख्यिकीय प्रवृत्ति से प्रसार उन क्षेत्रों से पुनर्वितरण के लिए उत्पन्न होता है जहां वे उन क्षेत्रों में अत्यधिक केंद्रित होते हैं जहां एकाग्रता अल्प होती है। | ||
=== वोल्टेज === | === वोल्टेज === | ||
| Line 37: | Line 37: | ||
इलेक्ट्रोफोरेटिक गतिशीलता}} | इलेक्ट्रोफोरेटिक गतिशीलता}} | ||
[[File:Diffusion.en.svg|thumb|right|250px|आयन (गुलाबी घेरे) झिल्ली में उच्च सांद्रता से | [[File:Diffusion.en.svg|thumb|right|250px|आयन (गुलाबी घेरे) झिल्ली में उच्च सांद्रता से अल्प सांद्रता (एक सांद्रता प्रवणता के नीचे) में प्रवाहित होंगे, जिससे करंट उत्पन्न होगा। चूँकि , यह झिल्ली के पार वोल्टेज बनाता है जो आयनों की गति का विरोध करता है। जब यह वोल्टेज संतुलन मूल्य तक पहुँचता है, तो दो संतुलन और आयनों का प्रवाह रुक जाता है।<ref>Campbell Biology, 6th edition</ref>|alt=दो बीकरों का योजनाबद्ध आरेख, प्रत्येक में पानी (हल्का-नीला) भरा हुआ है और एक अर्ध-पारगम्य झिल्ली है जिसे बीकर में डाली गई धराशायी ऊर्ध्वाधर रेखा द्वारा दर्शाया गया है जो बीकर की तरल सामग्री को दो समान भागों में विभाजित करती है। बाएं हाथ का बीकर समय शून्य पर एक प्रारंभिक अवस्था का प्रतिनिधित्व करता है, जहां झिल्ली के एक तरफ दूसरे की तुलना में आयनों (गुलाबी घेरे) की संख्या बहुत अधिक होती है। दाहिने हाथ का बीकर बाद के समय बिंदु पर स्थिति का प्रतिनिधित्व करता है, जिसके बाद आयन बीकर के उच्च से निम्न सांद्रता वाले कंपार्टमेंट से झिल्ली में प्रवाहित होते हैं ताकि झिल्ली के प्रत्येक तरफ आयनों की संख्या अब बराबर के करीब हो।]]जैविक जीवों के भीतर विद्युत संकेत सामान्य रूप से आयनों द्वारा संचालित होते हैं।<ref>Johnston and Wu, p. 9.</ref> ऐक्शन पोटेंशिअल के लिए सबसे महत्वपूर्ण धनायन हैं सोडियम (Na<sup>+</sup>) और पोटैशियम (K<sup>+</sup>).<ref name="bullock_140_141">[[थिओडोर होम्स बुलॉक]], ऑरकांड, और ग्रिनेल, पीपी. ऐक्शन पोटेंशिअल में [[कैल्शियम]] (Ca<sup>2+</sup>),<ref>[[Theodore Holmes Bullock|Bullock]], Orkand, and Grinnell, pp. 153–54.</ref> जो द्विसंयोजी धनायन है जो दोहरा धनावेश वहन करता है। क्लोराइड आयन (Cl<sup>−</sup>) कुछ [[शैवाल]] की क्रिया क्षमता में प्रमुख भूमिका निभाता है,<ref name="mummert_1991">{{cite journal |vauthors=Mummert H, Gradmann D | year = 1991 | title = एसिटाबुलरिया में कार्य क्षमता: वोल्टेज-गेटेड फ्लक्स का मापन और अनुकरण| journal = Journal of Membrane Biology | volume = 124 | pages = 265–73 | pmid = 1664861 | doi = 10.1007/BF01994359 | issue = 3| s2cid = 22063907 }}</ref> लेकिन अधिकांश जानवरों की कार्य क्षमता में नगण्य भूमिका निभाता है। संदर्भ>[[नट श्मिट-नीलसन]]|श्मिट-नीलसन, पृ. 483.</ref> | ||
आयन कोशिका झिल्ली को दो प्रभावों के अनुसार पार करते हैं: [[प्रसार]] और विद्युत क्षेत्र। सरल उदाहरण जिसमें दो समाधान-ए और बी-एक झरझरा अवरोध से अलग होते हैं, यह दर्शाता है कि प्रसार यह सुनिश्चित करेगा कि वे अंततः समान समाधानों में मिल जाएंगे। यह मिश्रण उनकी सांद्रता में अंतर के कारण होता है। उच्च सांद्रता वाला क्षेत्र | आयन कोशिका झिल्ली को दो प्रभावों के अनुसार पार करते हैं: [[प्रसार]] और विद्युत क्षेत्र। सरल उदाहरण जिसमें दो समाधान-ए और बी-एक झरझरा अवरोध से अलग होते हैं, यह दर्शाता है कि प्रसार यह सुनिश्चित करेगा कि वे अंततः समान समाधानों में मिल जाएंगे। यह मिश्रण उनकी सांद्रता में अंतर के कारण होता है। उच्च सांद्रता वाला क्षेत्र अल्प सांद्रता वाले क्षेत्र की ओर फैल जाएगा। उदाहरण का विस्तार करने के लिए, समाधान A में 30 सोडियम आयन और 30 क्लोराइड आयन हैं। साथ ही, मान लें कि विलयन B में केवल 20 सोडियम आयन और 20 क्लोराइड आयन हैं। यह मानते हुए कि अवरोध दोनों प्रकार के आयनों को इसके माध्यम से यात्रा करने की अनुमति देता है, तब स्थिर स्थिति प्राप्त होगी जिससे दोनों समाधानों में 25 सोडियम आयन और 25 क्लोराइड आयन होंगे। यदि, चूँकि , झरझरा बाधा चयनात्मक है जिसके माध्यम से आयनों को जाने दिया जाता है, तो केवल विसरण परिणामी समाधान का निर्धारण नहीं करेगा। पिछले उदाहरण पर लौटते हुए, आइए अब अवरोध का निर्माण करें जो केवल सोडियम आयनों के लिए पारगम्य है। अब, केवल सोडियम को समाधान ए में इसकी उच्च सांद्रता से समाधान बी में अल्प सांद्रता तक बाधा को पार करने की अनुमति है। इसके परिणामस्वरूप समाधान बी में क्लोराइड आयनों की तुलना में सोडियम आयनों का अधिक संचय होगा और सोडियम आयनों की संख्या अल्प होगी। समाधान ए में क्लोराइड आयन। | ||
इसका तात्पर्य यह है कि नकारात्मक रूप से चार्ज किए गए क्लोराइड आयनों की तुलना में सकारात्मक रूप से चार्ज किए गए सोडियम आयनों की उच्च सांद्रता से समाधान बी में शुद्ध सकारात्मक चार्ज होता है। इसी तरह, सकारात्मक सोडियम आयनों की तुलना में नकारात्मक क्लोराइड आयनों की अधिक सांद्रता से समाधान ए में शुद्ध नकारात्मक चार्ज होता है। चूँकि विपरीत आवेश आकर्षित होते हैं और समान आवेश प्रतिकर्षित होते हैं, आयन अब विद्युत क्षेत्रों के साथ-साथ विसरण की शक्तियों से भी प्रभावित होते हैं। इसलिए, सकारात्मक सोडियम आयनों की अब-अधिक-सकारात्मक बी समाधान की यात्रा करने की संभावना | इसका तात्पर्य यह है कि नकारात्मक रूप से चार्ज किए गए क्लोराइड आयनों की तुलना में सकारात्मक रूप से चार्ज किए गए सोडियम आयनों की उच्च सांद्रता से समाधान बी में शुद्ध सकारात्मक चार्ज होता है। इसी तरह, सकारात्मक सोडियम आयनों की तुलना में नकारात्मक क्लोराइड आयनों की अधिक सांद्रता से समाधान ए में शुद्ध नकारात्मक चार्ज होता है। चूँकि विपरीत आवेश आकर्षित होते हैं और समान आवेश प्रतिकर्षित होते हैं, आयन अब विद्युत क्षेत्रों के साथ-साथ विसरण की शक्तियों से भी प्रभावित होते हैं। इसलिए, सकारात्मक सोडियम आयनों की अब-अधिक-सकारात्मक बी समाधान की यात्रा करने की संभावना अल्प होगी और अब-अधिक-नकारात्मक ए समाधान में बने रहेंगे। जिस बिंदु पर विद्युत क्षेत्र के बल विसरण के कारण बल का पूरी तरह से प्रतिकार करते हैं उसे संतुलन क्षमता कहा जाता है। इस बिंदु पर, विशिष्ट आयन (इस स्थिति में सोडियम) का शुद्ध प्रवाह शून्य है। | ||
===प्लाज्मा झिल्ली === | ===प्लाज्मा झिल्ली === | ||
[[File:Cell membrane detailed diagram en.svg|thumb|right|500px|कोशिका झिल्ली, जिसे प्लाज़्मा झिल्ली या प्लाज़्मेलेम्मा भी कहा जाता है, [[अर्धपारगम्य झिल्ली]] लिपिड बाइलेयर है जो सभी जीवित कोशिकाओं के लिए आम है। इसमें विभिन्न प्रकार के जैविक अणु होते हैं, मुख्य रूप से प्रोटीन और लिपिड, जो सेलुलर प्रक्रियाओं की विस्तृत श्रृंखला में सम्मिलित होते हैं।]]प्रत्येक कोशिका प्लाज़्मा झिल्ली में घिरी होती है, जिसमें लिपिड बाईलेयर की संरचना होती है जिसमें अनेक प्रकार के बड़े अणु सन्निहित होते हैं। क्योंकि यह लिपिड अणुओं से बना है, प्लाज्मा झिल्ली में आंतरिक रूप से उच्च विद्युत प्रतिरोधकता होती है, दूसरे शब्दों में आयनों के लिए | [[File:Cell membrane detailed diagram en.svg|thumb|right|500px|कोशिका झिल्ली, जिसे प्लाज़्मा झिल्ली या प्लाज़्मेलेम्मा भी कहा जाता है, [[अर्धपारगम्य झिल्ली]] लिपिड बाइलेयर है जो सभी जीवित कोशिकाओं के लिए आम है। इसमें विभिन्न प्रकार के जैविक अणु होते हैं, मुख्य रूप से प्रोटीन और लिपिड, जो सेलुलर प्रक्रियाओं की विस्तृत श्रृंखला में सम्मिलित होते हैं।]]प्रत्येक कोशिका प्लाज़्मा झिल्ली में घिरी होती है, जिसमें लिपिड बाईलेयर की संरचना होती है जिसमें अनेक प्रकार के बड़े अणु सन्निहित होते हैं। क्योंकि यह लिपिड अणुओं से बना है, प्लाज्मा झिल्ली में आंतरिक रूप से उच्च विद्युत प्रतिरोधकता होती है, दूसरे शब्दों में आयनों के लिए अल्प आंतरिक पारगम्यता होती है। चूँकि , झिल्ली में एम्बेडेड कुछ अणु सक्रिय रूप से आयनों को झिल्ली के तरफ से दूसरी तरफ ले जाने या चैनल प्रदान करने में सक्षम होते हैं जिसके माध्यम से वे स्थानांतरित हो सकते हैं।<ref name="lieb_1986">{{cite book |vauthors=Lieb WR, Stein WD | year = 1986 | chapter = Chapter 2. Simple Diffusion across the Membrane Barrier | title = सेल मेम्ब्रेन में परिवहन और प्रसार| publisher = Academic Press | location = San Diego | isbn = 978-0-12-664661-0 | pages = 69–112}}</रेफरी> | ||
विद्युत शब्दावली में, प्लाज्मा झिल्ली एक संयुक्त प्रतिरोधक और [[संधारित्र]] के रूप में कार्य करती है। प्रतिरोध इस तथ्य से उत्पन्न होता है कि झिल्ली इसके पार आवेशों की गति को बाधित करती है। कैपेसिटेंस इस तथ्य से उत्पन्न होता है कि लिपिड बाइलेयर इतना पतला होता है कि एक तरफ आवेशित कणों का संचय एक विद्युत बल को जन्म देता है जो विपरीत आवेशित कणों को दूसरी ओर खींचता है। झिल्ली की समाई इसमें निहित अणुओं से अपेक्षाकृत अप्रभावित होती है, इसलिए इसमें 2 μF/cm पर अनुमानित मूल्य कम या ज्यादा होता है।<sup>2</sup> (झिल्ली के एक पैच की कुल धारिता उसके क्षेत्रफल के समानुपाती होती है)। दूसरी ओर, एक शुद्ध लिपिड बाईलेयर का चालन इतना कम होता है कि जैविक स्थितियों में यह हमेशा एम्बेडेड अणुओं द्वारा प्रदान किए गए वैकल्पिक मार्गों के संचालन पर हावी रहता है। इस प्रकार, झिल्ली की समाई कमोबेश स्थिर होती है, लेकिन प्रतिरोध अत्यधिक परिवर्तनशील होता है। | विद्युत शब्दावली में, प्लाज्मा झिल्ली एक संयुक्त प्रतिरोधक और [[संधारित्र]] के रूप में कार्य करती है। प्रतिरोध इस तथ्य से उत्पन्न होता है कि झिल्ली इसके पार आवेशों की गति को बाधित करती है। कैपेसिटेंस इस तथ्य से उत्पन्न होता है कि लिपिड बाइलेयर इतना पतला होता है कि एक तरफ आवेशित कणों का संचय एक विद्युत बल को जन्म देता है जो विपरीत आवेशित कणों को दूसरी ओर खींचता है। झिल्ली की समाई इसमें निहित अणुओं से अपेक्षाकृत अप्रभावित होती है, इसलिए इसमें 2 μF/cm पर अनुमानित मूल्य कम या ज्यादा होता है।<sup>2</sup> (झिल्ली के एक पैच की कुल धारिता उसके क्षेत्रफल के समानुपाती होती है)। दूसरी ओर, एक शुद्ध लिपिड बाईलेयर का चालन इतना कम होता है कि जैविक स्थितियों में यह हमेशा एम्बेडेड अणुओं द्वारा प्रदान किए गए वैकल्पिक मार्गों के संचालन पर हावी रहता है। इस प्रकार, झिल्ली की समाई कमोबेश स्थिर होती है, लेकिन प्रतिरोध अत्यधिक परिवर्तनशील होता है। | ||
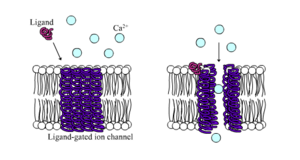
| Line 76: | Line 76: | ||
आयन चैनलों को वर्गीकृत किया जा सकता है कि वे अपने पर्यावरण पर कैसे प्रतिक्रिया करते हैं।<ref name="goldin_2007">{{cite book | author = Goldin AL | year = 2007 | chapter = Neuronal Channels and Receptors | title = आणविक न्यूरोलॉजी| editor = Waxman SG | publisher = Elsevier Academic Press | location = Burlington, MA | isbn = 978-0-12-369509-3 | pages = 43–58}}</ref> उदाहरण के लिए, ऐक्शन पोटेंशिअल में सम्मिलित आयन चैनल वोल्टेज-संवेदी चैनल हैं; वे झिल्ली के पार वोल्टेज की प्रतिक्रिया में खुलते और बंद होते हैं। लिगैंड-गेटेड चैनल और महत्वपूर्ण वर्ग बनाते हैं; ये आयन चैनल [[स्नायुसंचारी]] जैसे [[लिगैंड (जैव रसायन)]] के बंधन के जवाब में खुलते और बंद होते हैं। अन्य आयन चैनल यांत्रिक बलों के साथ खुलते और बंद होते हैं। अभी भी अन्य आयन चैनल- जैसे कि संवेदी न्यूरॉन्स- प्रकाश, तापमान या दबाव जैसे अन्य उत्तेजनाओं के जवाब में खुले और बंद होते हैं। | आयन चैनलों को वर्गीकृत किया जा सकता है कि वे अपने पर्यावरण पर कैसे प्रतिक्रिया करते हैं।<ref name="goldin_2007">{{cite book | author = Goldin AL | year = 2007 | chapter = Neuronal Channels and Receptors | title = आणविक न्यूरोलॉजी| editor = Waxman SG | publisher = Elsevier Academic Press | location = Burlington, MA | isbn = 978-0-12-369509-3 | pages = 43–58}}</ref> उदाहरण के लिए, ऐक्शन पोटेंशिअल में सम्मिलित आयन चैनल वोल्टेज-संवेदी चैनल हैं; वे झिल्ली के पार वोल्टेज की प्रतिक्रिया में खुलते और बंद होते हैं। लिगैंड-गेटेड चैनल और महत्वपूर्ण वर्ग बनाते हैं; ये आयन चैनल [[स्नायुसंचारी]] जैसे [[लिगैंड (जैव रसायन)]] के बंधन के जवाब में खुलते और बंद होते हैं। अन्य आयन चैनल यांत्रिक बलों के साथ खुलते और बंद होते हैं। अभी भी अन्य आयन चैनल- जैसे कि संवेदी न्यूरॉन्स- प्रकाश, तापमान या दबाव जैसे अन्य उत्तेजनाओं के जवाब में खुले और बंद होते हैं। | ||
==== [[रिसाव चैनल]] ==== | ==== [[रिसाव चैनल|बहिर्वाहचैनल]] ==== | ||
बहिर्वाहचैनल सबसे सरल प्रकार के आयन चैनल हैं, जिसमें उनकी पारगम्यता अल्प या ज्यादा स्थिर होती है। बहिर्वाहचैनलों के प्रकार जिनका न्यूरॉन्स में सबसे बड़ा महत्व है, पोटेशियम और क्लोराइड चैनल हैं। यहां तक कि ये अपने गुणों में पूरी तरह से स्थिर नहीं हैं: सबसे पहले, उनमें से अधिकतर वोल्टेज-निर्भर हैं इस अर्थ में कि वे दिशा में दूसरे की तुलना में बेहतर संचालन करते हैं (दूसरे शब्दों में, वे सुधारक हैं); दूसरा, उनमें से कुछ रासायनिक ligands द्वारा बंद करने में सक्षम हैं, भले ही उन्हें संचालित करने के लिए ligands की आवश्यकता न हो। | |||
==== लिगैंड-गेटेड चैनल ==== | ==== लिगैंड-गेटेड चैनल ==== | ||
| Line 113: | Line 113: | ||
सेल एक्साइटेबिलिटी का सबसे महत्वपूर्ण [[समस्थिति]] बाह्य [[इलेक्ट्रोलाइट]] सांद्रता (अर्थात Na<sup>+</sup>, के<sup>+</sup>, कैल्शियम मेटाबोलिज्म|सीए<sup>2+</sup>, सीएल<sup>−</sup>, जीव विज्ञान में मैग्नीशियम|मिलीग्राम<sup>2+</sup>) और संबंधित प्रोटीन। सेल एक्साइटेबिलिटी को नियंत्रित करने वाले महत्वपूर्ण प्रोटीन वोल्टेज-गेटेड आयन चैनल, आयन ट्रांसपोर्टर (जैसे Na + / K + -ATPase, [[मैग्नीशियम ट्रांसपोर्टर]], एसिड-बेस होमियोस्टेसिस | एसिड-बेस ट्रांसपोर्टर), [[रिसेप्टर (जैव रसायन)]] और HCN चैनल हैं। हाइपरपोलराइजेशन-एक्टिवेटेड साइक्लिक- न्यूक्लियोटाइड-गेटेड चैनल।<ref>{{Cite journal|last1=Spinelli|first1=Valentina|last2=Sartiani|first2=Laura|last3=Mugelli|first3=Alessandro|last4=Romanelli|first4=Maria Novella|last5=Cerbai|first5=Elisabetta|date=2018|title=Hyperpolarization-activated cyclic-nucleotide-gated channels: pathophysiological, developmental, and pharmacological insights into their function in cellular excitability|journal=Canadian Journal of Physiology and Pharmacology|volume=96|issue=10|pages=977–984|doi=10.1139/cjpp-2018-0115|pmid=29969572|issn=0008-4212|hdl=1807/90084|s2cid=49679747 |hdl-access=free}}</ref> उदाहरण के लिए, [[पोटेशियम चैनल]] और [[कैल्शियम-सेंसिंग रिसेप्टर]]्स [[न्यूरॉन्स]], [[कार्डियक मायोसाइट्स]] और अनेक अन्य उत्तेजक कोशिकाओं जैसे [[एस्ट्रोसाइट्स]] में उत्तेजना के महत्वपूर्ण नियामक हैं।<ref>{{Cite journal|last1=Jones|first1=Brian L.|last2=Smith|first2=Stephen M.|date=2016-03-30|title=Calcium-Sensing Receptor: A Key Target for Extracellular Calcium Signaling in Neurons|journal=Frontiers in Physiology|volume=7|page=116|doi=10.3389/fphys.2016.00116|pmid=27065884|pmc=4811949|issn=1664-042X|doi-access=free}}</ref> एक्साइटेबल [[सेल सिग्नलिंग]] में कैल्शियम आयन भी सबसे महत्वपूर्ण [[दूसरा दूत प्रणाली]] है। सिनैप्टिक रिसेप्टर्स की सक्रियता [[न्यूरोप्लास्टिकिटी]] की शुरुआत करती है। न्यूरोनल एक्साइटेबिलिटी में लंबे समय तक चलने वाले बदलाव।<ref>{{Cite journal|last1=Debanne|first1=Dominique|last2=Inglebert|first2=Yanis|last3=Russier|first3=Michaël|date=2019|title=Plasticity of intrinsic neuronal excitability|journal=Current Opinion in Neurobiology|language=en|volume=54|pages=73–82|doi=10.1016/j.conb.2018.09.001|pmid=30243042|s2cid=52812190|url=https://hal-amu.archives-ouvertes.fr/hal-01963474/file/Debannne-Russier-2019.pdf}}</ref> [[थायराइड हार्मोन]], अधिवृक्क ग्रंथि और अन्य हार्मोन भी कोशिका उत्तेजना को नियंत्रित करते हैं, उदाहरण के लिए, [[प्रोजेस्टेरोन]] और [[एस्ट्रोजन]] मायोमेट्रियल [[चिकनी पेशी]] कोशिका उत्तेजना को नियंत्रित करते हैं। | सेल एक्साइटेबिलिटी का सबसे महत्वपूर्ण [[समस्थिति]] बाह्य [[इलेक्ट्रोलाइट]] सांद्रता (अर्थात Na<sup>+</sup>, के<sup>+</sup>, कैल्शियम मेटाबोलिज्म|सीए<sup>2+</sup>, सीएल<sup>−</sup>, जीव विज्ञान में मैग्नीशियम|मिलीग्राम<sup>2+</sup>) और संबंधित प्रोटीन। सेल एक्साइटेबिलिटी को नियंत्रित करने वाले महत्वपूर्ण प्रोटीन वोल्टेज-गेटेड आयन चैनल, आयन ट्रांसपोर्टर (जैसे Na + / K + -ATPase, [[मैग्नीशियम ट्रांसपोर्टर]], एसिड-बेस होमियोस्टेसिस | एसिड-बेस ट्रांसपोर्टर), [[रिसेप्टर (जैव रसायन)]] और HCN चैनल हैं। हाइपरपोलराइजेशन-एक्टिवेटेड साइक्लिक- न्यूक्लियोटाइड-गेटेड चैनल।<ref>{{Cite journal|last1=Spinelli|first1=Valentina|last2=Sartiani|first2=Laura|last3=Mugelli|first3=Alessandro|last4=Romanelli|first4=Maria Novella|last5=Cerbai|first5=Elisabetta|date=2018|title=Hyperpolarization-activated cyclic-nucleotide-gated channels: pathophysiological, developmental, and pharmacological insights into their function in cellular excitability|journal=Canadian Journal of Physiology and Pharmacology|volume=96|issue=10|pages=977–984|doi=10.1139/cjpp-2018-0115|pmid=29969572|issn=0008-4212|hdl=1807/90084|s2cid=49679747 |hdl-access=free}}</ref> उदाहरण के लिए, [[पोटेशियम चैनल]] और [[कैल्शियम-सेंसिंग रिसेप्टर]]्स [[न्यूरॉन्स]], [[कार्डियक मायोसाइट्स]] और अनेक अन्य उत्तेजक कोशिकाओं जैसे [[एस्ट्रोसाइट्स]] में उत्तेजना के महत्वपूर्ण नियामक हैं।<ref>{{Cite journal|last1=Jones|first1=Brian L.|last2=Smith|first2=Stephen M.|date=2016-03-30|title=Calcium-Sensing Receptor: A Key Target for Extracellular Calcium Signaling in Neurons|journal=Frontiers in Physiology|volume=7|page=116|doi=10.3389/fphys.2016.00116|pmid=27065884|pmc=4811949|issn=1664-042X|doi-access=free}}</ref> एक्साइटेबल [[सेल सिग्नलिंग]] में कैल्शियम आयन भी सबसे महत्वपूर्ण [[दूसरा दूत प्रणाली]] है। सिनैप्टिक रिसेप्टर्स की सक्रियता [[न्यूरोप्लास्टिकिटी]] की शुरुआत करती है। न्यूरोनल एक्साइटेबिलिटी में लंबे समय तक चलने वाले बदलाव।<ref>{{Cite journal|last1=Debanne|first1=Dominique|last2=Inglebert|first2=Yanis|last3=Russier|first3=Michaël|date=2019|title=Plasticity of intrinsic neuronal excitability|journal=Current Opinion in Neurobiology|language=en|volume=54|pages=73–82|doi=10.1016/j.conb.2018.09.001|pmid=30243042|s2cid=52812190|url=https://hal-amu.archives-ouvertes.fr/hal-01963474/file/Debannne-Russier-2019.pdf}}</ref> [[थायराइड हार्मोन]], अधिवृक्क ग्रंथि और अन्य हार्मोन भी कोशिका उत्तेजना को नियंत्रित करते हैं, उदाहरण के लिए, [[प्रोजेस्टेरोन]] और [[एस्ट्रोजन]] मायोमेट्रियल [[चिकनी पेशी]] कोशिका उत्तेजना को नियंत्रित करते हैं। | ||
अनेक प्रकार की कोशिकाओं को उत्तेजनीय झिल्ली वाला माना जाता है। उत्तेजक कोशिकाएं न्यूरॉन्स, मायोसाइट्स (हृदय, कंकाल, चिकनी पेशी), संवहनी [[अन्तःचूचुक]], [[पेरिसाईट]], जूसटैग्लोमेरुलर कोशिकाएं[[काजल की अंतरालीय कोशिका]] सेल, अनेक प्रकार के [[उपकला]] (जैसे [[बीटा सेल]], [[अल्फा सेल]], [[डेल्टा सेल]], [[एंटरोएंडोक्राइन सेल]], न्यूरोएंडोक्राइन सेल # पल्मोनरी हैं) न्यूरोएंडोक्राइन कोशिकाएं, [[पीनियलोसाइट]]्स), ग्लियाल कोशिकाएं (जैसे एस्ट्रोसाइट्स), [[mechanoreceptor]] कोशिकाएं (जैसे [[बालों की कोशिका]]एं और मर्केल कोशिकाएं), [[chemoreceptor]] कोशिकाएं (जैसे ग्लोमस कोशिकाएं, [[स्वाद रिसेप्टर]]्स), कुछ पादप कोशिकाएं और संभवतः श्वेत रक्त कोशिका।<ref>{{Cite journal|last1=Davenport|first1=Bennett|last2=Li|first2=Yuan|last3=Heizer|first3=Justin W.|last4=Schmitz|first4=Carsten|last5=Perraud|first5=Anne-Laure|date=2015-07-23|title=Signature Channels of Excitability no More: L-Type Channels in Immune Cells|journal=Frontiers in Immunology|volume=6|page=375|doi=10.3389/fimmu.2015.00375|pmid=26257741|pmc=4512153|issn=1664-3224|doi-access=free}}</ref> एस्ट्रोसाइट्स अनेक रिसेप्टर्स की अभिव्यक्ति से संबंधित इंट्रासेल्युलर कैल्शियम विविधताओं के आधार पर | अनेक प्रकार की कोशिकाओं को उत्तेजनीय झिल्ली वाला माना जाता है। उत्तेजक कोशिकाएं न्यूरॉन्स, मायोसाइट्स (हृदय, कंकाल, चिकनी पेशी), संवहनी [[अन्तःचूचुक]], [[पेरिसाईट]], जूसटैग्लोमेरुलर कोशिकाएं[[काजल की अंतरालीय कोशिका]] सेल, अनेक प्रकार के [[उपकला]] (जैसे [[बीटा सेल]], [[अल्फा सेल]], [[डेल्टा सेल]], [[एंटरोएंडोक्राइन सेल]], न्यूरोएंडोक्राइन सेल # पल्मोनरी हैं) न्यूरोएंडोक्राइन कोशिकाएं, [[पीनियलोसाइट]]्स), ग्लियाल कोशिकाएं (जैसे एस्ट्रोसाइट्स), [[mechanoreceptor]] कोशिकाएं (जैसे [[बालों की कोशिका]]एं और मर्केल कोशिकाएं), [[chemoreceptor]] कोशिकाएं (जैसे ग्लोमस कोशिकाएं, [[स्वाद रिसेप्टर]]्स), कुछ पादप कोशिकाएं और संभवतः श्वेत रक्त कोशिका।<ref>{{Cite journal|last1=Davenport|first1=Bennett|last2=Li|first2=Yuan|last3=Heizer|first3=Justin W.|last4=Schmitz|first4=Carsten|last5=Perraud|first5=Anne-Laure|date=2015-07-23|title=Signature Channels of Excitability no More: L-Type Channels in Immune Cells|journal=Frontiers in Immunology|volume=6|page=375|doi=10.3389/fimmu.2015.00375|pmid=26257741|pmc=4512153|issn=1664-3224|doi-access=free}}</ref> एस्ट्रोसाइट्स अनेक रिसेप्टर्स की अभिव्यक्ति से संबंधित इंट्रासेल्युलर कैल्शियम विविधताओं के आधार पर अन्य -विद्युत उत्तेजना का रूप प्रदर्शित करते हैं जिसके माध्यम से वे सिनैप्टिक सिग्नल का पता लगा सकते हैं। न्यूरॉन्स में, सेल के कुछ हिस्सों में अलग-अलग झिल्ली गुण होते हैं, उदाहरण के लिए, डेंड्राइटिक एक्साइटेबिलिटी न्यूरॉन्स को स्थानिक रूप से अलग किए गए इनपुट के संयोग का पता लगाने की क्षमता प्रदान करती है।<ref>{{Cite journal|last=Sakmann|first=Bert|date=2017-04-21|title=From single cells and single columns to cortical networks: dendritic excitability, coincidence detection and synaptic transmission in brain slices and brains|journal=Experimental Physiology|volume=102|issue=5|pages=489–521|doi=10.1113/ep085776|pmid=28139019|pmc=5435930|issn=0958-0670|doi-access=free}}</ref> | ||
=== समतुल्य सर्किट === | === समतुल्य सर्किट === | ||
[[File:Cell membrane equivalent circuit.svg|thumb|right|350px|झिल्ली के पैच के लिए समतुल्य सर्किट, जिसमें चर चालन के साथ श्रृंखला में बैटरी वाले चार मार्गों के साथ समानांतर में निश्चित समाई होती है]]इलेक्ट्रोफिजियोलॉजिस्ट समतुल्य सर्किट के संदर्भ में आयनिक सांद्रता अंतर, आयन चैनल और झिल्ली समाई के प्रभाव को मॉडल करते हैं, जिसका उद्देश्य झिल्ली के छोटे पैच के विद्युत गुणों का प्रतिनिधित्व करना है। समतुल्य सर्किट में चार पाथवे के साथ समानांतर में संधारित्र होता है, जिसमें प्रत्येक में चर चालन के साथ श्रृंखला में बैटरी होती है। समाई लिपिड बाईलेयर के गुणों द्वारा निर्धारित की जाती है, और इसे तय करने के लिए लिया जाता है। चार समानांतर मार्गों में से प्रत्येक प्रमुख आयनों, सोडियम, पोटेशियम, क्लोराइड और कैल्शियम में से से आता है। प्रत्येक आयनिक मार्ग का वोल्टेज झिल्ली के प्रत्येक तरफ आयन की सांद्रता द्वारा निर्धारित किया जाता है; ऊपर मेम्ब्रेन पोटेंशिअल#रिवर्सल पोटेंशिअल सेक्शन देखें। किसी भी समय प्रत्येक आयनिक मार्ग का संचालन उन सभी आयन चैनलों की अवस्थाओं द्वारा निर्धारित किया जाता है जो उस आयन के लिए संभावित रूप से पारगम्य हैं, जिसमें | [[File:Cell membrane equivalent circuit.svg|thumb|right|350px|झिल्ली के पैच के लिए समतुल्य सर्किट, जिसमें चर चालन के साथ श्रृंखला में बैटरी वाले चार मार्गों के साथ समानांतर में निश्चित समाई होती है]]इलेक्ट्रोफिजियोलॉजिस्ट समतुल्य सर्किट के संदर्भ में आयनिक सांद्रता अंतर, आयन चैनल और झिल्ली समाई के प्रभाव को मॉडल करते हैं, जिसका उद्देश्य झिल्ली के छोटे पैच के विद्युत गुणों का प्रतिनिधित्व करना है। समतुल्य सर्किट में चार पाथवे के साथ समानांतर में संधारित्र होता है, जिसमें प्रत्येक में चर चालन के साथ श्रृंखला में बैटरी होती है। समाई लिपिड बाईलेयर के गुणों द्वारा निर्धारित की जाती है, और इसे तय करने के लिए लिया जाता है। चार समानांतर मार्गों में से प्रत्येक प्रमुख आयनों, सोडियम, पोटेशियम, क्लोराइड और कैल्शियम में से से आता है। प्रत्येक आयनिक मार्ग का वोल्टेज झिल्ली के प्रत्येक तरफ आयन की सांद्रता द्वारा निर्धारित किया जाता है; ऊपर मेम्ब्रेन पोटेंशिअल#रिवर्सल पोटेंशिअल सेक्शन देखें। किसी भी समय प्रत्येक आयनिक मार्ग का संचालन उन सभी आयन चैनलों की अवस्थाओं द्वारा निर्धारित किया जाता है जो उस आयन के लिए संभावित रूप से पारगम्य हैं, जिसमें बहिर्वाह चैनल, लिगैंड-गेटेड चैनल और वोल्टेज-गेटेड आयन चैनल सम्मिलित हैं। | ||
[[File:Cell membrane reduced circuit.svg|thumb|left|[[गोल्डमैन समीकरण]] का उपयोग करके आयन-विशिष्ट मार्गों के संयोजन से प्राप्त | [[File:Cell membrane reduced circuit.svg|thumb|left|[[गोल्डमैन समीकरण]] का उपयोग करके आयन-विशिष्ट मार्गों के संयोजन से प्राप्त अल्प सर्किट]]निश्चित आयन सांद्रता और आयन चैनल चालन के निश्चित मूल्यों के लिए, समतुल्य सर्किट को और अल्प किया जा सकता है, जैसा कि नीचे वर्णित गोल्डमैन समीकरण का उपयोग करके, बैटरी और चालन के समानांतर समाई वाले सर्किट में किया जा सकता है। विद्युत शब्दों में, यह प्रकार का [[आरसी सर्किट]] (प्रतिरोध-समाई सर्किट) है, और इसके विद्युत गुण बहुत सरल हैं। किसी भी प्रारंभिक अवस्था से प्रारंभ होकर, प्रवाहकत्त्व या समाई में बहने वाली धारा घातीय समय पाठ्यक्रम के साथ घटती है, समय स्थिर के साथ {{math|τ {{=}} RC}}, कहाँ {{math|C}} झिल्ली पैच की समाई है, और {{math|R {{=}} 1/g<sub>net</sub>}} शुद्ध प्रतिरोध है। यथार्थवादी स्थितियों के लिए, समय स्थिरांक सामान्यतः 1—100 मिलीसेकंड की सीमा में होता है। अधिकांशतः स्तिथियों में, आयन चैनलों के चालन में परिवर्तन तेजी से समय के पैमाने पर होता है, इसलिए आरसी सर्किट अच्छा सन्निकटन नहीं है; चूँकि , झिल्ली पैच को मॉडल करने के लिए उपयोग किया जाने वाला अंतर समीकरण सामान्यतः RC सर्किट समीकरण का संशोधित संस्करण है। | ||
== आराम करने की क्षमता == | == आराम करने की क्षमता == | ||
जब किसी कोशिका की झिल्ली क्षमता बिना महत्वपूर्ण बदलाव के लंबे समय तक चलती है, तो इसे आराम करने की क्षमता या आराम करने वाली वोल्टेज के रूप में संदर्भित किया जाता है। यह शब्द | जब किसी कोशिका की झिल्ली क्षमता बिना महत्वपूर्ण बदलाव के लंबे समय तक चलती है, तो इसे आराम करने की क्षमता या आराम करने वाली वोल्टेज के रूप में संदर्भित किया जाता है। यह शब्द अन्य -उत्तेजक कोशिकाओं की झिल्ली क्षमता के लिए प्रयोग किया जाता है, लेकिन उत्तेजना के अभाव में उत्तेजनीय कोशिकाओं की झिल्ली क्षमता के लिए भी। उत्तेजनीय कोशिकाओं में, अन्य संभावित अवस्थाएँ वर्गीकृत झिल्ली क्षमताएँ (चर आयाम वाली) हैं, और क्रिया क्षमताएँ, जो बड़ी हैं, झिल्ली क्षमता में सभी या कुछ भी नहीं उगती हैं जो सामान्यतः निश्चित समय पाठ्यक्रम का पालन करती हैं। उत्तेजक कोशिकाओं में न्यूरॉन्स, मांसपेशियों की कोशिकाएं और [[ग्रंथि]]यों में कुछ स्रावी कोशिकाएं सम्मिलित हैं। चूँकि , अन्य प्रकार की कोशिकाओं में भी, झिल्ली वोल्टेज पर्यावरण या इंट्रासेल्युलर उत्तेजनाओं के जवाब में परिवर्तन से गुजर सकता है। उदाहरण के लिए, प्लाज्मा झिल्ली का विध्रुवण [[apoptosis]] में महत्वपूर्ण कदम प्रतीत होता है।<ref>{{cite journal |vauthors=Franco R, Bortner CD, Cidlowski JA |title=Potential roles of electrogenic ion transport and plasma membrane depolarization in apoptosis |journal=J. Membr. Biol. |volume=209 |issue=1 |pages=43–58 |date=January 2006 |pmid=16685600 |doi=10.1007/s00232-005-0837-5|s2cid=849895 |url=https://zenodo.org/record/1232645 }}</ref> | ||
आराम करने की क्षमता उत्पन्न करने वाली बातचीत को गोल्डमैन समीकरण द्वारा प्रतिरूपित किया जाता है।<ref name="Goldman">Purves ''et al.'', pp. 32–33; [[Theodore Holmes Bullock|Bullock]], Orkand, and Grinnell, pp. 138–140; Schmidt-Nielsen, pp. 480; Junge, pp. 35–37</ref> यह ऊपर दिखाए गए नर्नस्ट समीकरण के रूप में समान है, जिसमें यह प्रश्न में आयनों के आरोपों के साथ-साथ उनके अंदर और बाहर की सांद्रता के मध्य के अंतर पर आधारित है। चूँकि , यह प्रश्न में प्रत्येक आयन के लिए प्लाज्मा झिल्ली की सापेक्ष पारगम्यता को भी ध्यान में रखता है। | आराम करने की क्षमता उत्पन्न करने वाली बातचीत को गोल्डमैन समीकरण द्वारा प्रतिरूपित किया जाता है।<ref name="Goldman">Purves ''et al.'', pp. 32–33; [[Theodore Holmes Bullock|Bullock]], Orkand, and Grinnell, pp. 138–140; Schmidt-Nielsen, pp. 480; Junge, pp. 35–37</ref> यह ऊपर दिखाए गए नर्नस्ट समीकरण के रूप में समान है, जिसमें यह प्रश्न में आयनों के आरोपों के साथ-साथ उनके अंदर और बाहर की सांद्रता के मध्य के अंतर पर आधारित है। चूँकि , यह प्रश्न में प्रत्येक आयन के लिए प्लाज्मा झिल्ली की सापेक्ष पारगम्यता को भी ध्यान में रखता है। | ||
| Line 132: | Line 132: | ||
अधिकांश पशु कोशिकाओं में आराम करने वाली झिल्ली क्षमता के मान सामान्यतः पोटेशियम उत्क्रमण क्षमता (सामान्यतः लगभग -80 mV) और लगभग -40 mV के मध्य भिन्न होते हैं। उत्तेजनीय कोशिकाओं (ऐक्शन पोटेंशिअल उत्पन्न करने में सक्षम) में विश्राम क्षमता सामान्यतः -60 mV के करीब होती है—अधिक विध्रुवित वोल्टेज से ऐक्शन पोटेंशिअल का सहज उत्पादन होता है। अपरिपक्व या अविभाजित कोशिकाएं आराम करने वाले वोल्टेज के अत्यधिक चर मान दिखाती हैं, सामान्यतः विभेदित कोशिकाओं की तुलना में काफी अधिक सकारात्मक होती हैं।<ref name = "Magnuson DS et al., 1995">{{cite journal | doi = 10.1016/0165-3806(94)00166-W |vauthors=Magnuson DS, Morassutti DJ, Staines WA, McBurney MW, Marshall KC | date = Jan 14, 1995| title = In vivo electrophysiological maturation of neurons derived from a multipotent precursor (embryonal carcinoma) cell line | journal = Developmental Brain Research| volume = 84|issue = 1| pages = 130–41 | pmid = 7720212}}</ref> ऐसी कोशिकाओं में, विश्राम संभावित मूल्य विभेदन की डिग्री के साथ सहसंबंधित होता है: कुछ स्तिथियों में अविभाजित कोशिकाएं किसी भी ट्रांसमेम्ब्रेन वोल्टेज अंतर को बिल्कुल नहीं दिखा सकती हैं। | अधिकांश पशु कोशिकाओं में आराम करने वाली झिल्ली क्षमता के मान सामान्यतः पोटेशियम उत्क्रमण क्षमता (सामान्यतः लगभग -80 mV) और लगभग -40 mV के मध्य भिन्न होते हैं। उत्तेजनीय कोशिकाओं (ऐक्शन पोटेंशिअल उत्पन्न करने में सक्षम) में विश्राम क्षमता सामान्यतः -60 mV के करीब होती है—अधिक विध्रुवित वोल्टेज से ऐक्शन पोटेंशिअल का सहज उत्पादन होता है। अपरिपक्व या अविभाजित कोशिकाएं आराम करने वाले वोल्टेज के अत्यधिक चर मान दिखाती हैं, सामान्यतः विभेदित कोशिकाओं की तुलना में काफी अधिक सकारात्मक होती हैं।<ref name = "Magnuson DS et al., 1995">{{cite journal | doi = 10.1016/0165-3806(94)00166-W |vauthors=Magnuson DS, Morassutti DJ, Staines WA, McBurney MW, Marshall KC | date = Jan 14, 1995| title = In vivo electrophysiological maturation of neurons derived from a multipotent precursor (embryonal carcinoma) cell line | journal = Developmental Brain Research| volume = 84|issue = 1| pages = 130–41 | pmid = 7720212}}</ref> ऐसी कोशिकाओं में, विश्राम संभावित मूल्य विभेदन की डिग्री के साथ सहसंबंधित होता है: कुछ स्तिथियों में अविभाजित कोशिकाएं किसी भी ट्रांसमेम्ब्रेन वोल्टेज अंतर को बिल्कुल नहीं दिखा सकती हैं। | ||
बहिर्वाहचैनलों के कारण नुकसान का मुकाबला करने के लिए आयनों के सक्रिय पंपिंग की आवश्यकता के कारण विश्राम क्षमता का रखरखाव सेल के लिए चयापचय रूप से महंगा हो सकता है। लागत सबसे अधिक होती है जब सेल फ़ंक्शन को झिल्ली वोल्टेज के विशेष रूप से विध्रुवित मूल्य की आवश्यकता होती है। उदाहरण के लिए, दिन के उजाले-अनुकूलित [[कैलीफोरिडे]] (कैलीफोरा विसिना) में आराम करने की क्षमता अकशेरूकीय में साधारण आँखें -30 mV जितनी अधिक हो सकती हैं।<ref name = "Juusola M et al., 1994">{{cite journal | doi = 10.1085/jgp.104.3.593 |vauthors=Juusola M, Kouvalainen E, Järvilehto M, Weckström M | date = Sep 1994| title = Contrast gain, signal-to-noise ratio, and linearity in light-adapted blowfly photoreceptors| journal = J Gen Physiol| volume = 104| issue = 3| pages = 593–621|pmid = 7807062 | pmc = 2229225}}</ref> यह उन्नत झिल्ली क्षमता कोशिकाओं को दृश्य आदानों के लिए बहुत तेजी से प्रतिक्रिया करने की अनुमति देती है; लागत यह है कि आराम करने की क्षमता का रखरखाव समग्र सेलुलर [[एडेनोसाइन ट्रायफ़ोस्फेट]] के 20% से अधिक का उपभोग कर सकता है।<ref name = "Laughlin SB et al., 2008">{{cite journal |vauthors=Laughlin SB, de Ruyter van Steveninck RR, Anderson JC | date = May 1998| title = The metabolic cost of neural information| journal = Nat. Neurosci.| volume = 1| issue = 1| pages = 36–41|pmid = 10195106 | doi = 10.1038/236| s2cid = 204995437}}</ref> | |||
दूसरी ओर, अविभेदित कोशिकाओं में उच्च विश्राम क्षमता के लिए आवश्यक रूप से उच्च चयापचय लागत नहीं होती है। यह स्पष्ट विरोधाभास उस विश्राम क्षमता की उत्पत्ति की जांच से हल हो गया है। छोटे-विभेदित कोशिकाओं को अत्यधिक उच्च इनपुट प्रतिरोध की विशेषता होती है,<ref name="Magnuson DS et al., 1995"/>जिसका तात्पर्य है कि कोशिका जीवन के इस चरण में कुछ | दूसरी ओर, अविभेदित कोशिकाओं में उच्च विश्राम क्षमता के लिए आवश्यक रूप से उच्च चयापचय लागत नहीं होती है। यह स्पष्ट विरोधाभास उस विश्राम क्षमता की उत्पत्ति की जांच से हल हो गया है। छोटे-विभेदित कोशिकाओं को अत्यधिक उच्च इनपुट प्रतिरोध की विशेषता होती है,<ref name="Magnuson DS et al., 1995"/>जिसका तात्पर्य है कि कोशिका जीवन के इस चरण में कुछ बहिर्वाहचैनल उपस्थित हैं। स्पष्ट परिणाम के रूप में, पोटेशियम पारगम्यता सोडियम आयनों के समान हो जाती है, जो ऊपर चर्चा के अनुसार सोडियम और पोटेशियम के उलटने की क्षमता के मध्य आराम करने की क्षमता रखती है। अल्प बहिर्वाहधाराओं का तात्पर्य यह भी है कि क्षतिपूर्ति के लिए सक्रिय पम्पिंग की बहुत अल्प आवश्यकता है, इसलिए अल्प चयापचय लागत। | ||
== वर्गीकृत क्षमता == | == वर्गीकृत क्षमता == | ||
जैसा कि ऊपर बताया गया है, कोशिका की झिल्ली में किसी भी बिंदु पर क्षमता इंट्रासेल्युलर और बाह्य क्षेत्रों के मध्य आयन एकाग्रता के अंतर और प्रत्येक प्रकार के आयन के लिए झिल्ली की पारगम्यता द्वारा निर्धारित की जाती है। आयन सांद्रता सामान्य रूप से बहुत तेज़ी से नहीं बदलती (सीए के अपवाद के साथ<sup>2+</sup>, जहां बेसलाइन इंट्रासेल्युलर सांद्रता इतनी | जैसा कि ऊपर बताया गया है, कोशिका की झिल्ली में किसी भी बिंदु पर क्षमता इंट्रासेल्युलर और बाह्य क्षेत्रों के मध्य आयन एकाग्रता के अंतर और प्रत्येक प्रकार के आयन के लिए झिल्ली की पारगम्यता द्वारा निर्धारित की जाती है। आयन सांद्रता सामान्य रूप से बहुत तेज़ी से नहीं बदलती (सीए के अपवाद के साथ<sup>2+</sup>, जहां बेसलाइन इंट्रासेल्युलर सांद्रता इतनी अल्प है कि परिमाण के क्रम में छोटा सा प्रवाह भी इसे बढ़ा सकता है), लेकिन आयनों की पारगम्यता मिलीसेकंड के अंश में बदल सकती है, सक्रियण के परिणामस्वरूप लिगैंड-गेटेड आयन चैनल। झिल्ली क्षमता में परिवर्तन या तो बड़ा या छोटा हो सकता है, यह इस बात पर निर्भर करता है कि कितने आयन चैनल सक्रिय हैं और वे किस प्रकार के हैं, और या तो लंबा या छोटा हो सकता है, जो चैनल के खुले रहने की अवधि पर निर्भर करता है। एक्शन पोटेंशिअल के विपरीत, इस प्रकार के परिवर्तनों को ग्रेडेड पोटेंशिअल कहा जाता है, जिनका निश्चित आयाम और समय पाठ्यक्रम होता है। | ||
जैसा कि ऊपर दिखाए गए गोल्डमैन समीकरण से प्राप्त किया जा सकता है, झिल्ली की पारगम्यता को विशेष प्रकार के आयन में बढ़ाने का प्रभाव झिल्ली क्षमता को उस आयन के उत्क्रमण क्षमता की ओर ले जाता है। इस प्रकार, ना खोलना<sup>+</sup> चैनल मेम्ब्रेन पोटेंशिअल को Na की ओर शिफ्ट करते हैं<sup>+</sup> उत्क्रमण क्षमता, जो सामान्यतः +100 mV के आसपास होती है। इसी तरह, K खोलना<sup>+</sup> चैनल झिल्ली क्षमता को लगभग -90 mV और ओपनिंग Cl की ओर स्थानांतरित करते हैं<sup>−</sup> चैनल इसे लगभग -70 mV (अधिकांश झिल्लियों की विश्राम क्षमता) की ओर स्थानांतरित करते हैं। इस प्रकार, ना<sup>+</sup> चैनल झिल्ली क्षमता को सकारात्मक दिशा में स्थानांतरित करते हैं, K<sup>+</sup> चैनल इसे नकारात्मक दिशा में शिफ्ट करते हैं (सिवाय तब जब झिल्ली हाइपरपोलराइज़्ड मान K से अधिक नकारात्मक हो<sup>+</sup> उत्क्रमण क्षमता), और Cl<sup>−</sup> चैनल इसे स्थिर क्षमता की ओर ले जाते हैं। | जैसा कि ऊपर दिखाए गए गोल्डमैन समीकरण से प्राप्त किया जा सकता है, झिल्ली की पारगम्यता को विशेष प्रकार के आयन में बढ़ाने का प्रभाव झिल्ली क्षमता को उस आयन के उत्क्रमण क्षमता की ओर ले जाता है। इस प्रकार, ना खोलना<sup>+</sup> चैनल मेम्ब्रेन पोटेंशिअल को Na की ओर शिफ्ट करते हैं<sup>+</sup> उत्क्रमण क्षमता, जो सामान्यतः +100 mV के आसपास होती है। इसी तरह, K खोलना<sup>+</sup> चैनल झिल्ली क्षमता को लगभग -90 mV और ओपनिंग Cl की ओर स्थानांतरित करते हैं<sup>−</sup> चैनल इसे लगभग -70 mV (अधिकांश झिल्लियों की विश्राम क्षमता) की ओर स्थानांतरित करते हैं। इस प्रकार, ना<sup>+</sup> चैनल झिल्ली क्षमता को सकारात्मक दिशा में स्थानांतरित करते हैं, K<sup>+</sup> चैनल इसे नकारात्मक दिशा में शिफ्ट करते हैं (सिवाय तब जब झिल्ली हाइपरपोलराइज़्ड मान K से अधिक नकारात्मक हो<sup>+</sup> उत्क्रमण क्षमता), और Cl<sup>−</sup> चैनल इसे स्थिर क्षमता की ओर ले जाते हैं। | ||
| Line 155: | Line 155: | ||
* पारगम्यता इस बात का माप है कि आयन कितनी आसानी से झिल्ली को पार कर सकता है। इसे सामान्यतः (विद्युत) चालन के रूप में मापा जाता है और इकाई, सीमेंस (इकाई), 1 C·s से मेल खाती है<sup>−1</sup>·वी<sup>-1</sup>, अर्थात कूलॉम प्रति सेकंड प्रति वोल्ट विभव। | * पारगम्यता इस बात का माप है कि आयन कितनी आसानी से झिल्ली को पार कर सकता है। इसे सामान्यतः (विद्युत) चालन के रूप में मापा जाता है और इकाई, सीमेंस (इकाई), 1 C·s से मेल खाती है<sup>−1</sup>·वी<sup>-1</sup>, अर्थात कूलॉम प्रति सेकंड प्रति वोल्ट विभव। | ||
तो, आराम करने वाली झिल्ली में, जबकि पोटेशियम के लिए प्रेरक बल | तो, आराम करने वाली झिल्ली में, जबकि पोटेशियम के लिए प्रेरक बल अल्प होता है, इसकी पारगम्यता बहुत अधिक होती है। सोडियम के पास विशाल प्रेरणा शक्ति है लेकिन लगभग कोई विश्राम पारगम्यता नहीं है। इस स्थिति में, पोटेशियम सोडियम की तुलना में लगभग 20 गुना अधिक धारा वहन करता है, और इस प्रकार ई पर 20 गुना अधिक प्रभाव पड़ता है<sub>m</sub> सोडियम की तुलना में। | ||
चूँकि , और स्थिति पर विचार करें- एक्शन पोटेंशिअल का चरम। यहाँ, Na की पारगम्यता अधिक है और K की पारगम्यता अपेक्षाकृत | चूँकि , और स्थिति पर विचार करें- एक्शन पोटेंशिअल का चरम। यहाँ, Na की पारगम्यता अधिक है और K की पारगम्यता अपेक्षाकृत अल्प है। इस प्रकार, झिल्ली E के पास चली जाती है<sub>Na</sub> और ई से दूर<sub>K</sub>. | ||
जितने अधिक आयन पारगम्य होते हैं, झिल्ली क्षमता का अनुमान लगाना उतना ही जटिल हो जाता है। चूँकि , यह गोल्डमैन समीकरण | गोल्डमैन-हॉजकिन-काट्ज़ समीकरण या भारित साधन समीकरण का उपयोग करके किया जा सकता है। समय पर किसी भी समय सांद्रता प्रवणताओं और आयनों की पारगम्यता में प्लगिंग करके, उस समय झिल्ली क्षमता का निर्धारण किया जा सकता है। GHK समीकरणों का अर्थ यह है कि किसी भी समय झिल्ली क्षमता का मान सभी पारगम्य आयनों की संतुलन क्षमता का भारित औसत होगा। भार झिल्ली के पार आयनों की सापेक्ष पारगम्यता है। | जितने अधिक आयन पारगम्य होते हैं, झिल्ली क्षमता का अनुमान लगाना उतना ही जटिल हो जाता है। चूँकि , यह गोल्डमैन समीकरण | गोल्डमैन-हॉजकिन-काट्ज़ समीकरण या भारित साधन समीकरण का उपयोग करके किया जा सकता है। समय पर किसी भी समय सांद्रता प्रवणताओं और आयनों की पारगम्यता में प्लगिंग करके, उस समय झिल्ली क्षमता का निर्धारण किया जा सकता है। GHK समीकरणों का अर्थ यह है कि किसी भी समय झिल्ली क्षमता का मान सभी पारगम्य आयनों की संतुलन क्षमता का भारित औसत होगा। भार झिल्ली के पार आयनों की सापेक्ष पारगम्यता है। | ||
| Line 167: | Line 167: | ||
प्लाज्मा झिल्ली के ढांकता हुआ गुणों में परिवर्तन मधुमेह और डिस्लिपिडेमिया जैसी अंतर्निहित स्थितियों की पहचान के रूप में कार्य कर सकता है।<ref name="pmid29029878">{{cite journal | vauthors = Ghoshal K, et al | title = Dielectric properties of plasma membrane: A signature for dyslipidemia in diabetes mellitus | journal = Arch Biochem Biophys | volume = 635 | pages = 27–36 | date = December 2017 | pmid = 29029878 | doi = 10.1016/j.abb.2017.10.002 }}</ref> | प्लाज्मा झिल्ली के ढांकता हुआ गुणों में परिवर्तन मधुमेह और डिस्लिपिडेमिया जैसी अंतर्निहित स्थितियों की पहचान के रूप में कार्य कर सकता है।<ref name="pmid29029878">{{cite journal | vauthors = Ghoshal K, et al | title = Dielectric properties of plasma membrane: A signature for dyslipidemia in diabetes mellitus | journal = Arch Biochem Biophys | volume = 635 | pages = 27–36 | date = December 2017 | pmid = 29029878 | doi = 10.1016/j.abb.2017.10.002 }}</ref> | ||
न्यूरोनल कोशिकाओं में, सोडियम चैनलों के माध्यम से सेल में सोडियम आयनों की भीड़ के साथ क्रिया क्षमता प्रारंभ होती है, जिसके परिणामस्वरूप विध्रुवण होता है, जबकि पुनर्प्राप्ति में पोटेशियम चैनलों के माध्यम से पोटेशियम की बाहरी भीड़ सम्मिलित होती है। ये दोनों प्रवाह निष्क्रिय परिवहन द्वारा होते हैं। | न्यूरोनल कोशिकाओं में, सोडियम चैनलों के माध्यम से सेल में सोडियम आयनों की भीड़ के साथ क्रिया क्षमता प्रारंभ होती है, जिसके परिणामस्वरूप विध्रुवण होता है, जबकि पुनर्प्राप्ति में पोटेशियम चैनलों के माध्यम से पोटेशियम की बाहरी भीड़ सम्मिलित होती है। ये दोनों प्रवाह निष्क्रिय परिवहन द्वारा होते हैं। | ||
Revision as of 11:06, 25 February 2023

झिल्ली क्षमता (ट्रांसमेम्ब्रेन क्षमता या झिल्ली वोल्टेज भी) जैविक कोशिका (जीव विज्ञान) के आंतरिक और बाहरी के मध्य विद्युत क्षमता में अंतर है। अर्थात्, विद्युत आवेशों को आंतरिक से बाहरी सेलुलर वातावरण में जाने के लिए आवश्यक ऊर्जा में अंतर होता है और इसके विपरीत, जब तक गतिज ऊर्जा का अधिग्रहण या विकिरण का उत्पादन नहीं होता है। आवेशों की सान्द्रता प्रवणता सीधे इस ऊर्जा आवश्यकता को निर्धारित करती है। सेल के बाहरी भाग के लिए, झिल्ली क्षमता के विशिष्ट मान, सामान्य रूप से मिली वोल्ट की इकाइयों में दिए जाते हैं और mV के रूप में दर्शाए जाते हैं, -80 mV से -40 mV तक होते हैं।
सभी जन्तु कोशिकाएं कोशिका झिल्ली से घिरी होती हैं जो लिपिड द्विस्तर से बनी होती है जिसमें प्रोटीन अंतःस्थापित होता है। झिल्ली आयनों की गति के लिए इन्सुलेटर और प्रसार बाधा दोनों के रूप में कार्य करती है। ट्रांसमेम्ब्रेन प्रोटीन, जिसे आयन ट्रांसपोर्टर या आयन पंप प्रोटीन के रूप में भी जाना जाता है, सक्रिय रूप से झिल्ली के पार आयनों को धकेलता है और झिल्ली के पार सांद्रता प्रवणता स्थापित करता है, और आयन चैनल आयनों को उन सांद्रता प्रवणताओं के नीचे झिल्ली में जाने की अनुमति देते हैं। आयन पंप और आयन चैनल विद्युत रूप से झिल्ली में डाली गई बैटरी और प्रतिरोधों के सेट के समतुल्य होते हैं, और इसलिए झिल्ली के दोनों किनारों के मध्य वोल्टेज बनाते हैं।
लगभग सभी प्लाज्मा झिल्लियों में विद्युत क्षमता होती है, जिसके अंदर सामान्यतः बाहर के संबंध में नकारात्मक होता है।[1] झिल्ली क्षमता के दो वास्तविक कार्य हैं। सबसे पहले, यह सेल को बैटरी के रूप में कार्य करने की अनुमति देता है, झिल्ली में एम्बेडेड विभिन्न प्रकार के "आणविक उपकरणों" को संचालित करने की शक्ति प्रदान करता है।[2] दूसरा, विद्युत रूप से उत्तेजनीय कोशिकाओं जैसे न्यूरॉन्स और पेशी कोशिकाओं में, इसका उपयोग कोशिका के विभिन्न भागों के मध्य संकेतों को प्रसारित करने के लिए किया जाता है। झिल्ली में बिंदु पर आयन चैनलों को खोलने या बंद करने से सिग्नल उत्पन्न होते हैं, जिससे झिल्ली क्षमता में स्थानीय परिवर्तन होता है। विद्युत क्षेत्र में इस परिवर्तन को झिल्ली में आसन्न या अधिक दूर के आयन चैनलों द्वारा शीघ्रता से अनुभूत किया जा सकता है। वे आयन चैनल सिग्नल को पुन: उत्पन्न करने वाले संभावित परिवर्तन के परिणामस्वरूप खुल या बंद हो सकते हैं।
अन्य -उत्तेजक कोशिकाओं में, और उनके आधारभूत राज्यों में उत्तेजनीय कोशिकाओं में, झिल्ली क्षमता अपेक्षाकृत स्थिर मूल्य पर होती है, जिसे विश्राम क्षमता कहा जाता है। न्यूरॉन्स के लिए, विश्राम क्षमता को -80 से -70 मिलीवोल्ट तक के रूप में परिभाषित किया गया है; अर्थात्, सेल के आंतरिक भाग में वोल्ट के दसवें भाग से थोड़ा अल्प ऋणात्मक आधारभूत वोल्टेज होता है। आयन चैनलों के खुलने और बंद होने से विश्राम क्षमता से प्रस्थान हो सकता है। इसे विध्रुवण कहा जाता है यदि आंतरिक वोल्टेज अल्प ऋणात्मक हो जाता है (जैसे -70 mV से -60 mV), या अतिध्रुवीकरण (जीव विज्ञान)जीवविज्ञान) यदि आंतरिक वोल्टेज अधिक ऋणात्मक हो जाता है (-70 mV से -80 mV तक)। उत्तेजनीय कोशिकाओं में, पर्याप्त रूप से बड़ा विध्रुवण ऐक्शन पोटेंशिअल उत्पन्न कर सकता है, जिसमें झिल्ली क्षमता थोड़े समय के लिए (1 से 100 मिलीसेकंड के क्रम में) तेजी से और महत्वपूर्ण रूप से बदलती है, प्रायः इसकी ध्रुवीयता को उलट देती है। संभावित कार्रवाई कुछ वोल्टेज-गेटेड आयन चैनलों की सक्रियता से उत्पन्न होते हैं।
न्यूरॉन्स में, झिल्ली क्षमता को प्रभावित करने वाले कारक विविध होते हैं। उनमें अनेक प्रकार के आयन चैनल सम्मिलित हैं, जिनमें से कुछ रासायनिक रूप से गेटेड हैं और कुछ वोल्टेज-गेटेड हैं। क्योंकि वोल्टेज-गेटेड आयन चैनल झिल्ली क्षमता द्वारा नियंत्रित होते हैं, जबकि झिल्ली क्षमता स्वयं इन्हीं आयन चैनलों से प्रभावित होती है, फीडबैक लूप जो जटिल लौकिक गतिकी की अनुमति देते हैं, जिसमें दोलन और पुनर्योजी घटनाएं जैसे क्रिया क्षमता सम्मिलित हैं।
भौतिक आधार
कोशिका में झिल्ली क्षमता अंततः दो कारकों से उत्पन्न होती है: विद्युत बल और प्रसार। विद्युत बल विपरीत विद्युत आवेशों (सकारात्मक और ऋणात्मक) वाले कणों के मध्य परस्पर आकर्षण और ही प्रकार के आवेश वाले कणों के मध्य पारस्परिक प्रतिकर्षण (धनात्मक या दोनों ऋणात्मक) से उत्पन्न होता है। कणों की सांख्यिकीय प्रवृत्ति से प्रसार उन क्षेत्रों से पुनर्वितरण के लिए उत्पन्न होता है जहां वे उन क्षेत्रों में अत्यधिक केंद्रित होते हैं जहां एकाग्रता अल्प होती है।
वोल्टेज
वोल्टेज, जो विद्युत क्षमता में अंतर का पर्याय है, प्रतिरोध में विद्युत प्रवाह को चलाने की क्षमता है। वास्तव में, वोल्टेज की सबसे सरल परिभाषा ओम के नियम द्वारा दी गई है: V = IR, जहाँ V वोल्टेज है, I करंट है और R प्रतिरोध है। यदि वोल्टेज स्रोत जैसे कि बैटरी को विद्युत परिपथ में रखा जाता है, तो स्रोत का वोल्टेज जितना अधिक होगा, उतनी ही अधिक मात्रा में यह उपलब्ध प्रतिरोध में प्रवाहित होगा। वोल्टेज का कार्यात्मक महत्व केवल सर्किट में दो बिंदुओं के मध्य संभावित अंतरों में निहित है। बिंदु पर वोल्टेज का विचार अर्थहीन है। सर्किट के कुछ मनमाने ढंग से चुने गए तत्व के लिए शून्य का वोल्टेज असाइन करना इलेक्ट्रॉनिक्स में पारंपरिक है, और फिर उस शून्य बिंदु के सापेक्ष मापे गए अन्य तत्वों के लिए वोल्टेज असाइन करना। इसमें कोई महत्व नहीं है कि किस तत्व को शून्य बिंदु के रूप में चुना जाता है- सर्किट का कार्य केवल अंतर पर निर्भर करता है न कि वोल्टेज प्रति से। चूँकि , अधिकांशतः स्तिथियों में और सम्मेलन द्वारा, शून्य स्तर को प्रायः सर्किट के भाग को सौंपा जाता है जो ग्राउंड (बिजली) | ग्राउंड के संपर्क में होता है।
सेल बायोलॉजी में वोल्टेज पर भी यही सिद्धांत प्रारम्भ होता है। विद्युत रूप से सक्रिय ऊतक में, किसी भी दो बिंदुओं के मध्य संभावित अंतर को प्रत्येक बिंदु पर इलेक्ट्रोड डालकर मापा जा सकता है, उदाहरण के लिए अंदर और सेल के बाहर, और दोनों इलेक्ट्रोड को विशेष वाल्टमीटर के सार से जोड़कर। प्रथा के अनुसार, शून्य संभावित मान को सेल के बाहर के लिए नियत किया जाता है और बाहरी और अंदर के मध्य संभावित अंतर का संकेत बाहरी शून्य के सापेक्ष अंदर की क्षमता से निर्धारित होता है।
गणितीय शब्दों में, वोल्टेज की परिभाषा विद्युत क्षेत्र की अवधारणा से प्रारंभ होती है E, अंतरिक्ष में प्रत्येक बिंदु को परिमाण और दिशा निर्दिष्ट करने वाला सदिश क्षेत्र। अनेक स्थितियों में, विद्युत क्षेत्र रूढ़िवादी क्षेत्र है, जिसका अर्थ है कि इसे स्केलर फ़ंक्शन के ढाल के रूप में व्यक्त किया जा सकता है V, वह है, E = –∇V. यह अदिश क्षेत्र V वोल्टेज वितरण के रूप में जाना जाता है। परिभाषा एकीकरण के मनमाने स्थिरांक की अनुमति देती है - यही कारण है कि वोल्टेज के निरपेक्ष मान अर्थपूर्ण नहीं हैं। सामान्य तौर पर, विद्युत क्षेत्रों को रूढ़िवादी माना जा सकता है यदि चुंबकीय क्षेत्र उन्हें महत्वपूर्ण रूप से प्रभावित नहीं करते हैं, लेकिन यह स्थिति सामान्यतः जैविक ऊतक पर अच्छी तरह से प्रारम्भ होती है।
क्योंकि विद्युत क्षेत्र वोल्टेज वितरण का ढाल है, छोटे से क्षेत्र में वोल्टेज में तेजी से परिवर्तन मजबूत विद्युत क्षेत्र का संकेत देता है; इसके विपरीत, यदि किसी बड़े क्षेत्र में वोल्टेज लगभग समान रहता है, तो उस क्षेत्र में विद्युत क्षेत्र कमजोर होना चाहिए। मजबूत विद्युत क्षेत्र, मजबूत वोल्टेज प्रवणता के बराबर, का तात्पर्य है कि किसी भी आवेशित कण पर मजबूत बल लगाया जाता है जो क्षेत्र के भीतर होता है।
आयन और अपनी गति चलाने वाले बल

जैविक जीवों के भीतर विद्युत संकेत सामान्य रूप से आयनों द्वारा संचालित होते हैं।[4] ऐक्शन पोटेंशिअल के लिए सबसे महत्वपूर्ण धनायन हैं सोडियम (Na+) और पोटैशियम (K+).Cite error: Closing </ref> missing for <ref> tag जो द्विसंयोजी धनायन है जो दोहरा धनावेश वहन करता है। क्लोराइड आयन (Cl−) कुछ शैवाल की क्रिया क्षमता में प्रमुख भूमिका निभाता है,[5] लेकिन अधिकांश जानवरों की कार्य क्षमता में नगण्य भूमिका निभाता है। संदर्भ>नट श्मिट-नीलसन|श्मिट-नीलसन, पृ. 483.</ref>
आयन कोशिका झिल्ली को दो प्रभावों के अनुसार पार करते हैं: प्रसार और विद्युत क्षेत्र। सरल उदाहरण जिसमें दो समाधान-ए और बी-एक झरझरा अवरोध से अलग होते हैं, यह दर्शाता है कि प्रसार यह सुनिश्चित करेगा कि वे अंततः समान समाधानों में मिल जाएंगे। यह मिश्रण उनकी सांद्रता में अंतर के कारण होता है। उच्च सांद्रता वाला क्षेत्र अल्प सांद्रता वाले क्षेत्र की ओर फैल जाएगा। उदाहरण का विस्तार करने के लिए, समाधान A में 30 सोडियम आयन और 30 क्लोराइड आयन हैं। साथ ही, मान लें कि विलयन B में केवल 20 सोडियम आयन और 20 क्लोराइड आयन हैं। यह मानते हुए कि अवरोध दोनों प्रकार के आयनों को इसके माध्यम से यात्रा करने की अनुमति देता है, तब स्थिर स्थिति प्राप्त होगी जिससे दोनों समाधानों में 25 सोडियम आयन और 25 क्लोराइड आयन होंगे। यदि, चूँकि , झरझरा बाधा चयनात्मक है जिसके माध्यम से आयनों को जाने दिया जाता है, तो केवल विसरण परिणामी समाधान का निर्धारण नहीं करेगा। पिछले उदाहरण पर लौटते हुए, आइए अब अवरोध का निर्माण करें जो केवल सोडियम आयनों के लिए पारगम्य है। अब, केवल सोडियम को समाधान ए में इसकी उच्च सांद्रता से समाधान बी में अल्प सांद्रता तक बाधा को पार करने की अनुमति है। इसके परिणामस्वरूप समाधान बी में क्लोराइड आयनों की तुलना में सोडियम आयनों का अधिक संचय होगा और सोडियम आयनों की संख्या अल्प होगी। समाधान ए में क्लोराइड आयन।
इसका तात्पर्य यह है कि नकारात्मक रूप से चार्ज किए गए क्लोराइड आयनों की तुलना में सकारात्मक रूप से चार्ज किए गए सोडियम आयनों की उच्च सांद्रता से समाधान बी में शुद्ध सकारात्मक चार्ज होता है। इसी तरह, सकारात्मक सोडियम आयनों की तुलना में नकारात्मक क्लोराइड आयनों की अधिक सांद्रता से समाधान ए में शुद्ध नकारात्मक चार्ज होता है। चूँकि विपरीत आवेश आकर्षित होते हैं और समान आवेश प्रतिकर्षित होते हैं, आयन अब विद्युत क्षेत्रों के साथ-साथ विसरण की शक्तियों से भी प्रभावित होते हैं। इसलिए, सकारात्मक सोडियम आयनों की अब-अधिक-सकारात्मक बी समाधान की यात्रा करने की संभावना अल्प होगी और अब-अधिक-नकारात्मक ए समाधान में बने रहेंगे। जिस बिंदु पर विद्युत क्षेत्र के बल विसरण के कारण बल का पूरी तरह से प्रतिकार करते हैं उसे संतुलन क्षमता कहा जाता है। इस बिंदु पर, विशिष्ट आयन (इस स्थिति में सोडियम) का शुद्ध प्रवाह शून्य है।
प्लाज्मा झिल्ली

प्रत्येक कोशिका प्लाज़्मा झिल्ली में घिरी होती है, जिसमें लिपिड बाईलेयर की संरचना होती है जिसमें अनेक प्रकार के बड़े अणु सन्निहित होते हैं। क्योंकि यह लिपिड अणुओं से बना है, प्लाज्मा झिल्ली में आंतरिक रूप से उच्च विद्युत प्रतिरोधकता होती है, दूसरे शब्दों में आयनों के लिए अल्प आंतरिक पारगम्यता होती है। चूँकि , झिल्ली में एम्बेडेड कुछ अणु सक्रिय रूप से आयनों को झिल्ली के तरफ से दूसरी तरफ ले जाने या चैनल प्रदान करने में सक्षम होते हैं जिसके माध्यम से वे स्थानांतरित हो सकते हैं।Cite error: Closing </ref> missing for <ref> tag परिणामस्वरूप, पोटेशियम आयनों की सांद्रता K+ न्यूरॉन के अंदर बाहरी सांद्रता की तुलना में लगभग 20 गुना बड़ा है, जबकि बाहर की सोडियम सांद्रता अंदर की तुलना में लगभग नौ गुना बड़ी है।Cite error: Closing </ref> missing for <ref> tag आयन शायद ही कभी गलत चैनल से गुजरते हैं। उदाहरण के लिए, सोडियम या कैल्शियम आयन पोटेशियम चैनल के माध्यम से शायद ही कभी गुजरते हैं। alt=सात गोले जिनकी त्रिज्या मोनो-वैलेंट लिथियम, सोडियम, पोटेशियम, रुबिडियम, सीज़ियम केशन (0.76, 1.02, 1.38, 1.52, और) की त्रिज्या के समानुपाती होती है। 1.67 Å, क्रमशः), डाइवेलेंट कैल्शियम केशन (1.00 Å) और मोनो-वैलेंट क्लोराइड (1.81 Å)।]]आयन चैनल छिद्र के साथ अभिन्न झिल्ली प्रोटीन होते हैं जिसके माध्यम से आयन बाह्य अंतरिक्ष और कोशिका आंतरिक के मध्य यात्रा कर सकते हैं। अधिकांश चैनल आयन के लिए विशिष्ट (चयनात्मक) होते हैं; उदाहरण के लिए, अधिकांश पोटेशियम चैनल 1000: 1 सोडियम पर पोटेशियम के लिए चयनात्मकता अनुपात की विशेषता है, चूँकि पोटेशियम और सोडियम आयनों का ही चार्ज होता है और उनके त्रिज्या में केवल थोड़ा भिन्न होता है। चैनल ताकना सामान्यतः इतना छोटा होता है कि आयनों को एकल-फ़ाइल क्रम में इसके माध्यम से गुजरना पड़ता है।Cite error: Closing </ref> missing for <ref> tag
एक चैनल में अनेक अलग-अलग अवस्थाएँ हो सकती हैं (प्रोटीन की विभिन्न प्रोटीन संरचना के अनुरूप), लेकिन ऐसी प्रत्येक अवस्था या तो खुली या बंद होती है। सामान्य तौर पर, बंद अवस्थाएँ या तो छिद्र के संकुचन के अनुरूप होती हैं - जिससे यह आयन के लिए अगम्य हो जाता है - या प्रोटीन के अलग भाग में, छिद्र को रोक देता है। उदाहरण के लिए, वोल्टेज पर निर्भर सोडियम चैनल निष्क्रियता से गुजरता है, जिसमें प्रोटीन का हिस्सा छिद्र में घुस जाता है, इसे सील कर देता है।[6] यह निष्क्रियता सोडियम करंट को बंद कर देती है और ऐक्शन पोटेंशिअल में महत्वपूर्ण भूमिका निभाती है।
आयन चैनलों को वर्गीकृत किया जा सकता है कि वे अपने पर्यावरण पर कैसे प्रतिक्रिया करते हैं।[7] उदाहरण के लिए, ऐक्शन पोटेंशिअल में सम्मिलित आयन चैनल वोल्टेज-संवेदी चैनल हैं; वे झिल्ली के पार वोल्टेज की प्रतिक्रिया में खुलते और बंद होते हैं। लिगैंड-गेटेड चैनल और महत्वपूर्ण वर्ग बनाते हैं; ये आयन चैनल स्नायुसंचारी जैसे लिगैंड (जैव रसायन) के बंधन के जवाब में खुलते और बंद होते हैं। अन्य आयन चैनल यांत्रिक बलों के साथ खुलते और बंद होते हैं। अभी भी अन्य आयन चैनल- जैसे कि संवेदी न्यूरॉन्स- प्रकाश, तापमान या दबाव जैसे अन्य उत्तेजनाओं के जवाब में खुले और बंद होते हैं।
बहिर्वाहचैनल
बहिर्वाहचैनल सबसे सरल प्रकार के आयन चैनल हैं, जिसमें उनकी पारगम्यता अल्प या ज्यादा स्थिर होती है। बहिर्वाहचैनलों के प्रकार जिनका न्यूरॉन्स में सबसे बड़ा महत्व है, पोटेशियम और क्लोराइड चैनल हैं। यहां तक कि ये अपने गुणों में पूरी तरह से स्थिर नहीं हैं: सबसे पहले, उनमें से अधिकतर वोल्टेज-निर्भर हैं इस अर्थ में कि वे दिशा में दूसरे की तुलना में बेहतर संचालन करते हैं (दूसरे शब्दों में, वे सुधारक हैं); दूसरा, उनमें से कुछ रासायनिक ligands द्वारा बंद करने में सक्षम हैं, भले ही उन्हें संचालित करने के लिए ligands की आवश्यकता न हो।
लिगैंड-गेटेड चैनल
लिगैंड-गेटेड आयन चैनल वे चैनल होते हैं जिनकी पारगम्यता बहुत बढ़ जाती है जब कुछ प्रकार के रासायनिक लिगैंड प्रोटीन संरचना से जुड़ जाते हैं। पशु कोशिकाओं में सैकड़ों नहीं तो हजारों प्रकार के होते हैं। न्यूरोट्रांसमीटर रिसेप्टर्स के रूप में बड़ा उपसमुच्चय कार्य - वे पोस्टअन्तर्ग्रथनी साइटों पर होते हैं, और रासायनिक लिगैंड जो उन्हें गेट करता है, प्रीसानेप्टिक एक्सज़ोन का अंत द्वारा जारी किया जाता है। इस प्रकार का उदाहरण AMPA रिसेप्टर है, न्यूरोट्रांसमीटर ग्लुटामिक एसिड के लिए रिसेप्टर है जो सक्रिय होने पर सोडियम और पोटेशियम आयनों को पारित करने की अनुमति देता है। अन्य उदाहरण GABAA रिसेप्टर | GABA हैA रिसेप्टर, न्यूरोट्रांसमीटर GABA के लिए रिसेप्टर जो सक्रिय होने पर क्लोराइड आयनों को पारित करने की अनुमति देता है।
न्यूरोट्रांसमीटर रिसेप्टर्स लिगेंड द्वारा सक्रिय होते हैं जो बाह्य क्षेत्र में दिखाई देते हैं, लेकिन अन्य प्रकार के लिगैंड-गेटेड चैनल हैं जो इंट्रासेल्युलर पक्ष पर बातचीत द्वारा नियंत्रित होते हैं।
वोल्टेज पर निर्भर चैनल
वोल्टेज-गेटेड आयन चैनल, जिन्हें वोल्टेज निर्भर आयन चैनल भी कहा जाता है, ऐसे चैनल हैं जिनकी पारगम्यता झिल्ली क्षमता से प्रभावित होती है। वे और बहुत बड़ा समूह बनाते हैं, जिसमें प्रत्येक सदस्य के पास विशेष आयन चयनात्मकता और विशेष वोल्टेज निर्भरता होती है। अनेक समय-निर्भर भी होते हैं - दूसरे शब्दों में, वे वोल्टेज परिवर्तन पर तुरंत प्रतिक्रिया नहीं देते हैं, लेकिन केवल देरी के पश्चात ।
इस समूह के सबसे महत्वपूर्ण सदस्यों में से एक प्रकार का वोल्टेज-गेटेड सोडियम चैनल है जो एक्शन पोटेंशिअल को रेखांकित करता है - इन्हें कभी-कभी हॉजकिन-हक्सले सोडियम चैनल कहा जाता है क्योंकि शुरुआत में उन्हें एलन लॉयड हॉजकिन और एंड्रयू हक्सले ने अपने नोबेल पुरस्कार विजेता में चित्रित किया था। क्रिया क्षमता के शरीर विज्ञान का अध्ययन। चैनल आराम करने वाले वोल्टेज स्तर पर बंद है, लेकिन जब वोल्टेज निश्चित सीमा से अधिक हो जाता है, तो सोडियम आयनों का बड़ा प्रवाह होता है जो झिल्ली क्षमता में बहुत तेजी से परिवर्तन उत्पन्न करता है। ऐक्शन पोटेंशिअल से रिकवरी आंशिक रूप से प्रकार के वोल्टेज-गेटेड पोटेशियम चैनल पर निर्भर करती है जो रेस्टिंग वोल्टेज स्तर पर बंद होता है लेकिन ऐक्शन पोटेंशिअल के समय उत्पन्न बड़े वोल्टेज परिवर्तन के परिणामस्वरूप खुलता है।
उत्क्रमण क्षमता
एक आयन की उत्क्रमण क्षमता (या संतुलन क्षमता) ट्रांसमेम्ब्रेन वोल्टेज का मान है, जिस पर विसारक और विद्युत बल प्रतिसंतुलन करते हैं, जिससे कि झिल्ली में कोई शुद्ध आयन प्रवाह न हो। इसका तात्पर्य यह है कि ट्रांसमेम्ब्रेन वोल्टेज आयन के प्रसार के बल का बिल्कुल विरोध करता है, जैसे कि झिल्ली के पार आयन का शुद्ध प्रवाह शून्य और अपरिवर्तनीय होता है। उत्क्रमण क्षमता महत्वपूर्ण है क्योंकि यह वोल्टेज देता है जो उस आयन के लिए पारगम्य चैनलों पर कार्य करता है - दूसरे शब्दों में, यह वोल्टेज देता है जो आयन एकाग्रता ढाल उत्पन्न करता है जब यह बैटरी (बिजली) के रूप में कार्य करता है।
किसी विशेष आयन की संतुलन क्षमता को सामान्यतः संकेतन E द्वारा निर्दिष्ट किया जाता हैionकिसी भी आयन के लिए संतुलन क्षमता की गणना नर्नस्ट समीकरण का उपयोग करके की जा सकती है।[8] उदाहरण के लिए, पोटेशियम आयनों की उत्क्रमण क्षमता इस प्रकार होगी:
कहाँ
- इeq,K+ वोल्ट में मापा पोटेशियम के लिए संतुलन क्षमता है
- आर सार्वभौमिक गैस स्थिरांक है, जो 8.314 जूल·के के बराबर है-1</सुपा> मोल-1
- T पूर्ण तापमान है, जिसे केल्विन में मापा जाता है (= K = डिग्री सेल्सियस + 273.15)
- जेड प्रतिक्रिया में सम्मिलित विचाराधीन आयन के प्राथमिक आवेशों की संख्या है
- F फैराडे स्थिरांक है, जो 96,485 कूलॉम·मोल के बराबर है−1 या जे·वी-1</सुपा> मोल-1
- [क+]o मोल (यूनिट)·m में मापी जाने वाली पोटैशियम की बाह्य कोशिकीय सांद्रता है−3 या mmol·l-1
- [क+]i पोटेशियम की इंट्रासेल्युलर एकाग्रता है
भले ही दो भिन्न आयनों का आवेश समान हो (अर्थात्, K+ और ना+), उनके पास अभी भी बहुत अलग संतुलन क्षमता हो सकती है, बशर्ते उनकी बाहरी और/या अंदर की सांद्रता अलग-अलग हो। उदाहरण के लिए, न्यूरॉन्स में पोटेशियम और सोडियम की संतुलन क्षमता को लें। पोटेशियम संतुलन क्षमता ईK -84 mV है जिसमें 5 मिलीमीटर पोटेशियम बाहर और 140 मिलीमीटर अंदर है। दूसरी ओर, सोडियम संतुलन क्षमता, ईNa, लगभग +66 एमवी है जिसमें लगभग 12 एमएम सोडियम अंदर और 140 एमएम बाहर है।[note 1]
विकास के समय झिल्ली क्षमता में परिवर्तन
एक जीव के तंत्रिका विकास के समय न्यूरॉन की आराम करने वाली झिल्ली क्षमता वास्तव में बदल जाती है। न्यूरॉन के लिए अंततः अपने पूर्ण वयस्क कार्य को अपनाने के लिए, विकास के समय इसकी क्षमता को कड़ाई से नियंत्रित किया जाना चाहिए। जैसे-जैसे जीव विकास के माध्यम से आगे बढ़ता है, आराम करने वाली झिल्ली क्षमता अधिक नकारात्मक हो जाती है।[9] मस्तिष्क में विकास की प्रगति के रूप में न्यूरोग्लिया भी विभेदित और प्रसार कर रहे हैं।[10] इन ग्लिअल कोशिकाओं के जुड़ने से बाह्य कोशिकीय पोटेशियम को विनियमित करने की जीव की क्षमता बढ़ जाती है। बाह्य पोटेशियम में गिरावट से झिल्ली क्षमता में 35 mV की कमी हो सकती है।[11]
सेल उत्तेजना
सेल एक्साइटेबिलिटी झिल्ली क्षमता में परिवर्तन है जो विभिन्न ऊतकों में सेलुलर प्रतिक्रियाओं के लिए आवश्यक है। सेल एक्साइटेबिलिटी संपत्ति है जो शुरुआती एम्ब्रियोजेनेसिस के समय प्रेरित होती है।[12] सेल की उत्तेजना को भी उस आसानी के रूप में परिभाषित किया गया है जिसके साथ प्रतिक्रिया प्रारंभ हो सकती है।[13] रेस्टिंग और दहलीज क्षमता सेल एक्साइटेबिलिटी का आधार बनाते हैं और ये प्रक्रियाएँ ग्रेडेड और एक्शन पोटेंशिअल के निर्माण के लिए मूलभूत हैं।
सेल एक्साइटेबिलिटी का सबसे महत्वपूर्ण समस्थिति बाह्य इलेक्ट्रोलाइट सांद्रता (अर्थात Na+, के+, कैल्शियम मेटाबोलिज्म|सीए2+, सीएल−, जीव विज्ञान में मैग्नीशियम|मिलीग्राम2+) और संबंधित प्रोटीन। सेल एक्साइटेबिलिटी को नियंत्रित करने वाले महत्वपूर्ण प्रोटीन वोल्टेज-गेटेड आयन चैनल, आयन ट्रांसपोर्टर (जैसे Na + / K + -ATPase, मैग्नीशियम ट्रांसपोर्टर, एसिड-बेस होमियोस्टेसिस | एसिड-बेस ट्रांसपोर्टर), रिसेप्टर (जैव रसायन) और HCN चैनल हैं। हाइपरपोलराइजेशन-एक्टिवेटेड साइक्लिक- न्यूक्लियोटाइड-गेटेड चैनल।[14] उदाहरण के लिए, पोटेशियम चैनल और कैल्शियम-सेंसिंग रिसेप्टर्स न्यूरॉन्स, कार्डियक मायोसाइट्स और अनेक अन्य उत्तेजक कोशिकाओं जैसे एस्ट्रोसाइट्स में उत्तेजना के महत्वपूर्ण नियामक हैं।[15] एक्साइटेबल सेल सिग्नलिंग में कैल्शियम आयन भी सबसे महत्वपूर्ण दूसरा दूत प्रणाली है। सिनैप्टिक रिसेप्टर्स की सक्रियता न्यूरोप्लास्टिकिटी की शुरुआत करती है। न्यूरोनल एक्साइटेबिलिटी में लंबे समय तक चलने वाले बदलाव।[16] थायराइड हार्मोन, अधिवृक्क ग्रंथि और अन्य हार्मोन भी कोशिका उत्तेजना को नियंत्रित करते हैं, उदाहरण के लिए, प्रोजेस्टेरोन और एस्ट्रोजन मायोमेट्रियल चिकनी पेशी कोशिका उत्तेजना को नियंत्रित करते हैं।
अनेक प्रकार की कोशिकाओं को उत्तेजनीय झिल्ली वाला माना जाता है। उत्तेजक कोशिकाएं न्यूरॉन्स, मायोसाइट्स (हृदय, कंकाल, चिकनी पेशी), संवहनी अन्तःचूचुक, पेरिसाईट, जूसटैग्लोमेरुलर कोशिकाएंकाजल की अंतरालीय कोशिका सेल, अनेक प्रकार के उपकला (जैसे बीटा सेल, अल्फा सेल, डेल्टा सेल, एंटरोएंडोक्राइन सेल, न्यूरोएंडोक्राइन सेल # पल्मोनरी हैं) न्यूरोएंडोक्राइन कोशिकाएं, पीनियलोसाइट्स), ग्लियाल कोशिकाएं (जैसे एस्ट्रोसाइट्स), mechanoreceptor कोशिकाएं (जैसे बालों की कोशिकाएं और मर्केल कोशिकाएं), chemoreceptor कोशिकाएं (जैसे ग्लोमस कोशिकाएं, स्वाद रिसेप्टर्स), कुछ पादप कोशिकाएं और संभवतः श्वेत रक्त कोशिका।[17] एस्ट्रोसाइट्स अनेक रिसेप्टर्स की अभिव्यक्ति से संबंधित इंट्रासेल्युलर कैल्शियम विविधताओं के आधार पर अन्य -विद्युत उत्तेजना का रूप प्रदर्शित करते हैं जिसके माध्यम से वे सिनैप्टिक सिग्नल का पता लगा सकते हैं। न्यूरॉन्स में, सेल के कुछ हिस्सों में अलग-अलग झिल्ली गुण होते हैं, उदाहरण के लिए, डेंड्राइटिक एक्साइटेबिलिटी न्यूरॉन्स को स्थानिक रूप से अलग किए गए इनपुट के संयोग का पता लगाने की क्षमता प्रदान करती है।[18]
समतुल्य सर्किट
इलेक्ट्रोफिजियोलॉजिस्ट समतुल्य सर्किट के संदर्भ में आयनिक सांद्रता अंतर, आयन चैनल और झिल्ली समाई के प्रभाव को मॉडल करते हैं, जिसका उद्देश्य झिल्ली के छोटे पैच के विद्युत गुणों का प्रतिनिधित्व करना है। समतुल्य सर्किट में चार पाथवे के साथ समानांतर में संधारित्र होता है, जिसमें प्रत्येक में चर चालन के साथ श्रृंखला में बैटरी होती है। समाई लिपिड बाईलेयर के गुणों द्वारा निर्धारित की जाती है, और इसे तय करने के लिए लिया जाता है। चार समानांतर मार्गों में से प्रत्येक प्रमुख आयनों, सोडियम, पोटेशियम, क्लोराइड और कैल्शियम में से से आता है। प्रत्येक आयनिक मार्ग का वोल्टेज झिल्ली के प्रत्येक तरफ आयन की सांद्रता द्वारा निर्धारित किया जाता है; ऊपर मेम्ब्रेन पोटेंशिअल#रिवर्सल पोटेंशिअल सेक्शन देखें। किसी भी समय प्रत्येक आयनिक मार्ग का संचालन उन सभी आयन चैनलों की अवस्थाओं द्वारा निर्धारित किया जाता है जो उस आयन के लिए संभावित रूप से पारगम्य हैं, जिसमें बहिर्वाह चैनल, लिगैंड-गेटेड चैनल और वोल्टेज-गेटेड आयन चैनल सम्मिलित हैं।

निश्चित आयन सांद्रता और आयन चैनल चालन के निश्चित मूल्यों के लिए, समतुल्य सर्किट को और अल्प किया जा सकता है, जैसा कि नीचे वर्णित गोल्डमैन समीकरण का उपयोग करके, बैटरी और चालन के समानांतर समाई वाले सर्किट में किया जा सकता है। विद्युत शब्दों में, यह प्रकार का आरसी सर्किट (प्रतिरोध-समाई सर्किट) है, और इसके विद्युत गुण बहुत सरल हैं। किसी भी प्रारंभिक अवस्था से प्रारंभ होकर, प्रवाहकत्त्व या समाई में बहने वाली धारा घातीय समय पाठ्यक्रम के साथ घटती है, समय स्थिर के साथ τ = RC, कहाँ C झिल्ली पैच की समाई है, और R = 1/gnet शुद्ध प्रतिरोध है। यथार्थवादी स्थितियों के लिए, समय स्थिरांक सामान्यतः 1—100 मिलीसेकंड की सीमा में होता है। अधिकांशतः स्तिथियों में, आयन चैनलों के चालन में परिवर्तन तेजी से समय के पैमाने पर होता है, इसलिए आरसी सर्किट अच्छा सन्निकटन नहीं है; चूँकि , झिल्ली पैच को मॉडल करने के लिए उपयोग किया जाने वाला अंतर समीकरण सामान्यतः RC सर्किट समीकरण का संशोधित संस्करण है।
आराम करने की क्षमता
जब किसी कोशिका की झिल्ली क्षमता बिना महत्वपूर्ण बदलाव के लंबे समय तक चलती है, तो इसे आराम करने की क्षमता या आराम करने वाली वोल्टेज के रूप में संदर्भित किया जाता है। यह शब्द अन्य -उत्तेजक कोशिकाओं की झिल्ली क्षमता के लिए प्रयोग किया जाता है, लेकिन उत्तेजना के अभाव में उत्तेजनीय कोशिकाओं की झिल्ली क्षमता के लिए भी। उत्तेजनीय कोशिकाओं में, अन्य संभावित अवस्थाएँ वर्गीकृत झिल्ली क्षमताएँ (चर आयाम वाली) हैं, और क्रिया क्षमताएँ, जो बड़ी हैं, झिल्ली क्षमता में सभी या कुछ भी नहीं उगती हैं जो सामान्यतः निश्चित समय पाठ्यक्रम का पालन करती हैं। उत्तेजक कोशिकाओं में न्यूरॉन्स, मांसपेशियों की कोशिकाएं और ग्रंथियों में कुछ स्रावी कोशिकाएं सम्मिलित हैं। चूँकि , अन्य प्रकार की कोशिकाओं में भी, झिल्ली वोल्टेज पर्यावरण या इंट्रासेल्युलर उत्तेजनाओं के जवाब में परिवर्तन से गुजर सकता है। उदाहरण के लिए, प्लाज्मा झिल्ली का विध्रुवण apoptosis में महत्वपूर्ण कदम प्रतीत होता है।[19] आराम करने की क्षमता उत्पन्न करने वाली बातचीत को गोल्डमैन समीकरण द्वारा प्रतिरूपित किया जाता है।[20] यह ऊपर दिखाए गए नर्नस्ट समीकरण के रूप में समान है, जिसमें यह प्रश्न में आयनों के आरोपों के साथ-साथ उनके अंदर और बाहर की सांद्रता के मध्य के अंतर पर आधारित है। चूँकि , यह प्रश्न में प्रत्येक आयन के लिए प्लाज्मा झिल्ली की सापेक्ष पारगम्यता को भी ध्यान में रखता है।
इस समीकरण में दिखाई देने वाले तीन आयन पोटेशियम (के+), सोडियम (Na+), और क्लोराइड (Cl-). कैल्शियम छोड़ दिया गया है, लेकिन उन स्थितियों से निपटने के लिए जोड़ा जा सकता है जिनमें यह महत्वपूर्ण भूमिका निभाता है।[21] ऋणायन होने के कारण, क्लोराइड पदों को धनायन पदों से भिन्न माना जाता है; इंट्रासेल्युलर एकाग्रता अंश में है, और हर में बाह्य एकाग्रता, जो कि कटियन शब्दों से उलट है। पीi आयन प्रकार i की सापेक्ष पारगम्यता के लिए खड़ा है।
संक्षेप में, गोल्डमैन सूत्र झिल्ली क्षमता को पारगम्यता द्वारा भारित व्यक्तिगत आयन प्रकारों के लिए उत्क्रमण क्षमता के भारित औसत के रूप में व्यक्त करता है। (चूँकि ऐक्शन पोटेंशिअल के समय झिल्ली क्षमता में लगभग 100 mV परिवर्तन होता है, कोशिका के अंदर और बाहर आयनों की सांद्रता महत्वपूर्ण रूप से नहीं बदलती है। वे अपनी संबंधित सांद्रता के करीब रहते हैं जब झिल्ली स्थिर क्षमता पर होती है।) अधिकांश पशु कोशिकाओं में, सोडियम की पारगम्यता की तुलना में आराम की अवस्था में पोटेशियम की पारगम्यता बहुत अधिक होती है। नतीजतन, आराम करने की क्षमता सामान्यतः पोटेशियम उत्क्रमण क्षमता के करीब होती है।[22][23] क्लोराइड की पारगम्यता महत्वपूर्ण होने के लिए पर्याप्त उच्च हो सकती है, लेकिन, अन्य आयनों के विपरीत, क्लोराइड को सक्रिय रूप से पंप नहीं किया जाता है, और इसलिए अन्य आयनों द्वारा निर्धारित विश्राम क्षमता के बहुत करीब उत्क्रमण क्षमता पर संतुलित होता है।
अधिकांश पशु कोशिकाओं में आराम करने वाली झिल्ली क्षमता के मान सामान्यतः पोटेशियम उत्क्रमण क्षमता (सामान्यतः लगभग -80 mV) और लगभग -40 mV के मध्य भिन्न होते हैं। उत्तेजनीय कोशिकाओं (ऐक्शन पोटेंशिअल उत्पन्न करने में सक्षम) में विश्राम क्षमता सामान्यतः -60 mV के करीब होती है—अधिक विध्रुवित वोल्टेज से ऐक्शन पोटेंशिअल का सहज उत्पादन होता है। अपरिपक्व या अविभाजित कोशिकाएं आराम करने वाले वोल्टेज के अत्यधिक चर मान दिखाती हैं, सामान्यतः विभेदित कोशिकाओं की तुलना में काफी अधिक सकारात्मक होती हैं।[24] ऐसी कोशिकाओं में, विश्राम संभावित मूल्य विभेदन की डिग्री के साथ सहसंबंधित होता है: कुछ स्तिथियों में अविभाजित कोशिकाएं किसी भी ट्रांसमेम्ब्रेन वोल्टेज अंतर को बिल्कुल नहीं दिखा सकती हैं।
बहिर्वाहचैनलों के कारण नुकसान का मुकाबला करने के लिए आयनों के सक्रिय पंपिंग की आवश्यकता के कारण विश्राम क्षमता का रखरखाव सेल के लिए चयापचय रूप से महंगा हो सकता है। लागत सबसे अधिक होती है जब सेल फ़ंक्शन को झिल्ली वोल्टेज के विशेष रूप से विध्रुवित मूल्य की आवश्यकता होती है। उदाहरण के लिए, दिन के उजाले-अनुकूलित कैलीफोरिडे (कैलीफोरा विसिना) में आराम करने की क्षमता अकशेरूकीय में साधारण आँखें -30 mV जितनी अधिक हो सकती हैं।[25] यह उन्नत झिल्ली क्षमता कोशिकाओं को दृश्य आदानों के लिए बहुत तेजी से प्रतिक्रिया करने की अनुमति देती है; लागत यह है कि आराम करने की क्षमता का रखरखाव समग्र सेलुलर एडेनोसाइन ट्रायफ़ोस्फेट के 20% से अधिक का उपभोग कर सकता है।[26] दूसरी ओर, अविभेदित कोशिकाओं में उच्च विश्राम क्षमता के लिए आवश्यक रूप से उच्च चयापचय लागत नहीं होती है। यह स्पष्ट विरोधाभास उस विश्राम क्षमता की उत्पत्ति की जांच से हल हो गया है। छोटे-विभेदित कोशिकाओं को अत्यधिक उच्च इनपुट प्रतिरोध की विशेषता होती है,[24]जिसका तात्पर्य है कि कोशिका जीवन के इस चरण में कुछ बहिर्वाहचैनल उपस्थित हैं। स्पष्ट परिणाम के रूप में, पोटेशियम पारगम्यता सोडियम आयनों के समान हो जाती है, जो ऊपर चर्चा के अनुसार सोडियम और पोटेशियम के उलटने की क्षमता के मध्य आराम करने की क्षमता रखती है। अल्प बहिर्वाहधाराओं का तात्पर्य यह भी है कि क्षतिपूर्ति के लिए सक्रिय पम्पिंग की बहुत अल्प आवश्यकता है, इसलिए अल्प चयापचय लागत।
वर्गीकृत क्षमता
जैसा कि ऊपर बताया गया है, कोशिका की झिल्ली में किसी भी बिंदु पर क्षमता इंट्रासेल्युलर और बाह्य क्षेत्रों के मध्य आयन एकाग्रता के अंतर और प्रत्येक प्रकार के आयन के लिए झिल्ली की पारगम्यता द्वारा निर्धारित की जाती है। आयन सांद्रता सामान्य रूप से बहुत तेज़ी से नहीं बदलती (सीए के अपवाद के साथ2+, जहां बेसलाइन इंट्रासेल्युलर सांद्रता इतनी अल्प है कि परिमाण के क्रम में छोटा सा प्रवाह भी इसे बढ़ा सकता है), लेकिन आयनों की पारगम्यता मिलीसेकंड के अंश में बदल सकती है, सक्रियण के परिणामस्वरूप लिगैंड-गेटेड आयन चैनल। झिल्ली क्षमता में परिवर्तन या तो बड़ा या छोटा हो सकता है, यह इस बात पर निर्भर करता है कि कितने आयन चैनल सक्रिय हैं और वे किस प्रकार के हैं, और या तो लंबा या छोटा हो सकता है, जो चैनल के खुले रहने की अवधि पर निर्भर करता है। एक्शन पोटेंशिअल के विपरीत, इस प्रकार के परिवर्तनों को ग्रेडेड पोटेंशिअल कहा जाता है, जिनका निश्चित आयाम और समय पाठ्यक्रम होता है।
जैसा कि ऊपर दिखाए गए गोल्डमैन समीकरण से प्राप्त किया जा सकता है, झिल्ली की पारगम्यता को विशेष प्रकार के आयन में बढ़ाने का प्रभाव झिल्ली क्षमता को उस आयन के उत्क्रमण क्षमता की ओर ले जाता है। इस प्रकार, ना खोलना+ चैनल मेम्ब्रेन पोटेंशिअल को Na की ओर शिफ्ट करते हैं+ उत्क्रमण क्षमता, जो सामान्यतः +100 mV के आसपास होती है। इसी तरह, K खोलना+ चैनल झिल्ली क्षमता को लगभग -90 mV और ओपनिंग Cl की ओर स्थानांतरित करते हैं− चैनल इसे लगभग -70 mV (अधिकांश झिल्लियों की विश्राम क्षमता) की ओर स्थानांतरित करते हैं। इस प्रकार, ना+ चैनल झिल्ली क्षमता को सकारात्मक दिशा में स्थानांतरित करते हैं, K+ चैनल इसे नकारात्मक दिशा में शिफ्ट करते हैं (सिवाय तब जब झिल्ली हाइपरपोलराइज़्ड मान K से अधिक नकारात्मक हो+ उत्क्रमण क्षमता), और Cl− चैनल इसे स्थिर क्षमता की ओर ले जाते हैं।
ग्रेडेड मेम्ब्रेन पोटेंशिअल विशेष रूप से न्यूरॉन्स में महत्वपूर्ण होते हैं, जहां वे निष्कर्ष द्वारा निर्मित होते हैं - सिंगल ग्रेडेड या एक्शन पोटेंशिअल द्वारा सिनैप्स के सक्रियण द्वारा उत्पन्न मेम्ब्रेन पोटेंशिअल में अस्थायी परिवर्तन को पोस्टसिनेप्टिक क्षमता कहा जाता है। न्यूरोट्रांसमीटर जो Na खोलने का कार्य करते हैं+ चैनल सामान्यतः झिल्ली क्षमता को अधिक सकारात्मक बनाते हैं, जबकि न्यूरोट्रांसमीटर जो K को सक्रिय करते हैं+ चैनल सामान्यतः इसे और अधिक नकारात्मक बना देते हैं; जो इन चैनलों को बाधित करते हैं उनका विपरीत प्रभाव पड़ता है।
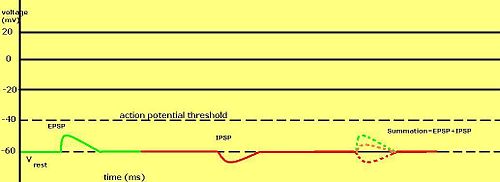
क्या पोस्टसिनेप्टिक क्षमता को उत्तेजक या निरोधात्मक माना जाता है, यह उस धारा के आयनों के लिए उत्क्रमण क्षमता पर निर्भर करता है, और सेल के लिए ऐक्शन पोटेंशिअल (लगभग -50mV) को आग लगाने की दहलीज। दहलीज से ऊपर उत्क्रमण क्षमता के साथ पोस्टसिनेप्टिक करंट, जैसे कि विशिष्ट ना+ करंट, उत्तेजक माना जाता है। दहलीज के नीचे उत्क्रमण क्षमता वाला करंट, जैसे कि विशिष्ट K+ वर्तमान, निरोधात्मक माना जाता है। रेस्टिंग पोटेंशिअल के ऊपर, लेकिन थ्रेसहोल्ड के नीचे रिवर्सल पोटेंशिअल के साथ करंट अपने आप में ऐक्शन पोटेंशिअल नहीं लाएगा, लेकिन सबथ्रेशोल्ड झिल्ली संभावित दोलन का उत्पादन करेगा। इस प्रकार, न्यूरोट्रांसमीटर जो Na को खोलने का कार्य करते हैं+ चैनल उत्तेजक पोस्टसिनेप्टिक क्षमता या ईपीएसपी उत्पन्न करते हैं, जबकि न्यूरोट्रांसमीटर जो के को खोलने का कार्य करते हैं+ या Cl− चैनल सामान्यतः निरोधात्मक पोस्टसिनेप्टिक क्षमता या IPSPs उत्पन्न करते हैं। जब ही समय अवधि के भीतर अनेक प्रकार के चैनल खुले होते हैं, तो उनकी पश्च-अन्तर्ग्रथनी क्षमताएँ योग करती हैं (एक साथ जुड़ जाती हैं)।
अन्य मूल्य
बायोफिजिक्स के दृष्टिकोण से, विश्राम झिल्ली क्षमता केवल झिल्ली क्षमता है जो कोशिका के आराम करने पर प्रबल होने वाली झिल्ली पारगम्यता से उत्पन्न होती है। भारित औसत का उपरोक्त समीकरण हमेशा प्रारम्भ होता है, लेकिन निम्नलिखित दृष्टिकोण को अधिक आसानी से देखा जा सकता है। किसी भी समय, आयन के लिए दो कारक होते हैं जो यह निर्धारित करते हैं कि कोशिका की झिल्ली क्षमता पर उस आयन का कितना प्रभाव होगा:
- वह आयन की प्रेरक शक्ति
- वह आयन की पारगम्यता
यदि चालन बल अधिक है, तो आयन को झिल्ली के आर-पार धकेला जा रहा है। यदि पारगम्यता अधिक है, तो आयन के लिए झिल्ली में फैलना आसान होगा।
- 'प्रेरक बल' उस आयन को झिल्ली के पार ले जाने के लिए उपलब्ध शुद्ध विद्युत बल है। इसकी गणना उस वोल्टेज के मध्य के अंतर के रूप में की जाती है जो आयन (इसकी संतुलन क्षमता) और वास्तविक झिल्ली क्षमता (E) पर होना चाहता है।m). अतः, औपचारिक शब्दों में, आयन के लिए प्रेरक बल = Em - औरion
- उदाहरण के लिए, -73 mV की हमारी पूर्वकी गणना की गई विश्राम क्षमता पर, पोटेशियम पर प्रेरक बल 7 mV है: (−73 mV) - (−80 mV) = 7 mV। सोडियम पर प्रेरक शक्ति (−73 mV) - (60 mV) = -133 mV होगी।
- पारगम्यता इस बात का माप है कि आयन कितनी आसानी से झिल्ली को पार कर सकता है। इसे सामान्यतः (विद्युत) चालन के रूप में मापा जाता है और इकाई, सीमेंस (इकाई), 1 C·s से मेल खाती है−1·वी-1, अर्थात कूलॉम प्रति सेकंड प्रति वोल्ट विभव।
तो, आराम करने वाली झिल्ली में, जबकि पोटेशियम के लिए प्रेरक बल अल्प होता है, इसकी पारगम्यता बहुत अधिक होती है। सोडियम के पास विशाल प्रेरणा शक्ति है लेकिन लगभग कोई विश्राम पारगम्यता नहीं है। इस स्थिति में, पोटेशियम सोडियम की तुलना में लगभग 20 गुना अधिक धारा वहन करता है, और इस प्रकार ई पर 20 गुना अधिक प्रभाव पड़ता हैm सोडियम की तुलना में।
चूँकि , और स्थिति पर विचार करें- एक्शन पोटेंशिअल का चरम। यहाँ, Na की पारगम्यता अधिक है और K की पारगम्यता अपेक्षाकृत अल्प है। इस प्रकार, झिल्ली E के पास चली जाती हैNa और ई से दूरK.
जितने अधिक आयन पारगम्य होते हैं, झिल्ली क्षमता का अनुमान लगाना उतना ही जटिल हो जाता है। चूँकि , यह गोल्डमैन समीकरण | गोल्डमैन-हॉजकिन-काट्ज़ समीकरण या भारित साधन समीकरण का उपयोग करके किया जा सकता है। समय पर किसी भी समय सांद्रता प्रवणताओं और आयनों की पारगम्यता में प्लगिंग करके, उस समय झिल्ली क्षमता का निर्धारण किया जा सकता है। GHK समीकरणों का अर्थ यह है कि किसी भी समय झिल्ली क्षमता का मान सभी पारगम्य आयनों की संतुलन क्षमता का भारित औसत होगा। भार झिल्ली के पार आयनों की सापेक्ष पारगम्यता है।
प्रभाव और निहितार्थ
जबकि कोशिकाएं आयनों के परिवहन के लिए ऊर्जा खर्च करती हैं और ट्रांसमेम्ब्रेन क्षमता स्थापित करती हैं, वे बदले में इस क्षमता का उपयोग अन्य आयनों और मेटाबोलाइट्स जैसे चीनी के परिवहन के लिए करती हैं। माइटोकॉन्ड्रियल झिल्ली की ट्रांसमेम्ब्रेन क्षमता एडेनोसिन ट्राइफॉस्फेट का उत्पादन करती है, जो जैविक ऊर्जा की सामान्य मुद्रा है।
क्रिया क्षमता या उत्तेजना के अन्य रूपों को चलाने के लिए कोशिकाएं उस ऊर्जा पर आकर्षित हो सकती हैं जिसे वे आराम करने की क्षमता में संग्रहीत करती हैं। झिल्ली क्षमता में ये परिवर्तन अन्य कोशिकाओं (एक्शन पोटेंशिअल के साथ) के साथ संचार को सक्षम करते हैं या कोशिका के अंदर परिवर्तन प्रारंभ करते हैं, जो शुक्राणु द्वारा निषेचन होने पर डिंब में होता है।
प्लाज्मा झिल्ली के ढांकता हुआ गुणों में परिवर्तन मधुमेह और डिस्लिपिडेमिया जैसी अंतर्निहित स्थितियों की पहचान के रूप में कार्य कर सकता है।[27]
न्यूरोनल कोशिकाओं में, सोडियम चैनलों के माध्यम से सेल में सोडियम आयनों की भीड़ के साथ क्रिया क्षमता प्रारंभ होती है, जिसके परिणामस्वरूप विध्रुवण होता है, जबकि पुनर्प्राप्ति में पोटेशियम चैनलों के माध्यम से पोटेशियम की बाहरी भीड़ सम्मिलित होती है। ये दोनों प्रवाह निष्क्रिय परिवहन द्वारा होते हैं।
सोडियम क्लोराइड की खुराक मांस के ताजा कट के अभी भी काम कर रहे न्यूरॉन्स को फायरिंग में ट्रिगर कर सकती है, जिससे मांसपेशियों में ऐंठन हो सकती है। <रेफ नाम = वैज्ञानिक अमेरिकी / 20110728 / तत्काल-ज़ोंबीWilcox, Christie (July 28, 2011). "इंस्टेंट जॉम्बी - बस नमक डालें।". Scientific American Blog Network (in English). Retrieved 30 January 2023.</Ref><रेफरी नाम = Sciencealert/बीफ-दालें>Crew, Bec (3 July 2015). "देखें: कसाई से घर लाए जाने के बाद कच्चे बीफ का स्लैब पल्स के रूप में दिखाई देता है". ScienceAlert. Retrieved 30 January 2023.</रेफरी>[28]<रेफरी नाम = न्यूजहब / मीट-पल्सेट>Gibson, Gray (January 11, 2023). "आम मसाला ताजा कटे हुए मांस को स्पंदित करने का कारण बनता है, भयानक ट्विटर". Newshub (in English). Retrieved 30 January 2023.</रेफरी> <रेफरी नाम = nypost/मांस की ऐंठन>Cost, Ben (10 January 2023). "बीफ ट्वर्की: ताजा मांस 'ऐंठन' के वीडियो से इंटरनेट भयभीत". nypost.com. Retrieved 30 January 2023.</रेफरी>
यह भी देखें
- बायोइलेक्ट्रोकैमिस्ट्री
- केमियोस्मोटिक क्षमता
- विद्युत रासायनिक क्षमता
- गोल्डमैन समीकरण
- मेम्ब्रेन बायोफिजिक्स
- माइक्रोइलेक्ट्रोड सरणी
- सल्तटोरी कोंडुक्ट्न
- भूतल क्षमता
- गिब्स-डोनन प्रभाव
- सिनैप्टिक क्षमता
टिप्पणियाँ
- ↑ The signs of ENa and EK are opposite. This is because the concentration gradient for potassium is directed out of the cell, while the concentration gradient for sodium is directed into the cell. Membrane potentials are defined relative to the exterior of the cell; thus, a potential of −70 mV implies that the interior of the cell is negative relative to the exterior.
संदर्भ
- ↑ Bruce, Alberts (2014-11-18). Molecular biology of the cell (Sixth ed.). New York, NY. ISBN 9780815344322. OCLC 887605755.
{{cite book}}: CS1 maint: location missing publisher (link) - ↑ Abdul Kadir, Lina; Stacey, Michael; Barrett-Jolley, Richard (2018). "Emerging Roles of the Membrane Potential: Action Beyond the Action Potential". Frontiers in Physiology (in English). 9: 1661. doi:10.3389/fphys.2018.01661. ISSN 1664-042X. PMC 6258788. PMID 30519193.
- ↑ Campbell Biology, 6th edition
- ↑ Johnston and Wu, p. 9.
- ↑ Mummert H, Gradmann D (1991). "एसिटाबुलरिया में कार्य क्षमता: वोल्टेज-गेटेड फ्लक्स का मापन और अनुकरण". Journal of Membrane Biology. 124 (3): 265–73. doi:10.1007/BF01994359. PMID 1664861. S2CID 22063907.
- ↑ Cai SQ, Li W, Sesti F (2007). "Multiple modes of a-type potassium current regulation". Curr. Pharm. Des. 13 (31): 3178–84. doi:10.2174/138161207782341286. PMID 18045167.
- ↑ Goldin AL (2007). "Neuronal Channels and Receptors". In Waxman SG (ed.). आणविक न्यूरोलॉजी. Burlington, MA: Elsevier Academic Press. pp. 43–58. ISBN 978-0-12-369509-3.
- ↑ Purves et al., pp. 28–32; Bullock, Orkand, and Grinnell, pp. 133–134; Schmidt-Nielsen, pp. 478–480, 596–597; Junge, pp. 33–35
- ↑ Sanes, Dan H.; Takács, Catherine (1993-06-01). "Activity-dependent Refinement of Inhibitory Connections". European Journal of Neuroscience (in English). 5 (6): 570–574. doi:10.1111/j.1460-9568.1993.tb00522.x. ISSN 1460-9568. PMID 8261131. S2CID 30714579.
- ↑ KOFUJI, P.; NEWMAN, E. A. (2004-01-01). "Potassium buffering in the central nervous system". Neuroscience. 129 (4): 1045–1056. doi:10.1016/j.neuroscience.2004.06.008. ISSN 0306-4522. PMC 2322935. PMID 15561419.
- ↑ Sanes, Dan H.; Reh, Thomas A (2012-01-01). Development of the nervous system (Third ed.). Elsevier Academic Press. pp. 211–214. ISBN 9780080923208. OCLC 762720374.
- ↑ Tosti, Elisabetta (2010-06-28). "Dynamic roles of ion currents in early development". Molecular Reproduction and Development. 77 (10): 856–867. doi:10.1002/mrd.21215. ISSN 1040-452X. PMID 20586098. S2CID 38314187.
- ↑ Boyet, M.R.; Jewell, B.R. (1981). "Analysis of the effects of changes in rate and rhythm upon electrical activity in the heart". Progress in Biophysics and Molecular Biology. 36 (1): 1–52. doi:10.1016/0079-6107(81)90003-1. ISSN 0079-6107. PMID 7001542.
- ↑ Spinelli, Valentina; Sartiani, Laura; Mugelli, Alessandro; Romanelli, Maria Novella; Cerbai, Elisabetta (2018). "Hyperpolarization-activated cyclic-nucleotide-gated channels: pathophysiological, developmental, and pharmacological insights into their function in cellular excitability". Canadian Journal of Physiology and Pharmacology. 96 (10): 977–984. doi:10.1139/cjpp-2018-0115. hdl:1807/90084. ISSN 0008-4212. PMID 29969572. S2CID 49679747.
- ↑ Jones, Brian L.; Smith, Stephen M. (2016-03-30). "Calcium-Sensing Receptor: A Key Target for Extracellular Calcium Signaling in Neurons". Frontiers in Physiology. 7: 116. doi:10.3389/fphys.2016.00116. ISSN 1664-042X. PMC 4811949. PMID 27065884.
- ↑ Debanne, Dominique; Inglebert, Yanis; Russier, Michaël (2019). "Plasticity of intrinsic neuronal excitability" (PDF). Current Opinion in Neurobiology (in English). 54: 73–82. doi:10.1016/j.conb.2018.09.001. PMID 30243042. S2CID 52812190.
- ↑ Davenport, Bennett; Li, Yuan; Heizer, Justin W.; Schmitz, Carsten; Perraud, Anne-Laure (2015-07-23). "Signature Channels of Excitability no More: L-Type Channels in Immune Cells". Frontiers in Immunology. 6: 375. doi:10.3389/fimmu.2015.00375. ISSN 1664-3224. PMC 4512153. PMID 26257741.
- ↑ Sakmann, Bert (2017-04-21). "From single cells and single columns to cortical networks: dendritic excitability, coincidence detection and synaptic transmission in brain slices and brains". Experimental Physiology. 102 (5): 489–521. doi:10.1113/ep085776. ISSN 0958-0670. PMC 5435930. PMID 28139019.
- ↑ Franco R, Bortner CD, Cidlowski JA (January 2006). "Potential roles of electrogenic ion transport and plasma membrane depolarization in apoptosis". J. Membr. Biol. 209 (1): 43–58. doi:10.1007/s00232-005-0837-5. PMID 16685600. S2CID 849895.
- ↑ Purves et al., pp. 32–33; Bullock, Orkand, and Grinnell, pp. 138–140; Schmidt-Nielsen, pp. 480; Junge, pp. 35–37
- ↑ Spangler SG (1972). "डाइवेलेंट और मोनोवैलेंट दोनों आयनों को शामिल करने के लिए स्थिर क्षेत्र समीकरण का विस्तार". Alabama Journal of Medical Sciences. 9 (2): 218–23. PMID 5045041.
- ↑ पूर्वेस एट अल।, पी। 34; थिओडोर होम्स बुलॉक, ऑरकांड, और ग्रिनेल, पी। 134; नट श्मिट-नीलसन | श्मिट-नीलसन, पीपी। 478–480.
- ↑ Purves et al., pp. 33–36; Bullock, Orkand, and Grinnell, p. 131.
- ↑ 24.0 24.1 Magnuson DS, Morassutti DJ, Staines WA, McBurney MW, Marshall KC (Jan 14, 1995). "In vivo electrophysiological maturation of neurons derived from a multipotent precursor (embryonal carcinoma) cell line". Developmental Brain Research. 84 (1): 130–41. doi:10.1016/0165-3806(94)00166-W. PMID 7720212.
- ↑ Juusola M, Kouvalainen E, Järvilehto M, Weckström M (Sep 1994). "Contrast gain, signal-to-noise ratio, and linearity in light-adapted blowfly photoreceptors". J Gen Physiol. 104 (3): 593–621. doi:10.1085/jgp.104.3.593. PMC 2229225. PMID 7807062.
- ↑ Laughlin SB, de Ruyter van Steveninck RR, Anderson JC (May 1998). "The metabolic cost of neural information". Nat. Neurosci. 1 (1): 36–41. doi:10.1038/236. PMID 10195106. S2CID 204995437.
- ↑ Ghoshal K, et al. (December 2017). "Dielectric properties of plasma membrane: A signature for dyslipidemia in diabetes mellitus". Arch Biochem Biophys. 635: 27–36. doi:10.1016/j.abb.2017.10.002. PMID 29029878.
- ↑ "女子切". legal.people.com.cn. Archived from the original on 3 July 2015. Retrieved 30 January 2023.
अग्रिम पठन
- Alberts et al. Molecular Biology of the Cell. Garland Publishing; 4th Bk&Cdr edition (March, 2002). ISBN 0-8153-3218-1. Undergraduate level.
- Guyton, Arthur C., John E. Hall. Textbook of medical physiology. W.B. Saunders Company; 10th edition (August 15, 2000). ISBN 0-7216-8677-X. Undergraduate level.
- Hille, B. Ionic Channel of Excitable Membranes Sinauer Associates, Sunderland, MA, USA; 1st Edition, 1984. ISBN 0-87893-322-0
- Nicholls, J.G., Martin, A.R. and Wallace, B.G. From Neuron to Brain Sinauer Associates, Inc. Sunderland, MA, USA 3rd Edition, 1992. ISBN 0-87893-580-0
- Ove-Sten Knudsen. Biological Membranes: Theory of Transport, Potentials and Electric Impulses. Cambridge University Press (September 26, 2002). ISBN 0-521-81018-3. Graduate level.
- National Medical Series for Independent Study. Physiology. Lippincott Williams & Wilkins. Philadelphia, PA, USA 4th Edition, 2001. ISBN 0-683-30603-0