पॉलीट्रोपिक प्रक्रिया: Difference between revisions
No edit summary |
No edit summary |
||
| Line 2: | Line 2: | ||
{{Redirect|पॉलीट्रोपिक|वायरस में पॉलीट्रोपिज्म|एम्फोट्रोपिज्म}} | {{Redirect|पॉलीट्रोपिक|वायरस में पॉलीट्रोपिज्म|एम्फोट्रोपिज्म}} | ||
{{Thermodynamics sidebar|cTopic=[[ | {{Thermodynamics sidebar|cTopic=[[थर्मोडायनामिक सिस्टम|सिस्टमस]]}} | ||
एक पॉलीट्रॉपिक प्रक्रिया एक [[थर्मोडायनामिक प्रक्रिया]] है जो संबंध का पालन करती है: | एक पॉलीट्रॉपिक प्रक्रिया एक [[थर्मोडायनामिक प्रक्रिया]] है जो संबंध का पालन करती है: | ||
<math display="block">p V^{n} = C</math> | <math display="block">p V^{n} = C</math> | ||
जहाँ p दाब है, V [[आयतन]] है, n 'पॉलीट्रोपिक तालिका ' है, और C एक स्थिरांक है। पॉलीट्रोपिक प्रक्रिया समीकरण विस्तार और संपीड़न प्रक्रियाओं का वर्णन करता है जिसमें ऊष्मा स्थानांतरण | जहाँ p दाब है, V [[आयतन]] है, n 'पॉलीट्रोपिक तालिका ' है, और C एक स्थिरांक है। पॉलीट्रोपिक प्रक्रिया समीकरण विस्तार और संपीड़न प्रक्रियाओं का वर्णन करता है जिसमें ऊष्मा स्थानांतरण संम्मिलित है। | ||
== विशेष स्थितियां == | == विशेष स्थितियां == | ||
| Line 18: | Line 18: | ||
== पॉलीट्रोपिक गुणांक और ऊर्जा स्थानांतरण के अनुपात के बीच समानता == | == पॉलीट्रोपिक गुणांक और ऊर्जा स्थानांतरण के अनुपात के बीच समानता == | ||
[[File:Polytropic.gif|thumbnail|पॉलीट्रॉपिक प्रक्रियाएं विभिन्न पॉलीट्रॉपिकतालिका के साथ अलग-अलग व्यवहार करती हैं। एक पॉलीट्रॉपिक प्रक्रिया अन्य बुनियादी थर्मोडायनामिक प्रक्रियाओं को उत्पन्न कर सकती है।]][[गतिज ऊर्जा]] और [[संभावित ऊर्जा|स्थितिज ऊर्जा]] में नगण्य परिवर्तन के साथ एक | [[File:Polytropic.gif|thumbnail|पॉलीट्रॉपिक प्रक्रियाएं विभिन्न पॉलीट्रॉपिकतालिका के साथ अलग-अलग व्यवहार करती हैं। एक पॉलीट्रॉपिक प्रक्रिया अन्य बुनियादी थर्मोडायनामिक प्रक्रियाओं को उत्पन्न कर सकती है।]][[गतिज ऊर्जा]] और [[संभावित ऊर्जा|स्थितिज ऊर्जा]] में नगण्य परिवर्तन के साथ एक मंद प्रक्रिया से घटित होने वाली एक संवृत [[बंद प्रणाली|प्रणाली]] में एक [[आदर्श गैस]] के लिए पॉलीट्रोपिक प्रक्रिया है, जैसे कि | ||
<math display="block">p v^{(1- \gamma)K + \gamma} = C</math> | <math display="block">p v^{(1- \gamma)K + \gamma} = C</math> | ||
जहां ''C'' स्थिर है, <math>K = \frac{\delta q}{\delta w}</math>, <math>\gamma = \frac{c_p}{c_v}</math>, और पॉलीट्रोपिक गुणांक के साथ <math>n={(1- \gamma)K + \gamma}</math>. | जहां ''C'' स्थिर है, <math>K = \frac{\delta q}{\delta w}</math>, <math>\gamma = \frac{c_p}{c_v}</math>, और पॉलीट्रोपिक गुणांक के साथ <math>n={(1- \gamma)K + \gamma}</math>. | ||
| Line 33: | Line 33: | ||
|style="text-align:center"|''n'' < 0 | |style="text-align:center"|''n'' < 0 | ||
|style="text-align:center"|— | |style="text-align:center"|— | ||
|नकारात्मक घातांक एक ऐसी प्रक्रिया को दर्शाते हैं जहां कार्य और ऊष्मा एक साथ सिस्टम के अंदर या बाहर प्रवाहित होते हैं. n दबाव के अतिरिक्त अन्य बलों की अनुपस्थिति, उष्मागतिकी के दूसरे नियम द्वारा ऐसी सहज प्रक्रिया की अनुमति नहीं है; चूँकि, नकारात्मक घातांक कुछ विशेष स्थितियों में सार्थक हो सकते हैं जो थर्मल इंटरैक्शन से प्रभावित नहीं होते हैं, [[astrophysics|जैसे खगोल भौतिकी में कुछ प्लास्मा की प्रक्रियाओं में]],<ref>{{cite book |first=G. P. |last=Horedt |url=https://books.google.com/books?id=vXhFjGj5PjIC&q=polytropic+with+negative+exponent&pg=PA24 |title=Polytropes: Applications in Astrophysics and Related Fields |publisher=Springer |date=2004-08-10 |page=24}}</ref> या यदि प्रक्रिया की स्थिति ऊर्जा के अन्य रूप (जैसे रासायनिक ऊर्जा) | |नकारात्मक घातांक एक ऐसी प्रक्रिया को दर्शाते हैं जहां कार्य और ऊष्मा एक साथ सिस्टम के अंदर या बाहर प्रवाहित होते हैं. n दबाव के अतिरिक्त अन्य बलों की अनुपस्थिति, उष्मागतिकी के दूसरे नियम द्वारा ऐसी सहज प्रक्रिया की अनुमति नहीं है; चूँकि, नकारात्मक घातांक कुछ विशेष स्थितियों में सार्थक हो सकते हैं जो थर्मल इंटरैक्शन से प्रभावित नहीं होते हैं, [[astrophysics|जैसे खगोल भौतिकी में कुछ प्लास्मा की प्रक्रियाओं में]],<ref>{{cite book |first=G. P. |last=Horedt |url=https://books.google.com/books?id=vXhFjGj5PjIC&q=polytropic+with+negative+exponent&pg=PA24 |title=Polytropes: Applications in Astrophysics and Related Fields |publisher=Springer |date=2004-08-10 |page=24}}</ref> या यदि प्रक्रिया की स्थिति ऊर्जा के अन्य रूप (जैसे रासायनिक ऊर्जा) संम्मिलित हैं (जैसे विस्फोट)। | ||
|- | |- | ||
|style="text-align:center"|''n'' = 0 | |style="text-align:center"|''n'' = 0 | ||
| Line 45: | Line 45: | ||
|style="text-align:center"|1 < ''n'' < ''γ'' | |style="text-align:center"|1 < ''n'' < ''γ'' | ||
|style="text-align:center"|— | |style="text-align:center"|— | ||
|आदर्श गैस नियम की धारणा के अनुसार, ऊष्मा और कार्य प्रवाह विपरीत दिशाओं में चलते हैं (''K'' > 0), जैसे वाष्प संपीड़न प्रशीतन में संपीड़न के स्थिति, जहां वाष्प पर कंप्रेसर द्वारा किए गए कार्य के परिणामस्वरूप बढ़े हुए वाष्प तापमान से वाष्प से आसपास के | |आदर्श गैस नियम की धारणा के अनुसार, ऊष्मा और कार्य प्रवाह विपरीत दिशाओं में चलते हैं (''K'' > 0), जैसे वाष्प संपीड़न प्रशीतन में संपीड़न के स्थिति, जहां वाष्प पर कंप्रेसर द्वारा किए गए कार्य के परिणामस्वरूप बढ़े हुए वाष्प तापमान से वाष्प से आसपास के शीत वातावरण में कुछ उष्मा की हानि होती है। | ||
|- | |- | ||
|style="text-align:center"|''n'' = ''γ'' | |style="text-align:center"|''n'' = ''γ'' | ||
| Line 53: | Line 53: | ||
|style="text-align:center"|''γ'' < ''n'' < ∞ | |style="text-align:center"|''γ'' < ''n'' < ∞ | ||
|style="text-align:center"|— | |style="text-align:center"|— | ||
|आदर्श गैस नियम की मान्यता के अंतर्गत ऊष्मा और कार्य प्रवाह एक ही दिशा में चलते हैं (''K'' < 0), जैसे पावर स्ट्रोक के स्थिति आंतरिक दहन इंजन में, जहां उष्मा दहन उत्पादों से उष्मा खो जाती है, सिलेंडर की दीवारों के माध्यम से, | |आदर्श गैस नियम की मान्यता के अंतर्गत ऊष्मा और कार्य प्रवाह एक ही दिशा में चलते हैं (''K'' < 0), जैसे पावर स्ट्रोक के स्थिति आंतरिक दहन इंजन में, जहां उष्मा दहन उत्पादों से उष्मा खो जाती है, सिलेंडर की दीवारों के माध्यम से, शीत वातावरण में, उसी समय जब वे उष्मा दहन उत्पाद पिस्टन पर धकेलते हैं. | ||
|- | |- | ||
|style="text-align:center"|''n'' = +∞ | |style="text-align:center"|''n'' = +∞ | ||
Revision as of 14:08, 20 March 2023
| थर्मोडायनामिक्स |
|---|
 |
एक पॉलीट्रॉपिक प्रक्रिया एक थर्मोडायनामिक प्रक्रिया है जो संबंध का पालन करती है:
विशेष स्थितियां
n के कुछ विशिष्ट मूल्य विशेष स्थितियों के अनुरूप हैं:
- समदाब रेखीय प्रक्रिया के लिए,
- एक आइसोकोरिक प्रक्रिया के लिए।
इसके अतिरिक्त, जब आदर्श गैस नियम लागू होता है:
- एक समतापी प्रक्रिया के लिए,
- एक आइसेंट्रोपिक प्रक्रिया के लिए।
जहाँ स्थिर दबाव पर ताप क्षमता का अनुपात है () स्थिर आयतन पर क्षमता को गर्म करने के लिए ().
पॉलीट्रोपिक गुणांक और ऊर्जा स्थानांतरण के अनुपात के बीच समानता
गतिज ऊर्जा और स्थितिज ऊर्जा में नगण्य परिवर्तन के साथ एक मंद प्रक्रिया से घटित होने वाली एक संवृत प्रणाली में एक आदर्श गैस के लिए पॉलीट्रोपिक प्रक्रिया है, जैसे कि
आदर्श प्रक्रियाओं से संबंध
पॉलीट्रोपिक तालिका के कुछ मूल्यों के लिए, प्रक्रिया अन्य सामान्य प्रक्रियाओं का पर्याय बन जाएगी। विभिन्न सूचकांक मूल्यों के प्रभावों के कुछ उदाहरण निम्न तालिका में दिए गए हैं।
| पॉलीट्रॉपिक तालिका |
संबंध | प्रभाव |
|---|---|---|
| n < 0 | — | नकारात्मक घातांक एक ऐसी प्रक्रिया को दर्शाते हैं जहां कार्य और ऊष्मा एक साथ सिस्टम के अंदर या बाहर प्रवाहित होते हैं. n दबाव के अतिरिक्त अन्य बलों की अनुपस्थिति, उष्मागतिकी के दूसरे नियम द्वारा ऐसी सहज प्रक्रिया की अनुमति नहीं है; चूँकि, नकारात्मक घातांक कुछ विशेष स्थितियों में सार्थक हो सकते हैं जो थर्मल इंटरैक्शन से प्रभावित नहीं होते हैं, जैसे खगोल भौतिकी में कुछ प्लास्मा की प्रक्रियाओं में,[1] या यदि प्रक्रिया की स्थिति ऊर्जा के अन्य रूप (जैसे रासायनिक ऊर्जा) संम्मिलित हैं (जैसे विस्फोट)। |
| n = 0 | एक आइसोबैरिक प्रक्रिया के समान (स्थिर दबाव) | |
| n = 1 | तब से आदर्श गैस नियम की धारणा के अनुसार, एक आइसोथर्मल प्रक्रिया (स्थिर तापमान) के समान . | |
| 1 < n < γ | — | आदर्श गैस नियम की धारणा के अनुसार, ऊष्मा और कार्य प्रवाह विपरीत दिशाओं में चलते हैं (K > 0), जैसे वाष्प संपीड़न प्रशीतन में संपीड़न के स्थिति, जहां वाष्प पर कंप्रेसर द्वारा किए गए कार्य के परिणामस्वरूप बढ़े हुए वाष्प तापमान से वाष्प से आसपास के शीत वातावरण में कुछ उष्मा की हानि होती है। |
| n = γ | — | आदर्श गैस कानून की धारणा के अनुसार एक आइसेंट्रोपिक प्रक्रिया (स्थिरोष्म और प्रतिवर्ती, ना उष्मा स्थानान्तरण) के समान. |
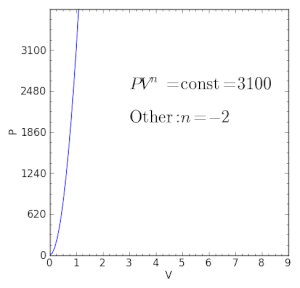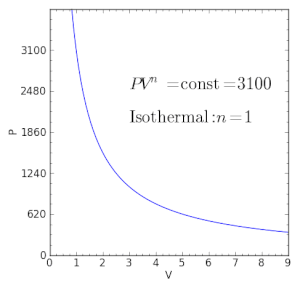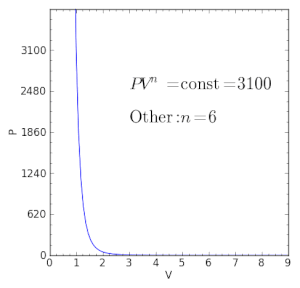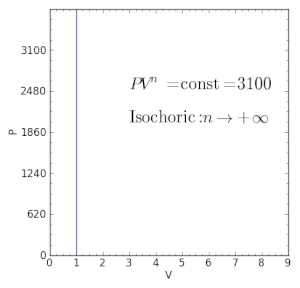
| γ < n < ∞ | — | आदर्श गैस नियम की मान्यता के अंतर्गत ऊष्मा और कार्य प्रवाह एक ही दिशा में चलते हैं (K < 0), जैसे पावर स्ट्रोक के स्थिति आंतरिक दहन इंजन में, जहां उष्मा दहन उत्पादों से उष्मा खो जाती है, सिलेंडर की दीवारों के माध्यम से, शीत वातावरण में, उसी समय जब वे उष्मा दहन उत्पाद पिस्टन पर धकेलते हैं. |
| n = +∞ | एक आइसोकोरिक प्रक्रिया के समान (स्थिर आयतन) |
जब तालिका n पूर्व मानों (0, 1, γ, या ∞) में से किसी दो के बीच होता है, तो इसका अर्थ है कि पॉलीट्रॉपिक वक्र दो बाध्यकारी सूचकांकों के घटता (द्वारा परिबद्ध होना) के माध्यम से कम हो जाएगा।
एक आदर्श गैस के लिए, 1 < γ < 5/3, चूंकि मेयर के वर्णन से
अन्य
पॉलीट्रॉपिक तरल पदार्थ का उपयोग करके लेन-एम्डेन समीकरण का समाधान एक पॉलीट्रॉप के रूप में जाना जाता है।
यह भी देखें
- एडियाबेटिक प्रक्रिया
- कंप्रेसर
- आंतरिक दहन इंजन
- आइसेंट्रोपिक प्रक्रिया
- आइसोबैरिक प्रक्रिया
- आइसोकोरिक प्रक्रिया
- इज़ोटेर्मल प्रक्रिया
- पॉलीट्रोप
- क्वासिस्टैटिक संतुलन
- ऊष्मप्रवैगिकी
- वाष्प-संपीड़न प्रशीतन
संदर्भ
- ↑ Horedt, G. P. (2004-08-10). Polytropes: Applications in Astrophysics and Related Fields. Springer. p. 24.