क्लोरीन उत्पादन: Difference between revisions
No edit summary |
No edit summary |
||
| (9 intermediate revisions by 3 users not shown) | |||
| Line 1: | Line 1: | ||
[[सोडियम क्लोराइड]] घोल ([[नमकीन]]) और अन्य विधियों के [[इलेक्ट्रोलीज़]] सहित प्राकृतिक पदार्थों से निकालने से [[क्लोरीन]] गैस का उत्पादन किया जा सकता है। | [[सोडियम क्लोराइड]] घोल ([[नमकीन|ब्राइन]]) और अन्य विधियों के [[इलेक्ट्रोलीज़]] सहित प्राकृतिक पदार्थों से निकालने से [[क्लोरीन]] गैस का उत्पादन किया जा सकता है। | ||
== गैस निष्कर्षण == | == गैस निष्कर्षण == | ||
क्लोरीन को सोडियम क्लोराइड घोल ( | क्लोरीन को सोडियम क्लोराइड घोल (ब्राइन) के इलेक्ट्रोलिसिस द्वारा निर्मित किया जा सकता है, जिसे क्लोराल्कली प्रक्रिया के रूप में जाना जाता है। क्लोरीन के उत्पादन से सह-उत्पाद [[कटू सोडियम|कास्टिक सोडा]] ([[सोडियम हाइड्रॉक्साइड]], NaOH) और [[हाइड्रोजन]] गैस (H<sub>2</sub>) बनते हैं। ये दो उत्पाद, साथ ही क्लोरीन भी अत्यधिक प्रतिक्रियाशील हैं। [[पोटेशियम क्लोराइड]] के घोल के इलेक्ट्रोलिसिस द्वारा क्लोरीन का उत्पादन भी किया जा सकता है, इस स्थिति में सह-उत्पाद हाइड्रोजन और कास्टिक पोटाश ([[पोटेशियम हाइड्रोक्साइड]]) हैं। क्लोराइड विलयनों के इलेक्ट्रोलिसिस द्वारा क्लोरीन के निष्कर्षण के लिए तीन औद्योगिक विधियाँ हैं, जो निम्नलिखित समीकरणों के अनुसार आगे बढ़ती हैं: | ||
: कैथोड: 2 H<sup>+</sup> (aq) + 2 e<sup>−</sup> → H<sub>2</sub> (g) | : कैथोड: 2 H<sup>+</sup> (aq) + 2 e<sup>−</sup> → H<sub>2</sub> (g) | ||
: एनोड: | : एनोड: 2 Cl<sup>−</sup> (aq) → Cl<sub>2</sub> (g) + 2 e<sup>−</sup> | ||
समग्र प्रक्रिया: 2 NaCl (or KCl) + 2 H<sub>2</sub>O → Cl<sub>2</sub> + H<sub>2</sub> + 2 NaOH (or KOH) | समग्र प्रक्रिया: 2 NaCl (or KCl) + 2 H<sub>2</sub>O → Cl<sub>2</sub> + H<sub>2</sub> + 2 NaOH (or KOH) | ||
=== पारा सेल इलेक्ट्रोलिसिस === | === पारा सेल इलेक्ट्रोलिसिस === | ||
[[Image:HgNaOHElectrolysis.png|thumb|400px|right|कास्टनर-केलनर सेल: साइड सेल में A एनोड और M मरकरी कैथोड के बीच सोडियम क्लोराइड का इलेक्ट्रोलाइज़ किया जाता है, जिसमें NaCl के ऊपर अंतरिक्ष में क्लोरीन बुदबुदाती है और पारा में सोडियम घुल जाता है। सोडियम-मर्करी अमलगम केंद्र | [[Image:HgNaOHElectrolysis.png|thumb|400px|right|कास्टनर-केलनर सेल: साइड सेल में A एनोड और M मरकरी कैथोड के बीच सोडियम क्लोराइड का इलेक्ट्रोलाइज़ किया जाता है, जिसमें NaCl के ऊपर अंतरिक्ष में क्लोरीन बुदबुदाती है और पारा में सोडियम घुल जाता है। सोडियम-मर्करी अमलगम केंद्र सेल में प्रवाहित होता है, जहां यह जल के साथ प्रतिक्रिया करके सोडियम हाइड्रॉक्साइड का उत्पादन करता है और पारा को पुन: उत्पन्न करता है।]][[पारा (तत्व)]] सेल इलेक्ट्रोलिसिस, जिसे कास्टनर-केलनर प्रक्रिया के रूप में भी जाना जाता है, औद्योगिक पैमाने पर क्लोरीन का उत्पादन करने के लिए उन्नीसवीं शताब्दी के अंत में उपयोग की जाने वाली पहली विधि थी।<ref name="pauling">Pauling, Linus, ''General Chemistry'', 1970 ed., Dover publications</ref><ref name="lenn2">{{cite web|accessdate=2007-03-17|title=क्लोरीन और कास्टिक सोडा के लिए इलेक्ट्रोलाइटिक प्रक्रियाएं|url=http://www.lenntech.com/Chemistry/electolytic-chlorine-caustic.htm|publisher=Lenntech Water treatment & air purification Holding B.V., Rotterdamseweg 402 M, 2629 HH Delft, The Netherlands}}</ref> उपयोग की जाने वाली रॉकिंग सेलों में वर्षों से संशोधन किया गया है।<ref name="Euro Chlor2">{{cite web |url=http://www.eurochlor.org/animations/mercury-cell.asp |title=बुध कोशिका|publisher=Euro Chlor |accessdate=2007-08-15 |url-status=dead |archiveurl=https://web.archive.org/web/20110918011944/http://www.eurochlor.org/animations/mercury-cell.asp |archivedate=2011-09-18 }}</ref> आज, प्राथमिक सेल में, [[प्लैटिनम]] के साथ [[टाइटेनियम]] एनोड पहने हुए हैं<ref name="Land1972">{{cite journal |title=प्लैटिनीकृत टाइटेनियम पर एनोडिक क्लोरेट का निर्माण|author=Landolt, D. |author2=Ibl, N. |journal=Journal of Applied Electrochemistry |volume=2 |issue=3 |year=1972 |pages=201–210 |publisher=Chapman and Hall Ltd. |doi=10.1007/BF02354977}}</ref> या [[मिश्रित धातु ऑक्साइड इलेक्ट्रोड]] (पूर्व में [[ग्रेफाइट]] [[एनोड]]) को तरल पारा [[कैथोड]] पर बहने वाले [[सोडियम]] (या [[पोटैशियम]]) क्लोराइड घोल में रखा जाता है। जब संभावित अंतर प्रयुक्त किया जाता है और धारा प्रवाहित होती है, तो टाइटेनियम एनोड पर क्लोरीन छोड़ा जाता है और सोडियम (या पोटेशियम) पारा कैथोड में घुलकर अमलगम (रसायन) बनाता है। यह अलग रिएक्टर (डेनुडर या द्वितीयक सेल) में निरंतर प्रवाहित होता है, जहां यह सामान्यतः [[पानी|जल]] के साथ प्रतिक्रिया करके पारा में परिवर्तित हो जाता है, व्यावसायिक रूप से उपयोगी एकाग्रता (भार से 50%) पर हाइड्रोजन और सोडियम (या पोटेशियम) [[ हीड्राकसीड |हीड्राकसीड]] का उत्पादन करता है। पारा फिर नीचे स्थित पंप द्वारा प्राथमिक सेल में पुनर्नवीनीकरण किया जाता है। | ||
पारा प्रक्रिया तीन मुख्य प्रौद्योगिकियों (पारा, [[डायाफ्राम (यांत्रिक उपकरण)]] और मेम्ब्रेन (चयनात्मक बाधा)) में सबसे कम ऊर्जा कुशल है और पारा [[प्रदूषण]] के बारे में भी | पारा प्रक्रिया तीन मुख्य प्रौद्योगिकियों (पारा, [[डायाफ्राम (यांत्रिक उपकरण)]] और मेम्ब्रेन (चयनात्मक बाधा)) में सबसे कम ऊर्जा कुशल है और पारा [[प्रदूषण]] के बारे में भी चिंताजनक हैं। | ||
अनुमान है कि विश्व भर में अभी भी लगभग 100 मरकरी-सेल संयंत्र काम कर रहे हैं। [[जापान]] में, पारा-आधारित क्लोराल्कली का उत्पादन वस्तुतः 1987 तक समाप्त हो गया था (2003 में बंद अंतिम दो पोटेशियम क्लोराइड इकाइयों को छोड़कर)। [[संयुक्त राज्य अमेरिका]] में, 2008 के अंत तक केवल पांच मरकरी संयंत्र परिचालन में शेष रहेंगे। [[यूरोप]] में, 2006 में पारा सेलों की क्षमता का 43% हिस्सा था और पश्चिमी यूरोपीय उत्पादकों ने शेष सभी क्लोरअल्कली पारा संयंत्रों को बंद करने या परिवर्तित करने के लिए प्रतिबद्ध किया है। | अनुमान है कि विश्व भर में अभी भी लगभग 100 मरकरी-सेल संयंत्र काम कर रहे हैं। [[जापान]] में, पारा-आधारित क्लोराल्कली का उत्पादन वस्तुतः 1987 तक समाप्त हो गया था (2003 में बंद अंतिम दो पोटेशियम क्लोराइड इकाइयों को छोड़कर)। [[संयुक्त राज्य अमेरिका]] में, 2008 के अंत तक केवल पांच मरकरी संयंत्र परिचालन में शेष रहेंगे। [[यूरोप]] में, 2006 में पारा सेलों की क्षमता का 43% हिस्सा था और पश्चिमी यूरोपीय उत्पादकों ने 2020 तक शेष सभी क्लोरअल्कली पारा संयंत्रों को बंद करने या परिवर्तित करने के लिए प्रतिबद्ध किया है।<ref name="unep">{{cite web|url=http://www.chem.unep.ch/Mercury/Pretoria-proceedings-finalPDFwriter.pdf|title=पारा प्रदूषण पर क्षेत्रीय जागरूकता बढ़ाने की कार्यशाला|publisher=UNEP|accessdate=2007-10-28|archive-url=https://web.archive.org/web/20071029014335/http://www.chem.unep.ch/Mercury/Pretoria-proceedings-finalPDFwriter.pdf|archive-date=2007-10-29|url-status=dead}}</ref> | ||
=== डायाफ्राम सेल इलेक्ट्रोलिसिस (द्विध्रुवीय) === | === डायाफ्राम सेल इलेक्ट्रोलिसिस (द्विध्रुवीय) === | ||
डायाफ्राम सेल इलेक्ट्रोलिसिस में, | डायाफ्राम सेल इलेक्ट्रोलिसिस में, [[अदह|एस्बेस्टस]] (या बहुलक-फाइबर) डायाफ्राम कैथोड और एनोड को अलग करता है, जो एनोड पर बनने वाले क्लोरीन को सोडियम हाइड्रॉक्साइड और कैथोड पर बनने वाले हाइड्रोजन के साथ फिर से मिलाने से रोकता है।<ref name="Euro Chlor3">{{cite web|url=http://www.eurochlor.org/animations/diaphragm-cell.asp|title=डायाफ्राम सेल|publisher=Euro Chlor|accessdate=2007-08-15|archive-url=https://web.archive.org/web/20070927011835/http://www.eurochlor.org/animations/diaphragm-cell.asp|archive-date=2007-09-27|url-status=dead}}</ref> इस विधि का विकास भी उन्नीसवीं शताब्दी के अंत में हुआ था। इस प्रक्रिया के कई रूप ले सुयूर सेल (1893), हारग्रेव्स-बर्ड सेल (1901), गिब्स सेल (1908) और टाउनसेंड सेल (1904) हैं।<ref name="saltman">{{cite web |url=http://www.saltsense.co.uk/hist-chem12.htm |title=ब्राइन का इलेक्ट्रोलिसिस|publisher=Salt Manufacturers' Association |accessdate=2007-03-17 |url-status=dead |archiveurl=https://web.archive.org/web/20070514034157/http://www.saltsense.co.uk/hist-chem12.htm |archivedate=2007-05-14 }}</ref><ref name="kiefer">{{cite web|url=http://pubs.acs.org/subscribe/journals/tcaw/11/i04/html/04chemistry.html|title=जब उद्योग ने आगे चार्ज किया|publisher=Chemistry Chronicles|first=David M.|last=Kiefer|accessdate=2007-03-17}}</ref> सेल डायफ्राम के निर्माण और प्लेसमेंट में भिन्न होती हैं, कुछ में डायफ्राम कैथोड के सीधे संपर्क में होता है। | ||
[[नमक]] का घोल निरंतर एनोड डिब्बे में डाला जाता है और डायाफ्राम के माध्यम से कैथोड डिब्बे में प्रवाहित होता है, जहां सं[[क्षार]]क पदार्थ क्षार का उत्पादन होता है और | [[नमक]] का घोल निरंतर एनोड डिब्बे में डाला जाता है और डायाफ्राम के माध्यम से कैथोड डिब्बे में प्रवाहित होता है, जहां सं[[क्षार]]क पदार्थ क्षार का उत्पादन होता है और ब्राइन आंशिक रूप से समाप्त हो जाता है। परिणामस्वरूप, डायाफ्राम विधियाँ क्षार का उत्पादन करती हैं, जो पारा सेल विधियों की तुलना में अत्यधिक पतला (लगभग 12%) और कम शुद्धता वाला होता है। | ||
पर्यावरण में पारे के निर्वहन को रोकने की समस्या से डायाफ्राम सेल बोझिल नहीं होती हैं; वे कम [[वोल्टेज]] पर भी काम करते हैं, जिसके परिणामस्वरूप पारा सेल पद्धति पर ऊर्जा की बचत होती है,<ref name="kiefer"/>लेकिन बड़ी मात्रा में [[भाप]] की आवश्यकता होती है यदि कास्टिक को 50% की व्यावसायिक सांद्रता तक वाष्पित करना है। | पर्यावरण में पारे के निर्वहन को रोकने की समस्या से डायाफ्राम सेल बोझिल नहीं होती हैं; वे कम [[वोल्टेज]] पर भी काम करते हैं, जिसके परिणामस्वरूप पारा सेल पद्धति पर ऊर्जा की बचत होती है,<ref name="kiefer"/> लेकिन बड़ी मात्रा में [[भाप]] की आवश्यकता होती है यदि कास्टिक को 50% की व्यावसायिक सांद्रता तक वाष्पित करना है। | ||
=== मेम्ब्रेन सेल इलेक्ट्रोलिसिस === | === मेम्ब्रेन सेल इलेक्ट्रोलिसिस === | ||
इस | इस विधि का विकास 1970 के दशक में प्रारंभ हुआ था। इलेक्ट्रोलिसिस सेल को [[कटियन]] पारगम्यता (इलेक्ट्रोमैग्नेटिज्म) मेम्ब्रेन द्वारा दो वर्गों में विभाजित किया जाता है जो [[कटियन एक्सचेंज|कटियन एक्सचेंजर]] के रूप में कार्य करता है। संतृप्त सोडियम (या पोटेशियम) क्लोराइड घोल को एनोड डिब्बे से निकाला जाता है, जिससे कम सांद्रता निकलती है।<ref name="Euro Chlor4">{{cite web|url=http://www.eurochlor.org/animations/membrane-cell.asp|title=झिल्ली कोशिका|publisher=Euro Chlor|accessdate=2007-08-15|archive-url=https://web.archive.org/web/20070814075109/http://www.eurochlor.org/animations/membrane-cell.asp|archive-date=2007-08-14|url-status=dead}}</ref> सोडियम (या पोटेशियम) हाइड्रॉक्साइड घोल कैथोड डिब्बे के माध्यम से परिचालित होता है, जो उच्च सांद्रता से बाहर निकलता है। सान्द्र सोडियम हाइड्रॉक्साइड विलयन का एक भाग जो सेल को छोड़ता है, उत्पाद के रूप में विपथित किया जाता है, जबकि शेष विआयनीकृत जल से तनुकृत किया जाता है और पुन: विद्युत अपघटन तंत्र से निकाला जाता है। | ||
यह विधि डायाफ्राम सेल की तुलना में अधिक कुशल है और लगभग 32% सांद्रता पर बहुत शुद्ध सोडियम (या पोटेशियम) हाइड्रॉक्साइड का उत्पादन करती है, लेकिन इसके लिए बहुत शुद्ध | यह विधि डायाफ्राम सेल की तुलना में अधिक कुशल है और लगभग 32% सांद्रता पर बहुत शुद्ध सोडियम (या पोटेशियम) हाइड्रॉक्साइड का उत्पादन करती है, लेकिन इसके लिए बहुत शुद्ध ब्राइन की आवश्यकता होती है। | ||
[[File:Chloralkali membrane.svg|center|600px|thumb|क्लोराल्कली उत्पादन के लिए मेम्ब्रेन सेल प्रक्रिया]] | [[File:Chloralkali membrane.svg|center|600px|thumb|क्लोराल्कली उत्पादन के लिए मेम्ब्रेन सेल प्रक्रिया]] | ||
=== अन्य इलेक्ट्रोलाइटिक प्रक्रियाएं === | === अन्य इलेक्ट्रोलाइटिक प्रक्रियाएं === | ||
यद्यपि बहुत कम उत्पादन पैमाने सम्मिलित है, इलेक्ट्रोलाइटिक डायाफ्राम और | यद्यपि बहुत कम उत्पादन पैमाने सम्मिलित है, इलेक्ट्रोलाइटिक डायाफ्राम और मेम्ब्रेन प्रौद्योगिकियों का उपयोग औद्योगिक रूप से [[हाइड्रोक्लोरिक एसिड]] घोलों से क्लोरीन को पुनर्प्राप्त करने के लिए किया जाता है, जो सह-उत्पाद के रूप में हाइड्रोजन (लेकिन कोई कास्टिक क्षार नहीं) का उत्पादन करता है। | ||
इसके | इसके अतिरिक्त, फ्यूज्ड क्लोराइड लवण ([[डाउन्स सेल]]) का इलेक्ट्रोलिसिस भी क्लोरीन का उत्पादन करने में सक्षम बनाता है, इस स्थिति में [[धातु]] सोडियम या [[मैगनीशियम]] के निर्माण के उप-उत्पाद के रूप में क्लोरीन का उत्पादन करने में सक्षम बनाता है। | ||
== अन्य | == अन्य विधियां == | ||
क्लोरीन उत्पादन के लिए इलेक्ट्रोलाइटिक विधियों का उपयोग करने से पहले, डीकॉन प्रक्रिया में [[ऑक्सीजन]] के साथ [[हाइड्रोजन क्लोराइड]] का प्रत्यक्ष [[ऑक्सीकरण]] (अधिकांशतः हवा के संपर्क में आने के माध्यम से) किया जाता था: | क्लोरीन उत्पादन के लिए इलेक्ट्रोलाइटिक विधियों का उपयोग करने से पहले, डीकॉन प्रक्रिया में [[ऑक्सीजन]] के साथ [[हाइड्रोजन क्लोराइड]] का प्रत्यक्ष [[ऑक्सीकरण]] (अधिकांशतः हवा के संपर्क में आने के माध्यम से) किया जाता था: | ||
:: 4 HCl + O<sub>2</sub> → 2 Cl<sub>2</sub> + 2 H<sub>2</sub>O | :: 4 HCl + O<sub>2</sub> → 2 Cl<sub>2</sub> + 2 H<sub>2</sub>O | ||
यह प्रतिक्रिया कॉपर (II) क्लोराइड (CuCl<sub>2</sub>) | यह प्रतिक्रिया कॉपर (II) क्लोराइड (CuCl<sub>2</sub>) [[उत्प्रेरक]] के रूप में और उच्च तापमान (लगभग 400 °C) पर किया जाता है। निकाले गए क्लोरीन की मात्रा लगभग 80% है। अत्यधिक संक्षारक प्रतिक्रिया मिश्रण के कारण, इस पद्धति का औद्योगिक उपयोग कठिन है और अतीत में कई प्रायोगिक परीक्षण विफल रहे हैं। फिर भी, हाल के घटनाक्रम आशाजनक हैं। हाल ही में [[सुमितोमो]] ने रूथेनियम (IV) ऑक्साइड (RuO<sub>2</sub>) का उपयोग करके डीकॉन प्रक्रिया के लिए उत्प्रेरक का पेटेंट कराया।<ref>{{cite journal | doi = 10.1016/j.jcat.2008.01.020 | volume=255 | title=Mechanism of HCl oxidation (Deacon process) over RuO2 | year=2008 | journal=Journal of Catalysis | pages=29–39 | last1 = López | first1 = Núria}}</ref> | ||
क्लोरीन का उत्पादन करने की | क्लोरीन का उत्पादन करने की अन्य पुरानी प्रक्रिया में ब्राइन को [[ अम्ल |अम्ल]] और [[मैंगनीज डाइऑक्साइड]] के साथ गर्म करना था। | ||
:: 2 NaCl + 2H<sub>2</sub>SO<sub>4</sub> + MnO<sub>2</sub> → Na<sub>2</sub>SO<sub>4</sub> + MnSO<sub>4</sub> + 2 H<sub>2</sub>O + Cl<sub>2</sub> | :: 2 NaCl + 2H<sub>2</sub>SO<sub>4</sub> + MnO<sub>2</sub> → Na<sub>2</sub>SO<sub>4</sub> + MnSO<sub>4</sub> + 2 H<sub>2</sub>O + Cl<sub>2</sub> | ||
इस प्रक्रिया का उपयोग करते हुए, रसायनज्ञ [[कार्ल विल्हेम शेहेल]] प्रयोगशाला में क्लोरीन को अलग करने वाले पहले व्यक्ति थे। [[वेल्डन प्रक्रिया]] द्वारा [[मैंगनीज]] को पुनर्प्राप्त किया जा सकता है।<ref name="lenn1">{{cite web|url=http://www.lenntech.com/Chemistry/chlorine-industry.htm|title=क्लोरीन उद्योग|publisher=Lenntech Water treatment & air purification Holding B.V., Rotterdamseweg 402 M, 2629 HH Delft, The Netherlands|accessdate=2007-03-17}}</ref> | इस प्रक्रिया का उपयोग करते हुए, रसायनज्ञ [[कार्ल विल्हेम शेहेल]] प्रयोगशाला में क्लोरीन को अलग करने वाले पहले व्यक्ति थे। [[वेल्डन प्रक्रिया]] द्वारा [[मैंगनीज]] को पुनर्प्राप्त किया जा सकता है।<ref name="lenn1">{{cite web|url=http://www.lenntech.com/Chemistry/chlorine-industry.htm|title=क्लोरीन उद्योग|publisher=Lenntech Water treatment & air purification Holding B.V., Rotterdamseweg 402 M, 2629 HH Delft, The Netherlands|accessdate=2007-03-17}}</ref> | ||
साइड आर्म और रबर टयूबिंग से जुड़े फ्लास्क में केंद्रित हाइड्रोक्लोरिक एसिड डालकर प्रयोगशाला में थोड़ी मात्रा में क्लोरीन गैस बनाई जा सकती है। इसके बाद मैंगनीज डाइऑक्साइड मिलाया जाता है और फ्लास्क को बंद कर दिया जाता है। प्रतिक्रिया बहुत अधिक एक्ज़ोथिर्मिक नहीं है। चूँकि क्लोरीन हवा से सघन होती है, इसे ट्यूब को फ्लास्क के अंदर रखकर सरलता से एकत्र किया जा सकता है, जहाँ यह हवा को विस्थापित कर देगी। एक बार भर जाने पर, एकत्रित फ्लास्क को रोका जा सकता है। | |||
प्रयोगशाला में क्लोरीन गैस की छोटी मात्रा का उत्पादन करने के लिए | प्रयोगशाला में क्लोरीन गैस की छोटी मात्रा का उत्पादन करने के लिए अन्य विधि [[सोडियम हाइपोक्लोराइट]] या [[सोडियम क्लोरेट]] घोल में केंद्रित हाइड्रोक्लोरिक एसिड (सामान्यतः लगभग 5M) मिलाकर है। | ||
हाइड्रोक्लोरिक एसिड में जोड़े जाने पर [[पोटेशियम परमैंगनेट]] का उपयोग क्लोरीन गैस उत्पन्न करने के लिए किया जा सकता है। | हाइड्रोक्लोरिक एसिड में जोड़े जाने पर [[पोटेशियम परमैंगनेट]] का उपयोग क्लोरीन गैस उत्पन्न करने के लिए किया जा सकता है। | ||
== मेम्ब्रेन औद्योगिक उत्पादन == | == मेम्ब्रेन औद्योगिक उत्पादन == | ||
क्लोरीन के बड़े पैमाने पर उत्पादन में कई चरण और कई उपकरण सम्मिलित होते हैं। नीचे दिया गया विवरण | क्लोरीन के बड़े पैमाने पर उत्पादन में कई चरण और कई उपकरण सम्मिलित होते हैं। नीचे दिया गया विवरण मेम्ब्रेन पौधे का विशिष्ट है। संयंत्र एक साथ सोडियम हाइड्रोक्साइड (कास्टिक सोडा) और हाइड्रोजन गैस भी उत्पन्न करता है। विशिष्ट संयंत्र में ब्राइन उत्पादन, सेल संचालन, क्लोरीन शीतलन और सुखाने, क्लोरीन संपीड़न और द्रवीकरण, तरल क्लोरीन भंडारण और लोडिंग, कास्टिक हैंडलिंग, वाष्पीकरण, भंडारण और लोडिंग और हाइड्रोजन हैंडलिंग सम्मिलित हैं। | ||
=== | === ब्राइन === | ||
क्लोरीन के उत्पादन की कुंजी ब्राइन संतृप्ति | क्लोरीन के उत्पादन की कुंजी ब्राइन संतृप्ति प्रणाली का संचालन है। विशेष रूप से मेम्ब्रेन सेलों के लिए, सही शुद्धता के साथ ठीक से संतृप्त घोल बनाए रखना महत्वपूर्ण है। कई पौधों में नमक का ढेर होता है, जिसे पुनर्नवीनीकरण ब्राइन के साथ छिड़का जाता है। दूसरों के पास स्लरी टैंक हैं, जिन्हें कच्चा नमक और पुनर्नवीनीकरण ब्राइन खिलाया जाता है। [[कैल्शियम]] और मैग्नीशियम को अवक्षेपित करने के लिए कच्चे ब्राइन को [[सोडियम कार्बोनेट]] और सोडियम हाइड्रॉक्साइड के साथ उपचारित किया जाता है। अभिक्रियाएं अधिकांशतः रिएक्टरों की श्रृंखला में की जाती हैं, इससे पहले उपचारित ब्राइन को बड़े स्पष्टीकरणक में भेजा जाता है, जहां कैल्शियम कार्बोनेट और मैग्नीशियम हाइड्रॉक्साइड व्यवस्थित होते हैं। निपटान में संशोधन के लिए स्पष्टक से ठीक पहले फ़्लोकुलेटिंग एजेंट जोड़ा जा सकता है। फिर [[अशुद्धियों]] को दूर करने के लिए [[आयन विनिमय|आयन विनिमयर्स]] की श्रृंखला में प्रवेश करने से पहले निथारने वाली ब्राइन को [[रेत फिल्टर]] या पत्ती फिल्टर का उपयोग करके यांत्रिक रूप से फ़िल्टर किया जाता है। इस प्रक्रिया में कई बिंदुओं पर [[कठोरता]] और शक्ति के लिए ब्राइन का परीक्षण किया जाता है। | ||
आयन एक्सचेंजर्स के बाद, | आयन एक्सचेंजर्स के बाद, ब्राइन को शुद्ध माना जाता है, और इसे सेल कमरे में पंप करने के लिए भंडारण टैंक में स्थानांतरित कर दिया जाता है। [[विद्युत भार]] के अनुसार निकास ब्राइन तापमान को नियंत्रित करने के लिए शुद्ध ब्राइन को सही तापमान पर गर्म किया जाता है। सेल कमरे से बाहर निकलने वाली ब्राइन को संतृप्त घोल चरण में वापस आने से पहले अवशिष्ट क्लोरीन को हटाने और [[पीएच|pH]] स्तर को नियंत्रित करने के लिए उपचार किया जाना चाहिए। इसे एसिड और [[सोडियम बाइसल्फाइट]] के साथ डीक्लोरिनेशन टावरों के माध्यम से पूरा किया जा सकता है। क्लोरीन को हटाने में विफल होने से आयन एक्सचेंज इकाइयों को हानि हो सकती है। [[ क्लोरट |क्लोरट]] और [[सल्फेट]] दोनों के संचय के लिए ब्राइन की देखभाल की जानी चाहिए, और या तो उपचार प्रणाली होनी चाहिए, या सुरक्षित स्तर बनाए रखने के लिए ब्राइन लूप को शुद्ध करना चाहिए, क्योंकि क्लोरेट आयन मेम्ब्रेन के माध्यम से फैल सकते हैं और कास्टिक को दूषित कर सकते हैं, जबकि सल्फेट आयन एनोड सतह कोटिंग को हानि पहुंचा सकते हैं। | ||
=== सेल | === सेल कमरा === | ||
जिस इमारत में कई इलेक्ट्रोलाइटिक सेल होती हैं, उसे सामान्यतः सेल | जिस इमारत में कई इलेक्ट्रोलाइटिक सेल होती हैं, उसे सामान्यतः सेल कमरा या सेल हाउस कहा जाता है, चूंकि कुछ पौधे बाहर बनाए जाते हैं। इस इमारत में सेलों के लिए सहायक संरचनाएं, सेलों को [[विद्युत शक्ति]] की आपूर्ति के लिए कनेक्शन और तरल पदार्थ के लिए पाइपिंग सम्मिलित हैं। निकास तापमान को नियंत्रित करने के लिए फ़ीड कास्टिक और ब्राइन के तापमान की देखभाल और नियंत्रण किया जाता है। यह भी देखभाल की जाती है, कि प्रत्येक सेल के वोल्टेज जो उत्पादन की दर को नियंत्रित करने के लिए उपयोग किए जाने वाले सेल कमरे पर विद्युत भार के साथ भिन्न होते हैं। दबाव राहत वाल्व के माध्यम से क्लोरीन और हाइड्रोजन हेडर में दबावों की देखभाल और नियंत्रण भी किया जाता है। | ||
[[एकदिश धारा]] की आपूर्ति | [[एकदिश धारा]] की आपूर्ति [[सही करनेवाला|संशोधित]] शक्ति स्रोत के माध्यम से की जाती है। प्लांट लोड को सेलों में [[विद्युत प्रवाह]] को बदलकर नियंत्रित किया जाता है। जैसे-जैसे धारा बढती है, फ़ीड तापमान को कम करते हुए, ब्राइन और कास्टिक और विआयनीकृत जल के लिए प्रवाह दर बढ़ जाती है। | ||
=== ठंडा करना और सुखाना === | === ठंडा करना और सुखाना === | ||
सेल लाइन से निकलने वाली क्लोरीन गैस को ठंडा और सुखाया जाना चाहिए क्योंकि निकास गैस 80 | सेल लाइन से निकलने वाली क्लोरीन गैस को ठंडा और सुखाया जाना चाहिए क्योंकि निकास गैस 80 °C से अधिक हो सकती है और इसमें [[नमी]] होती है, जो क्लोरीन गैस को लोहे के पाइपिंग के लिए संक्षारक होने देती है। गैस को ठंडा करने से ब्राइन से नमी की बड़ी मात्रा को गैस की धारा से संघनन के लिए अनुमति मिलती है। कूलिंग [[गैस कंप्रेसर]] और इसके बाद के द्रवीकरण चरण दोनों के [[कुशल ऊर्जा उपयोग]] में भी संशोधन करता है। क्लोरीन का निकास आदर्श रूप से 18°C और 25°C के बीच होता है। ठंडा करने के बाद गैस की धारा काउंटर प्रवाह [[सल्फ्यूरिक एसिड]] के साथ टावरों की श्रृंखला से होकर निकलती है। ये टावर धीरे-धीरे क्लोरीन गैस से बची हुई नमी को हटाते हैं। सुखाने वाले टावरों से बाहर निकलने के बाद किसी भी शेष सल्फ्यूरिक एसिड को हटाने के लिए क्लोरीन को फ़िल्टर किया जाता है। | ||
===संपीड़न और द्रवीकरण === | ===संपीड़न और द्रवीकरण === | ||
संपीड़न के कई विधियों | संपीड़न के कई विधियों [[तरल अंगूठी]], प्रत्यागामी कंप्रेसर, या [[केन्द्रापसारक कंप्रेसर]] का उपयोग किया जा सकता है । इस स्तर पर क्लोरीन गैस को संकुचित किया जाता है और इसे इंटर और आफ्टर-कूलर द्वारा और ठंडा किया जा सकता है। संपीड़न के बाद यह द्रवीभूतों में प्रवाहित होता है, जहाँ इसे द्रवीभूत करने के लिए पर्याप्त ठंडा किया जाता है। द्रवीकरण प्रणालियों के दबाव नियंत्रण के भाग के रूप में गैर संघनित गैसों और शेष क्लोरीन गैस को बाहर निकाल दिया जाता है। इन गैसों को गैस स्क्रबर में भेजा जाता है, जो सोडियम हाइपोक्लोराइट का उत्पादन करता है, या हाइड्रोक्लोरिक एसिड (हाइड्रोजन के साथ दहन द्वारा) या [[ईथीलीन]] डाइक्लोराइड (एथिलीन के साथ प्रतिक्रिया द्वारा) के उत्पादन में उपयोग किया जाता है। | ||
=== भंडारण और | === भंडारण और लोडिंग === | ||
तरल क्लोरीन सामान्यतः भंडारण टैंकों को | तरल क्लोरीन सामान्यतः भंडारण टैंकों को गंभीरता से सिंचित किया जाता है। इसे रेल या सड़क टैंकरों में पंपों के माध्यम से लोड किया जा सकता है या संपीड़ित सूखी गैस के साथ गद्देदार किया जा सकता है। | ||
=== कास्टिक हैंडलिंग, वाष्पीकरण, भंडारण और लोडिंग === | === कास्टिक हैंडलिंग, वाष्पीकरण, भंडारण और लोडिंग === | ||
कास्टिक, सेल | कास्टिक, सेल कमरे में प्रवाहित होता है, जो लूप में बहता है, जो एक साथ विआयनीकृत जल से पतला एक भाग के साथ भंडारण के लिए बंद हो जाता है और सेलों के अन्दर कठोर करने के लिए सेल लाइन में वापस आ जाता है। सुरक्षित सांद्रता बनाए रखने के लिए, सेल लाइन से निकलने वाली कास्टिक की शक्ति के लिए देखभाल की जानी चाहिए। बहुत कठोर या बहुत अशक्त घोल मेम्ब्रेन को हानि पहुंचा सकता है। मेम्ब्रेन सेल सामान्यतः भार के अनुसार से 30% से 33% तक कास्टिक का उत्पादन करती हैं। इसके निकास तापमान को नियंत्रित करने के लिए फ़ीड कास्टिक प्रवाह को कम विद्युत भार पर गर्म किया जाता है। सही निकास तापमान बनाए रखने के लिए उच्च भार के लिए कास्टिक को ठंडा करने की आवश्यकता होती है। भंडारण के लिए निकलने वाली कास्टिक को भंडारण टैंक से खींचा जाता है और अशक्त कास्टिक की आवश्यकता वाले ग्राहकों को बिक्री के लिए या साइट पर उपयोग के लिए पतला किया जा सकता है। वाणिज्यिक 50% कास्टिक का उत्पादन करने के लिए अन्य धारा को बहु प्रभाव बाष्पीकरणकर्ता में पंप किया जा सकता है। पंपों के माध्यम से लोडिंग स्टेशनों पर रेल कारों और टैंकर ट्रकों को लोड किया जाता है। | ||
=== हाइड्रोजन हैंडलिंग === | === हाइड्रोजन हैंडलिंग === | ||
उपोत्पाद के रूप में उत्पादित हाइड्रोजन को सीधे वातावरण में असंसाधित किया जा सकता है या साइट पर अन्य प्रक्रियाओं में उपयोग के लिए ठंडा, संपीड़ित और सुखाया जा सकता है या पाइपलाइन, सिलेंडर या ट्रकों के माध्यम से ग्राहक को बेचा जा सकता है। कुछ संभावित उपयोगों में हाइड्रोक्लोरिक एसिड या [[हाइड्रोजन पेरोक्साइड]] का निर्माण, साथ ही [[पेट्रोलियम]] का [[डीसल्फराइजेशन]], या [[ बायलर ]] या [[ईंधन]] सेल में ईंधन के रूप में उपयोग सम्मिलित हैं। | उपोत्पाद के रूप में उत्पादित हाइड्रोजन को सीधे वातावरण में असंसाधित किया जा सकता है, या साइट पर अन्य प्रक्रियाओं में उपयोग के लिए ठंडा, संपीड़ित और सुखाया जा सकता है, या पाइपलाइन, सिलेंडर या ट्रकों के माध्यम से ग्राहक को बेचा जा सकता है। कुछ संभावित उपयोगों में हाइड्रोक्लोरिक एसिड या [[हाइड्रोजन पेरोक्साइड]] का निर्माण, साथ ही [[पेट्रोलियम]] का [[डीसल्फराइजेशन]], या [[ बायलर |बायलर]] या [[ईंधन]] सेल में ईंधन के रूप में उपयोग सम्मिलित हैं। | ||
=== ऊर्जा का व्यय === | === ऊर्जा का व्यय === | ||
क्लोरीन का उत्पादन अत्यंत ऊर्जा गहन है।<ref name="European Commission1">{{cite web|url=http://www.jrc.es/pub/english.cgi/d733217/05%20Reference%20Document%20on%20Best%20Available%20Techniques%20in%20the%20Chlor-Alkali%20Manufacturing%20industry%20%28adopted%20Dec%202001%29%20-%205.2%20Mb|title=एकीकृत प्रदूषण रोकथाम और नियंत्रण (आईपीपीसी) - क्लोर-अल्कली विनिर्माण उद्योग में सर्वोत्तम उपलब्ध तकनीकों पर संदर्भ दस्तावेज़|publisher=European Commission|accessdate=2007-09-02}}</ref> उत्पाद के प्रति | क्लोरीन का उत्पादन अत्यंत ऊर्जा गहन है।<ref name="European Commission1">{{cite web|url=http://www.jrc.es/pub/english.cgi/d733217/05%20Reference%20Document%20on%20Best%20Available%20Techniques%20in%20the%20Chlor-Alkali%20Manufacturing%20industry%20%28adopted%20Dec%202001%29%20-%205.2%20Mb|title=एकीकृत प्रदूषण रोकथाम और नियंत्रण (आईपीपीसी) - क्लोर-अल्कली विनिर्माण उद्योग में सर्वोत्तम उपलब्ध तकनीकों पर संदर्भ दस्तावेज़|publisher=European Commission|accessdate=2007-09-02}}</ref> उत्पाद के प्रति इकाई भार में ऊर्जा का व्यय लोहा और इस्पात निर्माण के लिए<ref name="European Commission2">{{cite web|url=http://www.jrc.es/pub/english.cgi/d733208/02%20Best%20Available%20Techniques%20Reference%20Document%20on%20the%20Production%20of%20Iron%20and%20Steel%20%28adopted%20Dec%202001%29%20-%209.4Mb|title=एकीकृत प्रदूषण रोकथाम और नियंत्रण (आईपीपीसी) - लौह और इस्पात के उत्पादन पर सर्वोत्तम उपलब्ध तकनीक संदर्भ दस्तावेज़|publisher=European Commission|accessdate=2007-09-02}}</ref> और कांच के उत्पादन के लिए अधिक से अधिक<ref name="European Commission3">{{cite web|url=http://www.jrc.es/pub/english.cgi/d733226/08%20Reference%20Document%20on%20Best%20Available%20Techniques%20in%20the%20Glass%20Manufacturing%20Industry%20%28adopted%20Dec%202001%29%20-%202.7%20Mb|title=एकीकृत प्रदूषण रोकथाम और नियंत्रण (आईपीपीसी) - ग्लास निर्माण उद्योग में सर्वोत्तम उपलब्ध तकनीकों पर संदर्भ दस्तावेज़|publisher=European Commission|accessdate=2007-09-02}}</ref> या सीमेंट के उत्पादन से अधिक नहीं है।<ref name="European Commission4">{{cite web|url=http://www.jrc.es/pub/english.cgi/d733211/03%20Reference%20Document%20on%20Best%20Available%20Techniques%20in%20the%20Cement%20and%20Lime%20Manufacturing%20Industries%20%28adopted%20Dec%202001%29%20-%201.3%20Mb|title=एकीकृत प्रदूषण रोकथाम और नियंत्रण (आईपीपीसी) - सीमेंट और चूना निर्माण उद्योगों में सर्वोत्तम उपलब्ध तकनीकों पर संदर्भ दस्तावेज़|publisher=European Commission|accessdate=2007-09-02}}</ref> | ||
चूंकि क्लोरीन के उत्पादन के लिए [[बिजली]] | चूंकि क्लोरीन के उत्पादन के लिए [[बिजली|विद्युत्]] अनिवार्य कच्चा माल है, इसलिए [[इलेक्ट्रोकैमिस्ट्री]] प्रतिक्रिया से संबंधित ऊर्जा व्यय को कम नहीं किया जा सकता है। ऊर्जा बचत मुख्य रूप से अधिक कुशल प्रौद्योगिकियों को प्रयुक्त करने और सहायक ऊर्जा उपयोग को कम करने के माध्यम से उत्पन्न होती है। | ||
==संदर्भ== | ==संदर्भ== | ||
| Line 98: | Line 96: | ||
{{Authority control}} | {{Authority control}} | ||
{{DEFAULTSORT:Chlorine Production}} | {{DEFAULTSORT:Chlorine Production}} | ||
[[Category: Machine Translated Page]] | [[Category:Created On 25/03/2023|Chlorine Production]] | ||
[[Category: | [[Category:Machine Translated Page|Chlorine Production]] | ||
[[Category:Pages with script errors|Chlorine Production]] | |||
[[Category:Templates Vigyan Ready|Chlorine Production]] | |||
[[Category:क्लोरीन|Chlorine Production]] | |||
Latest revision as of 16:25, 13 April 2023
सोडियम क्लोराइड घोल (ब्राइन) और अन्य विधियों के इलेक्ट्रोलीज़ सहित प्राकृतिक पदार्थों से निकालने से क्लोरीन गैस का उत्पादन किया जा सकता है।
गैस निष्कर्षण
क्लोरीन को सोडियम क्लोराइड घोल (ब्राइन) के इलेक्ट्रोलिसिस द्वारा निर्मित किया जा सकता है, जिसे क्लोराल्कली प्रक्रिया के रूप में जाना जाता है। क्लोरीन के उत्पादन से सह-उत्पाद कास्टिक सोडा (सोडियम हाइड्रॉक्साइड, NaOH) और हाइड्रोजन गैस (H2) बनते हैं। ये दो उत्पाद, साथ ही क्लोरीन भी अत्यधिक प्रतिक्रियाशील हैं। पोटेशियम क्लोराइड के घोल के इलेक्ट्रोलिसिस द्वारा क्लोरीन का उत्पादन भी किया जा सकता है, इस स्थिति में सह-उत्पाद हाइड्रोजन और कास्टिक पोटाश (पोटेशियम हाइड्रोक्साइड) हैं। क्लोराइड विलयनों के इलेक्ट्रोलिसिस द्वारा क्लोरीन के निष्कर्षण के लिए तीन औद्योगिक विधियाँ हैं, जो निम्नलिखित समीकरणों के अनुसार आगे बढ़ती हैं:
- कैथोड: 2 H+ (aq) + 2 e− → H2 (g)
- एनोड: 2 Cl− (aq) → Cl2 (g) + 2 e−
समग्र प्रक्रिया: 2 NaCl (or KCl) + 2 H2O → Cl2 + H2 + 2 NaOH (or KOH)
पारा सेल इलेक्ट्रोलिसिस
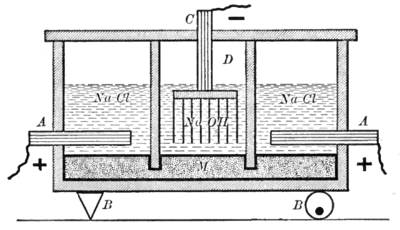
पारा (तत्व) सेल इलेक्ट्रोलिसिस, जिसे कास्टनर-केलनर प्रक्रिया के रूप में भी जाना जाता है, औद्योगिक पैमाने पर क्लोरीन का उत्पादन करने के लिए उन्नीसवीं शताब्दी के अंत में उपयोग की जाने वाली पहली विधि थी।[1][2] उपयोग की जाने वाली रॉकिंग सेलों में वर्षों से संशोधन किया गया है।[3] आज, प्राथमिक सेल में, प्लैटिनम के साथ टाइटेनियम एनोड पहने हुए हैं[4] या मिश्रित धातु ऑक्साइड इलेक्ट्रोड (पूर्व में ग्रेफाइट एनोड) को तरल पारा कैथोड पर बहने वाले सोडियम (या पोटैशियम) क्लोराइड घोल में रखा जाता है। जब संभावित अंतर प्रयुक्त किया जाता है और धारा प्रवाहित होती है, तो टाइटेनियम एनोड पर क्लोरीन छोड़ा जाता है और सोडियम (या पोटेशियम) पारा कैथोड में घुलकर अमलगम (रसायन) बनाता है। यह अलग रिएक्टर (डेनुडर या द्वितीयक सेल) में निरंतर प्रवाहित होता है, जहां यह सामान्यतः जल के साथ प्रतिक्रिया करके पारा में परिवर्तित हो जाता है, व्यावसायिक रूप से उपयोगी एकाग्रता (भार से 50%) पर हाइड्रोजन और सोडियम (या पोटेशियम) हीड्राकसीड का उत्पादन करता है। पारा फिर नीचे स्थित पंप द्वारा प्राथमिक सेल में पुनर्नवीनीकरण किया जाता है।
पारा प्रक्रिया तीन मुख्य प्रौद्योगिकियों (पारा, डायाफ्राम (यांत्रिक उपकरण) और मेम्ब्रेन (चयनात्मक बाधा)) में सबसे कम ऊर्जा कुशल है और पारा प्रदूषण के बारे में भी चिंताजनक हैं।
अनुमान है कि विश्व भर में अभी भी लगभग 100 मरकरी-सेल संयंत्र काम कर रहे हैं। जापान में, पारा-आधारित क्लोराल्कली का उत्पादन वस्तुतः 1987 तक समाप्त हो गया था (2003 में बंद अंतिम दो पोटेशियम क्लोराइड इकाइयों को छोड़कर)। संयुक्त राज्य अमेरिका में, 2008 के अंत तक केवल पांच मरकरी संयंत्र परिचालन में शेष रहेंगे। यूरोप में, 2006 में पारा सेलों की क्षमता का 43% हिस्सा था और पश्चिमी यूरोपीय उत्पादकों ने 2020 तक शेष सभी क्लोरअल्कली पारा संयंत्रों को बंद करने या परिवर्तित करने के लिए प्रतिबद्ध किया है।[5]
डायाफ्राम सेल इलेक्ट्रोलिसिस (द्विध्रुवीय)
डायाफ्राम सेल इलेक्ट्रोलिसिस में, एस्बेस्टस (या बहुलक-फाइबर) डायाफ्राम कैथोड और एनोड को अलग करता है, जो एनोड पर बनने वाले क्लोरीन को सोडियम हाइड्रॉक्साइड और कैथोड पर बनने वाले हाइड्रोजन के साथ फिर से मिलाने से रोकता है।[6] इस विधि का विकास भी उन्नीसवीं शताब्दी के अंत में हुआ था। इस प्रक्रिया के कई रूप ले सुयूर सेल (1893), हारग्रेव्स-बर्ड सेल (1901), गिब्स सेल (1908) और टाउनसेंड सेल (1904) हैं।[7][8] सेल डायफ्राम के निर्माण और प्लेसमेंट में भिन्न होती हैं, कुछ में डायफ्राम कैथोड के सीधे संपर्क में होता है।
नमक का घोल निरंतर एनोड डिब्बे में डाला जाता है और डायाफ्राम के माध्यम से कैथोड डिब्बे में प्रवाहित होता है, जहां संक्षारक पदार्थ क्षार का उत्पादन होता है और ब्राइन आंशिक रूप से समाप्त हो जाता है। परिणामस्वरूप, डायाफ्राम विधियाँ क्षार का उत्पादन करती हैं, जो पारा सेल विधियों की तुलना में अत्यधिक पतला (लगभग 12%) और कम शुद्धता वाला होता है।
पर्यावरण में पारे के निर्वहन को रोकने की समस्या से डायाफ्राम सेल बोझिल नहीं होती हैं; वे कम वोल्टेज पर भी काम करते हैं, जिसके परिणामस्वरूप पारा सेल पद्धति पर ऊर्जा की बचत होती है,[8] लेकिन बड़ी मात्रा में भाप की आवश्यकता होती है यदि कास्टिक को 50% की व्यावसायिक सांद्रता तक वाष्पित करना है।
मेम्ब्रेन सेल इलेक्ट्रोलिसिस
इस विधि का विकास 1970 के दशक में प्रारंभ हुआ था। इलेक्ट्रोलिसिस सेल को कटियन पारगम्यता (इलेक्ट्रोमैग्नेटिज्म) मेम्ब्रेन द्वारा दो वर्गों में विभाजित किया जाता है जो कटियन एक्सचेंजर के रूप में कार्य करता है। संतृप्त सोडियम (या पोटेशियम) क्लोराइड घोल को एनोड डिब्बे से निकाला जाता है, जिससे कम सांद्रता निकलती है।[9] सोडियम (या पोटेशियम) हाइड्रॉक्साइड घोल कैथोड डिब्बे के माध्यम से परिचालित होता है, जो उच्च सांद्रता से बाहर निकलता है। सान्द्र सोडियम हाइड्रॉक्साइड विलयन का एक भाग जो सेल को छोड़ता है, उत्पाद के रूप में विपथित किया जाता है, जबकि शेष विआयनीकृत जल से तनुकृत किया जाता है और पुन: विद्युत अपघटन तंत्र से निकाला जाता है।
यह विधि डायाफ्राम सेल की तुलना में अधिक कुशल है और लगभग 32% सांद्रता पर बहुत शुद्ध सोडियम (या पोटेशियम) हाइड्रॉक्साइड का उत्पादन करती है, लेकिन इसके लिए बहुत शुद्ध ब्राइन की आवश्यकता होती है।
अन्य इलेक्ट्रोलाइटिक प्रक्रियाएं
यद्यपि बहुत कम उत्पादन पैमाने सम्मिलित है, इलेक्ट्रोलाइटिक डायाफ्राम और मेम्ब्रेन प्रौद्योगिकियों का उपयोग औद्योगिक रूप से हाइड्रोक्लोरिक एसिड घोलों से क्लोरीन को पुनर्प्राप्त करने के लिए किया जाता है, जो सह-उत्पाद के रूप में हाइड्रोजन (लेकिन कोई कास्टिक क्षार नहीं) का उत्पादन करता है।
इसके अतिरिक्त, फ्यूज्ड क्लोराइड लवण (डाउन्स सेल) का इलेक्ट्रोलिसिस भी क्लोरीन का उत्पादन करने में सक्षम बनाता है, इस स्थिति में धातु सोडियम या मैगनीशियम के निर्माण के उप-उत्पाद के रूप में क्लोरीन का उत्पादन करने में सक्षम बनाता है।
अन्य विधियां
क्लोरीन उत्पादन के लिए इलेक्ट्रोलाइटिक विधियों का उपयोग करने से पहले, डीकॉन प्रक्रिया में ऑक्सीजन के साथ हाइड्रोजन क्लोराइड का प्रत्यक्ष ऑक्सीकरण (अधिकांशतः हवा के संपर्क में आने के माध्यम से) किया जाता था:
- 4 HCl + O2 → 2 Cl2 + 2 H2O
यह प्रतिक्रिया कॉपर (II) क्लोराइड (CuCl2) उत्प्रेरक के रूप में और उच्च तापमान (लगभग 400 °C) पर किया जाता है। निकाले गए क्लोरीन की मात्रा लगभग 80% है। अत्यधिक संक्षारक प्रतिक्रिया मिश्रण के कारण, इस पद्धति का औद्योगिक उपयोग कठिन है और अतीत में कई प्रायोगिक परीक्षण विफल रहे हैं। फिर भी, हाल के घटनाक्रम आशाजनक हैं। हाल ही में सुमितोमो ने रूथेनियम (IV) ऑक्साइड (RuO2) का उपयोग करके डीकॉन प्रक्रिया के लिए उत्प्रेरक का पेटेंट कराया।[10]
क्लोरीन का उत्पादन करने की अन्य पुरानी प्रक्रिया में ब्राइन को अम्ल और मैंगनीज डाइऑक्साइड के साथ गर्म करना था।
- 2 NaCl + 2H2SO4 + MnO2 → Na2SO4 + MnSO4 + 2 H2O + Cl2
इस प्रक्रिया का उपयोग करते हुए, रसायनज्ञ कार्ल विल्हेम शेहेल प्रयोगशाला में क्लोरीन को अलग करने वाले पहले व्यक्ति थे। वेल्डन प्रक्रिया द्वारा मैंगनीज को पुनर्प्राप्त किया जा सकता है।[11]
साइड आर्म और रबर टयूबिंग से जुड़े फ्लास्क में केंद्रित हाइड्रोक्लोरिक एसिड डालकर प्रयोगशाला में थोड़ी मात्रा में क्लोरीन गैस बनाई जा सकती है। इसके बाद मैंगनीज डाइऑक्साइड मिलाया जाता है और फ्लास्क को बंद कर दिया जाता है। प्रतिक्रिया बहुत अधिक एक्ज़ोथिर्मिक नहीं है। चूँकि क्लोरीन हवा से सघन होती है, इसे ट्यूब को फ्लास्क के अंदर रखकर सरलता से एकत्र किया जा सकता है, जहाँ यह हवा को विस्थापित कर देगी। एक बार भर जाने पर, एकत्रित फ्लास्क को रोका जा सकता है।
प्रयोगशाला में क्लोरीन गैस की छोटी मात्रा का उत्पादन करने के लिए अन्य विधि सोडियम हाइपोक्लोराइट या सोडियम क्लोरेट घोल में केंद्रित हाइड्रोक्लोरिक एसिड (सामान्यतः लगभग 5M) मिलाकर है।
हाइड्रोक्लोरिक एसिड में जोड़े जाने पर पोटेशियम परमैंगनेट का उपयोग क्लोरीन गैस उत्पन्न करने के लिए किया जा सकता है।
मेम्ब्रेन औद्योगिक उत्पादन
क्लोरीन के बड़े पैमाने पर उत्पादन में कई चरण और कई उपकरण सम्मिलित होते हैं। नीचे दिया गया विवरण मेम्ब्रेन पौधे का विशिष्ट है। संयंत्र एक साथ सोडियम हाइड्रोक्साइड (कास्टिक सोडा) और हाइड्रोजन गैस भी उत्पन्न करता है। विशिष्ट संयंत्र में ब्राइन उत्पादन, सेल संचालन, क्लोरीन शीतलन और सुखाने, क्लोरीन संपीड़न और द्रवीकरण, तरल क्लोरीन भंडारण और लोडिंग, कास्टिक हैंडलिंग, वाष्पीकरण, भंडारण और लोडिंग और हाइड्रोजन हैंडलिंग सम्मिलित हैं।
ब्राइन
क्लोरीन के उत्पादन की कुंजी ब्राइन संतृप्ति प्रणाली का संचालन है। विशेष रूप से मेम्ब्रेन सेलों के लिए, सही शुद्धता के साथ ठीक से संतृप्त घोल बनाए रखना महत्वपूर्ण है। कई पौधों में नमक का ढेर होता है, जिसे पुनर्नवीनीकरण ब्राइन के साथ छिड़का जाता है। दूसरों के पास स्लरी टैंक हैं, जिन्हें कच्चा नमक और पुनर्नवीनीकरण ब्राइन खिलाया जाता है। कैल्शियम और मैग्नीशियम को अवक्षेपित करने के लिए कच्चे ब्राइन को सोडियम कार्बोनेट और सोडियम हाइड्रॉक्साइड के साथ उपचारित किया जाता है। अभिक्रियाएं अधिकांशतः रिएक्टरों की श्रृंखला में की जाती हैं, इससे पहले उपचारित ब्राइन को बड़े स्पष्टीकरणक में भेजा जाता है, जहां कैल्शियम कार्बोनेट और मैग्नीशियम हाइड्रॉक्साइड व्यवस्थित होते हैं। निपटान में संशोधन के लिए स्पष्टक से ठीक पहले फ़्लोकुलेटिंग एजेंट जोड़ा जा सकता है। फिर अशुद्धियों को दूर करने के लिए आयन विनिमयर्स की श्रृंखला में प्रवेश करने से पहले निथारने वाली ब्राइन को रेत फिल्टर या पत्ती फिल्टर का उपयोग करके यांत्रिक रूप से फ़िल्टर किया जाता है। इस प्रक्रिया में कई बिंदुओं पर कठोरता और शक्ति के लिए ब्राइन का परीक्षण किया जाता है।
आयन एक्सचेंजर्स के बाद, ब्राइन को शुद्ध माना जाता है, और इसे सेल कमरे में पंप करने के लिए भंडारण टैंक में स्थानांतरित कर दिया जाता है। विद्युत भार के अनुसार निकास ब्राइन तापमान को नियंत्रित करने के लिए शुद्ध ब्राइन को सही तापमान पर गर्म किया जाता है। सेल कमरे से बाहर निकलने वाली ब्राइन को संतृप्त घोल चरण में वापस आने से पहले अवशिष्ट क्लोरीन को हटाने और pH स्तर को नियंत्रित करने के लिए उपचार किया जाना चाहिए। इसे एसिड और सोडियम बाइसल्फाइट के साथ डीक्लोरिनेशन टावरों के माध्यम से पूरा किया जा सकता है। क्लोरीन को हटाने में विफल होने से आयन एक्सचेंज इकाइयों को हानि हो सकती है। क्लोरट और सल्फेट दोनों के संचय के लिए ब्राइन की देखभाल की जानी चाहिए, और या तो उपचार प्रणाली होनी चाहिए, या सुरक्षित स्तर बनाए रखने के लिए ब्राइन लूप को शुद्ध करना चाहिए, क्योंकि क्लोरेट आयन मेम्ब्रेन के माध्यम से फैल सकते हैं और कास्टिक को दूषित कर सकते हैं, जबकि सल्फेट आयन एनोड सतह कोटिंग को हानि पहुंचा सकते हैं।
सेल कमरा
जिस इमारत में कई इलेक्ट्रोलाइटिक सेल होती हैं, उसे सामान्यतः सेल कमरा या सेल हाउस कहा जाता है, चूंकि कुछ पौधे बाहर बनाए जाते हैं। इस इमारत में सेलों के लिए सहायक संरचनाएं, सेलों को विद्युत शक्ति की आपूर्ति के लिए कनेक्शन और तरल पदार्थ के लिए पाइपिंग सम्मिलित हैं। निकास तापमान को नियंत्रित करने के लिए फ़ीड कास्टिक और ब्राइन के तापमान की देखभाल और नियंत्रण किया जाता है। यह भी देखभाल की जाती है, कि प्रत्येक सेल के वोल्टेज जो उत्पादन की दर को नियंत्रित करने के लिए उपयोग किए जाने वाले सेल कमरे पर विद्युत भार के साथ भिन्न होते हैं। दबाव राहत वाल्व के माध्यम से क्लोरीन और हाइड्रोजन हेडर में दबावों की देखभाल और नियंत्रण भी किया जाता है।
एकदिश धारा की आपूर्ति संशोधित शक्ति स्रोत के माध्यम से की जाती है। प्लांट लोड को सेलों में विद्युत प्रवाह को बदलकर नियंत्रित किया जाता है। जैसे-जैसे धारा बढती है, फ़ीड तापमान को कम करते हुए, ब्राइन और कास्टिक और विआयनीकृत जल के लिए प्रवाह दर बढ़ जाती है।
ठंडा करना और सुखाना
सेल लाइन से निकलने वाली क्लोरीन गैस को ठंडा और सुखाया जाना चाहिए क्योंकि निकास गैस 80 °C से अधिक हो सकती है और इसमें नमी होती है, जो क्लोरीन गैस को लोहे के पाइपिंग के लिए संक्षारक होने देती है। गैस को ठंडा करने से ब्राइन से नमी की बड़ी मात्रा को गैस की धारा से संघनन के लिए अनुमति मिलती है। कूलिंग गैस कंप्रेसर और इसके बाद के द्रवीकरण चरण दोनों के कुशल ऊर्जा उपयोग में भी संशोधन करता है। क्लोरीन का निकास आदर्श रूप से 18°C और 25°C के बीच होता है। ठंडा करने के बाद गैस की धारा काउंटर प्रवाह सल्फ्यूरिक एसिड के साथ टावरों की श्रृंखला से होकर निकलती है। ये टावर धीरे-धीरे क्लोरीन गैस से बची हुई नमी को हटाते हैं। सुखाने वाले टावरों से बाहर निकलने के बाद किसी भी शेष सल्फ्यूरिक एसिड को हटाने के लिए क्लोरीन को फ़िल्टर किया जाता है।
संपीड़न और द्रवीकरण
संपीड़न के कई विधियों तरल अंगूठी, प्रत्यागामी कंप्रेसर, या केन्द्रापसारक कंप्रेसर का उपयोग किया जा सकता है । इस स्तर पर क्लोरीन गैस को संकुचित किया जाता है और इसे इंटर और आफ्टर-कूलर द्वारा और ठंडा किया जा सकता है। संपीड़न के बाद यह द्रवीभूतों में प्रवाहित होता है, जहाँ इसे द्रवीभूत करने के लिए पर्याप्त ठंडा किया जाता है। द्रवीकरण प्रणालियों के दबाव नियंत्रण के भाग के रूप में गैर संघनित गैसों और शेष क्लोरीन गैस को बाहर निकाल दिया जाता है। इन गैसों को गैस स्क्रबर में भेजा जाता है, जो सोडियम हाइपोक्लोराइट का उत्पादन करता है, या हाइड्रोक्लोरिक एसिड (हाइड्रोजन के साथ दहन द्वारा) या ईथीलीन डाइक्लोराइड (एथिलीन के साथ प्रतिक्रिया द्वारा) के उत्पादन में उपयोग किया जाता है।
भंडारण और लोडिंग
तरल क्लोरीन सामान्यतः भंडारण टैंकों को गंभीरता से सिंचित किया जाता है। इसे रेल या सड़क टैंकरों में पंपों के माध्यम से लोड किया जा सकता है या संपीड़ित सूखी गैस के साथ गद्देदार किया जा सकता है।
कास्टिक हैंडलिंग, वाष्पीकरण, भंडारण और लोडिंग
कास्टिक, सेल कमरे में प्रवाहित होता है, जो लूप में बहता है, जो एक साथ विआयनीकृत जल से पतला एक भाग के साथ भंडारण के लिए बंद हो जाता है और सेलों के अन्दर कठोर करने के लिए सेल लाइन में वापस आ जाता है। सुरक्षित सांद्रता बनाए रखने के लिए, सेल लाइन से निकलने वाली कास्टिक की शक्ति के लिए देखभाल की जानी चाहिए। बहुत कठोर या बहुत अशक्त घोल मेम्ब्रेन को हानि पहुंचा सकता है। मेम्ब्रेन सेल सामान्यतः भार के अनुसार से 30% से 33% तक कास्टिक का उत्पादन करती हैं। इसके निकास तापमान को नियंत्रित करने के लिए फ़ीड कास्टिक प्रवाह को कम विद्युत भार पर गर्म किया जाता है। सही निकास तापमान बनाए रखने के लिए उच्च भार के लिए कास्टिक को ठंडा करने की आवश्यकता होती है। भंडारण के लिए निकलने वाली कास्टिक को भंडारण टैंक से खींचा जाता है और अशक्त कास्टिक की आवश्यकता वाले ग्राहकों को बिक्री के लिए या साइट पर उपयोग के लिए पतला किया जा सकता है। वाणिज्यिक 50% कास्टिक का उत्पादन करने के लिए अन्य धारा को बहु प्रभाव बाष्पीकरणकर्ता में पंप किया जा सकता है। पंपों के माध्यम से लोडिंग स्टेशनों पर रेल कारों और टैंकर ट्रकों को लोड किया जाता है।
हाइड्रोजन हैंडलिंग
उपोत्पाद के रूप में उत्पादित हाइड्रोजन को सीधे वातावरण में असंसाधित किया जा सकता है, या साइट पर अन्य प्रक्रियाओं में उपयोग के लिए ठंडा, संपीड़ित और सुखाया जा सकता है, या पाइपलाइन, सिलेंडर या ट्रकों के माध्यम से ग्राहक को बेचा जा सकता है। कुछ संभावित उपयोगों में हाइड्रोक्लोरिक एसिड या हाइड्रोजन पेरोक्साइड का निर्माण, साथ ही पेट्रोलियम का डीसल्फराइजेशन, या बायलर या ईंधन सेल में ईंधन के रूप में उपयोग सम्मिलित हैं।
ऊर्जा का व्यय
क्लोरीन का उत्पादन अत्यंत ऊर्जा गहन है।[12] उत्पाद के प्रति इकाई भार में ऊर्जा का व्यय लोहा और इस्पात निर्माण के लिए[13] और कांच के उत्पादन के लिए अधिक से अधिक[14] या सीमेंट के उत्पादन से अधिक नहीं है।[15]
चूंकि क्लोरीन के उत्पादन के लिए विद्युत् अनिवार्य कच्चा माल है, इसलिए इलेक्ट्रोकैमिस्ट्री प्रतिक्रिया से संबंधित ऊर्जा व्यय को कम नहीं किया जा सकता है। ऊर्जा बचत मुख्य रूप से अधिक कुशल प्रौद्योगिकियों को प्रयुक्त करने और सहायक ऊर्जा उपयोग को कम करने के माध्यम से उत्पन्न होती है।
संदर्भ
- ↑ Pauling, Linus, General Chemistry, 1970 ed., Dover publications
- ↑ "क्लोरीन और कास्टिक सोडा के लिए इलेक्ट्रोलाइटिक प्रक्रियाएं". Lenntech Water treatment & air purification Holding B.V., Rotterdamseweg 402 M, 2629 HH Delft, The Netherlands. Retrieved 2007-03-17.
- ↑ "बुध कोशिका". Euro Chlor. Archived from the original on 2011-09-18. Retrieved 2007-08-15.
- ↑ Landolt, D.; Ibl, N. (1972). "प्लैटिनीकृत टाइटेनियम पर एनोडिक क्लोरेट का निर्माण". Journal of Applied Electrochemistry. Chapman and Hall Ltd. 2 (3): 201–210. doi:10.1007/BF02354977.
- ↑ "पारा प्रदूषण पर क्षेत्रीय जागरूकता बढ़ाने की कार्यशाला" (PDF). UNEP. Archived from the original (PDF) on 2007-10-29. Retrieved 2007-10-28.
- ↑ "डायाफ्राम सेल". Euro Chlor. Archived from the original on 2007-09-27. Retrieved 2007-08-15.
- ↑ "ब्राइन का इलेक्ट्रोलिसिस". Salt Manufacturers' Association. Archived from the original on 2007-05-14. Retrieved 2007-03-17.
- ↑ 8.0 8.1 Kiefer, David M. "जब उद्योग ने आगे चार्ज किया". Chemistry Chronicles. Retrieved 2007-03-17.
- ↑ "झिल्ली कोशिका". Euro Chlor. Archived from the original on 2007-08-14. Retrieved 2007-08-15.
- ↑ López, Núria (2008). "Mechanism of HCl oxidation (Deacon process) over RuO2". Journal of Catalysis. 255: 29–39. doi:10.1016/j.jcat.2008.01.020.
- ↑ "क्लोरीन उद्योग". Lenntech Water treatment & air purification Holding B.V., Rotterdamseweg 402 M, 2629 HH Delft, The Netherlands. Retrieved 2007-03-17.
- ↑ "एकीकृत प्रदूषण रोकथाम और नियंत्रण (आईपीपीसी) - क्लोर-अल्कली विनिर्माण उद्योग में सर्वोत्तम उपलब्ध तकनीकों पर संदर्भ दस्तावेज़". European Commission. Retrieved 2007-09-02.
- ↑ "एकीकृत प्रदूषण रोकथाम और नियंत्रण (आईपीपीसी) - लौह और इस्पात के उत्पादन पर सर्वोत्तम उपलब्ध तकनीक संदर्भ दस्तावेज़". European Commission. Retrieved 2007-09-02.
- ↑ "एकीकृत प्रदूषण रोकथाम और नियंत्रण (आईपीपीसी) - ग्लास निर्माण उद्योग में सर्वोत्तम उपलब्ध तकनीकों पर संदर्भ दस्तावेज़". European Commission. Retrieved 2007-09-02.
- ↑ "एकीकृत प्रदूषण रोकथाम और नियंत्रण (आईपीपीसी) - सीमेंट और चूना निर्माण उद्योगों में सर्वोत्तम उपलब्ध तकनीकों पर संदर्भ दस्तावेज़". European Commission. Retrieved 2007-09-02.
