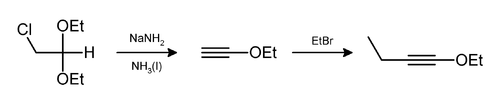सोडियम एमाइड: Difference between revisions
No edit summary |
No edit summary |
||
| (2 intermediate revisions by 2 users not shown) | |||
| Line 127: | Line 127: | ||
==संदर्भ== | ==संदर्भ== | ||
{{Reflist}}{{Authority control}} | {{Reflist}}{{Authority control}} | ||
[[Category:Articles containing unverified chemical infoboxes]] | |||
[[Category:Articles with changed ChemSpider identifier]] | |||
[[Category: | [[Category:Articles with changed InChI identifier]] | ||
[[Category:Articles without InChI source]] | |||
[[Category:Articles without KEGG source]] | |||
[[Category:CS1 maint]] | |||
[[Category:Chemical articles with multiple compound IDs|B]] | |||
[[Category:Created On 02/03/2023]] | [[Category:Created On 02/03/2023]] | ||
[[Category:ECHA InfoCard ID from Wikidata]] | |||
[[Category:E number from Wikidata]] | |||
[[Category:Lua-based templates]] | |||
[[Category:Machine Translated Page]] | |||
[[Category:Multiple chemicals in an infobox that need indexing]] | |||
[[Category:Pages using collapsible list with both background and text-align in titlestyle|background:transparent;font-weight:normal;text-align:left ]] | |||
[[Category:Pages with script errors]] | |||
[[Category:Templates Vigyan Ready]] | |||
[[Category:Templates that add a tracking category]] | |||
[[Category:Templates that generate short descriptions]] | |||
[[Category:Templates using TemplateData]] | |||
[[Category:कार्बनिक रसायन विज्ञान के लिए अभिकर्मकों]] | |||
[[Category:धातु एमाइड्स]] | |||
[[Category:सोडियम यौगिक]] | |||
Latest revision as of 21:53, 3 May 2023

| |

| |
| Names | |
|---|---|
| IUPAC name
Sodium amide, sodium azanide[1]
| |
| Other names
Sodamide
| |
| Identifiers | |
3D model (JSmol)
|
|
| ChEBI | |
| ChemSpider | |
| EC Number |
|
PubChem CID
|
|
| UNII | |
| UN number | 1390 |
| |
| |
| Properties | |
| NaNH2 | |
| Molar mass | 39.013 g·mol−1 |
| Appearance | Colourless crystals |
| Odor | Ammonia-like |
| Density | 1.39 g/cm3 |
| Melting point | 210 °C (410 °F; 483 K) |
| Boiling point | 400 °C (752 °F; 673 K) |
| Reacts | |
| Solubility | 40 mg/L (liquid ammonia), reacts with ethanol |
| Acidity (pKa) | 38 (conjugate acid)[2] |
| Structure | |
| orthorhombic | |
| Thermochemistry | |
Heat capacity (C)
|
66.15 J/(mol·K) |
Std molar
entropy (S⦵298) |
76.9 J/(mol·K) |
Std enthalpy of
formation (ΔfH⦵298) |
-118.8 kJ/mol |
Gibbs free energy (ΔfG⦵)
|
-59 kJ/mol |
| Hazards | |
| NFPA 704 (fire diamond) | |
| Flash point | 4.44 °C (39.99 °F; 277.59 K) |
| 450 °C (842 °F; 723 K) | |
| Related compounds | |
Other anions
|
Sodium bis(trimethylsilyl)amide |
Other cations
|
Lithium amide Potassium amide |
Related compounds
|
Ammonia |
Except where otherwise noted, data are given for materials in their standard state (at 25 °C [77 °F], 100 kPa).
| |
सोडियम एमाइड, जिसे साधारणतः सोडामाइड (व्यवस्थित नाम सोडियम एज़ैनाइड) कहा जाता है, रासायनिक सूत्र NaNH2 के साथ अकार्बनिक यौगिक है। यह एक लवण (रसायन) है ,जो सोडियम धनायन और एज़ैनाइड ऋणायन से बना है। यह ठोस, जो जल के प्रति खतरनाक रूप से प्रतिक्रियाशील है, सफेद है, परन्तु निर्माण प्रक्रिया से धातु के लोहे की छोटी मात्रा की उपस्थिति के कारण वाणिज्यिक नमूने साधारणतः भूरे रंग के होते हैं। ऐसी अशुद्धियाँ साधारणतः अभिकर्मक की उपयोगिता को प्रभावित नहीं करती हैं। NaNH2 संगलित अवस्था में बिजली का संचालन करता है, इसकी चालकता समान अवस्था में NaOH के समान होती है। NaNH2 को कार्बनिक संश्लेषण में एक प्रबल क्षार के रूप में व्यापक रूप से नियोजित किया गया है।
तैयारी और संरचना
सोडियम एमाइड अमोनिया गैस के साथ सोडियम की अभिक्रिया से तैयार किया जा सकता है,[3] परन्तु यह साधारणतः एक उत्प्रेरक के रूप में आयरन (III) नाइट्रेट का उपयोग करके द्रव अमोनिया में अभिक्रिया द्वारा तैयार किया जाता है। अभिक्रिया अमोनिया के क्वथनांक पर सबसे तेज होती है, c. -33 डिग्री सेल्सियस। एक इलेक्ट्राइड , [Na(NH3)6]+e−, अभिक्रिया मध्यवर्ती के रूप में निर्मित है।[4]
- 2 Na + 2 NH3 → 2 NaNH2 + H2
NaNH2 एक लवण जैसी सामग्री है और इस तरह, एक अनंत बहुलक के रूप में क्रिस्टलीकृत होती है।[5] सोडियम के बारे में ज्यामिति चतुष्फलकीय है।[6] अमोनिया में, [Na(NH3)6]+ और NH−2 आयन की उपस्थिति के अनुरूप NaNH2 प्रवाहकीय विलयन बनाता है।
उपयोग करता है
सोडियम एमाइड मुख्य रूप से कार्बनिक रसायन शास्त्र में एक प्रबल क्षार के रूप में प्रयोग किया जाता है, प्राय: द्रव अमोनिया विलयन में। यह अमोनिया (द्रव या गैसीय) के सुखाने के लिए पसंद का अभिकर्मक है, सोडियम एमाइड के उपयोग का एक मुख्य लाभ यह है कि यह मुख्य रूप से न्यूक्लियोफाइल के रूप में कार्य करता है। इंडिगो डाई के औद्योगिक उत्पादन में, सोडियम एमाइड अत्यधिक मूल मिश्रण का एक घटक है जो N-फेनिलग्लिसिन के चक्रीकरण को प्रेरित करता है। अभिक्रिया अमोनिया का उत्पादन करती है, जिसे साधारणतः पुनर्नवीनीकरण किया जाता है।[7]
डीहाइड्रोहैलोजनीकरण
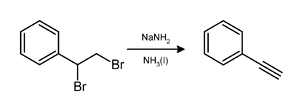
सोडियम एमाइड कार्बन-कार्बन त्रिक आबंध देने के लिए एक संनिधि डाइब्रोमोएल्केन से हाइड्रोजन ब्रोमाइड के दो समकक्षों के नुकसान को प्रेरित करता है। जैसा कि फेनिलएसिटिलीन तैयारी में होता है। [8] साधारणतः सोडियम एमाइड के दो समतुल्य वांछित ऐल्कीन उत्पन्न करते हैं। एक अंत्य एल्काइन की तैयारी में तीन समतुल्य आवश्यक हैं क्योंकि परिणामी ऐल्कीन का टर्मिनल CH क्षार के बराबर मात्रा में प्रोटोनेट करता है।
हाइड्रोजन क्लोराइड और इथेनॉल को भी इस प्रकार समाप्त किया जा सकता है,[9] जैसा कि 1-एथॉक्सी-1-ब्यूटाइन बनाने में होता है।[10]
चक्रीय अभिक्रियाएँ
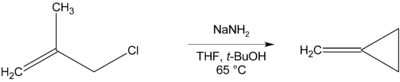
जहां कोई β-हाइड्रोजन समाप्त नहीं होता है, चक्रीय यौगिकों का निर्माण किया जा सकता है, जैसा कि नीचे मेथिलीनसाइक्लोप्रोपेन की विरचना में होता है।[11]
साइक्लोप्रोपीन,[12] एज़िरिडाइन्स [13] और साइक्लोब्यूटेन[14] इसी प्रकार बन सकता है।
कार्बन और नाइट्रोजन अम्ल का अवक्षेपण
द्रव अमोनिया में सोडियम एमाइड द्वारा अवक्षेपित किए जा सकने वाले कार्बन अम्ल में अंतक एल्काइन्स [15] मिथाइल कीटोन्स, [16]साइक्लोहेक्सानोन,[17] फेनिलएसेटिक अम्ल और इसके व्युत्पन्न [18] और डाइफेनिलमीथेन साम्मिलित है। द्विऋणायन बनाने के लिए।[19] एसिटाइलैसटोन दो प्रोटॉन बाहर निकल देता है।[20] सोडियम एमाइड इण्डोल और पाइपरिडाइन [21] को भी अवक्षेपित [22] करेगा ।
संबंधित गैर-नाभिकरागी क्षार
यद्यपि यह अमोनिया के अतिरिक्त विलयन में अपूर्णतः घुलनशील है। इसके उपयोग को संबंधित अभिकर्मकों सोडियम हाइड्राइड, सोडियम bis (ट्राइमिथाइलसिइल) एमाइड (NaHMDS) और लिथियम डायसोप्रोपाइलमाइड (LDA) द्वारा प्रतिस्थापित किया गया है।
अन्य अभिक्रियाएँ
- ऑर्थोडेप्रोटोनेशन के साथ पुनर्व्यवस्थापन[23]
- ऑक्सीरेन संश्लेषण[24]
- इण्डोल संश्लेषण[25]
- चिचिबाबिन अभिक्रिया
सुरक्षा
सोडियम एमाइड जल के संपर्क में प्रबल रूप से विघटित हो जाता है, अमोनिया और सोडियम हाइड्रॉक्साइड का उत्पादन करता है:
- NaNH2 + H2O → NH3 + NaOH
जब ऑक्सीजन में जलाया जाता है, तो यह नाइट्रोजन ऑक्साइड के साथ सोडियम ऑक्साइड (जो उत्पादित जल के साथ अभिक्रिया करता है, सोडियम हाइड्रॉक्साइड देता है) देगा:
- 4 NaNH2 + 5 O2 → 4 NaOH + 4 NO + 2 H2O
- 4 NaNH2 + 7 O2 → 4 NaOH + 4 NO2 + 2 H2O
सीमित मात्रा में वायु और नमी की उपस्थिति में, जैसे खराब बंद कंटेनर में, पेरोक्साइड के विस्फोटक मिश्रण बन सकते हैं।[26] यह ठोस के पीले या भूरे रंग के साथ होता है। जैसे, सोडियम एमाइड को एक अक्रिय गैस के वातावरण के तहत कसकर बंद कंटेनर में संग्रहित किया जाना है। सोडियम एमाइड के नमूने जो पीले या भूरे रंग के होते हैं, विस्फोट जोखिम का प्रतिनिधित्व करते हैं।[27]
संदर्भ
- ↑ IUPAC, Compendium of Chemical Terminology, 2nd ed. (the "Gold Book") (1997). Online corrected version: (2006–) "amides". doi:10.1351/goldbook.A00266
- ↑ Buncel, E.; Menon, B. (1977). "Carbanion mechanisms: VII. Metallation of hydrocarbon acids by potassium amide and potassium methylamide in tetrahydrofuran and the relative hydride acidities". Journal of Organometallic Chemistry. 141 (1): 1–7. doi:10.1016/S0022-328X(00)90661-2.
- ↑ Bergstrom, F. W. (1955). "Sodium amide". Organic Syntheses.; Collective Volume, vol. 3, p. 778
- ↑ Greenlee, K. W.; Henne, A. L. (1946). "Sodium Amide". अकार्बनिक संश्लेषण. अकार्बनिक संश्लेषण. Vol. 2. pp. 128–135. doi:10.1002/9780470132333.ch38. ISBN 9780470132333.
- ↑ Zalkin, A.; Templeton, D. H. (1956). "सोडियम एमाइड की क्रिस्टल संरचना". Journal of Physical Chemistry. 60 (6): 821–823. doi:10.1021/j150540a042. hdl:2027/mdp.39015086484659.
- ↑ Wells, A. F. (1984). संरचनात्मक अकार्बनिक रसायन. Oxford: Clarendon Press. ISBN 0-19-855370-6.
- ↑ L. Lange, W. Treibel "Sodium Amide" in Ullmann's Encyclopedia of Industrial Chemistry 2005, Wiley-VCH, Weinheim. doi:10.1002/14356007.a24_267
- ↑ Campbell, K. N.; Campbell, B. K. (1950). "Phenylacetylene". Organic Syntheses. 30: 72.
{{cite journal}}: CS1 maint: multiple names: authors list (link); Collective Volume, vol. 4, p. 763 - ↑ Jones, E. R. H.; Eglinton, G.; Whiting, M. C.; Shaw, B. L. (1954). "Ethoxyacetylene". Organic Syntheses. 34: 46.
{{cite journal}}: CS1 maint: multiple names: authors list (link); Collective Volume, vol. 4, p. 404
Bou, A.; Pericàs, M. A.; Riera, A.; Serratosa, F. (1987). "Dialkoxyacetylenes: di-tert-butoxyethyne, a valuable synthetic intermediate". Organic Syntheses. 65: 58.{{cite journal}}: CS1 maint: multiple names: authors list (link); Collective Volume, vol. 8, p. 161
Magriotis, P. A.; Brown, J. T. (1995). "Phenylthioacetylene". Organic Syntheses. 72: 252.{{cite journal}}: CS1 maint: multiple names: authors list (link); Collective Volume, vol. 9, p. 656
Ashworth, P. J.; Mansfield, G. H.; Whiting, M. C. (1955). "2-Butyn-1-ol". Organic Syntheses. 35: 20.{{cite journal}}: CS1 maint: multiple names: authors list (link); Collective Volume, vol. 4, p. 128 - ↑ Newman, M. S.; Stalick, W. M. (1977). "1-Ethoxy-1-butyne". Organic Syntheses. 57: 65.
{{cite journal}}: CS1 maint: multiple names: authors list (link); Collective Volume, vol. 6, p. 564 - ↑ Salaun, J. R.; Champion, J.; Conia, J. M. (1977). "Cyclobutanone from methylenecyclopropane via oxaspiropentane". Organic Syntheses. 57: 36.
{{cite journal}}: CS1 maint: multiple names: authors list (link); Collective Volume, vol. 6, p. 320 - ↑ Nakamura, M.; Wang, X. Q.; Isaka, M.; Yamago, S.; Nakamura, E. (2003). "Synthesis and (3+2)-cycloaddition of a 2,2-dialkoxy-1-methylenecyclopropane: 6,6-dimethyl-1-methylene-4,8-dioxaspiro(2.5)octane and cis-5-(5,5-dimethyl-1,3-dioxan-2-ylidene)hexahydro-1(2H)-pentalen-2-one". Organic Syntheses. 80: 144.
{{cite journal}}: CS1 maint: multiple names: authors list (link) - ↑ Bottini, A. T.; Olsen, R. E. (1964). "N-Ethylallenimine". Organic Syntheses. 44: 53.
{{cite journal}}: CS1 maint: multiple names: authors list (link); Collective Volume, vol. 5, p. 541 - ↑ Skorcz, J. A.; Kaminski, F. E. (1968). "1-Cyanobenzocyclobutene". Organic Syntheses. 48: 55.
{{cite journal}}: CS1 maint: multiple names: authors list (link); Collective Volume, vol. 5, p. 263 - ↑ Saunders, J. H. (1949). "1-Ethynylcyclohexanol". Organic Syntheses. 29: 47.; Collective Volume, vol. 3, p. 416
Peterson, P. E.; Dunham, M. (1977). "(Z)-4-Chloro-4-hexenyl trifluoroacetate". Organic Syntheses. 57: 26.{{cite journal}}: CS1 maint: multiple names: authors list (link); Collective Volume, vol. 6, p. 273
Kauer, J. C.; Brown, M. (1962). "Tetrolic acid". Organic Syntheses. 42: 97.{{cite journal}}: CS1 maint: multiple names: authors list (link); Collective Volume, vol. 5, p. 1043 - ↑ Coffman, D. D. (1940). "Dimethylethynylcarbinol". Organic Syntheses. 20: 40.; Collective Volume, vol. 3, p. 320Hauser, C. R.; Adams, J. T.; Levine, R. (1948). "Diisovalerylmethane". Organic Syntheses. 28: 44.
{{cite journal}}: CS1 maint: multiple names: authors list (link); Collective Volume, vol. 3, p. 291 - ↑ Vanderwerf, C. A.; Lemmerman, L. V. (1948). "2-Allylcyclohexanone". Organic Syntheses. 28: 8.
{{cite journal}}: CS1 maint: multiple names: authors list (link); Collective Volume, vol. 3, p. 44 - ↑ Hauser, C. R.; Dunnavant, W. R. (1960). "α,β-Diphenylpropionic acid". Organic Syntheses. 40: 38.
{{cite journal}}: CS1 maint: multiple names: authors list (link); Collective Volume, vol. 5, p. 526
Kaiser, E. M.; Kenyon, W. G.; Hauser, C. R. (1967). "Ethyl 2,4-diphenylbutanoate". Organic Syntheses. 47: 72.{{cite journal}}: CS1 maint: multiple names: authors list (link); Collective Volume, vol. 5, p. 559
Wawzonek, S.; Smolin, E. M. (1951). "α,β-Diphenylcinnamonitrile". Organic Syntheses. 31: 52.{{cite journal}}: CS1 maint: multiple names: authors list (link); Collective Volume, vol. 4, p. 387 - ↑ Murphy, W. S.; Hamrick, P. J.; Hauser, C. R. (1968). "1,1-Diphenylpentane". Organic Syntheses. 48: 80.
{{cite journal}}: CS1 maint: multiple names: authors list (link); Collective Volume, vol. 5, p. 523 - ↑ Hampton, K. G.; Harris, T. M.; Hauser, C. R. (1971). "Phenylation of diphenyliodonium chloride: 1-phenyl-2,4-pentanedione". Organic Syntheses. 51: 128.
{{cite journal}}: CS1 maint: multiple names: authors list (link); Collective Volume, vol. 6, p. 928
Hampton, K. G.; Harris, T. M.; Hauser, C. R. (1967). "2,4-Nonanedione". Organic Syntheses. 47: 92.{{cite journal}}: CS1 maint: multiple names: authors list (link); Collective Volume, vol. 5, p. 848 - ↑ Potts, K. T.; Saxton, J. E. (1960). "1-Methylindole". Organic Syntheses. 40: 68.
{{cite journal}}: CS1 maint: multiple names: authors list (link); Collective Volume, vol. 5, p. 769 - ↑ Bunnett, J. F.; Brotherton, T. K.; Williamson, S. M. (1960). "N-β-Naphthylpiperidine". Organic Syntheses. 40: 74.
{{cite journal}}: CS1 maint: multiple names: authors list (link); Collective Volume, vol. 5, p. 816 - ↑ Brazen, W. R.; Hauser, C. R. (1954). "2-Methylbenzyldimethylamine". Organic Syntheses. 34: 61.
{{cite journal}}: CS1 maint: multiple names: authors list (link); Collective Volume, vol. 4, p. 585 - ↑ Allen, C. F. H.; VanAllan, J. (1944). "Phenylmethylglycidic ester". Organic Syntheses. 24: 82.
{{cite journal}}: CS1 maint: multiple names: authors list (link); Collective Volume, vol. 3, p. 727 - ↑ Allen, C. F. H.; VanAllan, J. (1942). "2-Methylindole". Organic Syntheses. 22: 94.
{{cite journal}}: CS1 maint: multiple names: authors list (link); Collective Volume, vol. 3, p. 597 - ↑ Clark, Donald E (2001). "पेरोक्साइड और पेरोक्साइड बनाने वाले यौगिक". Chemical Health and Safety. 8 (5): 12–22. doi:10.1016/S1074-9098(01)00247-7. ISSN 1074-9098.
- ↑ "सोडियम एमाइड एसओपी". Princeton.