फॉर्मेट: Difference between revisions
(Created page with "{{Short description|Salt or ester of formic acid}} {{Chembox | ImageFile1 =Formate.svg | ImageFile1_Ref = {{chemboximage|correct|??}} | ImageSize1 = 200 | ImageName1 = Stereo...") |
|
(No difference)
| |
Revision as of 14:59, 22 June 2023
| |||
|
| |||
| Names | |||
|---|---|---|---|
| Preferred IUPAC name
Formate | |||
| Systematic IUPAC name
Methanoate | |||
| Other names
Formylate
Methylate Isocarbonite Carbonite(1-) Hydrogencarboxylate Metacarbonoate Oxocarbinate Oxomethyl oxide ion Oxomethoxide | |||
| Identifiers | |||
3D model (JSmol)
|
|||
| ChemSpider | |||
| MeSH | Formates | ||
PubChem CID
|
|||
| UNII | |||
| |||
| Properties | |||
| HCOO− or HCO− 2 | |||
| Molar mass | 45.017 g mol−1 | ||
| Conjugate acid | Formic acid | ||
Except where otherwise noted, data are given for materials in their standard state (at 25 °C [77 °F], 100 kPa).
| |||
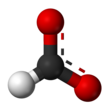
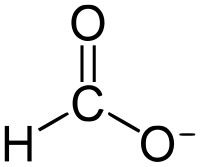
Formate (IUPAC नाम: मीथेनोएट) फार्मिक अम्ल का संयुग्मी क्षार है। Formate एक आयन है (HCO−2) या इसके डेरिवेटिव जैसे फॉर्मिक एसिड का एस्टर। लवण और एस्टर आमतौर पर रंगहीन होते हैं।[1]
मूल बातें
पानी में घुलने पर, फॉर्मिक एसिड फॉर्मेट में परिवर्तित हो जाता है:
- HCO2H → HCO−2 + H+
फॉर्मेट एक प्लानर आयन है। दो ऑक्सीजन परमाणु समतुल्य हैं और आंशिक ऋणात्मक आवेश धारण करते हैं। शेष C-H बंध अम्लीय नहीं होता है।
जैव रसायन
- जीवित प्रणालियों में फॉर्मेट एक सामान्य सी-1 स्रोत है। यह कोलीन, सेरीन और सार्कोसिन सहित कई अग्रदूतों से बनता है। यह कुछ न्यूक्लिक अम्लों के जैवसंश्लेषण में C-1 स्रोत प्रदान करता है। कुछ स्टेरोल्स के डिमिथाइलेशन में फॉर्मेट (या फॉर्मिक एसिड) एक छोड़ने वाला समूह है।[2] इन रूपांतरणों को O का उपयोग करके एरोमाटेज़ एंजाइम द्वारा उत्प्रेरित किया जाता है2 ऑक्सीडेंट के रूप में। विशिष्ट रूपांतरणों में टेस्टोस्टेरोन से एस्ट्राडियोल और androstenedione से estrone शामिल हैं।[3] Desulfovibrio gigas से एंजाइम फॉर्मेट डिहाइड्रोजनेज द्वारा फॉर्मेट को विपरीत रूप से ऑक्सीकृत किया जाता है:[4]
- HCO−2 → CO2 + H+ + 2 e−
फॉर्मेट एस्टर
फ़ॉर्मेट एस्टर का सूत्र HCOOR (वैकल्पिक रूप से सूत्र ROC(O)H या RO लिखने का तरीका है2सीएच)। फार्मिक अम्ल में एल्कोहल के घुलने पर कई स्वतःस्फूर्त रूप से बनते हैं।
सबसे महत्वपूर्ण फॉर्मेट एस्टर मिथाइल फॉर्मेट है, जो फॉर्मिक एसिड के रास्ते में एक मध्यवर्ती के रूप में उत्पादित होता है। मेथनॉल और कार्बन मोनोआक्साइड एक मजबूत आधार की उपस्थिति में प्रतिक्रिया करते हैं, जैसे सोडियम मेथॉक्साइड:[1]: मिथाइल फॉर्मेट का हाइड्रोलिसिस फार्मिक एसिड देता है और मेथनॉल को पुन: उत्पन्न करता है:
उद्योग में कई अनुप्रयोगों के लिए फॉर्मिक एसिड का उपयोग किया जाता है।
फॉर्मेट एस्टर अक्सर सुगंधित होते हैं या विशिष्ट गंध होते हैं। अधिक सामान्य एसीटेट एस्टर की तुलना में, फॉर्मेट एस्टर का व्यावसायिक रूप से कम उपयोग किया जाता है क्योंकि वे कम स्थिर होते हैं।[5] कुछ कन्फेक्शनरी में एथिल फॉर्मेट पाया जाता है।[1]
फॉर्मेट लवण
फॉर्मेट लवण का सूत्र M(O2सीएच) (एच2ओ)x. इस तरह के लवण डीकार्बाक्सिलेशन के लिए प्रवण होते हैं। उदाहरण के लिए, हाइड्रेटेड निकेल नी की कमी के साथ लगभग 200 डिग्री सेल्सियस पर डीकार्बाक्सिलेट करता है2+ निकेल धातु को बारीक चूर्ण करने के लिए:
- Ni(HCO2)2(H2O)2 → Ni + 2 CO2 + 2 H2O + H2
इस तरह के महीन चूर्ण हाइड्रोजनीकरण उत्प्रेरक के रूप में उपयोगी होते हैं।[1]
उदाहरण
* एथिल फॉर्मेट, सीएच3चौधरी2(एचसीओओ)
- सोडियम फॉर्मेट, ना (एचसीओओ)
- पोटेशियम तैयार करें , के (एचसीओओ)
- क्रूसिबल बनाओ , सीएस (एचसीओओ); देखें सीज़ियम#पेट्रोलियम की खोज|सीज़ियम: पेट्रोलियम की खोज
- मिथाइल फॉर्मेट, सीएच3(एचसीओओ)
- मिथाइल क्लोरोफॉर्मेट, सी एच3OCOCl
- ट्राइथाइल ऑर्थोफोर्मेट
- ट्राइमिथाइल ऑर्थोफोर्मेट, सी4H10O3
- फिनाइल फॉर्मेट HCOOC6H5
- एमिल फॉर्मेट
संदर्भ
- ↑ 1.0 1.1 1.2 1.3 औद्योगिक रसायन विज्ञान 2002, विले-वीसीएच, वेनहेम के उल्मन के विश्वकोश में वर्नर रुटेमैन और हेंज किज़्का फॉर्मिक एसिड। doi:10.1002/14356007.a12_013
- ↑ Pietzke, Matthias; Meiser, Johannes; Vazquez, Alexei (2020). "स्वास्थ्य और रोग में मेटाबोलिज्म को फॉर्मेट करें". Molecular Metabolism. 33: 23–37. doi:10.1016/j.molmet.2019.05.012. PMC 7056922. PMID 31402327.
- ↑ Lephart, E. D. (1996). "A Review of Brain Aromatase Cytochrome P450". Brain Res. Rev. 22 (1): 1–26. doi:10.1016/0165-0173(96)00002-1. PMID 8871783. S2CID 11987113.
- ↑ T. Reda, C. M. Plugge, N. J. Abram and J. Hirst, "Reversible interconversion of carbon dioxide and formate by an electroactive enzyme", PNAS 2008 105, 10654–10658. doi:10.1073/pnas.0801290105
- ↑ Johannes Panten and Horst Surburg "Flavors and Fragrances, 2. Aliphatic Compounds" in Ullmann's Encyclopedia of Industrial Chemistry, 2015, Wiley-VCH, Weinheim.doi:10.1002/14356007.t11_t01