न्यूक्लियोफिलिक प्रतिस्थापन: Difference between revisions
No edit summary |
No edit summary |
||
| Line 4: | Line 4: | ||
:<math chem>\text{Nuc}\mathbf{:} + \ce{R-LG -> R-Nuc} + \text{LG}\mathbf{:}</math> | :<math chem>\text{Nuc}\mathbf{:} + \ce{R-LG -> R-Nuc} + \text{LG}\mathbf{:}</math> | ||
न्यूक्लियोफाइल (Nuc) से इलेक्ट्रॉन युग्म (:) विक्षनरी:हमला क्रिया सब्सट्रेट ({{chem2|R\sLG}}) और इसके साथ बंध जाता है। इसके साथ ही, छोड़ने वाला समूह (LG) एक इलेक्ट्रॉन जोड़ी के साथ प्रस्थान करता है। इस परिस्थिति में प्रमुख उत्पाद है {{chem2|R\sNuc}}. न्यूक्लियोफाइल विद्युत रूप से तटस्थ या | न्यूक्लियोफाइल (Nuc) से इलेक्ट्रॉन युग्म (:) विक्षनरी:हमला क्रिया सब्सट्रेट ({{chem2|R\sLG}}) और इसके साथ बंध जाता है। इसके साथ ही, छोड़ने वाला समूह (LG) एक इलेक्ट्रॉन जोड़ी के साथ प्रस्थान करता है। इस परिस्थिति में प्रमुख उत्पाद है {{chem2|R\sNuc}}. न्यूक्लियोफाइल विद्युत रूप से तटस्थ या ऋणात्मक रूप से चार्ज हो सकता है, जबकि सब्सट्रेट सामान्यतः तटस्थ या घनात्मक रूप से चार्ज होता है। | ||
न्यूक्लियोफिलिक प्रतिस्थापन का एक उदाहरण बुनियादी परिस्थितियों में [[एल्काइल]] [[ब्रोमाइड]], R-Br का [[हाइड्रोलिसिस]] है, जहां हमलावर न्यूक्लियोफाइल [[ हाइड्रॉकसिल ]] है ({{chem2|OH-}}) और छोड़ने वाला समूह ब्रोमाइड है ({{chem2|Br-}}). | न्यूक्लियोफिलिक प्रतिस्थापन का एक उदाहरण बुनियादी परिस्थितियों में [[एल्काइल]] [[ब्रोमाइड]], R-Br का [[हाइड्रोलिसिस]] है, जहां हमलावर न्यूक्लियोफाइल [[ हाइड्रॉकसिल ]] है ({{chem2|OH-}}) और छोड़ने वाला समूह ब्रोमाइड है ({{chem2|Br-}}). | ||
:<chem>R-Br + OH- -> R-OH + Br-</chem> | :<chem>R-Br + OH- -> R-OH + Br-</chem> | ||
[[कार्बनिक रसायन विज्ञान]] में न्यूक्लियोफिलिक प्रतिस्थापन प्रतिक्रियाएं आम हैं। न्यूक्लियोफाइल प्रायः [[संतृप्त और असंतृप्त यौगिक]]ों स्निग्ध कार्बन पर हमला करते हैं। | [[कार्बनिक रसायन विज्ञान]] में न्यूक्लियोफिलिक प्रतिस्थापन प्रतिक्रियाएं आम हैं। न्यूक्लियोफाइल प्रायः [[संतृप्त और असंतृप्त यौगिक]]ों स्निग्ध कार्बन पर हमला करते हैं। कम लेकिन कई बार, वे सुगंधित या असंतृप्त कार्बन पर हमला कर सकते हैं।<ref>L. G. Wade, ''Organic Chemistry'', 5th ed., Prentice Hall, Upper Saddle River, New Jersey, 2003.</ref> | ||
| Line 15: | Line 15: | ||
=== S<sub>N</sub>1 और S<sub>N</sub>2 प्रतिक्रियाएँ === | === S<sub>N</sub>1 और S<sub>N</sub>2 प्रतिक्रियाएँ === | ||
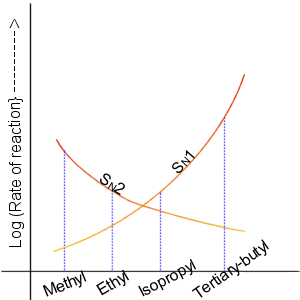
[[File:Sn2 Sn1 Graph en.png|thumb|300px| | [[File:Sn2 Sn1 Graph en.png|thumb|300px|विभिन्न एल्काइल हैलाइडों की सापेक्ष प्रतिक्रिया दर्शाने वाला एक ग्राफ S<sub>N</sub>1 और S<sub>N</sub>2 प्रतिक्रियाएं (तालिका 1 भी देखें)।]]1935 में, एडवर्ड डी. ह्यूजेस और [[क्रिस्टोफर केल्क इंगोल्ड]] ने [[एल्काइल हैलाइड]]्स और संबंधित यौगिकों की न्यूक्लियोफिलिक प्रतिस्थापन प्रतिक्रियाओं का अध्ययन किये थे। उन्होंने प्रस्तावित किया कि दो मुख्य तंत्र काम कर रहे हैं, दोनों एक-दूसरे के साथ प्रतिस्पर्धा कर रहे हैं। दो मुख्य तंत्र S<sub>N</sub>1 प्रतिक्रिया और S<sub>N</sub>2 प्रतिक्रिया थे| S<sub>N</sub>2 प्रतिक्रिया, जहां ''S'' का अर्थ प्रतिस्थापन है, ''N'' का अर्थ न्यूक्लियोफिलिक है, और संख्या प्रतिक्रिया के क्रम (रसायन विज्ञान) का प्रतिनिधित्व करती है।<ref>S. R. Hartshorn, ''Aliphatic Nucleophilic Substitution'', Cambridge University Press, London, 1973. {{ISBN|0-521-09801-7}}</ref> | ||
S<sub>N</sub>2 प्रतिक्रिया में, न्यूक्लियोफाइल का जुड़ाव और समूह छोड़ने का उन्मूलन एक साथ होता है (यानी एक ठोस प्रतिक्रिया)। S<sub>N</sub>2 तब होता है जब केंद्रीय कार्बन परमाणु न्यूक्लियोफाइल के लिए आसानी से पहुंच योग्य होता है।<ref>''Introducing Aliphatic Substitution with a Discovery Experiment Using Competing Electrophiles'' Timothy P. Curran, Amelia J. Mostovoy, Margaret E. Curran, and Clara Berger Journal of Chemical Education 2016 93 (4), 757-761 {{doi|10.1021/acs.jchemed.5b00394}} </ref> | |||
{| align="center" class="wikitable" | {| align="center" class="wikitable" | ||
|- | |- | ||
!colspan="2"| | !colspan="2"|कार्बन पर न्यूक्लियोफिलिक प्रतिस्थापन | ||
|- | |- | ||
|bgcolor="#FFFFFF"| [[File:Sn2EtCl+bromide.png|340px|mechanism]] | |bgcolor="#FFFFFF"| [[File:Sn2EtCl+bromide.png|340px|mechanism]] | ||
| Line 26: | Line 26: | ||
|bgcolor="#FFFFFF"| [[File:Sn2_reaction.gif|400px|SN2 reaction of CH3Cl and Cl-]] | |bgcolor="#FFFFFF"| [[File:Sn2_reaction.gif|400px|SN2 reaction of CH3Cl and Cl-]] | ||
|- | |- | ||
| [[SN2|S<sub>N</sub>2 | | [[SN2|S<sub>N</sub>2 तंत्र]] | ||
|} | |} | ||
S<sub>N</sub>2 प्रतिक्रियाएँ में, कुछ स्थितियाँ हैं जो प्रतिक्रिया की दर को प्रभावित करती हैं। सबसे पहले,2 में S<sub>N</sub>2 का तात्पर्य है कि पदार्थों की दो सांद्रताएँ हैं जो प्रतिक्रिया की दर को प्रभावित करती हैं: सब्सट्रेट (उप) और न्यूक्लियोफाइल। इस प्रतिक्रिया के लिए दर समीकरण दर=k[Sub][Nuc] होगा। S<sub>N</sub>2 प्रतिक्रिया के लिए, एक प्रोटिक_सॉल्वेंट सर्वोत्तम है, जैसे एसीटोन, डीएमएफ, या डीएमएसओ। एप्रोटिक सॉल्वैंट्स प्रोटॉन नहीं जोड़ते (एच<sup>+</sup>आयनों) घोल में; यदि प्रोटॉन एस में मौजूद थे<sub>N</sub>2 प्रतिक्रियाएं, वे न्यूक्लियोफाइल के साथ प्रतिक्रिया करेंगी और प्रतिक्रिया दर को गंभीर रूप से सीमित कर देंगी। चूँकि यह प्रतिक्रिया एक चरण में होती है, [[स्थैतिक प्रभाव]] प्रतिक्रिया की गति को बढ़ाते हैं। मध्यवर्ती चरण में, न्यूक्लियोफाइल छोड़ने वाले समूह से 185 डिग्री है और उत्पाद बनाने के लिए न्यूक्लियोफाइल बॉन्ड के रूप में स्टीरियोकैमिस्ट्री को उलट दिया जाता है। इसके अलावा, क्योंकि मध्यवर्ती आंशिक रूप से न्यूक्लियोफाइल और छोड़ने वाले समूह से जुड़ा हुआ है, सब्सट्रेट के लिए खुद को पुनर्व्यवस्थित करने का कोई समय नहीं है: न्यूक्लियोफाइल उसी कार्बन से बंधेगा जिससे छोड़ने वाला समूह जुड़ा हुआ था। प्रतिक्रिया दर को प्रभावित करने वाला एक अंतिम कारक न्यूक्लियोफिलिसिटी है; न्यूक्लियोफाइल को हाइड्रोजन के अलावा किसी अन्य परमाणु पर हमला करना चाहिए। | |||
इसके विपरीत एस<sub>N</sub>1 प्रतिक्रिया में दो चरण शामिल होते हैं। एस<sub>N</sub>1 प्रतिक्रियाएं तब महत्वपूर्ण होती हैं जब सब्सट्रेट का केंद्रीय कार्बन परमाणु भारी समूहों से घिरा होता है, क्योंकि ऐसे समूह एस के साथ स्टेरिक रूप से हस्तक्षेप करते हैं<sub>N</sub>2 प्रतिक्रिया (ऊपर चर्चा की गई) और क्योंकि अत्यधिक प्रतिस्थापित कार्बन एक स्थिर [[कार्बोकेशन]] बनाता है। | इसके विपरीत एस<sub>N</sub>1 प्रतिक्रिया में दो चरण शामिल होते हैं। एस<sub>N</sub>1 प्रतिक्रियाएं तब महत्वपूर्ण होती हैं जब सब्सट्रेट का केंद्रीय कार्बन परमाणु भारी समूहों से घिरा होता है, क्योंकि ऐसे समूह एस के साथ स्टेरिक रूप से हस्तक्षेप करते हैं<sub>N</sub>2 प्रतिक्रिया (ऊपर चर्चा की गई) और क्योंकि अत्यधिक प्रतिस्थापित कार्बन एक स्थिर [[कार्बोकेशन]] बनाता है। | ||
Revision as of 17:21, 30 September 2023
रसायन विज्ञान में, न्यूक्लियोफिलिक प्रतिस्थापन रासायनिक प्रतिक्रियाओं का एक वर्ग है जिसमें एक इलेक्ट्रॉन-समृद्ध रासायनिक प्रजाति (न्यूक्लियोफाइल के रूप में जाना जाता है) एक अन्य इलेक्ट्रॉन-कमी वाले अणु (इलेक्ट्रोफाइल के रूप में जाना जाता है) के भीतर एक कार्यात्मक समूह को प्रतिस्थापित करता है। जिस अणु में इलेक्ट्रोफाइल और छोड़ने वाला कार्यात्मक समूह होता है उसे सबस्ट्रेट (रसायन विज्ञान) कहा जाता है।[1][2] प्रतिक्रिया का सबसे सामान्य रूप निम्नलिखित के रूप में दिया जा सकता है:
न्यूक्लियोफाइल (Nuc) से इलेक्ट्रॉन युग्म (:) विक्षनरी:हमला क्रिया सब्सट्रेट (R−LG) और इसके साथ बंध जाता है। इसके साथ ही, छोड़ने वाला समूह (LG) एक इलेक्ट्रॉन जोड़ी के साथ प्रस्थान करता है। इस परिस्थिति में प्रमुख उत्पाद है R−Nuc. न्यूक्लियोफाइल विद्युत रूप से तटस्थ या ऋणात्मक रूप से चार्ज हो सकता है, जबकि सब्सट्रेट सामान्यतः तटस्थ या घनात्मक रूप से चार्ज होता है।
न्यूक्लियोफिलिक प्रतिस्थापन का एक उदाहरण बुनियादी परिस्थितियों में एल्काइल ब्रोमाइड, R-Br का हाइड्रोलिसिस है, जहां हमलावर न्यूक्लियोफाइल हाइड्रॉकसिल है (OH−) और छोड़ने वाला समूह ब्रोमाइड है (Br−).
कार्बनिक रसायन विज्ञान में न्यूक्लियोफिलिक प्रतिस्थापन प्रतिक्रियाएं आम हैं। न्यूक्लियोफाइल प्रायः संतृप्त और असंतृप्त यौगिकों स्निग्ध कार्बन पर हमला करते हैं। कम लेकिन कई बार, वे सुगंधित या असंतृप्त कार्बन पर हमला कर सकते हैं।[3]
संतृप्त कार्बन केंद्र
SN1 और SN2 प्रतिक्रियाएँ
1935 में, एडवर्ड डी. ह्यूजेस और क्रिस्टोफर केल्क इंगोल्ड ने एल्काइल हैलाइड्स और संबंधित यौगिकों की न्यूक्लियोफिलिक प्रतिस्थापन प्रतिक्रियाओं का अध्ययन किये थे। उन्होंने प्रस्तावित किया कि दो मुख्य तंत्र काम कर रहे हैं, दोनों एक-दूसरे के साथ प्रतिस्पर्धा कर रहे हैं। दो मुख्य तंत्र SN1 प्रतिक्रिया और SN2 प्रतिक्रिया थे| SN2 प्रतिक्रिया, जहां S का अर्थ प्रतिस्थापन है, N का अर्थ न्यूक्लियोफिलिक है, और संख्या प्रतिक्रिया के क्रम (रसायन विज्ञान) का प्रतिनिधित्व करती है।[4]
SN2 प्रतिक्रिया में, न्यूक्लियोफाइल का जुड़ाव और समूह छोड़ने का उन्मूलन एक साथ होता है (यानी एक ठोस प्रतिक्रिया)। SN2 तब होता है जब केंद्रीय कार्बन परमाणु न्यूक्लियोफाइल के लिए आसानी से पहुंच योग्य होता है।[5]
| कार्बन पर न्यूक्लियोफिलिक प्रतिस्थापन | |
|---|---|

| |

| |
| SN2 तंत्र | |
SN2 प्रतिक्रियाएँ में, कुछ स्थितियाँ हैं जो प्रतिक्रिया की दर को प्रभावित करती हैं। सबसे पहले,2 में SN2 का तात्पर्य है कि पदार्थों की दो सांद्रताएँ हैं जो प्रतिक्रिया की दर को प्रभावित करती हैं: सब्सट्रेट (उप) और न्यूक्लियोफाइल। इस प्रतिक्रिया के लिए दर समीकरण दर=k[Sub][Nuc] होगा। SN2 प्रतिक्रिया के लिए, एक प्रोटिक_सॉल्वेंट सर्वोत्तम है, जैसे एसीटोन, डीएमएफ, या डीएमएसओ। एप्रोटिक सॉल्वैंट्स प्रोटॉन नहीं जोड़ते (एच+आयनों) घोल में; यदि प्रोटॉन एस में मौजूद थेN2 प्रतिक्रियाएं, वे न्यूक्लियोफाइल के साथ प्रतिक्रिया करेंगी और प्रतिक्रिया दर को गंभीर रूप से सीमित कर देंगी। चूँकि यह प्रतिक्रिया एक चरण में होती है, स्थैतिक प्रभाव प्रतिक्रिया की गति को बढ़ाते हैं। मध्यवर्ती चरण में, न्यूक्लियोफाइल छोड़ने वाले समूह से 185 डिग्री है और उत्पाद बनाने के लिए न्यूक्लियोफाइल बॉन्ड के रूप में स्टीरियोकैमिस्ट्री को उलट दिया जाता है। इसके अलावा, क्योंकि मध्यवर्ती आंशिक रूप से न्यूक्लियोफाइल और छोड़ने वाले समूह से जुड़ा हुआ है, सब्सट्रेट के लिए खुद को पुनर्व्यवस्थित करने का कोई समय नहीं है: न्यूक्लियोफाइल उसी कार्बन से बंधेगा जिससे छोड़ने वाला समूह जुड़ा हुआ था। प्रतिक्रिया दर को प्रभावित करने वाला एक अंतिम कारक न्यूक्लियोफिलिसिटी है; न्यूक्लियोफाइल को हाइड्रोजन के अलावा किसी अन्य परमाणु पर हमला करना चाहिए।
इसके विपरीत एसN1 प्रतिक्रिया में दो चरण शामिल होते हैं। एसN1 प्रतिक्रियाएं तब महत्वपूर्ण होती हैं जब सब्सट्रेट का केंद्रीय कार्बन परमाणु भारी समूहों से घिरा होता है, क्योंकि ऐसे समूह एस के साथ स्टेरिक रूप से हस्तक्षेप करते हैंN2 प्रतिक्रिया (ऊपर चर्चा की गई) और क्योंकि अत्यधिक प्रतिस्थापित कार्बन एक स्थिर कार्बोकेशन बनाता है।
| Nucleophilic substitution at carbon | |
|---|---|

| |
| SN1 mechanism | |
को यह पसंद हैN2 प्रतिक्रियाएं, ऐसे कई कारक हैं जो एस की प्रतिक्रिया दर को प्रभावित करते हैंN1 प्रतिक्रियाएँ. प्रतिक्रिया दर को प्रभावित करने वाली दो सांद्रता के बजाय, केवल एक ही सब्सट्रेट है। इसके लिए दर समीकरण दर=k[उप] होगा। चूँकि किसी प्रतिक्रिया की दर केवल उसके सबसे धीमे चरण से निर्धारित होती है, जिस दर पर छोड़ने वाला समूह प्रतिक्रिया की गति निर्धारित करता है। इसका मतलब यह है कि छोड़ने वाला समूह जितना बेहतर होगा, प्रतिक्रिया दर उतनी ही तेज़ होगी। एक अच्छा छोड़ने वाला समूह बनाने के लिए एक सामान्य नियम यह है कि संयुग्म आधार जितना कमजोर होगा, छोड़ने वाला समूह उतना ही बेहतर होगा। इस मामले में, हैलोजन सबसे अच्छा छोड़ने वाला समूह बनने जा रहा है, जबकि एमाइन, हाइड्रोजन और अल्केन्स जैसे यौगिक काफी खराब छोड़ने वाले समूह बनने जा रहे हैं। जैसा कि एसN2 प्रतिक्रियाएं स्टेरिक्स, एस से प्रभावित थींN1 प्रतिक्रियाएं कार्बोकेशन से जुड़े भारी समूहों द्वारा निर्धारित की जाती हैं। चूंकि एक मध्यवर्ती है जिसमें वास्तव में एक घनात्मक चार्ज होता है, इससे जुड़े भारी समूह चार्ज के अनुनाद और वितरण के माध्यम से कार्बोकेशन पर चार्ज को स्थिर करने में मदद करने जा रहे हैं। इस मामले में, तृतीयक कार्बोकेशन द्वितीयक की तुलना में तेजी से प्रतिक्रिया करेगा जो प्राथमिक की तुलना में बहुत तेजी से प्रतिक्रिया करेगा। इस कार्बोकेशन मध्यवर्ती के कारण ही उत्पाद में व्युत्क्रमण नहीं होता है। न्यूक्लियोफाइल ऊपर या नीचे से हमला कर सकता है और इसलिए एक रेसमिक उत्पाद बना सकता है। एक प्रोटिक विलायक, पानी और अल्कोहल का उपयोग करना महत्वपूर्ण है, क्योंकि एक एप्रोटिक विलायक मध्यवर्ती पर हमला कर सकता है और अवांछित उत्पाद का कारण बन सकता है। इससे कोई फर्क नहीं पड़ता कि प्रोटिक विलायक से हाइड्रोजन न्यूक्लियोफाइल के साथ प्रतिक्रिया करता है क्योंकि न्यूक्लियोफाइल दर निर्धारण चरण में शामिल नहीं है।
| Table 1. Nucleophilic substitutions on RX (an alkyl halide or equivalent) | |||||||
|---|---|---|---|---|---|---|---|
| Factor | SN1 | SN2 | Comments | ||||
| Kinetics | Rate = k[RX] | Rate = k[RX][Nuc] | |||||
| Primary alkyl | Never unless additional stabilising groups present | Good unless a hindered nucleophile is used | |||||
| Secondary alkyl | Moderate | Moderate | |||||
| Tertiary alkyl | Excellent | Never | Elimination likely if heated or if strong base used | ||||
| Leaving group | Important | Important | For halogens, I > Br > Cl >> F | ||||
| Nucleophilicity | Unimportant | Important | |||||
| Preferred solvent | Polar protic | Polar aprotic | |||||
| Stereochemistry | Racemisation (+ partial inversion possible) | Inversion | |||||
| Rearrangements | Common | Rare | Side reaction | ||||
| Eliminations | Common, especially with basic nucleophiles | Only with heat & basic nucleophiles | Side reaction esp. if heated | ||||
प्रतिक्रियाएँ
कार्बनिक रसायन विज्ञान में इस प्रकार की तंत्र से जुड़ी कई प्रतिक्रियाएं हैं। सामान्य उदाहरणों में शामिल हैं:
- उदाहरण के लिए, हाइड्राइड्स के साथ कार्बनिक कटौती
- हाइड्रोलिसिस प्रतिक्रियाएं जैसे
- वेंकर संश्लेषण, अमीनोअल्कोहल की एक रिंग-क्लोजिंग प्रतिक्रिया।
- फिंकेलस्टीन प्रतिक्रिया, एक हैलाइड विनिमय प्रतिक्रिया। फॉस्फोरस न्यूक्लियोफाइल पर्को प्रतिक्रिया और माइकलिस-अर्बुज़ोव प्रतिक्रिया में दिखाई देते हैं।
- कोल्बे नाइट्राइल संश्लेषण, साइनाइड के साथ एल्काइल हैलाइड की प्रतिक्रिया।
सीमा रेखा तंत्र
तथाकथित सीमा रेखा तंत्र द्वारा होने वाली प्रतिस्थापन प्रतिक्रिया का एक उदाहरण जैसा कि मूल रूप से ह्यूजेस और इंगोल्ड द्वारा अध्ययन किया गया था[6] मेथनॉल में सोडियम मेथॉक्साइड के साथ 1-फिनाइलथाइल क्लोराइड की प्रतिक्रिया है।
 प्रतिक्रिया दर एस के योग से पाई जाती हैN1 और एसN61% (3,5 एम, 70 डिग्री सेल्सियस) के साथ 2 घटक बाद वाले द्वारा होते हैं।
प्रतिक्रिया दर एस के योग से पाई जाती हैN1 और एसN61% (3,5 एम, 70 डिग्री सेल्सियस) के साथ 2 घटक बाद वाले द्वारा होते हैं।
अन्य तंत्र
एस के अलावाN1 और एसN2, अन्य तंत्र ज्ञात हैं, हालांकि वे कम आम हैं। एसएनआई|एसNi तंत्र अल्कोहल (रसायन विज्ञान) के साथ थियोनिल क्लोराइड की प्रतिक्रियाओं में देखा जाता है, और यह S के समान हैN1 सिवाय इसके कि न्यूक्लियोफाइल को छोड़ने वाले समूह के समान तरफ से वितरित किया जाता है।
न्यूक्लियोफिलिक प्रतिस्थापन के साथ एलिलिक पुनर्व्यवस्था भी हो सकती है जैसा कि फेरियर पुनर्व्यवस्था जैसी प्रतिक्रियाओं में देखा जाता है। इस प्रकार के तंत्र को एस कहा जाता हैN1' या एसN2' प्रतिक्रिया (गतिकी पर निर्भर करता है)। उदाहरण के लिए, एलिलिक हैलाइड्स या सल्फोनेट्स के साथ, न्यूक्लियोफाइल छोड़ने वाले समूह वाले कार्बन के स्थान पर γ असंतृप्त कार्बन पर हमला कर सकता है। इसे 2-ब्यूटेन-1-ओएल और 1-ब्यूटेन-3-ओएल का मिश्रण देने के लिए सोडियम हाइड्रॉक्साइड के साथ 1-क्लोरो-2-ब्यूटेन की प्रतिक्रिया में देखा जा सकता है:
Sn1CB तंत्र अकार्बनिक रसायन विज्ञान में प्रकट होता है। प्रतिस्पर्धी तंत्र मौजूद हैं।[7][8] ऑर्गेनोमेटेलिक रसायन विज्ञान में न्यूक्लियोफिलिक अमूर्त प्रतिक्रिया न्यूक्लियोफिलिक प्रतिस्थापन तंत्र के साथ होती है।
असंतृप्त कार्बन केंद्र
एस के माध्यम से न्यूक्लियोफिलिक प्रतिस्थापनN1 या एसN2 तंत्र सामान्यतः विनाइल या एरिल हैलाइड या संबंधित यौगिकों के साथ नहीं होता है। कुछ शर्तों के तहत न्यूक्लियोफिलिक प्रतिस्थापन अन्य तंत्रों के माध्यम से हो सकता है, जैसे कि न्यूक्लियोफिलिक सुगंधित प्रतिस्थापन लेख में वर्णित हैं।
जब कार्बोनिल समूह में प्रतिस्थापन होता है, तो एसाइल समूह न्यूक्लियोफिलिक एसाइल प्रतिस्थापन से गुजर सकता है। यह एसाइल क्लोराइड, एस्टर और एमाइड्स जैसे कार्बोज़ाइलिक तेजाब डेरिवेटिव के साथ प्रतिस्थापन का सामान्य तरीका है।
संदर्भ
- ↑ J. March, Advanced Organic Chemistry, 4th ed., Wiley, New York, 1992.
- ↑ R. A. Rossi, R. H. de Rossi, Aromatic Substitution by the SRN1 Mechanism, ACS Monograph Series No. 178, American Chemical Society, 1983. ISBN 0-8412-0648-1.
- ↑ L. G. Wade, Organic Chemistry, 5th ed., Prentice Hall, Upper Saddle River, New Jersey, 2003.
- ↑ S. R. Hartshorn, Aliphatic Nucleophilic Substitution, Cambridge University Press, London, 1973. ISBN 0-521-09801-7
- ↑ Introducing Aliphatic Substitution with a Discovery Experiment Using Competing Electrophiles Timothy P. Curran, Amelia J. Mostovoy, Margaret E. Curran, and Clara Berger Journal of Chemical Education 2016 93 (4), 757-761 doi:10.1021/acs.jchemed.5b00394
- ↑ 253. Reaction kinetics and the Walden inversion. Part II. Homogeneous hydrolysis, alcoholysis, and ammonolysis of -phenylethyl halides Edward D. Hughes, Christopher K. Ingold and Alan D. Scott, J. Chem. Soc., 1937, 1201 doi:10.1039/JR9370001201
- ↑ N.S.Imyanitov. Electrophilic Bimolecular Substitution as an Alternative to Nucleophilic Monomolecular Substitution in Inorganic and Organic Chemistry. J. Gen. Chem. USSR (Engl. Transl.) 1990; 60 (3); 417-419.
- ↑ Unimolecular Nucleophilic Substitution does not Exist! / N.S.Imyanitov. SciTecLibrary