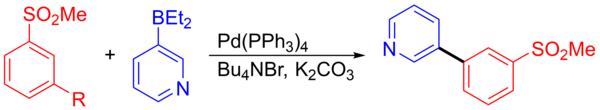सुजुकी अभिक्रिया: Difference between revisions
No edit summary |
No edit summary |
||
| Line 36: | Line 36: | ||
[[File:Transmetallation in Suzuki reaction.png|center|350px|सुजुकी प्रतिक्रिया में ट्रांसमेटलेशन।]] | [[File:Transmetallation in Suzuki reaction.png|center|350px|सुजुकी प्रतिक्रिया में ट्रांसमेटलेशन।]] | ||
=== | === अपचायक निष्कासन === | ||
{{main article| | {{main article|अपचायक निष्कासन}} | ||
[[File:Suzuki Coupling Reductive Elimination.png|center|200px|सुजुकी प्रतिक्रिया के उत्प्रेरक चक्र में रिडक्टिव एलिमिनेशन स्टेप।]] | अंतिम चरण अपचायक निष्कासन चरण है जहां पैलेडियम (II) जटिल (ई) उत्पाद (3) को हटा देता है और पैलेडियम (0) उत्प्रेरक (ए) को पुन: उत्पन्न करता है। ड्यूटेरियम लेबलिंग का उपयोग करते हुए, रिडग्वे एट अल ने त्रिविम रसायन के अवरोधन के साथ अपचायक निष्कासन प्रक्रिया को दिखाया है।<ref>{{cite journal|doi=10.1021/jo970803d|title=सुजुकी कपलिंग रिएक्शन में अल्काइलबोरेन का पैलेडियम में ट्रांसमेटेशन स्टीरियोकेमिस्ट्री के प्रतिधारण के साथ आगे बढ़ता है|year=1998|last1=Ridgway|first1=Brian H.|last2=Woerpel|first2=K. A.|journal=The Journal of Organic Chemistry|volume=63|issue=3|pages=458–460|pmid=11672033}}</ref> | ||
[[File:Suzuki Coupling Reductive Elimination.png|center|200px|सुजुकी प्रतिक्रिया के उत्प्रेरक चक्र में रिडक्टिव एलिमिनेशन स्टेप।]]सुज़ुकी अभिक्रिया में लिगेंड एक महत्वपूर्ण भूमिका निभाता है। प्रायः, सुजुकी अभिक्रिया में फॉस्फीन लिगेंड का उपयोग किया जाता है। फॉस्फीन लिगेंड जटिल के धातु केंद्र में इलेक्ट्रॉन घनत्व बढ़ाता है और इसलिए ऑक्सीकृत योग चरण में मदद करता है। इसके अलावा, फॉस्फीन लिगेंड के प्रतिस्थापन की भारीता अपचायक निष्कासन चरण में मदद करती है। हालांकि, सुजुकी अभिक्रिया स्थितियों के तहत फॉस्फीन लिगेंड की अस्थिरता के कारण, हाल ही में इस क्रॉस युग्मन में एन-विषमचक्रीय कार्बीन लिगेंड का उपयोग किया गया है।<ref>{{Cite web|title=संश्लेषण का विज्ञान: सर्वोत्तम तरीके। सर्वोत्तम परिणाम - थिएम रसायन विज्ञान|url=https://science-of-synthesis.thieme.com/app/text/|access-date=2021-04-14|website=science-of-synthesis.thieme.com}}</ref> एन-विषमचक्रीय कार्बीन फॉस्फीन लिगेंड की तुलना में अधिक इलेक्ट्रॉन समृद्ध और अधिक भारी हैं। इसलिए, एन-विषमचक्रीय कार्बीन लिगेंड के त्रिविमी और इलेक्ट्रॉनिक दोनों कारक सक्रिय Pd(0) उत्प्रेरक को स्थिर करने में मदद करते हैं।<ref>{{Cite journal|last1=Hopkinson|first1=Matthew N.|last2=Richter|first2=Christian|last3=Schedler|first3=Michael|last4=Glorius|first4=Frank|date=June 2014|title=एन-विषमचक्रीय कार्बेनेस का एक सिंहावलोकन|url=https://www.nature.com/articles/nature13384|journal=Nature|language=en|volume=510|issue=7506|pages=485–496|doi=10.1038/nature13384|pmid=24965649|bibcode=2014Natur.510..485H|s2cid=672379|issn=1476-4687}}</ref> | |||
Revision as of 00:31, 1 December 2022
| Suzuki reaction | |
|---|---|
| Named after | Akira Suzuki |
| Reaction type | Coupling reaction |
| Identifiers | |
| Organic Chemistry Portal | suzuki-coupling |
| RSC ontology ID | RXNO:0000140 |
सुज़ुकी अभिक्रिया एक कार्बनिक प्रतिक्रिया है, जिसे क्रॉस-युग्मन अभिक्रिया के रूप में वर्गीकृत किया गया है, जहां युग्मन भागीदार एक बोरोनिक अम्ल और ऑर्गेनोहैलाइड हैं और उत्प्रेरक एक पैलेडियम (0) जटिल है।[1][2][3] यह पहली बार 1979 में अकीरा सुज़ुकी द्वारा प्रकाशित किया गया था, और उन्होंने कार्बनिक संश्लेषण में पैलेडियम-उत्प्रेरित क्रॉस-युग्मन की खोज और विकास में उनके योगदान के लिए रिचर्ड एफ. हेक और ई-इची नेगिशी के साथ रसायन विज्ञान में 2010 का नोबेल पुरस्कार साझा किया था।[4] इस अभिक्रिया को सुज़ुकी-मियौरा अभिक्रिया या केवल सुज़ुकी युग्मन के रूप में भी जाना जाता है। यह व्यापक रूप से पॉलीओलेफ़िन, स्टाइरीन और प्रतिस्थापित बाइफिनाइल को संश्लेषित करने के लिए उपयोग किया जाता है। प्रगति और सुजुकी अभिक्रिया के विकास का वर्णन करते हुए कई समीक्षाएं प्रकाशित की गई हैं।[5][6][7] सुजुकी अभिक्रिया के लिए सामान्य योजना नीचे दिखाई गई है, जहां एक पैलेडियम उत्प्रेरक और एक क्षार का उपयोग करके एक ऑर्गनोबोरोन वर्ग (R2-BY2) के साथ एक हैलाइड (R1-X) को जोड़कर एक कार्बन-कार्बन एकल बंधन का निर्माण किया जाता है।
अभिक्रिया क्रियाविधि
सुजुकी अभिक्रिया की अभिक्रिया क्रियाविधि को पैलेडियम उत्प्रेरक के दृष्टिकोण से सबसे अच्छी तरह से देखा जाता है। उत्प्रेरक चक्र का प्रारम्भ एक सक्रिय Pd0 उत्प्रेरक वर्ग,ए के गठन से होता है। यह ऑर्गनोपैलेडियम मध्यवर्ती बी बनाने के लिए हैलाइड अभिकर्मक 1 में पैलेडियम के ऑक्सीकृत योग में भाग लेता है। क्षार के साथ अभिक्रिया (विपर्यय) मध्यवर्ती C देता है, जो ट्रांसमेटलेशन के माध्यम से[8] बोरॉन-एटी जटिल डी (क्षार के साथ बोरोनिक अम्ल अभिकर्मक 2 की अभिक्रिया द्वारा उत्पादित) के साथ क्षणिक ऑर्गोपैलेडियम वर्ग ई बनाता है। अपचायक निष्कासन चरण से वांछित उत्पाद 3 का निर्माण होता है और मूल पैलेडियम उत्प्रेरक ए को पुनर्स्थापित करता है जो उत्प्रेरक चक्र को पूरा करता है।
ट्राईएल्काइलबोरेन (BR3) और एल्कोक्साइड (−OR) की अभिक्रिया की स्थिति में क्षार को पहले एक ट्राईएल्काइल बोरेट (R3B-OR) बनाने के लिए माना जाता था इस वर्ग को अधिक नाभिकरागी (न्यूक्लियोफिलिक) माना जा सकता है और फिर ट्रांसमेटलेशन चरण में मौजूद पैलेडियम जटिल के प्रति अधिक अभिक्रियाशील हो सकता है।[9][10][11] डक और सहकर्मियों ने सुज़ुकी युग्मन के लिए अभिक्रिया क्रियाविधि में क्षार की भूमिका की जांच की और उन्होंने पाया कि क्षार की तीन भूमिकाएँ हैं- पैलेडियम जटिल का निर्माण [ArPd(OR)L2], ट्राईएल्काइल बोरेट का निर्माण और पैलेडियम जटिल के साथ एल्कोक्साइड की अभिक्रिया से अपचायक निष्कासन चरण का त्वरण।[9]
ऑक्सीकृत योग
अधिकतर स्थितियों में ऑक्सीकृत योग उत्प्रेरक चक्र का दर निर्धारित करने वाला चरण है।[12] इस चरण के दौरान, पैलेडियम उत्प्रेरक को पैलेडियम (0) से पैलेडियम (II) में ऑक्सीकृत किया जाता है। उत्प्रेरक रूप से सक्रिय पैलेडियम वर्ग A को एरिल हैलाइड क्रियाधार 1 के साथ मिलकर एक ऑर्गेनोपैलेडियम जटिल बी प्राप्त होता है। जैसा कि नीचे दिए गए आरेख में देखा गया है, ऑक्सीकृत योग चरण कार्बन-हैलोजन बंधन को तोड़ता है जहां पैलेडियम अब दोनों हैलोजन (X) साथ ही साथ आर1 समूह से बंधा हुआ है।
ऐलिलिक और बेंजिलिक हैलाइड्स के साथ त्रिविम रसायन का व्युत्क्रम देते हुए, ऑक्सीकृत योग विनाइल हैलाइड्स के साथ त्रिविम रसायन के अवरोधन के साथ आगे बढ़ता है।[13] ऑक्सीकृत योग प्रारम्भ में सीस-पैलेडियम जटिल बनाता है, जो तेजी से ट्रांस-जटिल में समावयव हो जाता है।[14]
सुज़ुकी युग्मन ऑर्गनोबोरोन अभिकर्मक या हैलाइड दोनों के लिए द्वि आबंध पर विन्यास की अवधारण के साथ होता है।[15] हालाँकि, उस समावयवन, सीस या ट्रांस का विन्यास ऑक्सीकृत योग चरण में पैलेडियम जटिल के सीस-से-ट्रांस समावयवन द्वारा निर्धारित किया जाता है, जहां ट्रांस पैलेडियम जटिल प्रमुख रूप है। जब ऑर्गनोबोरोन एक समावयवन से जुड़ा होता है और इसे एक एल्केनाइल हैलाइड से जोड़ा जाता है, तो उत्पाद एक डाइईन होता है जैसा कि नीचे दिखाया गया है।
ट्रांसमेटलेशन
ट्रांसमेटेलेशन एक कार्बधात्विक अभिक्रिया है जहां संलग्नी (लिगेंड) एक वर्ग से दूसरे में स्थानांतरित होते हैं। सुज़ुकी युग्मन की स्थिति में लिगेंड्स को ऑर्गेनोबोरोन वर्ग डी से पैलेडियम (II) जटिल सी में स्थानांतरित किया जाता है, जहां पहले चरण में जोड़े गए क्षार को नए पैलेडियम (II) जटिल ई देने के लिए ऑर्गोबोरोन प्रजातियों पर R2 प्रतिस्थापी के साथ आदान-प्रदान किया जाता है। सुज़ुकी युग्मन के लिए ट्रांसमेटलेशन की सटीक प्रणाली की खोज की जानी बाकी है। ऑर्गेनोबोरोन यौगिक क्षार की अनुपस्थिति में ट्रांसमेटलेशन से नहीं गुजरते हैं और इसलिए यह व्यापक रूप से माना जाता है कि क्षार की भूमिका ऑर्गोबोरोन यौगिक को सक्रिय करने के साथ-साथ ऑक्सीकृत योग उत्पाद R1-Pdll-X (बी) से R1-Pdll-OtBu मध्यवर्ती (सी) के निर्माण को सुविधा प्रदान करती है।[12]
अपचायक निष्कासन
अंतिम चरण अपचायक निष्कासन चरण है जहां पैलेडियम (II) जटिल (ई) उत्पाद (3) को हटा देता है और पैलेडियम (0) उत्प्रेरक (ए) को पुन: उत्पन्न करता है। ड्यूटेरियम लेबलिंग का उपयोग करते हुए, रिडग्वे एट अल ने त्रिविम रसायन के अवरोधन के साथ अपचायक निष्कासन प्रक्रिया को दिखाया है।[16]
सुज़ुकी अभिक्रिया में लिगेंड एक महत्वपूर्ण भूमिका निभाता है। प्रायः, सुजुकी अभिक्रिया में फॉस्फीन लिगेंड का उपयोग किया जाता है। फॉस्फीन लिगेंड जटिल के धातु केंद्र में इलेक्ट्रॉन घनत्व बढ़ाता है और इसलिए ऑक्सीकृत योग चरण में मदद करता है। इसके अलावा, फॉस्फीन लिगेंड के प्रतिस्थापन की भारीता अपचायक निष्कासन चरण में मदद करती है। हालांकि, सुजुकी अभिक्रिया स्थितियों के तहत फॉस्फीन लिगेंड की अस्थिरता के कारण, हाल ही में इस क्रॉस युग्मन में एन-विषमचक्रीय कार्बीन लिगेंड का उपयोग किया गया है।[17] एन-विषमचक्रीय कार्बीन फॉस्फीन लिगेंड की तुलना में अधिक इलेक्ट्रॉन समृद्ध और अधिक भारी हैं। इसलिए, एन-विषमचक्रीय कार्बीन लिगेंड के त्रिविमी और इलेक्ट्रॉनिक दोनों कारक सक्रिय Pd(0) उत्प्रेरक को स्थिर करने में मदद करते हैं।[18]
फायदे
अन्य समान प्रतिक्रियाओं पर सुजुकी युग्मन के लाभों में सामान्य बोरोनिक एसिड की उपलब्धता, हल्की प्रतिक्रिया की स्थिति और इसकी कम विषाक्त प्रकृति शामिल है। बोरोनिक एसिड ऑर्गनोटिन और ऑर्गेनोजिंक यौगिकों की तुलना में पर्यावरण के लिए कम विषाक्त और सुरक्षित हैं। प्रतिक्रिया मिश्रण से अकार्बनिक उप-उत्पादों को निकालना आसान है। इसके अलावा, यह प्रतिक्रिया बेहतर है क्योंकि यह अपेक्षाकृत सस्ते और आसानी से तैयार अभिकर्मकों का उपयोग करती है। विलायक के रूप में पानी का उपयोग करने में सक्षम होने के नाते[19]इस प्रतिक्रिया को पानी में घुलनशील अभिकर्मकों की एक किस्म के साथ उपयोग करने के लिए अधिक किफायती, पर्यावरण के अनुकूल और व्यावहारिक बनाता है। सुजुकी युग्मन के लिए विभिन्न प्रकार के अभिकर्मकों का उपयोग किया जा सकता है, उदाहरण के लिए, एरिल- या विनाइल समूह-बोरोनिक एसिड और एरिल- या विनाइल समूह-हैलाइड। कार्य ने एल्काइल ब्रोमाइड को शामिल करने के लिए प्रतिक्रिया के दायरे को भी बढ़ा दिया है।[20] सुजुकी युग्मन प्रतिक्रिया के लिए कई अलग-अलग प्रकार के हैलाइड संभव होने के अलावा, प्रतिक्रिया स्यूडोहैलाइड्स जैसे ट्राइफ्लेट्स (ओटीएफ) के साथ भी काम करती है, हैलाइड के प्रतिस्थापन के रूप में। हैलाइड या स्यूडोहैलाइड के साथ युग्मन साझेदार के लिए आपेक्षिक प्रतिक्रियाशीलता है: R2-मैं> आर2-ओटीएफ> आर2-बीआर >> आर2-सीएल। बोरोनिक एसिड के बजाय बोरोनिक एस्टर और ऑर्गनोट्रिफ्लोरोबोरेट का उपयोग किया जा सकता है। उत्प्रेरक पैलेडियम नैनोमटेरियल-आधारित उत्प्रेरक भी हो सकता है।[21] एक उपन्यास ऑर्गनोफॉस्फीन लिगैंड (एसपीओएस) के साथ, 0.001 मोल% तक उत्प्रेरक लोडिंग की सूचना मिली है:।[22] इन अग्रिमों और प्रक्रिया के समग्र लचीलेपन ने सुजुकी कपलिंग को रासायनिक संश्लेषण के लिए व्यापक रूप से स्वीकार कर लिया है।
आवेदन
औद्योगिक अनुप्रयोग
सुजुकी कपलिंग प्रतिक्रिया फार्मास्यूटिकल्स या ठीक रसायनों के लिए मध्यवर्ती के संश्लेषण में उपयोग के लिए स्केलेबल और लागत प्रभावी है।[23] सुजुकी प्रतिक्रिया एक बार उत्प्रेरक के उच्च स्तर और बोरोनिक एसिड की सीमित उपलब्धता से सीमित थी। हैलाइड के प्रतिस्थापन भी पाए गए, जिससे हैलाइड या स्यूडोहैलाइड के लिए युग्मन भागीदारों की संख्या में भी वृद्धि हुई। सीआई-1034 जैसे कई महत्वपूर्ण जैविक यौगिकों के संश्लेषण में स्केल्ड अप प्रतिक्रियाएं की गई हैं, जो एक ट्राइफलेट और बोरोनिक एसिड युग्मन भागीदारों का उपयोग करते थे जो कि 95% उपज के साथ 80 किलोग्राम पैमाने पर चलाया जाता था।[24] एक अन्य उदाहरण 3-पाइरिडाइलबोरेन और 1-ब्रोमो-3- (मिथाइलसल्फ़ोनिल) बेंजीन का युग्मन है जिसने एक मध्यवर्ती का गठन किया जो एक संभावित केंद्रीय तंत्रिका तंत्र एजेंट के संश्लेषण में उपयोग किया गया था। 92.5% उपज में उत्पादित मध्यवर्ती (278 किलोग्राम) बनाने के लिए युग्मन प्रतिक्रिया।[15][23]
सुज़ुकी सीसी प्रतिक्रिया के लिए विषम उत्प्रेरक के विकास में महत्वपूर्ण प्रयास किए गए हैं, जो औद्योगिक प्रक्रिया में प्रदर्शन लाभ (सब्सट्रेट से उत्प्रेरक पृथक्करण को समाप्त करने) से प्रेरित है, और हाल ही में एक पीडी एकल परमाणु विषम उत्प्रेरक को बेहतर प्रदर्शन करने के लिए दिखाया गया है। उद्योग डिफ़ॉल्ट सजातीय पीडी (पीपीएच)3)4 उत्प्रेरक[25]
सिंथेटिक अनुप्रयोग
सुजुकी कपलिंग का उपयोग अक्सर जटिल यौगिकों के संश्लेषण में किया जाता है।[26][27] सुज़ुकी कपलिंग का उपयोग सिट्रोनेलल व्युत्पन्न पर कैपराट्रिएन के संश्लेषण के लिए किया गया है, एक प्राकृतिक उत्पाद जो ल्यूकेमिया के खिलाफ अत्यधिक सक्रिय है:[28] फ़ाइल:सुजुकी कपलिंग capparatriene.tif|frameless|center
विविधताएं
धातु उत्प्रेरक
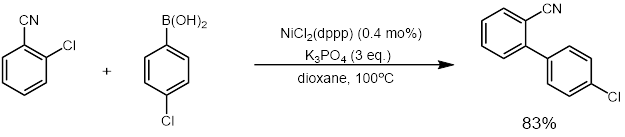
पैलेडियम (विशेषकर निकल) के अलावा अन्य धातुओं के विभिन्न उत्प्रेरक उपयोग विकसित किए गए हैं।[29] पहली निकेल उत्प्रेरित क्रॉस-कपलिंग प्रतिक्रिया को पर्सेक और सहकर्मियों द्वारा 1995 में एरिल मेसाइलेट्स और बोरोनिक एसिड का उपयोग करके रिपोर्ट किया गया था।[30] भले ही प्रतिक्रिया के लिए निकल उत्प्रेरक की अधिक मात्रा की आवश्यकता थी, लगभग 5 मोल%, निकल उतना महंगा या कीमती धातु नहीं है जितना कि पैलेडियम। निकल उत्प्रेरित सुजुकी युग्मन प्रतिक्रिया ने कई यौगिकों को भी अनुमति दी जो निकल-उत्प्रेरित प्रणाली की तुलना में पैलेडियम उत्प्रेरित प्रणाली के लिए काम नहीं करते थे या बदतर काम करते थे।[29]निकल उत्प्रेरक के उपयोग ने इलेक्ट्रोफाइल के लिए अनुमति दी है जो पैलेडियम का उपयोग करके मूल सुजुकी युग्मन के लिए चुनौतीपूर्ण साबित हुई है, जिसमें फिनोल, एरिल ईथर, एस्टर, फॉस्फेट और फ्लोराइड जैसे सब्सट्रेट शामिल हैं।[29]
निकेल उत्प्रेरित क्रॉस-कपलिंग की जांच जारी रही और इन पहले उदाहरणों के दिखाए जाने के बाद प्रतिक्रिया का दायरा बढ़ गया और अनुसंधान की रुचि बढ़ गई। मियाउरा और इनाडा ने 2000 में बताया कि एक सस्ता निकल उत्प्रेरक का उपयोग युग्मन प्रतिक्रिया के लिए किया जा सकता है।3) पहले इस्तेमाल किए गए अधिक महंगे लिगेंड के बजाय।[31] हालांकि, निकल-उत्प्रेरित क्रॉस-कपलिंग को अभी भी उच्च उत्प्रेरक लोडिंग (3-10%) की आवश्यकता होती है, अतिरिक्त लिगैंड (1-5 समकक्ष) की आवश्यकता होती है और हवा और नमी के प्रति संवेदनशील रहती है।[29]हान और सहकर्मियों की प्रगति ने कम मात्रा में निकल उत्प्रेरक (<1 मोल%) और लिगैंड के अतिरिक्त समकक्षों का उपयोग करके एक विधि विकसित करके उस समस्या का समाधान करने का प्रयास किया है।[32]
2011 में वू और सहकर्मियों द्वारा यह भी बताया गया था कि एरिल क्लोराइड्स के क्रॉस-कपलिंग के लिए एक अत्यधिक सक्रिय निकल उत्प्रेरक का उपयोग किया जा सकता है जिसके लिए केवल 0.01-0.1 मोल% निकल उत्प्रेरक की आवश्यकता होती है। उन्होंने यह भी दिखाया कि उत्प्रेरक गतिविधि में लगभग कोई नुकसान नहीं होने के साथ उत्प्रेरक को छह गुना तक पुनर्नवीनीकरण किया जा सकता है।[33] उत्प्रेरक पुनर्चक्रण योग्य था क्योंकि यह एक फॉस्फीन निकल नैनोपार्टिकल उत्प्रेरक (G .) था3DenP-Ni) जिसे डेंड्रिमर से बनाया गया था।
फायदे और नुकसान दोनों पैलेडियम और निकल-उत्प्रेरित सुजुकी युग्मन प्रतिक्रियाओं पर लागू होते हैं। पीडी और नी उत्प्रेरक प्रणाली के अलावा, लोहे और तांबे जैसे सस्ते और गैर विषैले धातु स्रोत[34] सुजुकी युग्मन प्रतिक्रिया में इस्तेमाल किया गया है। बेडफोर्ड अनुसंधान समूह[35] और नाकामुरा अनुसंधान समूह[36] लौह उत्प्रेरित सुजुकी युग्मन प्रतिक्रिया की पद्धति विकसित करने पर व्यापक रूप से काम किया है। रूथेनियम एक अन्य धातु स्रोत है जिसका उपयोग सुजुकी युग्मन प्रतिक्रिया में किया गया है।[37]
युग्मन के बीच
निकेल कटैलिसीस एमाइड से सीसी बांड का निर्माण कर सकता है। सिन्थॉन के रूप में एमाइड की स्वाभाविक रूप से निष्क्रिय प्रकृति के बावजूद, सीसी बांड तैयार करने के लिए निम्नलिखित पद्धति का उपयोग किया जा सकता है। युग्मन प्रक्रिया असंख्य कार्यात्मक समूहों की हल्की और सहिष्णु है, जिनमें शामिल हैं: अमाइन, केटोन्स, हेटरोसायकल, अम्लीय प्रोटॉन वाले समूह। इस तकनीक का उपयोग बायोएक्टिव अणुओं को तैयार करने और चतुर अनुक्रमिक क्रॉस-कपलिंग के माध्यम से नियंत्रित तरीकों से हेट्रोसायकल को एकजुट करने के लिए भी किया जा सकता है। प्रतिक्रिया योजना की एक सामान्य समीक्षा नीचे दी गई है।[38]
 ट्यूबुलिन बाइंडिंग कंपाउंड (साइटोस्टेसिस एजेंट) का संश्लेषण ट्राइमेथोक्सीमाइड और एक हेट्रोसायक्लिक पिनाकोलाटोबोरोन कपलिंग पार्टनर का उपयोग करके एक ग्राम पैमाने पर किया गया था।[38]
ट्यूबुलिन बाइंडिंग कंपाउंड (साइटोस्टेसिस एजेंट) का संश्लेषण ट्राइमेथोक्सीमाइड और एक हेट्रोसायक्लिक पिनाकोलाटोबोरोन कपलिंग पार्टनर का उपयोग करके एक ग्राम पैमाने पर किया गया था।[38]

ऑर्गनोबोरेन्स
आर्यल बोरोनिक एसिड अन्य ऑर्गेनोबोरेन की तुलना में तुलनात्मक रूप से सस्ता है और व्यावसायिक रूप से उपलब्ध एरिल बोरोनिक एसिड की एक विस्तृत विविधता है। इसलिए, यह सुज़ुकी प्रतिक्रिया में एक ऑर्गेनोबोरेन पार्टनर के रूप में व्यापक रूप से उपयोग किया गया है। ऑर्गनोट्रिफ्लोरोबोरेट ऑर्गेनोबोरेन का एक अन्य वर्ग है जो अक्सर उपयोग किया जाता है क्योंकि वे एरिल बोरोनिक एसिड की तुलना में प्रोटोडेबोरोनेशन के लिए कम प्रवण होते हैं। वे संश्लेषित करने में आसान होते हैं और आसानी से शुद्ध किए जा सकते हैं।[39] पोटेशियम हाइड्रोजन फ्लोराइड के साथ उपचार द्वारा बोरोनिक एसिड से आर्यलट्रिफ्लोरोबोरेट लवण का निर्माण किया जा सकता है जिसे सुजुकी युग्मन प्रतिक्रिया में इस्तेमाल किया जा सकता है।[40]
विलायक विविधताएं
सुजुकी युग्मन प्रतिक्रिया अन्य युग्मन प्रतिक्रियाओं से अलग है, जिसमें इसे द्विध्रुवीय कार्बनिक-पानी में चलाया जा सकता है,[41] केवल पानी,[19] या कोई विलायक नहीं।[42] इसने युग्मन प्रतिक्रियाओं के दायरे में वृद्धि की, क्योंकि विभिन्न प्रकार के पानी में घुलनशील आधार, उत्प्रेरक प्रणाली और अभिकर्मकों का उपयोग कार्बनिक विलायक में उनकी घुलनशीलता पर चिंता किए बिना किया जा सकता है। आर्थिक और सुरक्षा लाभों के कारण विलायक प्रणाली के रूप में पानी का उपयोग भी आकर्षक है। सुज़ुकी कपलिंग के लिए सॉल्वेंट सिस्टम में अक्सर उपयोग किए जाने वाले टोल्यूनि हैं,[43] टेट्राहाइड्रोफुरन,[44] डाइऑक्साइन,[44]और डाइमिथाइलफॉर्मैमाइड।[45] सबसे अधिक उपयोग किए जाने वाले क्षार हैं पोटेशियम कार्बोनेट | K2सीओ3,[41]पोटेशियम टर्ट-ब्यूटॉक्साइड,[46] सीज़ियम कार्बोनेट2सीओ3,[47] ट्रिपोटेशियम फॉस्फेट|K3बाद में4,[48] नाओह,[49] और ट्राइथाइलामाइन | एनईटी3.[50]
यह भी देखें
- चान-लैम युग्मन
- हेक रिएक्शन
- हियामा कपलिंग
- कुमाड़ा कपलिंग
- नेगिशी कपलिंग
- पेटासिस प्रतिक्रिया
- सोनोगाशिरा कपलिंग
- स्थिर प्रतिक्रिया
- जैविक प्रतिक्रियाओं की सूची
संदर्भ
- ↑ Miyaura, Norio; Yamada, Kinji; Suzuki, Akira (1979). "1-एल्केनिल या 1-एल्किनिल हैलाइड्स के साथ 1-एल्केनिलबोरेन्स की पैलेडियम-उत्प्रेरित प्रतिक्रिया द्वारा एक नया स्टीरियोस्पेसिफिक क्रॉस-कपलिंग". Tetrahedron Letters. 20 (36): 3437–3440. doi:10.1016/S0040-4039(01)95429-2. hdl:2115/44006.
- ↑ Miyaura, Norio; Suzuki, Akira (1979). "पैलेडियम उत्प्रेरक की उपस्थिति में ऐरिल हैलाइड के साथ एल्क-1-एनिलबोरेन्स की अभिक्रिया द्वारा ऐरिलेटेड (ई)-ऐल्कीन का त्रिविम चयनी संश्लेषण". Chem. Comm. (19): 866–867. doi:10.1039/C39790000866.
- ↑ Miyaura, Norio; Suzuki, Akira (1995). "ऑर्गनोबोरोन यौगिकों के पैलेडियम-उत्प्रेरित क्रॉस-युग्मन प्रतिक्रियाएं". Chemical Reviews. 95 (7): 2457–2483. CiteSeerX 10.1.1.735.7660. doi:10.1021/cr00039a007.
- ↑ Nobelprize.org. "रसायन विज्ञान में नोबेल पुरस्कार 2010". Nobel Prize Foundation. Retrieved 2013-10-25.
- ↑ Suzuki, Akira (1991). "कार्बनिक हलाइड्स के साथ ऑर्गेनोबोरोन डेरिवेटिव की क्रॉस-कपलिंग प्रतिक्रिया के माध्यम से सिंथेटिक अध्ययन". Pure Appl. Chem. 63 (3): 419–422. doi:10.1351/pac199163030419.
- ↑ Miyaura, Norio; Suzuki, Akira (1979). "ऑर्गनोबोरोन यौगिकों के पैलेडियम-उत्प्रेरित क्रॉस-युग्मन प्रतिक्रियाएं". Chemical Reviews. 95 (7): 2457–2483. CiteSeerX 10.1.1.735.7660. doi:10.1021/cr00039a007.(Review)
- ↑ Suzuki, Akira (1999). "ऑर्गेनिक इलेक्ट्रोफाइल्स के साथ ऑर्गेनोबोरोन डेरिवेटिव्स की क्रॉस-कपलिंग प्रतिक्रियाओं में हालिया प्रगति, 1995-1998". Journal of Organometallic Chemistry. 576 (1–2): 147–168. doi:10.1016/S0022-328X(98)01055-9.
- ↑ Matos, K.; Soderquist, J. A. (1998). "सुजुकी-मियाउरा कपलिंग में अल्काइलबोरेन्स: स्टीरियोकेमिकल और मैकेनिस्टिक स्टडीज". J. Org. Chem. 63 (3): 461–470. doi:10.1021/jo971681s. PMID 11672034.
- ↑ 9.0 9.1 Amatore, Christian; Jutand, Anny; Le Duc, Gaëtan (18 February 2011). "पैलेडियम-उत्प्रेरित सुजुकी-मियाउरा प्रतिक्रियाओं में ट्रांसमेटलेशन / रिडक्टिव एलिमिनेशन के लिए काइनेटिक डेटा: बेस के रूप में उपयोग किए जाने वाले हाइड्रॉक्साइड आयनों की अप्रत्याशित ट्रिपल भूमिका". Chemistry: A European Journal. 17 (8): 2492–2503. doi:10.1002/chem.201001911. PMID 21319240.
- ↑ Smith, George B.; Dezeny, George C.; Hughes, David L.; King, Anthony O.; Verhoeven, Thomas R. (1 December 1994). "सुजुकी क्रॉस-युग्मन प्रतिक्रिया का यंत्रवत अध्ययन". The Journal of Organic Chemistry. 59 (26): 8151–8156. doi:10.1021/jo00105a036.
- ↑ Matos, Karl; Soderquist, John A. (1 February 1998). "सुजुकी-मियाउरा कपलिंग में अल्काइलबोरेन्स: स्टीरियोकेमिकल और मैकेनिस्टिक स्टडीज". The Journal of Organic Chemistry. 63 (3): 461–470. doi:10.1021/jo971681s. PMID 11672034.
- ↑ 12.0 12.1 Kurti, Laszlo (2005). कार्बनिक संश्लेषण में नामित प्रतिक्रियाओं के सामरिक अनुप्रयोग. Elsevier Academic Press. ISBN 978-0124297852.
- ↑ Stille, John K.; Lau, Kreisler S. Y. (1977). "समूह 8 संक्रमण-धातु परिसरों में कार्बनिक हैलाइडों के ऑक्सीडेटिव जोड़ के तंत्र". Accounts of Chemical Research. 10 (12): 434–442. doi:10.1021/ar50120a002.
- ↑ Casado, Arturo L.; Espinet, Pablo (1998). "RX से Pd(PPh3)4 और \PdRX(PPh3)2 के सिस-टू-ट्रांसआइसोमेराइजेशन के तंत्र के ऑक्सीडेटिव जोड़ के परिणामस्वरूप कॉन्फ़िगरेशन पर] कॉम्प्लेक्स (R = aryl, X = halide)†". Organometallics. 17 (5): 954–959. doi:10.1021/om9709502.
- ↑ 15.0 15.1 उन्नत कार्बनिक रसायन. Springer. 2007. pp. 739–747.
- ↑ Ridgway, Brian H.; Woerpel, K. A. (1998). "सुजुकी कपलिंग रिएक्शन में अल्काइलबोरेन का पैलेडियम में ट्रांसमेटेशन स्टीरियोकेमिस्ट्री के प्रतिधारण के साथ आगे बढ़ता है". The Journal of Organic Chemistry. 63 (3): 458–460. doi:10.1021/jo970803d. PMID 11672033.
- ↑ "संश्लेषण का विज्ञान: सर्वोत्तम तरीके। सर्वोत्तम परिणाम - थिएम रसायन विज्ञान". science-of-synthesis.thieme.com. Retrieved 2021-04-14.
- ↑ Hopkinson, Matthew N.; Richter, Christian; Schedler, Michael; Glorius, Frank (June 2014). "एन-विषमचक्रीय कार्बेनेस का एक सिंहावलोकन". Nature (in English). 510 (7506): 485–496. Bibcode:2014Natur.510..485H. doi:10.1038/nature13384. ISSN 1476-4687. PMID 24965649. S2CID 672379.
- ↑ 19.0 19.1 Casalnuovo, Albert L.; Calabrese (1990). "जलीय मीडिया में पैलेडियम-उत्प्रेरित क्षारीकरण". J. Am. Chem. Soc. 112 (11): 4324–4330. doi:10.1021/ja00167a032.
- ↑ Kirchhoff, Jan H.; Netherton, Matthew R.; Hills, Ivory D.; Fu, Gregory C. (2002). "बोरोनिक एसिड: अल्काइल ब्रोमाइड्स के कमरे के तापमान सुजुकी प्रतिक्रियाओं में नए युग्मन भागीदार। उल्लेखनीय रूप से हल्की स्थितियों के तहत उत्पन्न ऑक्सीडेटिव-अतिरिक्त जोड़ का क्रिस्टलोग्राफिक लक्षण वर्णन". Journal of the American Chemical Society. 124 (46): 13662–3. doi:10.1021/ja0283899. PMID 12431081.
- ↑ Ohtaka, Atsushi (2013). "पानी में पुन: प्रयोज्य पॉलिमर-समर्थित नैनोमेटल उत्प्रेरक". The Chemical Record. 13 (3): 274–285. doi:10.1002/tcr.201300001. PMID 23568378.
- ↑ Martin, R.; Buchwald, S. L. (2008). "पैलेडियम-उत्प्रेरित सुजुकी-मियाउरा क्रॉस-कपलिंग प्रतिक्रियाएं डायलकाइलबिरियल फॉस्फीन लिगैंड्स को नियोजित करती हैं". Accounts of Chemical Research. 41 (11): 1461–1473. doi:10.1021/ar800036s. PMC 2645945. PMID 18620434.
- ↑ 23.0 23.1 Rouhi, A. Maureen (6 September 2004). "सूक्ष्म रसायन". C&EN.
- ↑ Jacks1, Thomas E.; Belmont, Daniel T.; Briggs, Christopher A.; Horne, Nicole M.; Kanter, Gerald D.; Karrick, Greg L.; Krikke, James J.; McCabe, Richard J.; Mustakis; Nanninga, Thomas N. (1 March 2004). "एंडोटिलिन प्रतिपक्षी, सीआई-1034 के लिए एक स्केलेबल प्रक्रिया का विकास". Organic Process Research & Development. 8 (2): 201–212. doi:10.1021/op034104g.
- ↑ Chen, Zupeng; Vorobyeva, Evgeniya; Mitchell, Sharon; Fako, Edvin; Ortuño, Manuel A.; López, Núria; Collins, Sean M.; Midgley, Paul A.; Richard, Sylvia; Vilé, Gianvito; Pérez-Ramírez, Javier (2018). "सुजुकी युग्मन के लिए सजातीय प्रणालियों को पार करने वाला एक विषम एकल-परमाणु पैलेडियम उत्प्रेरक" (PDF). Nature Nanotechnology. 13 (8): 702–707. Bibcode:2018NatNa..13..702C. doi:10.1038/s41565-018-0167-2. hdl:2072/359786. PMID 29941887. S2CID 49415437.
- ↑ Balog, Aaron; Meng, Dongfang; Kamenecka, Ted; Bertinato, Peter; Su, Dai-Shi; Sorensen, Erik J.; Danishefsky, Samuel J. (1996). "(-) का कुल संश्लेषण - एपोथिलोन ए". Angewandte Chemie International Edition in English. 35 (2324): 2801–2803. doi:10.1002/anie.199628011.
- ↑ Liu, Junjia; Lotesta, Stephen D.; Sorensen, Erik J. (2011). "प्लुरोमुटिलिन के आणविक ढांचे का संक्षिप्त संश्लेषण". Chemical Communications. 47 (5): 1500–2. doi:10.1039/C0CC04077K. PMC 3156455. PMID 21079876.
- ↑ Vyvyan, J. R.; Peterson, Emily A.; Stephan, Mari L. (1999). "(+/−) - caparratriene . का एक समीचीन कुल संश्लेषण". Tetrahedron Letters. 40 (27): 4947–4949. doi:10.1016/S0040-4039(99)00865-5.
- ↑ 29.0 29.1 29.2 29.3 Han, Fu-She (1 January 2013). "संक्रमण-धातु-उत्प्रेरित सुजुकी-मियाउरा क्रॉस-कपलिंग प्रतिक्रियाएं: पैलेडियम से निकल उत्प्रेरक के लिए एक उल्लेखनीय प्रगति". Chemical Society Reviews. 42 (12): 5270–98. doi:10.1039/c3cs35521g. PMID 23460083.
- ↑ Percec, Virgil; Bae, Jin-Young; Hill, Dale (1995). "धातु उत्प्रेरित होमोकूप्लिंग और क्रॉस-युग्मन प्रतिक्रियाओं में एरिल मेसाइलेट्स। 2. सुज़ुकी-प्रकार निकेल-उत्प्रेरित क्रॉस-कपलिंग ऑफ़ एरिल एरेनसल्फ़ोनेट्स और एरिल मेसाइलेट्स एरिलबोरोनिक एसिड के साथ". Journal of Organic Chemistry. 60 (4): 1060–1065. doi:10.1021/jo00109a044.
- ↑ Inada, Kaoru; Norio Miyaura (2000). "NiCl2 / Triphenylphosphine परिसरों द्वारा उत्प्रेरित आर्यल क्लोराइड के साथ आर्यलबोरोनिक एसिड के क्रॉस-युग्मन प्रतिक्रिया के माध्यम से बायरिल्स का संश्लेषण". Tetrahedron. 56 (44): 8657–8660. doi:10.1016/S0040-4020(00)00814-0.
- ↑ Zhao, Yu-Long; Li, You; Li, Shui-Ming; Zhou, Yi-Guo; Sun, Feng-Yi; Gao, Lian-Xun; Han, Fu-She (1 June 2011). "एरिल हैलाइड्स के सुजुकी-मियाउरा युग्मन के लिए एक अत्यधिक व्यावहारिक और विश्वसनीय निकेल उत्प्रेरक". Advanced Synthesis & Catalysis. 353 (9): 1543–1550. doi:10.1002/adsc.201100101.
- ↑ Wu, Lei; Ling, Jie; Wu, Zong-Quan (1 June 2011). "एक अत्यधिक सक्रिय और पुन: प्रयोज्य उत्प्रेरक: सुजुकी युग्मन प्रतिक्रिया के लिए फॉस्फीन डेंड्रिमर-स्थिर निकेल नैनोपार्टिकल्स". Advanced Synthesis & Catalysis. 353 (9): 1452–1456. doi:10.1002/adsc.201100134.
- ↑ Yang, C.T.; Zhang, Zhen-Qi; Liu, Yu-Chen; Liu, Lei (2011). "प्राथमिक एल्काइल हैलाइड्स और स्यूडोहैलाइड्स के साथ ऑर्गेनोबोरोन यौगिकों की कॉपर-उत्प्रेरित क्रॉस-युग्मन प्रतिक्रिया". Angew. Chem. Int. Ed. 50 (17): 3904–3907. doi:10.1002/anie.201008007. PMID 21455914.
- ↑ Bredford, R.B.; Hall, Mark A.; Hodges, George R.; Huwe, Michael; Wilkinson, Mark C. (2009). "बेंज़िल हैलाइड्स और 2-हैलोपाइरीडीन के साथ टेट्राएरिलबोरेट्स के सुजुकी कपलिंग के लिए सरल मिश्रित Fe-Zn उत्प्रेरक". Chem. Commun. (42): 6430–6432. doi:10.1039/B915945B. PMID 19841799. S2CID 40428708.
- ↑ Nakamura, M; Hashimoto, Toru; Kathriarachchi, Kalum K. A. D. S.; Zenmyo, Takeshi; Seike, Hirofumi; Nakamura, Masaharu (2012). "आयरन-उत्प्रेरित अल्काइल-अल्काइल सुजुकी-मियाउरा युग्मन". Angew. Chem. Int. Ed. 51 (35): 8834–883. doi:10.1002/anie.201202797. PMID 22848024.
- ↑ Na, Y; Park, Soyoung; Han, Soo Bong; Han, Hoon; Ko, Sangwon; Chang, Sukbok (2004). "रूथेनियम-उत्प्रेरित हेक-टाइप ओलेफिनेशन और सुजुकी युग्मन प्रतिक्रियाएं: उत्प्रेरक प्रजातियों की प्रकृति पर अध्ययन". J. Am. Chem. Soc. 126 (1): 250–258. doi:10.1021/ja038742q. PMID 14709090.
- ↑ 38.0 38.1 Weires, Nicholas A.; Baker, Emma L.; Garg, Neil K. (2015). "एमाइड्स का निकल-उत्प्रेरित सुजुकी-मियाउरा युग्मन". Nature Chemistry. 8 (1): 75–79. Bibcode:2016NatCh...8...75W. doi:10.1038/nchem.2388. PMID 26673267.
- ↑ Molander, Gary A.; Biolatto, Betina (2003). "पैलेडियम-उत्प्रेरित सुजुकी-मियाउरा पोटेशियम एरिल- और हेटेरोरिलट्रिफ्लोरोबोरेट्स की क्रॉस-युग्मन प्रतिक्रियाएं". J. Org. Chem. 68 (11): 4302–4314. doi:10.1021/jo0342368. PMID 12762730.
- ↑ Bates, Roderick (2012). संक्रमण धातुओं का उपयोग कर कार्बनिक संश्लेषण. Wiley. ISBN 978-1119978930.
- ↑ 41.0 41.1 Dolliver, Debra; Bhattarai, Bijay T.; Pandey, Arjun; Lanier, Megan L.; Bordelon, Amber S.; Adhikari, Sarju; Dinser, Jordan A.; Flowers, Patrick F.; Wills, Veronica S.; Schneider, Caroline L.; Shaughnessy, Kevin H.; Moore, Jane N.; Raders, Steven M.; Snowden, Timothy S.; McKim, Artie S.; Fronczek, Frank R. (2013). "स्टीरियोस्पेसिफिक सुजुकी, सोनोगाशिरा, और नेगीशी युग्मन प्रतिक्रियाएं एन-अल्कोक्सीमिडॉयल आयोडाइड्स और ब्रोमाइड्स". J. Org. Chem. 78 (8): 3676–3687. doi:10.1021/jo400179u. PMID 23534335.
- ↑ Asachenko, Andrey; Sorochkina, Kristina; Dzhevakov, Pavel; Topchiy, Maxim; Nechaev, Mikhail (2013). "सॉल्वेंट-मुक्त शर्तों के तहत सुजुकी-मियाउरा क्रॉस-कपलिंग". Adv. Synth. Catal. 355 (18): 3553–3557. doi:10.1002/adsc.201300741.
- ↑ Pan, Changduo; Liu, Zhang; Wu, Huayue; Din, Jinchang; Cheng, Jiang (2008). "पैलेडियम उत्प्रेरित लिगैंड-मुक्त सुजुकी क्रॉस-कपलिंग प्रतिक्रिया". Catalysis Communications. 9 (4): 321–323. doi:10.1016/j.catcom.2007.06.022.
- ↑ 44.0 44.1 Littke, Adam F.; Fu (2000). "सुज़ुकी क्रॉस-कपलिंग के लिए ऐरिल और विनाइल हैलाइड्स के साथ आर्यलबोरोनिक एसिड और माइल्ड परिस्थितियों में ट्राइफ्लेट्स के लिए बहुमुखी उत्प्रेरक". J. Am. Chem. Soc. 122 (17): 4020–4028. doi:10.1021/ja0002058.
- ↑ Hu, Ming-Gang; Wei, Song; Jian, Ai-Ai (2007). "अत्यधिक कुशल पीडी/सी-उत्प्रेरित सुजुकी युग्मन प्रतिक्रिया (पी-प्रतिस्थापित फिनाइल) बोरोनिक एसिड के साथ पी-(संयुक्त राष्ट्र) प्रतिस्थापित फेनिल हैलाइड". Chinese Journal of Chemistry. 25 (8): 1183–1186. doi:10.1002/cjoc.200790220.
- ↑ Saito, B; Fu (2007). "कमरे के तापमान पर अल्काइल-अल्काइल सुजुकी क्रॉस-कपलिंग्स ऑफ अनएक्टिवेटेड सेकेंडरी अल्काइल हैलाइड्स". J. Am. Chem. Soc. 129 (31): 9602–9603. doi:10.1021/ja074008l. PMC 2569998. PMID 17628067.
- ↑ Kingston, J.V.; Verkade, John G. (2007). "R2PNP(iBuNCH2CH2)3N का संश्लेषण और विशेषता: कुशल पीडी-असिस्टेड सुजुकी-मियाउरा क्रॉस-कपलिंग प्रतिक्रियाओं के लिए एक नया भारी इलेक्ट्रॉन-समृद्ध फॉस्फीन". J. Org. Chem. 72 (8): 2816–2822. doi:10.1021/jo062452l. PMID 17378611.
- ↑ Baillie, C; Zhang, Lixin; Xiao, Jianliang (2004). "फेरोसेनिल मोनोफॉस्फीन लिगैंड्स: एरिल क्लोराइड्स के सुजुकी-मियाउरा युग्मन में संश्लेषण और अनुप्रयोग". J. Org. Chem. 69 (22): 7779–7782. doi:10.1021/jo048963u. PMID 15498017.
- ↑ Han, J; Liu, Y; Guo, R (2009). "अत्यधिक स्थिर सोने के नैनोकणों का सुगम संश्लेषण और पानी में सुजुकी-मियाउरा क्रॉस-कपलिंग प्रतिक्रिया के लिए उनकी अप्रत्याशित उत्कृष्ट उत्प्रेरक गतिविधि". J. Am. Chem. Soc. 131 (6): 2060–2061. doi:10.1021/ja808935n. PMID 19170490.
- ↑ Lipshutz, B.H.; Petersen, Tue B.; Abela, Alexander R. (2008). "कमरे-तापमान सुजुकी-पानी में मियाउरा कपलिंग नॉनऑनिक एम्फीफाइल्स द्वारा सुगम किया गया†". Org. Lett. 10 (7): 1333–1336. doi:10.1021/ol702714y. PMID 18335944.