अनबिबियम
| Unbibium | ||||||
|---|---|---|---|---|---|---|
| उच्चारण | /ˌuːnbaɪˈbaɪəm/ | |||||
| Alternative names | element 122, eka-thorium | |||||
| Unbibium in the periodic table | ||||||
| ||||||
| Atomic number (Z) | 122 | |||||
| समूह | group n/a | |||||
| अवधि | period 8 | |||||
| ब्लॉक | g-block | |||||
| ऋणावेशित सूक्ष्म अणु का विन्यास | predictions vary, see text | |||||
| भौतिक गुण | ||||||
| Phase at STP | unknown | |||||
| परमाणु गुण | ||||||
| ऑक्सीकरण राज्य | (+4) (predicted)[1] | |||||
| Ionization energies | ||||||
| अन्य गुण | ||||||
| CAS नंबर | 54576-73-7 | |||||
| History | ||||||
| नामी | IUPAC systematic element name | |||||
| ||||||
अनबिबियम, जिसे तत्व 122 या ईका-थोरियम के रूप में भी जाना जाता है, आवर्त सारणी में Ubb के प्लेसहोल्डर प्रतीक और परमाणु संख्या 122 के साथ काल्पनिक रासायनिक तत्व है। अनबिबियम और Ubb क्रमशः अस्थायी व्यवस्थित आईयूपीएसी नाम और प्रतीक हैं, जिनका उपयोग तत्व के शोध पुष्टि और स्थायी नाम तय होने तक किया जाता है। तत्वों की आवर्त सारणी में, सुपरएक्टिनाइड्स के दूसरे तत्व और 8वें आवर्त के चौथे तत्व के रूप में अनबिनियम का अनुसरण करने की अपेक्षा है। यूनिनियम के समान, यह स्थिरता के द्वीप की सीमा के अंदर आने की अपेक्षा है, जो संभावित रूप से कुछ समस्थानिकों पर अतिरिक्त स्थिरता प्रदान करता है, विशेष रूप से 306Ubb जिसमें न्यूट्रॉन की आकर्षण संख्या (184) होने की अपेक्षा है।
कई प्रयासों के अतिरिक्त, अनबिबियम को अभी तक संश्लेषित नहीं किया गया है, न ही कोई प्राकृतिक रूप से पाए जाने वाले समस्थानिक पाए गए हैं। अनबिबियम को संश्लेषित करने का प्रयास करने की वर्तमान में कोई योजना नहीं है। 2008 में, यह प्रमाणित किया गया था कि यह प्राकृतिक थोरियम के प्रतिरूपों में शोध किया गया था,[3] किन्तु वह प्रमाण अब अधिक त्रुटिहीन प्रौद्योगिकी का उपयोग करके प्रयोग की वर्तमान पुनरावृत्तियों द्वारा समाप्त कर दिया गया है।
रासायनिक रूप से, अनबिबियम मोम और थोरियम के कुछ समानता दिखाने की अपेक्षा है। चूँकि, सापेक्षतावादी प्रभावों के कारण इसके कुछ गुण भिन्न हो सकते हैं; उदाहरण के लिए, g-ब्लॉक सुपरएक्टिनाइड श्रृंखला में इसकी अनुमानित स्थिति के अतिरिक्त, इसकी भूमिगत स्थिति इलेक्ट्रॉन विन्यास [Og] 7d1 8s2 8p1 या [Og] 8s2 8p2, होने की अपेक्षा है।[1]
परिचय
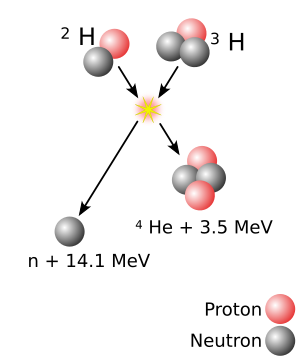
| External video | |
|---|---|
The heaviest[lower-alpha 1] atomic nuclei are created in nuclear reactions that combine two other nuclei of unequal size[lower-alpha 2] into one; roughly, the more unequal the two nuclei in terms of mass, the greater the possibility that the two react.[10] The material made of the heavier nuclei is made into a target, which is then bombarded by the beam of lighter nuclei. Two nuclei can fuse into one only if they approach each other closely enough; normally, nuclei (all positively charged) repel each other due to electrostatic repulsion. The strong interaction can overcome this repulsion but only within a very short distance from a nucleus; beam nuclei are thus greatly accelerated in order to make such repulsion insignificant compared to the velocity of the beam nucleus.[11] Coming close alone is not enough for two nuclei to fuse: when two nuclei approach each other, they usually remain together for approximately 10−20 seconds and then part ways (not necessarily in the same composition as before the reaction) rather than form a single nucleus.[11][12] If fusion does occur, the temporary merger—termed a compound nucleus—is an excited state. To lose its excitation energy and reach a more stable state, a compound nucleus either fissions or ejects one or several neutrons,[lower-alpha 3] which carry away the energy. This occurs in approximately 10−16 seconds after the initial collision.[13][lower-alpha 4]
The beam passes through the target and reaches the next chamber, the separator; if a new nucleus is produced, it is carried with this beam.[16] In the separator, the newly produced nucleus is separated from other nuclides (that of the original beam and any other reaction products)[lower-alpha 5] and transferred to a surface-barrier detector, which stops the nucleus. The exact location of the upcoming impact on the detector is marked; also marked are its energy and the time of the arrival.[16] The transfer takes about 10−6 seconds; in order to be detected, the nucleus must survive this long.[19] The nucleus is recorded again once its decay is registered, and the location, the energy, and the time of the decay are measured.[16]
Stability of a nucleus is provided by the strong interaction. However, its range is very short; as nuclei become larger, their influence on the outermost nucleons (protons and neutrons) weakens. At the same time, the nucleus is torn apart by electrostatic repulsion between protons, as it has unlimited range.[20] Nuclei of the heaviest elements are thus theoretically predicted[21] and have so far been observed[22] to primarily decay via decay modes that are caused by such repulsion: alpha decay and spontaneous fission;[lower-alpha 6] these modes are predominant for nuclei of superheavy elements. Alpha decays are registered by the emitted alpha particles, and the decay products are easy to determine before the actual decay; if such a decay or a series of consecutive decays produces a known nucleus, the original product of a reaction can be determined arithmetically.[lower-alpha 7] Spontaneous fission, however, produces various nuclei as products, so the original nuclide cannot be determined from its daughters.[lower-alpha 8]
The information available to physicists aiming to synthesize one of the heaviest elements is thus the information collected at the detectors: location, energy, and time of arrival of a particle to the detector, and those of its decay. The physicists analyze this data and seek to conclude that it was indeed caused by a new element and could not have been caused by a different nuclide than the one claimed. Often, provided data is insufficient for a conclusion that a new element was definitely created and there is no other explanation for the observed effects; errors in interpreting data have been made.[lower-alpha 9]
इतिहास
संश्लेषण प्रयास
संलयन-वाष्पीकरण
1970 के दशक में अनबिबियम को संश्लेषित करने के दो प्रयास किए गए थे, दोनों N = 184 और Z > 120 पर स्थिरता के द्वीप पर प्रारंभिक भविष्यवाणियों से प्रेरित थे,[34] और विशेष रूप से क्या अतिभारी तत्व संभावित रूप से स्वाभाविक रूप से उत्पन्न हो सकते हैं।[35] अनबिबियम को संश्लेषित करने का प्रथम प्रयास 1972 में फ्लेरोव एट अल द्वारा किया गया था। संयुक्त परमाणु अनुसंधान संस्थान (जेआईएनआर) में, भारी-आयन प्रेरित गर्म संलयन प्रतिक्रियाओं का उपयोग करते हुए:[35]
- 238
92U
+ 66,68
30Zn
→ 304,306
122Ubb
* → कोई परमाणु नहीं
अनबिबियम को संश्लेषित करने का एक और असफल प्रयास 1978 में जीएसआई हेल्महोल्ट्ज़ सेंटर में किया गया था, जहाँ प्राकृतिक एर्बियम लक्ष्य को क्सीनन-136 आयनों के साथ बमबारी की गई थी:[35]
- nat
68Er
+ 136
54Xe
→ 298,300,302,303,304,306
Ubb
* → कोई परमाणु नहीं
किसी परमाणु का पता नहीं चला और 5 nb (5,000 pb) की उपज सीमा मापी गई। वर्तमान परिणामों (फ्लोरोवियम देखें) ने दिखाया है कि इन प्रयोगों की संवेदनशीलता परिमाण के कम से कम 3 क्रमों से अधिक अल्प थी।[34] विशेष रूप से, के बीच प्रतिक्रिया 170Er और 136Xe के मध्य प्रतिक्रिया से माइक्रोसेकंड के अर्ध जीवन के साथ अल्फा उत्सर्जक उत्पन्न होने की अपेक्षा थी जो कि फ्लोरोवियम के समस्थानिकों में क्षय हो जाएगा, और अर्ध जीवन संभवतः कई घंटों तक बढ़ जाएगा, क्योंकि फ्लोरोवियम के स्थिरता द्वीप के केंद्र के निकट स्थित होने की भविष्यवाणी की गई है। बारह घंटे के विकिरण के पश्चात इस प्रतिक्रिया में कुछ भी नहीं मिला। 238U और 65Cu से यूनिनियम को संश्लेषित करने के समान असफल प्रयास के पश्चात, यह निष्कर्ष निकाला गया कि अतिभारी नाभिकों का अर्ध जीवन माइक्रोसेकंड से अल्प होना चाहिए या क्रॉस सेक्शन बहुत छोटे हैं।[36] अतिभारी तत्वों के संश्लेषण पर वर्तमान शोध से ज्ञात हुआ है कि दोनों निष्कर्ष सत्य हैं।[37][38]
2000 में, गेसेलशाफ्ट फर श्वेरियोनएनफोर्सचुंग (जीएसआई) हेल्महोल्ट्ज़ सेंटर फॉर हेवी आयन रिसर्च ने अत्यधिक संवेदनशीलता के साथ एक समान प्रयोग किया:[35]
- 238
92U
+ 70
30Zn
→ 308
122Ubb
* → कोई परमाणु नहीं
इन परिणामों से संकेत मिलता है कि ऐसे भारी तत्वों का संश्लेषण महत्वपूर्ण चुनौती बना हुआ है और बीम की तीव्रता और प्रायोगिक दक्षता में और सुधार की आवश्यकता है। अधिक गुणवत्ता वाले परिणामों के लिए भविष्य में संवेदनशीलता को 1 fb तक बढ़ाया जाना चाहिए।
यौगिक नाभिक विखंडन
306Ubb जैसे विभिन्न अतिभारी यौगिक नाभिकों की विखंडन विशेषताओं का अध्ययन करने वाले कई प्रयोग 2000 और 2004 के मध्य परमाणु प्रतिक्रियाओं की फ्लेरोव प्रयोगशाला में प्रदर्शित किए गए थे। दो परमाणु प्रतिक्रियाओं अर्थात् 248Cm + 58Fe और 242Pu + 64Ni का उपयोग किया गया।[35] परिणाम बताते हैं कि 132Sn (Z = 50, N = 82) जैसे सुपरहैवी नाभिक को बाहर निकालकर मुख्य रूप से अतिभारी नाभिक का विखंडन कैसे होता है। यह भी पाया गया कि संलयन-विखंडन मार्ग के लिए उपज 48Ca और 58Fe प्रोजेक्टाइल के मध्य समान थी, जो सुपरहैवी तत्व निर्माण में 58Fe प्रोजेक्टाइल के संभावित भविष्य के उपयोग का सुझाव देते हैं।[39]
स्वाभाविक रूप से पाए जाने वाले तत्व के रूप में शोध को प्रमाणित
2008 में, यरुशलम के हिब्रू विश्वविद्यालय में इज़राइली भौतिक विज्ञानी अम्नोन मारिनोव के नेतृत्व में समूह ने दावा किया कि प्राकृतिक रूप से पाए जाने वाले थोरियम जमा में यूनिबियम -292 के एकल परमाणु 10 के बीच बहुतायत में पाए गए हैं।-11 और 10-12 थोरियम के सापेक्ष।[3]69 वर्षों में यह पहली बार था कि मारगुएराइट पेरे की 1939 में फ्रैनशियम की खोज के बाद प्रकृति में नए तत्व की खोज का दावा किया गया था।[lower-alpha 10] मेरिनोव एट अल का दावा। वैज्ञानिक समुदाय के हिस्से द्वारा आलोचना की गई थी, और मारिनोव का कहना है कि उन्होंने प्रकृति (पत्रिका) और प्रकृति भौतिकी पत्रिकाओं को लेख प्रस्तुत किया है, किन्तु दोनों ने इसे सहकर्मी समीक्षा के लिए भेजे बिना इसे ठुकरा दिया।[40] अनबिबियम-292 परमाणुओं को सुपर विरूपण या अतिविरूपण परमाणु आइसोमर होने का दावा किया गया था, जिसमें कम से कम 100 मिलियन वर्षों का आधा जीवन था।[35]
तकनीक की आलोचना, जिसे पहले मास स्पेक्ट्रोमेट्री द्वारा हल्के थोरियम समस्थानिकों की पहचान करने के लिए इस्तेमाल किया गया था,[41] 2008 में भौतिक समीक्षा सी में प्रकाशित हुआ था।[42] मारिनोव समूह द्वारा खंडन प्रकाशित टिप्पणी के बाद फिजिकल रिव्यू सी में प्रकाशित किया गया था।[43] त्वरक मास स्पेक्ट्रोमेट्री (एएमएस) की बेहतर विधि का उपयोग करते हुए थोरियम प्रयोग की पुनरावृत्ति 100 गुना बेहतर संवेदनशीलता के बावजूद परिणामों की पुष्टि करने में विफल रही।[44] यह परिणाम थोरियम के लंबे समय तक रहने वाले समस्थानिकों के उनके दावों के संबंध में मारिनोव सहयोग के परिणामों पर काफी संदेह पैदा करता है,[41]रेन्टजेनियम,[45] और अनबिबियम।[3]अत्यधिक भारी तत्वों की वर्तमान समझ इंगित करती है कि प्राकृतिक थोरियम के नमूनों में अनबिबियम के किसी भी निशान के बने रहने की संभावना बहुत कम है।[35]
नामकरण
मेंडेलीव के पूर्वानुमानित तत्वों का उपयोग करना। अज्ञात और अनदेखे तत्वों के लिए मेंडेलीव के नामकरण, इसके बजाय अनबिबियम को इका-थोरियम के रूप में जाना जाना चाहिए।[46] 1979 में IUPAC के व्यवस्थित तत्व नाम के बाद, तत्व को बड़े पैमाने पर (Ubb) के परमाणु प्रतीक के साथ अनबिबियम के रूप में संदर्भित किया गया है।[47] इसके प्लेसहोल्डर का नाम के रूप में जब तक कि तत्व को आधिकारिक तौर पर खोजा और संश्लेषित नहीं किया जाता है, और स्थायी नाम तय किया जाता है। वैज्ञानिक इस नामकरण परंपरा को बड़े पैमाने पर अनदेखा करते हैं, और इसके बजाय केवल (122), या कभी-कभी E122 या 122 के प्रतीक के साथ तत्व 122 के रूप में अनबिबियम का उल्लेख करते हैं।[48]
भविष्य के संश्लेषण के लिए संभावनाएँ
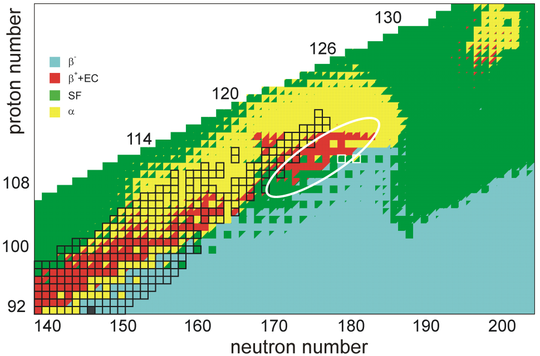
मेंडलीव से आगे के प्रत्येक तत्व को संलयन-वाष्पीकरण प्रतिक्रियाओं में उत्पादित किया गया था, जिसकी परिणति 2002 में सबसे भारी ज्ञात तत्व ओगनेसन की खोज में हुई थी।[50][51] और हाल ही में Tennessine 2010 में।[52] ये प्रतिक्रियाएँ वर्तमान प्रौद्योगिकी की सीमा तक पहुँच गईं; उदाहरण के लिए, Tennessine के संश्लेषण के लिए 22 मिलीग्राम की आवश्यकता होती है 249बीके और तीव्र 48छह महीने के लिए सीए बीम। अतिभारी तत्व अनुसंधान में बीम की तीव्रता 10 से अधिक नहीं हो सकती
लक्ष्य और डिटेक्टर को नुकसान पहुंचाए बिना प्रति सेकंड 12 प्रोजेक्टाइल, और तेजी से दुर्लभ और अस्थिर एक्टिनाइड लक्ष्यों की बड़ी मात्रा का उत्पादन करना अव्यावहारिक है।[53]नतीजतन, परमाणु अनुसंधान के लिए संयुक्त संस्थान (JINR) या RIKEN में सुपरहैवी एलिमेंट फैक्ट्री (SHE-Factory) जैसी सुविधाओं पर भविष्य के प्रयोग किए जाने चाहिए, जो प्रयोगों को अधिक समय तक चलने की अनुमति देगा और पहचान की क्षमताओं में वृद्धि करेगा और सक्षम करेगा। अन्यथा दुर्गम प्रतिक्रियाएँ।[54] यह संभव है कि संलयन-वाष्पीकरण अभिक्रियाएं अनबिबियम या भारी तत्वों की खोज के लिए उपयुक्त न हों। विभिन्न मॉडल Z = 122 और N ~ 180 के साथ माइक्रोसेकंड या उससे कम के क्रम में आइसोटोप के लिए तेजी से कम अल्फा क्षय और सहज विखंडन आधा जीवन की भविष्यवाणी करते हैं,[55] वर्तमान उपकरणों के साथ पता लगाना लगभग असंभव है।[37]सहज विखंडन का बढ़ता प्रभुत्व भी लिवरमोरियम या ओगानेसन के ज्ञात नाभिकों के संभावित संबंधों को तोड़ सकता है और पहचान और पुष्टि को और अधिक कठिन बना सकता है; की क्षय श्रृंखला की पुष्टि के मार्ग में भी ऐसी ही समस्या उत्पन्न हुई 294Og जिसका ज्ञात नाभिकों के लिए कोई लंगर नहीं है।[56] इन कारणों से, उत्पादन के अन्य तरीकों पर शोध करने की आवश्यकता हो सकती है जैसे बहु-नाभिक स्थानांतरण प्रतिक्रियाएं जो लंबे समय तक रहने वाले नाभिकों को आबाद करने में सक्षम हैं। प्रायोगिक तकनीक में एक समान स्विच तब हुआ जब गर्म संलयन का उपयोग किया गया 48Z > 113 के साथ तत्वों को आबाद करने के लिए कोल्ड फ्यूज़न (जिसमें परमाणु संख्या बढ़ने के साथ क्रॉस सेक्शन तेजी से घटते हैं) के बजाय Ca प्रोजेक्टाइल का उपयोग किया गया था।[38]
फिर भी, कई संलयन-वाष्पीकरण प्रतिक्रियाएं जो अनबिबियम की ओर ले जाती हैं, उन लोगों के अलावा प्रस्तावित की गई हैं जो पहले से ही असफल प्रयास कर चुके हैं, हालांकि किसी भी संस्था के पास संश्लेषण के प्रयास करने की तत्काल योजना नहीं है, इसके बजाय पहले 119, 120 और संभवतः 121 तत्वों पर ध्यान केंद्रित किया गया है। क्योंकि क्रॉस सेक्शन बढ़ते हैं प्रतिक्रिया की विषमता,[38]एक कलिफ़ोरनियम लक्ष्य के साथ संयोजन में एक क्रोमियम बीम सबसे अनुकूल होगा,[37]विशेष रूप से यदि N = 184 पर अनुमानित बंद न्यूट्रॉन खोल को अधिक न्यूट्रॉन-समृद्ध उत्पादों में पहुँचा जा सकता है और अतिरिक्त स्थिरता प्रदान की जा सकती है। विशेष रूप से, के बीच प्रतिक्रिया 54
24Cr
और 252
98Cf
यौगिक नाभिक उत्पन्न करेगा 306
122Ubb
और एन = 184 पर शेल तक पहुंचें, हालांकि ए के साथ समान प्रतिक्रिया 249
98Cf
से अवांछित विखंडन उत्पादों की उपस्थिति के कारण लक्ष्य को अधिक व्यवहार्य माना जाता है 252
98Cf
और लक्ष्य सामग्री की आवश्यक मात्रा जमा करने में कठिनाई।[57] अनबिबियम का एक संभावित संश्लेषण निम्नानुसार हो सकता है:[37]
- 249
98Cf
+ 54
24Cr
→ 300
122Ubb
+ 3 1
0
n
क्या यह प्रतिक्रिया सफल होनी चाहिए और अल्फा क्षय सहज विखंडन पर हावी रहता है, परिणामी 300Ubb समाप्त हो जाएगा 296यूबीएन जो बीच में क्रॉस-बमबारी में आबाद हो सकता है 249सीएफ और 50ती. यद्यपि यह प्रतिक्रिया निकट भविष्य में अनबिबियम के संश्लेषण के लिए सबसे आशाजनक विकल्पों में से एक है, अधिकतम अनुप्रस्थ काट 3 खलिहान (यूनिट) होने की भविष्यवाणी की गई है,[57]एक सफल प्रतिक्रिया में सबसे कम मापा क्रॉस सेक्शन से कम परिमाण का एक क्रम। अधिक सममित प्रतिक्रियाएं 244पु + 64न तो और 248सेमी + 58फे[37]भी प्रस्तावित किया गया है और अधिक न्यूट्रॉन युक्त समस्थानिकों का उत्पादन कर सकता है। बढ़ती परमाणु संख्या के साथ, किसी को भी विखंडन बाधा ऊंचाई घटने के बारे में पता होना चाहिए, जिसके परिणामस्वरूप यौगिक नाभिक की जीवित रहने की संभावना कम हो जाती है, विशेष रूप से जेड = 126 और एन = 184 पर अनुमानित जादुई संख्या से ऊपर।[57]
अनुमानित गुण
परमाणु स्थिरता और समस्थानिक

आवर्त सारणी के इस क्षेत्र में, N = 184 को परमाणु खोल मॉडल के रूप में सुझाया गया है, और विभिन्न परमाणु संख्याओं को बंद प्रोटॉन गोले के रूप में प्रस्तावित किया गया है, जैसे Z = 114, 120, 122, 124, और 126। स्थिरता को इन जादुई संख्याओं के पास स्थित नाभिक के लंबे आधे जीवन की विशेषता होगी, हालांकि प्रोटॉन शेल क्लोजर के कमजोर होने और दोहरे जादू के संभावित नुकसान की भविष्यवाणी के कारण स्थिरीकरण प्रभाव की सीमा अनिश्चित है।[60] अधिक हाल के शोध ने भविष्यवाणी की है कि स्थिरता का द्वीप इसके बजाय बीटा-क्षय स्थिर आइसोबार पर केंद्रित होगा। बीटा-स्थिर कॉपरनिकियम समस्थानिक 291सीएन और 293[38][61]जो द्वीप के ऊपर अनबिबियम को अच्छी तरह से रखता है और शेल प्रभावों की परवाह किए बिना कम आधा जीवन देता है। 112–118 तत्वों की बढ़ी हुई स्थिरता को ऐसे नाभिकों के चपटे गोलाकार आकार और सहज विखंडन के प्रतिरोध के लिए भी जिम्मेदार ठहराया गया है। यही मॉडल भी प्रस्तावित करता है 306Ubb अगले गोलाकार दोहरे जादुई नाभिक के रूप में, इस प्रकार गोलाकार नाभिक के लिए स्थिरता के वास्तविक द्वीप को परिभाषित करता है।[62]

रासायनिक
अनबिबियम को रसायन विज्ञान में सीरियम और थोरियम के समान होने की भविष्यवाणी की जाती है, इसी तरह एक महान गैस कोर के ऊपर चार रासायनिक संयोजन इलेक्ट्रॉन होते हैं, हालांकि यह अधिक प्रतिक्रियाशील हो सकता है। इसके अतिरिक्त, अनबिबियम को वैलेंस इलेक्ट्रॉन जी-इलेक्ट्रॉन परमाणुओं के एक नए ब्लॉक से संबंधित होने की भविष्यवाणी की जाती है, हालांकि 5 जी ऑर्बिटल को तत्व 125 तक भरना शुरू करने की उम्मीद नहीं है। अनबिबियम का अनुमानित ग्राउंड-स्टेट इलेक्ट्रॉन कॉन्फ़िगरेशन या तो [ओगानेसन] 7d है1 8s2 8p1</उप>[1][66] या 8s2 8p2</सुप>,[67] अपेक्षित [ओगानेसन] 5g के विपरीत2 8s2 जिसमें 5g कक्षीय तत्व 121 पर भरना शुरू करता है। (ds2पी और एस2</सुप>प2 कॉन्फ़िगरेशन के केवल लगभग 0.02 eV से अलग होने की उम्मीद है।)[67]सुपरएक्टिनाइड्स में, रिलेटिविस्टिक क्वांटम केमिस्ट्री औफबाऊ सिद्धांत के टूटने का कारण बन सकती है और 5g, 6f, 7d और 8p ऑर्बिटल्स का ओवरलैपिंग बना सकती है;[68] कॉपरनिकियम और फ्लोरोवियम के रसायन विज्ञान पर प्रयोग सापेक्षतावादी प्रभावों की बढ़ती भूमिका के मजबूत संकेत प्रदान करते हैं। जैसे, अनबिबियम के बाद तत्वों की रसायन शास्त्र भविष्यवाणी करना अधिक कठिन हो जाता है।
अनबिबियम सबसे अधिक संभावना एक डाइऑक्साइड, UbbOxygen का निर्माण करेगा2, और टेट्राहैलाइड्स, जैसे कि UbbFluorine4 और Ubb क्लोरीन4.[1]सेरियम और थोरियम के समान मुख्य ऑक्सीकरण अवस्था +4 होने की भविष्यवाणी की गई है।[35]5.651 इलेक्ट्रॉन वोल्ट की पहली आयनीकरण ऊर्जा और 11.332 eV की दूसरी आयनीकरण ऊर्जा की भविष्यवाणी अनबिबियम के लिए की जाती है; यह और अन्य गणना की गई आयनीकरण ऊर्जाएं थोरियम के अनुरूप मूल्यों से कम हैं, यह सुझाव देते हुए कि थोरियम की तुलना में अनबिबियम अधिक प्रतिक्रियाशील होगा।[66][2]
टिप्पणियाँ
- ↑ In nuclear physics, an element is called heavy if its atomic number is high; lead (element 82) is one example of such a heavy element. The term "superheavy elements" typically refers to elements with atomic number greater than 103 (although there are other definitions, such as atomic number greater than 100[5] or 112;[6] sometimes, the term is presented an equivalent to the term "transactinide", which puts an upper limit before the beginning of the hypothetical superactinide series).[7] Terms "heavy isotopes" (of a given element) and "heavy nuclei" mean what could be understood in the common language—isotopes of high mass (for the given element) and nuclei of high mass, respectively.
- ↑ In 2009, a team at JINR led by Oganessian published results of their attempt to create hassium in a symmetric 136Xe + 136Xe reaction. They failed to observe a single atom in such a reaction, putting the upper limit on the cross section, the measure of probability of a nuclear reaction, as 2.5 pb.[8] In comparison, the reaction that resulted in hassium discovery, 208Pb + 58Fe, had a cross section of ~20 pb (more specifically, 19+19
−11 pb), as estimated by the discoverers.[9] - ↑ The greater the excitation energy, the more neutrons are ejected. If the excitation energy is lower than energy binding each neutron to the rest of the nucleus, neutrons are not emitted; instead, the compound nucleus de-excites by emitting a gamma ray.[13]
- ↑ The definition by the IUPAC/IUPAP Joint Working Party states that a chemical element can only be recognized as discovered if a nucleus of it has not decayed within 10−14 seconds. This value was chosen as an estimate of how long it takes a nucleus to acquire its outer electrons and thus display its chemical properties.[14] This figure also marks the generally accepted upper limit for lifetime of a compound nucleus.[15]
- ↑ This separation is based on that the resulting nuclei move past the target more slowly then the unreacted beam nuclei. The separator contains electric and magnetic fields whose effects on a moving particle cancel out for a specific velocity of a particle.[17] Such separation can also be aided by a time-of-flight measurement and a recoil energy measurement; a combination of the two may allow to estimate the mass of a nucleus.[18]
- ↑ Not all decay modes are caused by electrostatic repulsion. For example, beta decay is caused by the weak interaction.[23]
- ↑ Since mass of a nucleus is not measured directly but is rather calculated from that of another nucleus, such measurement is called indirect. Direct measurements are also possible, but for the most part they have remained unavailable for heaviest nuclei.[24] The first direct measurement of mass of a superheavy nucleus was reported in 2018 at LBNL.[25] Mass was determined from the location of a nucleus after the transfer (the location helps determine its trajectory, which is linked to the mass-to-charge ratio of the nucleus, since the transfer was done in presence of a magnet).[26]
- ↑ Spontaneous fission was discovered by Soviet physicist Georgy Flerov,[27] a leading scientist at JINR, and thus it was a "hobbyhorse" for the facility.[28] In contrast, the LBL scientists believed fission information was not sufficient for a claim of synthesis of an element. They believed spontaneous fission had not been studied enough to use it for identification of a new element, since there was a difficulty of establishing that a compound nucleus had only ejected neutrons and not charged particles like protons or alpha particles.[15] They thus preferred to link new isotopes to the already known ones by successive alpha decays.[27]
- ↑ For instance, element 102 was mistakenly identified in 1957 at the Nobel Institute of Physics in Stockholm, Stockholm County, Sweden.[29] There were no earlier definitive claims of creation of this element, and the element was assigned a name by its Swedish, American, and British discoverers, nobelium. It was later shown that the identification was incorrect.[30] The following year, LBNL was unable to reproduce the Swedish results and announced instead their synthesis of the element; that claim was also disproved later.[30] JINR insisted that they were the first to create the element and suggested a name of their own for the new element, joliotium;[31] the Soviet name was also not accepted (JINR later referred to the naming of element 102 as "hasty").[32] The name "nobelium" remained unchanged on account of its widespread usage.[33]
- ↑ Four more elements were discovered after 1939 through synthesis, but were later found to also occur naturally: these were promethium, astatine, neptunium, and plutonium, all of which had been found by 1945.
संदर्भ
- ↑ 1.0 1.1 1.2 1.3 Pyykkö, Pekka (2011). "A suggested periodic table up to Z ≤ 172, based on Dirac–Fock calculations on atoms and ions". Physical Chemistry Chemical Physics. 13 (1): 161–8. Bibcode:2011PCCP...13..161P. doi:10.1039/c0cp01575j. PMID 20967377.
- ↑ 2.0 2.1 2.2 Eliav, E.; Fritzsche, S.; Kaldor, U. (2015). "Electronic structure theory of the superheavy elements". Nuclear Physics A. 944 (December 2015): 518–550. doi:10.1016/j.nuclphysa.2015.06.017.
- ↑ 3.0 3.1 3.2 Marinov, A.; Rodushkin, I.; Kolb, D.; et al. (2010). "Evidence for a long-lived superheavy nucleus with atomic mass number A=292 and atomic number Z=~122 in natural Th". International Journal of Modern Physics E. 19 (1): 131–140. arXiv:0804.3869. Bibcode:2010IJMPE..19..131M. doi:10.1142/S0218301310014662. S2CID 117956340.
- ↑ Wakhle, A.; Simenel, C.; Hinde, D. J.; et al. (2015). Simenel, C.; Gomes, P. R. S.; Hinde, D. J.; et al. (eds.). "Comparing Experimental and Theoretical Quasifission Mass Angle Distributions". European Physical Journal Web of Conferences. 86: 00061. Bibcode:2015EPJWC..8600061W. doi:10.1051/epjconf/20158600061. ISSN 2100-014X.
- ↑ Krämer, K. (2016). "Explainer: superheavy elements". Chemistry World. Retrieved 2020-03-15.
- ↑ "Discovery of Elements 113 and 115". Lawrence Livermore National Laboratory. Archived from the original on 2015-09-11. Retrieved 2020-03-15.
- ↑ Eliav, E.; Kaldor, U.; Borschevsky, A. (2018). "Electronic Structure of the Transactinide Atoms". In Scott, R. A. (ed.). Encyclopedia of Inorganic and Bioinorganic Chemistry. John Wiley & Sons. pp. 1–16. doi:10.1002/9781119951438.eibc2632. ISBN 978-1-119-95143-8. S2CID 127060181.
- ↑ Oganessian, Yu. Ts.; Dmitriev, S. N.; Yeremin, A. V.; et al. (2009). "Attempt to produce the isotopes of element 108 in the fusion reaction 136Xe + 136Xe". Physical Review C. 79 (2): 024608. doi:10.1103/PhysRevC.79.024608. ISSN 0556-2813.
- ↑ Münzenberg, G.; Armbruster, P.; Folger, H.; et al. (1984). "The identification of element 108" (PDF). Zeitschrift für Physik A. 317 (2): 235–236. Bibcode:1984ZPhyA.317..235M. doi:10.1007/BF01421260. S2CID 123288075. Archived from the original (PDF) on 7 June 2015. Retrieved 20 October 2012.
- ↑ Subramanian, S. (2019). "Making New Elements Doesn't Pay. Just Ask This Berkeley Scientist". Bloomberg Businessweek. Archived from the original on November 14, 2020. Retrieved 2020-01-18.
- ↑ 11.0 11.1 Ivanov, D. (2019). "Сверхтяжелые шаги в неизвестное" [Superheavy steps into the unknown]. N+1 (in русский). Retrieved 2020-02-02.
- ↑ Hinde, D. (2014). "Something new and superheavy at the periodic table". The Conversation. Retrieved 2020-01-30.
- ↑ 13.0 13.1 Krása, A. (2010). "Neutron Sources for ADS" (PDF). Czech Technical University in Prague. pp. 4–8. S2CID 28796927. Archived from the original (PDF) on 2019-03-03. Retrieved October 20, 2019.
- ↑ Wapstra, A. H. (1991). "Criteria that must be satisfied for the discovery of a new chemical element to be recognized" (PDF). Pure and Applied Chemistry. 63 (6): 883. doi:10.1351/pac199163060879. ISSN 1365-3075. S2CID 95737691. Retrieved 2020-08-28.
- ↑ 15.0 15.1 Hyde, E. K.; Hoffman, D. C.; Keller, O. L. (1987). "A History and Analysis of the Discovery of Elements 104 and 105". Radiochimica Acta. 42 (2): 67–68. doi:10.1524/ract.1987.42.2.57. ISSN 2193-3405. S2CID 99193729.
- ↑ 16.0 16.1 16.2 Chemistry World (2016). "How to Make Superheavy Elements and Finish the Periodic Table [Video]". Scientific American. Retrieved 2020-01-27.
- ↑ Hoffman, Ghiorso & Seaborg 2000, p. 334.
- ↑ Hoffman, Ghiorso & Seaborg 2000, p. 335.
- ↑ Zagrebaev, Karpov & Greiner 2013, p. 3.
- ↑ Beiser 2003, p. 432.
- ↑ Staszczak, A.; Baran, A.; Nazarewicz, W. (2013). "Spontaneous fission modes and lifetimes of superheavy elements in the nuclear density functional theory". Physical Review C. 87 (2): 024320–1. arXiv:1208.1215. Bibcode:2013PhRvC..87b4320S. doi:10.1103/physrevc.87.024320. ISSN 0556-2813. S2CID 118134429.
- ↑ Audi, G.; Kondev, F. G.; Wang, M.; et al. (2017). "The NUBASE2016 evaluation of nuclear properties". Chinese Physics C. 41 (3): 030001-128–030001-138. Bibcode:2017ChPhC..41c0001A. doi:10.1088/1674-1137/41/3/030001.
- ↑ Beiser 2003, p. 439.
- ↑ Oganessian, Yu. Ts.; Rykaczewski, K. P. (2015). "A beachhead on the island of stability". Physics Today. 68 (8): 32–38. Bibcode:2015PhT....68h..32O. doi:10.1063/PT.3.2880. ISSN 0031-9228. OSTI 1337838. S2CID 119531411.
- ↑ Grant, A. (2018). "Weighing the heaviest elements". Physics Today. doi:10.1063/PT.6.1.20181113a. S2CID 239775403.
- ↑ Howes, L. (2019). "Exploring the superheavy elements at the end of the periodic table". Chemical & Engineering News. Retrieved 2020-01-27.
- ↑ 27.0 27.1 Robinson, A. E. (2019). "The Transfermium Wars: Scientific Brawling and Name-Calling during the Cold War". Distillations. Retrieved 2020-02-22.
- ↑ "Популярная библиотека химических элементов. Сиборгий (экавольфрам)" [Popular library of chemical elements. Seaborgium (eka-tungsten)]. n-t.ru (in русский). Retrieved 2020-01-07. Reprinted from "Экавольфрам" [Eka-tungsten]. Популярная библиотека химических элементов. Серебро — Нильсборий и далее [Popular library of chemical elements. Silver through nielsbohrium and beyond] (in русский). Nauka. 1977.
- ↑ "Nobelium – Element information, properties and uses | Periodic Table". Royal Society of Chemistry. Retrieved 2020-03-01.
- ↑ 30.0 30.1 Kragh 2018, pp. 38–39.
- ↑ Kragh 2018, p. 40.
- ↑ Ghiorso, A.; Seaborg, G. T.; Oganessian, Yu. Ts.; et al. (1993). "Responses on the report 'Discovery of the Transfermium elements' followed by reply to the responses by Transfermium Working Group" (PDF). Pure and Applied Chemistry. 65 (8): 1815–1824. doi:10.1351/pac199365081815. S2CID 95069384. Archived (PDF) from the original on 25 November 2013. Retrieved 7 September 2016.
- ↑ Commission on Nomenclature of Inorganic Chemistry (1997). "Names and symbols of transfermium elements (IUPAC Recommendations 1997)" (PDF). Pure and Applied Chemistry. 69 (12): 2471–2474. doi:10.1351/pac199769122471.
- ↑ 34.0 34.1 Epherre, M.; Stephan, C. (1975). "Les éléments superlourds" (PDF). Le Journal de Physique Colloques (in français). 11 (36): C5–159–164. doi:10.1051/jphyscol:1975541.
- ↑ 35.0 35.1 35.2 35.3 35.4 35.5 35.6 35.7 Emsley, John (2011). Nature's Building Blocks: An A-Z Guide to the Elements (New ed.). New York, NY: Oxford University Press. p. 588. ISBN 978-0-19-960563-7.
- ↑ Hofmann, Sigurd (2014). On Beyond Uranium: Journey to the End of the Periodic Table. CRC Press. p. 105. ISBN 978-0415284950.
- ↑ 37.0 37.1 37.2 37.3 37.4 37.5 Karpov, A; Zagrebaev, V; Greiner, W (2015). "Superheavy Nuclei: which regions of nuclear map are accessible in the nearest studies" (PDF). cyclotron.tamu.edu. Texas A & M University. Retrieved 30 October 2018.
- ↑ 38.0 38.1 38.2 38.3 38.4 Zagrebaev, Karpov & Greiner 2013
- ↑ see Flerov lab annual reports 2000–2004 inclusive http://www1.jinr.ru/Reports/Reports_eng_arh.html
- ↑ Richard Van Noorden (2 May 2008). "सबसे भारी तत्व के दावे की आलोचना". Chemical World.
- ↑ 41.0 41.1 Marinov, A.; Rodushkin, I.; Kashiv, Y.; et al. (2007). "प्राकृतिक रूप से पाए जाने वाले न्यूट्रॉन की कमी वाले Th समस्थानिकों में लंबे समय तक रहने वाले आइसोमेरिक राज्यों का अस्तित्व". Phys. Rev. C. 76 (2). 021303(R). arXiv:nucl-ex/0605008. Bibcode:2007PhRvC..76b1303M. doi:10.1103/PhysRevC.76.021303. S2CID 119443571.
- ↑ Barber, R. C.; De Laeter, J. R. (2009). ""प्राकृतिक रूप से पाए जाने वाले न्यूट्रॉन की कमी वाले थ समस्थानिकों में लंबे समय तक रहने वाले आइसोमेरिक राज्यों के अस्तित्व पर टिप्पणी"". Phys. Rev. C. 79 (4). 049801. Bibcode:2009PhRvC..79d9801B. doi:10.1103/PhysRevC.79.049801.
- ↑ Marinov, A.; Rodushkin, I.; Kashiv, Y.; et al. (2009). ""प्राकृतिक रूप से पाए जाने वाले न्यूट्रॉन की कमी वाले थ समस्थानिकों में लंबे समय तक रहने वाले आइसोमेरिक राज्यों के अस्तित्व पर टिप्पणी करें" का उत्तर दें"". Phys. Rev. C. 79 (4). 049802. Bibcode:2009PhRvC..79d9802M. doi:10.1103/PhysRevC.79.049802.
- ↑ Lachner, J.; Dillmann, I.; Faestermann, T.; et al. (2008). "न्यूट्रॉन की कमी वाले थोरियम समस्थानिकों में लंबे समय तक रहने वाले आइसोमेरिक राज्यों की खोज करें". Phys. Rev. C. 78 (6). 064313. arXiv:0907.0126. Bibcode:2008PhRvC..78f4313L. doi:10.1103/PhysRevC.78.064313. S2CID 118655846.
- ↑ Marinov, A.; Rodushkin, I.; Pape, A.; et al. (2009). "प्राकृतिक एयू में एक अत्यधिक भारी तत्व के लंबे समय तक रहने वाले समस्थानिकों का अस्तित्व" (PDF). International Journal of Modern Physics E. World Scientific. 18 (3): 621–629. arXiv:nucl-ex/0702051. Bibcode:2009IJMPE..18..621M. doi:10.1142/S021830130901280X. S2CID 119103410. Archived from the original (PDF) on 2014-07-14. Retrieved February 12, 2012.
- ↑ Eliav, Ephraim; Landau, Arie; Ishikawa, Yasuyuki; Kaldor, Uzi (26 March 2002). "Electronic structure of eka-thorium (element 122) compared with thorium". Journal of Physics B: Atomic, Molecular and Optical Physics. 35 (7): 1693–1700. Bibcode:2002JPhB...35.1693E. doi:10.1088/0953-4075/35/7/307. S2CID 250750167.
- ↑ Chatt, J. (1979). "100 से बड़ी परमाणु संख्या के तत्वों के नामकरण के लिए अनुशंसाएँ". Pure Appl. Chem. 51 (2): 381–384. doi:10.1351/pac197951020381.
- ↑ Hoffman, Lee & Pershina 2006, p. 1724.
- ↑ Greiner, W (2013). "Nuclei: superheavy–superneutronic–strange–and of antimatter" (PDF). Journal of Physics: Conference Series. 413 (1). 012002. Bibcode:2013JPhCS.413a2002G. doi:10.1088/1742-6596/413/1/012002. Retrieved 30 April 2017.
- ↑ Oganessian, Y. T.; et al. (2002). "Element 118: results from the first 249
Cf
+ 48
Ca
experiment". Communication of the Joint Institute for Nuclear Research. Archived from the original on 22 July 2011. - ↑ "Livermore scientists team with Russia to discover element 118" (Press release). Livermore. 3 December 2006. Archived from the original on 17 October 2011. Retrieved 18 January 2008.
- ↑ Oganessian, Y. T.; Abdullin, F.; Bailey, P. D.; et al. (April 2010). "Synthesis of a New Element with Atomic Number 117" (PDF). Physical Review Letters. 104 (14). 142502. Bibcode:2010PhRvL.104n2502O. doi:10.1103/PhysRevLett.104.142502. PMID 20481935.
- ↑ Roberto, J. B. (2015). "अति-भारी तत्व अनुसंधान के लिए एक्टिनाइड लक्ष्य" (PDF). cyclotron.tamu.edu. Texas A & M University. Retrieved 30 October 2018.
- ↑ Hagino, Kouichi; Hofmann, Sigurd; Miyatake, Hiroari; Nakahara, Hiromichi (July 2012). "平成23年度 研究業績レビュー(中間レビュー)の実施について" [Implementation of the 2011 Research Achievement Review (Interim Review)] (PDF). www.riken.jp (in 日本語). RIKEN. Archived from the original (PDF) on 2019-03-30. Retrieved 5 May 2017.
- ↑ 55.0 55.1 55.2 Koura, H.; Katakura, J; Tachibana, T; Minato, F (2015). "न्यूक्लाइड्स का चार्ट". Japan Atomic Energy Agency. Retrieved 30 October 2018.
- ↑ Barber, R. C.; Karol, P. J.; Nakahara, H.; Vardaci, E.; Vogt, E. W. (2011). "Discovery of the elements with atomic numbers greater than or equal to 113 (IUPAC Technical Report)". Pure and Applied Chemistry. 83 (7): 1. doi:10.1351/PAC-REP-10-05-01.
- ↑ 57.0 57.1 57.2 57.3 Ghahramany, N.; Ansari, A. (September 2016). "Synthesis and decay process of superheavy nuclei with Z = 119-122 via hot fusion reactions" (PDF). European Physical Journal A. 52 (287): 287. Bibcode:2016EPJA...52..287G. doi:10.1140/epja/i2016-16287-6. S2CID 125102374.
- ↑ Pierre de Marcillac; Noël Coron; Gérard Dambier; Jacques Leblanc; Jean-Pierre Moalic (April 2003). "Experimental detection of α-particles from the radioactive decay of natural bismuth". Nature. 422 (6934): 876–878. Bibcode:2003Natur.422..876D. doi:10.1038/nature01541. PMID 12712201. S2CID 4415582.
- ↑ Considine, Glenn D.; Kulik, Peter H. (2002). वैन नोस्ट्रैंड का वैज्ञानिक विश्वकोश (9 ed.). Wiley-Interscience. ISBN 978-0-471-33230-5. OCLC 223349096.
- ↑ Koura, H.; Chiba, S. (2013). "अतिभारी और अत्यधिक अतिभारी द्रव्यमान क्षेत्र में गोलाकार नाभिक के एकल-कण स्तर". Journal of the Physical Society of Japan. 82 (1). 014201. Bibcode:2013JPSJ...82a4201K. doi:10.7566/JPSJ.82.014201.
- ↑ 61.0 61.1 Palenzuela, Y. M.; Ruiz, L. F.; Karpov, A.; Greiner, W. (2012). "सबसे भारी तत्वों के क्षय गुणों का व्यवस्थित अध्ययन" (PDF). Bulletin of the Russian Academy of Sciences: Physics. 76 (11): 1165–1171. Bibcode:2012BRASP..76.1165P. doi:10.3103/s1062873812110172. ISSN 1062-8738. S2CID 120690838.
- ↑ 62.0 62.1 Kratz, J. V. (5 September 2011). रासायनिक और भौतिक विज्ञान पर अतिभारी तत्वों का प्रभाव (PDF). 4th International Conference on the Chemistry and Physics of the Transactinide Elements. Retrieved 27 August 2013.
- ↑ Chowdhury, R. P.; Samanta, C.; Basu, D.N. (2008). "Nuclear half-lives for α -radioactivity of elements with 100 ≤ Z ≤ 130". Atomic Data and Nuclear Data Tables. 94 (6): 781–806. arXiv:0802.4161. Bibcode:2008ADNDT..94..781C. doi:10.1016/j.adt.2008.01.003. S2CID 96718440.
- ↑ 64.0 64.1 Santhosh, K.P.; Priyanka, B.; Nithya, C. (2016). "Feasibility of observing the α decay chains from isotopes of SHN with Z = 128, Z = 126, Z = 124 and Z = 122". Nuclear Physics A. 955 (November 2016): 156–180. arXiv:1609.05498. Bibcode:2016NuPhA.955..156S. doi:10.1016/j.nuclphysa.2016.06.010. S2CID 119219218.
- ↑ Poenaru, Dorin N.; Gherghescu, R. A.; Greiner, W. (2012). "अत्यधिक भारी नाभिक का क्लस्टर क्षय". Physical Review C. 85 (3): 034615. Bibcode:2012PhRvC..85c4615P. doi:10.1103/PhysRevC.85.034615. Retrieved 2 May 2017.
- ↑ 66.0 66.1 Hoffman, Lee & Pershina 2006, p. [page needed].
- ↑ 67.0 67.1 Umemoto, Koichiro; Saito, Susumu (1996). "अत्यधिक भारी तत्वों का इलेक्ट्रॉनिक विन्यास". Journal of the Physical Society of Japan. 65 (10): 3175–3179. Bibcode:1996JPSJ...65.3175U. doi:10.1143/JPSJ.65.3175. Retrieved 31 January 2021.
- ↑ Seaborg (c. 2006). "ट्रांसयूरेनियम तत्व (रासायनिक तत्व)". Encyclopædia Britannica. Retrieved 2010-03-16.
ग्रन्थसूची
- Audi, G.; Kondev, F. G.; Wang, M.; Huang, W. J.; Naimi, S. (2017). "The NUBASE2016 evaluation of nuclear properties" (PDF). Chinese Physics C. 41 (3): 030001. Bibcode:2017ChPhC..41c0001A. doi:10.1088/1674-1137/41/3/030001.
- Beiser, A. (2003). Concepts of modern physics (6th ed.). McGraw-Hill. ISBN 978-0-07-244848-1. OCLC 48965418.
- Hoffman, D. C.; Ghiorso, A.; Seaborg, G. T. (2000). The Transuranium People: The Inside Story. World Scientific. ISBN 978-1-78-326244-1.
- Hoffman, D. C.; Lee, D. M.; Pershina, V. (2006). "Transactinides and the future elements". In Morss, L. R.; Edelstein, N. M.; Fuger, J. (eds.). The Chemistry of the Actinide and Transactinide Elements. Vol. 3 (3rd ed.). Dordrecht, The Netherlands: Springer. pp. 1652–1752. ISBN 1-4020-3555-1.
- Kragh, H. (2018). From Transuranic to Superheavy Elements: A Story of Dispute and Creation. Springer. ISBN 978-3-319-75813-8.
- Zagrebaev, V.; Karpov, A.; Greiner, W. (2013). "Future of superheavy element research: Which nuclei could be synthesized within the next few years?". Journal of Physics: Conference Series. 420 (1). 012001. arXiv:1207.5700. Bibcode:2013JPhCS.420a2001Z. doi:10.1088/1742-6596/420/1/012001. ISSN 1742-6588. S2CID 55434734.