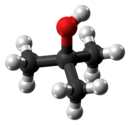
टर्ट-ब्यूटाइल अल्कोहल
|
| |||

| |||
| Names | |||
|---|---|---|---|
| Preferred IUPAC name
2-Methylpropan-2-ol | |||
Other names
| |||
| Identifiers | |||
3D model (JSmol)
|
|||
| 906698 | |||
| ChEBI | |||
| ChEMBL | |||
| ChemSpider | |||
| DrugBank | |||
| EC Number |
| ||
| 1833 | |||
| MeSH | tert-Butyl+Alcohol | ||
PubChem CID
|
|||
| RTECS number |
| ||
| UNII | |||
| UN number | 1120 | ||
| |||
| |||
| Properties | |||
| C4H10O | |||
| Molar mass | 74.123 g·mol−1 | ||
| Appearance | Colorless solid | ||
| Odor | Camphorous | ||
| Density | 0.775 g/mL | ||
| Melting point | 25 to 26 °C; 77 to 79 °F; 298 to 299 K | ||
| Boiling point | 82 to 83 °C; 179 to 181 °F; 355 to 356 K | ||
| miscible[2] | |||
| log P | 0.584 | ||
| Vapor pressure | 4.1 kPa (at 20 °C) | ||
| Acidity (pKa) | 16.54 [3] | ||
| 5.742×10−5 cm3/mol | |||
Refractive index (nD)
|
1.387 | ||
| 1.31 D | |||
| Thermochemistry | |||
Heat capacity (C)
|
215.37 J K−1 mol−1 | ||
Std molar
entropy (S⦵298) |
189.5 J K−1 mol−1 | ||
Std enthalpy of
formation (ΔfH⦵298) |
−360.04 to −358.36 kJ mol−1 | ||
Std enthalpy of
combustion (ΔcH⦵298) |
−2.64479 to −2.64321 MJ mol−1 | ||
| Hazards | |||
| GHS labelling: | |||
 
| |||
| Danger | |||
| H225, H319, H332, H335 | |||
| P210, P261, P305+P351+P338 | |||
| NFPA 704 (fire diamond) | |||
| Flash point | 11 °C (52 °F; 284 K) | ||
| 480 °C (896 °F; 753 K) | |||
| Explosive limits | 2.4–8.0% | ||
| Lethal dose or concentration (LD, LC): | |||
LD50 (median dose)
|
3559 mg/kg (rabbit, oral) 3500 mg/kg (rat, oral)[4] | ||
| NIOSH (US health exposure limits): | |||
PEL (Permissible)
|
TWA 100 ppm (300 mg/m3)[1] | ||
REL (Recommended)
|
TWA 100 ppm (300 mg/m3) ST 150 ppm (450 mg/m3)[1] | ||
IDLH (Immediate danger)
|
1600 ppm[1] | ||
| Safety data sheet (SDS) | inchem.org | ||
| Related compounds | |||
Related butanols
|
2-Butanol | ||
Related compounds
|
2-Methyl-2-butanol Trimethylsilanol | ||
Except where otherwise noted, data are given for materials in their standard state (at 25 °C [77 °F], 100 kPa).
| |||
टर्ट- ब्यूटाइल अल्कोहल सबसे सरल तृतीयक अल्कोहल है, जिसका रासायनिक सूत्र (CH3)3COH (कभी-कभी t-BuOH के रूप में दर्शाया जाता है) होता है। इसके आइसोमर्स 1-ब्यूटेनॉल, आइसोब्यूटेनॉल और ब्यूटेन-2-ओल हैं। टर्ट-ब्यूटाइल अल्कोहल एक रंगहीन ठोस होता है, जो कमरे के तापमान के करीब पिघलता है और इसमें कपूर जैसी गंध होती है। यह पानी, इथेनॉल और डाइथिलीन ईथर के साथ मिश्रण होता है।
प्राकृतिक घटना
बीयर और छोले में टर्ट-ब्यूटाइल अल्कोहल की पहचान की गई है।[5] यह कसावा में भी पाया जाता है,[6] जिसका उपयोग कुछ मादक पेय पदार्थों में किण्वन घटक के रूप में किया जाता है।
तैयारी
टर्ट- ब्यूटाइल अल्कोहल प्रोपलीन ऑक्साइड उत्पादन के सह-उत्पाद के रूप में आइसोब्यूटेन से व्यावसायिक रूप से प्राप्त होता है। यह आइसोब्यूटिलीन के उत्प्रेरक हाइड्रेशन द्वारा या एसीटोन और मिथाइलमैग्नीशियम क्लोराइड के बीच ग्रिग्नार्ड प्रतिक्रिया द्वारा भी उत्पादित किया जा सकता है।
शुद्धिकरण पानी के साथ स्थिर आसवन के निर्माण के कारण साधारण आसवन द्वारा नहीं किया जा सकता है, चूँकि पानी युक्त विलायक का प्रारंभिक शुष्कन को बेंजीन मे जोड़कर तृतीयक स्थिरक्वाथी बनाने और पानी को आसवित करने से किया जाता है। भिन्नात्मक आसवन के बाद कैल्शियम ऑक्साइड (CaO), पोटैशियम कार्बोनेट (K2CO3), कैल्शियम सल्फेट (CaSO4), या मैग्नीशियम सल्फेट (MgSO4), के साथ शुष्कन से पानी की थोड़ी मात्रा निकल जाती है। आयोडीन के साथ सक्रिय मैग्नीशियम, या सोडियम या पोटेशियम जैसी क्षार धातुओं से आगे पश्चवहन और आसवन द्वारा निर्जल टर्ट-ब्यूटाइल अल्कोहल प्राप्त किया जाता है। अन्य विधियों में 4 ångström|Å आणविक छलनी, एल्युमीनियम टर्ट-ब्यूटिलेट|एल्युमिनियम टर्ट-ब्यूटिलेट, कैल्शियम हाइड्राइड (CaH) का उपयोग शामिल है2), या निष्क्रिय वातावरण के तहत भिन्नात्मक क्रिस्टलीकरण।[7]
अनुप्रयोग
tert-ब्यूटाइल अल्कोहल का उपयोग सॉल्वेंट, इथेनॉल जहरीली शराब, पेंट रिमूवर इंग्रीडिएंट और पेट्रोल ऑक्टेन रेटिंग बूस्टर और ऑक्सीजनेट के रूप में किया जाता है। यह एक रासायनिक मध्यवर्ती है जिसका उपयोग मिथाइल टर्ट-ब्यूटाइल ईथर | मिथाइल टर्ट-ब्यूटाइल ईथर (MTBE) और एथिल टर्ट-ब्यूटाइल ईथर | एथिल टर्ट-ब्यूटाइल ईथर (ETBE) क्रमशः मेथनॉल और इथेनॉल के साथ प्रतिक्रिया करके, और टर्ट-ब्यूटाइल के उत्पादन के लिए किया जाता है। हाइड्रोपरॉक्साइड|टर्ट-ब्यूटाइल हाइड्रोपरॉक्साइड (टीबीएचपी) हाइड्रोजन पेरोक्साइड के साथ प्रतिक्रिया द्वारा।
प्रतिक्रियाएं
तृतीयक अल्कोहल के रूप में, टर्ट-ब्यूटाइल अल्कोहल ब्यूटेनॉल के अन्य आइसोमर्स की तुलना में ऑक्सीकरण के लिए अधिक प्रतिरोधी है।
एल्कोक्साइड देने के लिए टर्ट-ब्यूटिल अल्कोहल को एक मजबूत आधार (रसायन) के साथ अवक्षेपित किया जाता है। विशेष रूप से आम है पोटेशियम टर्ट-ब्यूटोऑक्साइड|[8]
- K + t-BuOH → t-BuO−के+ + 1/2 एच2
कार्बनिक रसायन विज्ञान में टर्ट-ब्यूटोक्साइड एक मजबूत, गैर-न्यूक्लियोफिलिक आधार है। यह सबस्ट्रेट्स से अम्लीय प्रोटॉनों को आसानी से सार कर देता है, लेकिन इसका स्टेरिक बल्क समूह को न्यूक्लियोफिलिक प्रतिस्थापन में भाग लेने से रोकता है, जैसे कि विलियमसन ईथर संश्लेषण या एसएन2|एसN2 प्रतिक्रिया।
टर्ट-ब्यूटिल अल्कोहल हाइड्रोजन क्लोराइड के साथ अभिक्रिया करके टर्ट-ब्यूटाइल क्लोराइड|टर्ट-ब्यूटाइल क्लोराइड बनाता है।
टर्ट-ब्यूटाइल हाइपोक्लोराइट देने के लिए हाइपोक्लोरस एसिड के साथ टर्ट-ब्यूटिल अल्कोहल का ओ-क्लोरिनेशन:[9]
- (सीएच3)3सीओएच + एचओसीएल → (सीएच3)3सीओसीएल + एच2हे
औषध विज्ञान और विष विज्ञान
मनुष्यों और अन्य जानवरों में tert-butanol के औषध विज्ञान और विष विज्ञान पर सीमित डेटा है।[10] ईंधन ऑक्सीजनयुक्त चयापचय के कारण मानव जोखिम हो सकता है। टर्ट-ब्यूटेनॉल त्वचा के माध्यम से खराब अवशोषित होता है लेकिन अगर साँस या अंतर्ग्रहण किया जाता है तो यह तेजी से अवशोषित हो जाता है। टर्ट-ब्यूटेनॉल त्वचा या आंखों में जलन पैदा कर रहा है। एकल खुराक की विषाक्तता आमतौर पर कम होती है लेकिन उच्च खुराक एक शामक या संवेदनाहारी प्रभाव पैदा कर सकती है।
संदर्भ
- ↑ 1.0 1.1 1.2 1.3 NIOSH Pocket Guide to Chemical Hazards. "#0078". National Institute for Occupational Safety and Health (NIOSH).
- ↑ "ICSC 0114 – tert-Butanol". Inchem.org. Retrieved 29 March 2018.
- ↑ Reeve, W.; Erikson, C. M.; Aluotto, P. F. (1979). "tert-Butyl alcohol". Can. J. Chem. 57: 2747. doi:10.1139/v79-444.
- ↑ "tert-Butyl alcohol". Immediately Dangerous to Life or Health Concentrations (IDLH). National Institute for Occupational Safety and Health (NIOSH).
- ↑ "टी- ब्यूटाइल अल्कोहल". National Library of Medicine HSDB Database. National Institute for Health. Retrieved 29 March 2018.
- ↑ "संग्रहीत प्रति" (PDF). Archived from the original (PDF) on 2016-03-04. Retrieved 2013-03-05.
- ↑ Perrin, D. D.; Armarego, W. L. F. (1988). प्रयोगशाला रसायनों का शुद्धिकरण (3rd ed.). Pergamon Press. ISBN 9780080347141.
- ↑ Johnson, W. S.; Schneider, W. P. (1950). "β-Carbethoxy-γ,γ-diphenylvinylacetic acid". Organic Syntheses. 30: 18. doi:10.15227/orgsyn.030.0018.
- ↑ Mintz, H. M.; Walling, C. (1969). "t-Butyl Hypochlorite". Org. Synth. 49: 9. doi:10.15227/orgsyn.049.0009.
- ↑ Douglas McGregor (2010). "Tertiary-Butanol: a toxicological review". Critical Reviews in Toxicology. 40 (8): 697–727. doi:10.3109/10408444.2010.494249. PMID 20722584. S2CID 26041562.
बाहरी संबंध
- International Chemical Safety Card 0114
- NIOSH Pocket Guide to Chemical Hazards. "#0078". National Institute for Occupational Safety and Health (NIOSH).
- IPCS Environmental Health Criteria 65: Butanols: four isomers
- IPCS Health and Safety Guide 7: tert-Butanol