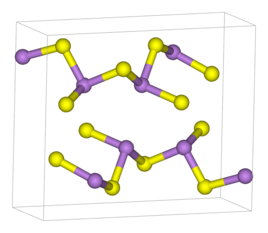
चाकोजेनाइड
चाकोजेनाइड एक रासायनिक यौगिक होता है जिसमें कम से कम एक चाकोजेन आयन और कम से कम एक अधिक विद्युत-धनात्मक तत्व होता है। चूंकि आवर्त सारणी के सभी समूह 16 तत्वों को चाकोजेन्स के रूप में परिभाषित किया गया है, लेकिन ऑक्साइड के अतिरिक्त सल्फाइड्स, सेलेनाइड्स, टेलुराइड (रसायन विज्ञान) और पोलोनाइड्स के लिए शल्कोजेनाइड शब्द अधिक सामान्य रूप से आरक्षित होते है।[1] कई धातु अयस्क चॉकोजेनाइड्स के रूप में उपस्थित होते है। जैरोग्राफी में फोटोकंडक्टिव चाकोजेनाइड ग्लास का उपयोग किया जाता है। कुछ रंजक और उत्प्रेरक भी चाकोजेनाइड्स पर आधारित होते है। धातु डाइक्लोजेनाइड MoS2 एक सामान्य ठोस स्नेहक होता है।
क्षार धातु और क्षारीय पृथ्वी चाकोजेनाइड्स
क्षार धातु और क्षारीय पृथ्वी मोनो चाकोजेनाइड्स नमक की तरह होते है, रंगहीन होते है और अधिकांशतः पानी में घुलनशील होते है। सल्फाइड हाइड्रोलिसिस से गुजरते है, जिसमें बाइसल्फ़ाइड (SH−) आयनों वाले डेरिवेटिव होते है। क्षार धातु चॉकोजेनाइड्स अधिकांशतः सोडियम क्लोराइड रूपांकनों में एंटीफ्लोराइट संरचना और क्षारीय पृथ्वी लवण के साथ क्रिस्टलीकृत होते है।
संक्रमण धातु चाकोजेनाइड्स
संक्रमण धातु चाकोजेनाइड्स कई स्टोइकियोमेट्री और कई संरचनाओं के साथ होते है।[2] तकनीकी रूप से सबसे सबसे महत्वपूर्ण, सरल स्टोइकोमेट्रीज़ चाकोजेनाइड्स होते है, जैसे 1: 1 और 1: 2। चरम स्थितियों में धातु-समृद्ध चरण (जैसे Ta2S) सम्मलित होते है, जो व्यापक धातु-धातु बंधन,[3] और क्लैकोजेनाइड-समृद्ध सामग्री जैसे Re2S7 प्रदर्शित करते है, जिसमें व्यापक चाकोजेन-चाल्कोजन बंधन सम्मलित होते है।
इन सामग्रियों को वर्गीकृत करने के उद्देश्य से, चाकोजेनाइड को अधिकांशतः डायनियन के रूप में देखा जाता है, अर्थात, S2−, Se2−, Te2−, और Po2−। वास्तव में, संक्रमण धातु चाकोजेनाइड अत्यधिक सहसंयोजक होते है, जैसा कि उनके अर्धचालक गुणों से संकेत मिलता है।[2]
धातु से भरपूर चाकोजेनाइड्स

उनके अधिकांश चाकोजेनाइड्स में, संक्रमण धातु या अधिक ऑक्सीकरण को अपनाते है। ऐसे कई उदाहरण उपस्थित है जहां धातु के परमाणुओं की संख्या चाकोजेन्स से कहीं अधिक होती है। ऐसे यौगिकों में सामान्यतः व्यापक धातु संबंध होते है।[5]
मोनोक्लेकोजेनाइड्स
धातु मोनो चाकोजेनाइड्स का सूत्र ME होता है, जहाँ M = एक संक्रमण धातु और E = S, Se, Te होता है। वे सामान्यतः जिंक सल्फाइड के संबंधित रूपों के नाम पर दो रूपों में से एक में क्रिस्टलीकृत होते है। जिंक मिश्रण संरचना में, सल्फाइड परमाणु एक घन समरूपता में पैक होते है और Zn2+ आयन टेट्राहेड्रल छिद्रों के आधे हिस्से पर कब्जा कर लेते है। परिणाम एक डायमंडॉइड फ्रेमवर्क होता है। मोनोक्लेकोजेनाइड्स के लिए मुख्य वैकल्पिक संरचना वर्टज़ाइट संरचना होती है जिसमें परमाणु संपर्क समान (टेट्राहेड्रल) होता है, लेकिन क्रिस्टल समरूपता हेक्सागोनल होती है। धातु मोनोक्लेकोजेनाइड के लिए एक तीसरा मूल भाव निकल आर्सेनाइड होती है, जहां धातु और क्लैकोजेनाइड प्रत्येक में क्रमशः ऑक्टाहेड्रल और ट्राइगोनल प्रिज्मीय समन्वय होता है। यह सामान्यतः नॉनस्टोइकियोमेट्री के अधीन होता है।[6]
महत्वपूर्ण मोनोक्लेकोजेनाइड्स में कुछ वर्णक सम्मलित होते है, विशेष रूप से कैडमियम सल्फाइड होता है। कई खनिज और अयस्क मोनोसल्फाइड होते है।[1]
डाइचलकोजेनाइड्स
धातु डाइक्लोजेनाइड्स का सूत्र ME2 होता है, जहां M = एक संक्रमण धातु और E = S, Se, Te होता है।[7] सबसे महत्वपूर्ण सल्फाइड होता है। वे हमेशा गहरे प्रतिचुंबकीय ठोस होते है, सभी सॉल्वैंट्स में अघुलनशील होते है, और अर्धचालक गुण प्रदर्शित करते है। कुछ अतिचालक भी होते है।[8]
उनकी विद्युतिए संरचनाओं के संदर्भ में, इन यौगिकों को सामान्यतः M4+ के डेरिवेटिव के रूप में देखा जाता है, जहां M4+ = Ti4+ (d0 विन्यास), V4+ (d1 विन्यास), Mo4+ (d2 विन्यास)। माध्यमिक बैटरियों के लिए प्रोटोटाइप कैथोड में टाइटेनियम डाइसल्फ़ाइड की जांच की गई थी, लिथियम द्वारा उत्क्रमणीय रूप से अंतर्संबंध से गुजरने की इसकी क्षमता का शोषण किया गया था। मोलिब्डेनम डाइसल्फ़ाइड हजारों लेखों का विषय होता है और मोलिब्डेनम का मुख्य अयस्क होता है, जिसे मोलिब्डेनाईट कहा जाता है। यह हाइड्रोडीसल्फराइजेशन के लिए एक ठोस स्नेहक और उत्प्रेरक के रूप में प्रयोग किया जाता है। संबंधित डिसेलेनाइड्स और यहां तक कि डिटेल्यूराइड्स भी ज्ञात होता है, उदाहरण के लिए, TiSe2, MoSe2 और WSe2।
संक्रमण धातु
संक्रमण धातु डाइक्लोजेनाइड्स सामान्यतः या तो कैडमियम डायोडाइड या मोलिब्डेनम डाइसल्फ़ाइड संरचनाओं को अपनाते है। CdI2 रूपांकन में, धातुएँ अष्टफलकीय संरचनाओं का प्रदर्शन करते है। MoS2 में, जो डाइहैलाइड्स के लिए नहीं देखा गया है, धातु त्रिकोणीय प्रिज्मीय संरचनाओं को प्रदर्शित करते है।[1] धातु और चाकोजेनाइड लिगैंड्स के बीच मजबूत बंधन, परतों के बीच कमजोर चाकोजेनाइड बंधन के विपरीत होते है। इन विपरीत बंधन ऊर्जा के कारण, ये सामग्रियां क्षार धातुओं द्वारा अंतः क्रिया में संलग्न होती है। इंटरकैलेशन प्रक्रिया चार्ज स्थानांतरण के साथ होती है, एम (IV) केंद्रों को एम (III) तक कम कर देती है। 2डी टंगस्टन डिसेलेनाइड में इलेक्ट्रॉनों और छिद्रों के बीच का आकर्षण एक विशिष्ट 3डी अर्धचालक की तुलना में 100 गुना अधिक मजबूत होता है।[8]
पाइराइट और संबंधित डाइसल्फ़ाइड
मौलिक धातु डाइक्लोजेनाइड्स के विपरीत, आयरन पाइराइट, एक सामान्य खनिज होता है, जो सामान्यतः Fe2+ और पर्सल्फ़िडो आयन S22− से मिलकर वर्णित किया जाता है। डाइसल्फ़िडो डायनियन के भीतर सल्फर परमाणु एक छोटे एस-एस बंधन के माध्यम से एक साथ बंधे होते है।[2] प्रारंभिक धातुओं (V, Ti, Mo, W) के विपरीत संक्रमण धातु डाइसल्फ़ाइड्स (Mn, Fe, Co, Ni) लगभग हमेशा पाइराइट या संबंधित मार्कासाइट रूपांकनों को अपनाते है, जो दो चाकोजेनाइड डायनियन्स के साथ 4+ ऑक्सीकरण अवस्था को अपनाते है। .
त्रि- और टेट्राचलकोजेनाइड्स
कई धातुएँ, मुख्य रूप से प्रारंभिक धातुओं (Ti, V, Cr, Mn समूह) के लिए भी ट्राइकलकोजेनाइड्स बनाती है। इन सामग्रियों को सामान्यतः M4+(E22−)(E2−) (जहां E = S, Se, Te) के रूप में वर्णित किया जाता है। एक प्रसिद्ध उदाहरण नाइओबियम ट्राइसेलेनाइड है। अम्ल के साथ टेट्राथियोमोलीबडेट के उपचार द्वारा अनाकार MoS3 का उत्पादन किया जाता है:
- MoS42− + 2 H+ → MoS3 + H2S
खनिज पेट्रोनाइट, जिसका सूत्र VS4 होता है, धातु टेट्राचलकोजेनाइड का एक उदाहरण होता है। क्रिस्टलोग्राफिक विश्लेषण से पता चलता है कि सामग्री को बीआईएस (पर्सल्फ़ाइड) माना जा सकता है, अर्थात V4+,(S22−)2 [2]
मुख्य समूह चाकोजेनाइड्स
चाकोजेन डेरिवेटिव महान गैसों को छोड़कर सभी मुख्य समूह तत्वों के लिए जाने जाते है। सामान्यतः, उनके स्टोइकियोमेट्रीज क्लासिकल वैलेंस ट्रेंड का पालन करते है, उदाहरण SiS2, B2S3, Sb2S3। चूंकि कई अपवाद उपस्थित होते है, उदाहरण P4S3 और S4N4। कई मुख्य समूह सामग्रियों की संरचनाएं निकट पैकिंग के अतिरिक्त दिशात्मक सहसंयोजक बंधन द्वारा निर्धारित होती है।[1]
हैलाइड्स, नाइट्राइड्स और ऑक्साइड्स के लिए चाकोजेन को सकारात्मक ऑक्सीकरण दर्जे दिए गए है।
यह भी देखें
- कार्बन डाइक्लोजेनाइड
- चालकोजेन
- चाकोजेनाइड ग्लास
- हाइड्रोजन चाकोजेनाइड
- नकारात्मक प्रतिरोध
- चरण-परिवर्तन स्मृति
संदर्भ
- ↑ 1.0 1.1 1.2 1.3 Greenwood, N. N.; & Earnshaw, A. (1997). Chemistry of the Elements (2nd Edn.), Oxford:Butterworth-Heinemann. ISBN 0-7506-3365-4.
- ↑ 2.0 2.1 2.2 2.3 Vaughan, D. J.; Craig, J. R. “Mineral Chemistry of Metal Sulfides" Cambridge University Press, Cambridge: 1978. ISBN 0521214890.
- ↑ Hughbanks, Timothy (1995). "प्रारंभिक संक्रमण तत्वों के धातु-समृद्ध रसायन की खोज". Journal of Alloys and Compounds. 229: 40–53. doi:10.1016/0925-8388(95)01688-0.
- ↑ Franzen, H.F.; Beineke, T.A.; Conrad, B.R. (1968). "The crystal structure of Nb21S8". Acta Crystallographica B. 24 (3): 412–p416. doi:10.1107/S0567740868002463.
- ↑ Franzen, Hugo F. (1978). "Structure and Bonding of Metal-Rich Compounds: Pnictides, chalcogenides and halides". Progress in Solid State Chemistry. 12: 1–39. doi:10.1016/0079-6786(78)90002-X.
{{cite journal}}: CS1 maint: uses authors parameter (link) - ↑ "Sulfide Mineralogy: Volume 1" Paul H. Ribbe, editor, 1974, Mineralogical Society of America. ISBN 0-939950-01-4
- ↑ Wells, A.F. (1984) Structural Inorganic Chemistry, Oxford: Clarendon Press. ISBN 0-19-855370-6.
- ↑ 8.0 8.1 Wood, Charlie (2022-08-16). "फिजिक्स डुओ को दो आयामों में जादू लगता है". Quanta Magazine (in English). Retrieved 2022-08-22.
बाहरी संबंध
- Advanced Chalcogenide Technologies and Applications Lab ACTAlab Jun 14, 2016
- Phase change memory-based 'moneta' system points to the future of computer storage ScienceBlog Jun 03, 2011
- Kovalenko, Maksym V.; Scheele, Marcus; Talapin, Dmitri V. (2009). "Colloidal Nanocrystals with Molecular Metal Chalcogenide Surface Ligands". Science. 324 (5933): 1417–1420. Bibcode:2009Sci...324.1417K. doi:10.1126/science.1170524. PMID 19520953. S2CID 21845356.
- Big Blue boffins hatch dirt-cheap solar cells The Register, 12 February 2010