डाईनाइट्रोजन डाईफ्लोराइड
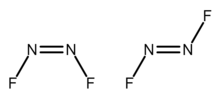 cis-Dinitrogen difluoride (left) and trans-dinitrogen difluoride (right)
| |||
|
| |||
| Names | |||
|---|---|---|---|
| IUPAC name
cis- or trans-dinitrogen difluoride
| |||
| Other names
cis- or trans-difluorodiazene
| |||
| Identifiers | |||
| |||
3D model (JSmol)
|
| ||
| ChemSpider | |||
PubChem CID
|
|||
| |||
| |||
| Properties | |||
| FN=NF | |||
| Molar mass | 66.011 g·mol−1 | ||
| Appearance | Colorless gas | ||
| Density | 2.698 g/L | ||
| Melting point | cis: less than −195 °C (−319.0 °F; 78.1 K) trans: −172 °C (−278 °F) | ||
| Boiling point | cis: −105.75 °C (−158.35 °F; 167.40 K) trans: −111.45 °C (−168.61 °F) | ||
| cis: 0.16 D trans: 0 D | |||
| Thermochemistry | |||
Std enthalpy of
formation (ΔfH⦵298) |
cis: 69.5 kJ/mol trans: 82.0 kJ/mol | ||
| Related compounds | |||
Other anions
|
Azide | ||
Other cations
|
|||
Related compounds
|
|||
Except where otherwise noted, data are given for materials in their standard state (at 25 °C [77 °F], 100 kPa).
| |||
डाईनाइट्रोजन डाईफ्लोराइड एक रासायनिक यौगिक है जिसका सूत्र N2F2 है। यह कमरे के तापमान पर एक गैस है और पहली बार 1952 में एजाइड FN3 के थर्मल अपघटन उत्पाद के रूप में पहचाना गया था। इसकी संरचना F−N=N−F है और यह सिस - और ट्रांस -रूप दोनों में स्थित होता है।
आइसोमर्स
सिस विन्यास C2v सममिति में निहित है और ट्रांस -रूप में C2h की सममिति है। ये समावयवी ऊष्मीय रूप से अंतरपरिवर्तनीय होते हैं लेकिन इन्हें कम तापमान के प्रभाजन द्वारा अलग किया जा सकता है। ट्रांस-फॉर्म कम थर्मोडायनामिक रूप से स्थिर है लेकिन कांच के बर्तनों में संग्रहीत किया जा सकता है। सिस-फॉर्म सिलिकॉन टेट्राफ्लोराइड और नाइट्रस ऑक्साइड बनाने के लिए लगभग 2 सप्ताह के समय के पैमाने पर कांच पर आक्रमण करता है:[2]
- 2 N2F2 + SiO2 → SiF4 + 2 N2O
तैयारी
डिनाइट्रोजन डिफ्लोराइड की अधिकांश तैयारी दो आइसोमर्स के मिश्रण देती है लेकिन उन्हें स्वतंत्र रूप से तैयार किया जा सकता है।
एक जलीय विधि में केंद्रित पोटेशियम हाइड्रोक्साइड के साथ एन, एन -डिफ्लोरो यूरिया सम्मिलित है। यह ट्रांस आइसोमर के तीन गुना अधिक के साथ 40% उपज देता है।
डाइफ्लुओरोमाइन पोटेशियम फ्लोराइड (या रुबिडियम फ्लोराइड या सीज़ियम फ्लोराइड) के साथ एक ठोस अस्थिर यौगिक बनाता है जो डाइनाइट्रोजन डिफ्लोराइड में विघटित हो जाता है।[3]
यह टेट्राफ्लोरोहाइड्राजाइन और ब्रोमिन के फोटोलीसिस द्वारा भी तैयार किया जा सकता है:[4]
- N2F4 N2F2 + byproducts
प्रतिक्रियाएं
डाइफ्लुओरोडियाज़ीन का सीआईएस रूप रेखीय आणविक ज्यामिति बनाने के लिए एंटीमनी पेंटाफ्लोराइड जैसे मजबूत फ्लोराइड आयन स्वीकर्ता के साथ प्रतिक्रिया करेगा।[5] [N≡N−F]+ धनायन (फ्लोरोडियाज़ोनियम धनायन[5]) जो सूत्र के साथ लवण (रसायन) बनाता है [N≡N−F]+[SbF6]− (फ्लोरोडियाज़ोनियम हेक्साफ्लोरोएंटीमोनेट (वी))।
- F−N=N−F + SbF5 → [N≡N−F]+[SbF6]−
आर्सेनिक पेंटाफ्लोराइड के साथ सिस -डिफ्लुओरोडियाज़ीन की अनुरूप प्रतिक्रिया सूत्र के साथ सफेद ठोस नमक देती है [N≡N−F]+[AsF6]−[5] (फ्लोरोडियाज़ोनियम हेक्साफ्लोरोअरसेनेट (वी))।
- F−N=N−F + AsF5 → [N≡N−F]+[AsF6]−
ठोस चरण में [N≡N−F] + केशन में देखे गए N≡N और N−F बॉन्ड की दूरी क्रमशः 1.089(9) और 1.257(8) Å हैं जो सबसे कम प्रयोगात्मक रूप से देखे गए NN और NF बॉन्ड हैं।
संदर्भ
- ↑ Lide, David R. (1998). Handbook of Chemistry and Physics (87th ed.). Boca Raton, FL: CRC Press. pp. 4–73, 5–15, 9–46. ISBN 0-8493-0594-2.
- ↑ Greenwood, Norman N.; Earnshaw, Alan (1997). Chemistry of the Elements (2nd ed.). Butterworth-Heinemann. ISBN 978-0-08-037941-8.
- ↑ Sykes, A. G. (1989-07-17). अकार्बनिक रसायन विज्ञान में अग्रिम. Academic Press. p. 171. ISBN 9780080578828. Retrieved 21 June 2014.
- ↑ Leon M. Zaborowski; et al. (1973), Aaron Wold and John K. Ruff (ed.), Chlorodifluoroamine and Difluorodiazene - B. Difluorodiazene (Dinitrogen difluoride), Inorganic Syntheses (in German), vol. 14, McGraw-Hill Book Company, Inc., pp. 34–39
{{citation}}: CS1 maint: unrecognized language (link) - ↑ 5.0 5.1 5.2 Cacace, Fulvio; Grandinetti, Felice; Pepi, Federico (1995). "Gaseous Fluorodiazonium Ions. Experimental and Theoretical Study on Formation and Structure of FN2+". Inorganic Chemistry. 34 (6): 1325–1332. doi:10.1021/ic00110a007.

