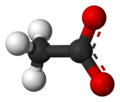
पोटेशियम एसीटेट

| |||
|
| |||
| Names | |||
|---|---|---|---|
| Preferred IUPAC name
Potassium acetate | |||
| Other names
Potassium ethanoate, E261
| |||
| Identifiers | |||
3D model (JSmol)
|
|||
| ChEMBL | |||
| ChemSpider | |||
PubChem CID
|
|||
| UNII | |||
| Properties | |||
| C2H3KO2 | |||
| Molar mass | 98.142 g·mol−1 | ||
| Appearance | White deliquescent crystalline powder | ||
| Density | 1.8 g/cm3 (20 °C)[1] 1.57 g/cm3 (25 °C) | ||
| Melting point | 292 °C (558 °F; 565 K) | ||
| Boiling point | Decomposes | ||
| 216.7 g/100 mL (0.1 °C) 233.8 g/100 mL (10 °C) 268.6 g/100 mL (25 °C) 320.8 g/100 mL (40 °C) 390.7 g/100 mL (96 °C)[2] | |||
| Solubility | Soluble in alcohol, liquid ammonia Insoluble in ether, acetone | ||
| Solubility in methanol | 24.24 g/100 g (15 °C) 53.54 g/100 g (73.4 °C)[1] | ||
| Solubility in ethanol | 16.3 g/100 g[1] | ||
| Solubility in sulfur dioxide | 0.06 g/kg (0 °C)[1] | ||
| Acidity (pKa) | 4.76 | ||
| Structure | |||
| Monoclinic | |||
| Thermochemistry | |||
Heat capacity (C)
|
109.38 J/mol·K[3] | ||
Std molar
entropy (S⦵298) |
150.82 J/mol·K[3] | ||
Std enthalpy of
formation (ΔfH⦵298) |
−722.6 kJ/mol[1] | ||
| Pharmacology | |||
| B05XA17 (WHO) | |||
| Hazards | |||
| NFPA 704 (fire diamond) | |||
| Lethal dose or concentration (LD, LC): | |||
LD50 (median dose)
|
3250 mg/kg (oral, rat)[4] | ||
Except where otherwise noted, data are given for materials in their standard state (at 25 °C [77 °F], 100 kPa).
| |||
पोटेशियम एसीटेट (जिसे पोटेशियम एथेनोएट भी कहा जाता है), (CH3COOK) एसिटिक अम्ल का पोटेशियम लवण है। यह कमरे के तापमान पर एक आर्द्रताग्राही ठोस है।
तैयारी
इसे पोटेशियम युक्त क्षार जैसे पोटेशियम हाइड्रॉक्साइड या पोटेशियम कार्बोनेट को एसिटिक अम्ल के साथ उपचारित करके तैयार किया जा सकता है:
- CH3COOH + KOH → CH3COOK + H2O
इस प्रकार की अभिक्रिया को अम्ल-क्षार उदासीनीकरण अभिक्रिया के रूप में जाना जाता है।
जल के घोल में सेसक्विहाइड्रेट (CH3COOK·1½H2O) 41.3 डिग्री सेल्सियस पर सेमीहाइड्रेट बनना प्रारम्भ कर देता है।[2]
अनुप्रयोग
विहिमन
पोटेशियम एसीटेट (कैल्शियम क्लोराइड या मैग्नीशियम क्लोराइड के विकल्प के रूप में) का उपयोग बर्फ हटाने या इसके गठन को रोकने के लिए विहिमक के रूप में किया जा सकता है। यह मिट्टी पर कम आक्रामक और कम संक्षारक होने का लाभ प्रदान करता है: इस कारण से, इसे हवाई अड्डे के दौड़पथ के लिए उपयोग किया जाता है, यद्यपि यह अधिक महंगा है।
आग बुझाने
पोटेशियम एसीटेट कक्षा K वाले अग्निशामक यंत्रों में प्रयोग किया जाने वाला और आग बुझाने वाला कारक है क्योंकि इसमें ठंडा करने और जलते हुए तेल पर परत बनाने की क्षमता होती है।
खाद्य योज्य
पोटेशियम एसीटेट का उपयोग प्रसंस्कृत खाद्य पदार्थों में परिरक्षक और अम्लता नियामक के रूप में किया जाता है। यूरोपीय संघ में, इसे इ नंबर E261 द्वारा चिन्हित किया गया है;[5]इसे संयुक्त राज्य अमेरिका[6] ऑस्ट्रेलिया और न्यूजीलैंड में भी उपयोग के लिए अनुमोदित किया गया है।[7] पोटेशियम हाइड्रोजन डाइएसीटेट (CAS) सूत्र KH(OOCCH3)2 पोटेशियम एसीटेट के समान E नंबर वाला एक संबंधित खाद्य योज्य है।
चिकित्सा और जैव रसायन
दवा में, पोटेशियम एसीटेट का उपयोग मधुमेह केटोएसिडोसिस के उपचार में इलेक्ट्रोलाइट प्रतिस्थापन प्रोटोकॉल के एक भाग के रूप में किया जाता है क्योंकि इसकी अम्लीय अवस्था को प्रभावहीन करने में मदद करने के लिए बाइकार्बोनेट को तोड़ने की क्षमता होती है।
आणविक जीव विज्ञान में, पोटेशियम एसीटेट का उपयोग डीएनए से इथेनॉल निकालने के लिए डोडेसिल सल्फेट (DS) और DS-बंध प्रोटीन को अवक्षेपित करने के लिए किया जाता है।
पोटेशियम एसीटेट का उपयोग ऊतक संरक्षण, निर्धारण और ममीकरण के लिए लगाए जाने वाले मिश्रण में किया जाता है। आज अधिकांश संग्रहालय 1897 में कैसरलिंग द्वारा अनुशंसित फॉर्मेल्डिहाइड-आधारित विधि का उपयोग करते हैं जिसमें पोटेशियम एसीटेट होता है।[8] इस प्रक्रिया का उपयोग लेनिन को भिगोने के लिए किया गया था।[9]
निष्पादन में प्रयोग करें
जनवरी 2015 में ओक्लाहोमा में एक कैदी को मौत की सजा देते समय पोटेशियम क्लोराइड के स्थान पर पोटेशियम एसीटेट का गलत तरीके से उपयोग किया गया था। चार्ल्स फ्रेडरिक वार्नर को 15 जनवरी 2015 को पोटेशियम एसीटेट का प्रयोग करके मार डाला गया था; जब तक रिचर्ड ग्लॉसिप की निर्धारित फांसी को रद्द नहीं किया गया, तब तक यह जानकारी सार्वजनिक नहीं थी। [10] अगस्त 2017, अमेरिकी राज्य फ्लोरिडा ने एटोमिडेट, रोकुरोनियम ब्रोमाइड और पोटेशियम एसीटेट के संयोजन का उपयोग करके मार्क जेम्स एसे को मार डाला।[11] एक बार फिर एटोमिडेट और रोकुरोनियम ब्रोमाइड के संयोजन में इस दवा का उपयोग फरवरी 2023 में डोनाल्ड डिलबेक की फांसी में भी किया गया था। [12]
उद्योग
पोटेशियम एसीटेट का उपयोग पॉलीयुरेथेन के उत्पादन में उत्प्रेरक के रूप में किया जाता है।[13]
ऐतिहासिक
इसका उपयोग मूत्रवर्धक और मूत्र क्षार कारक के रूप में किया जाता है। इसका उपयोग कैडेट के धुँआ छोड़ने वाले तरल ((CH3)2As)2O के निर्माण में किया गया था, जो अब तक का पहला कार्बधात्विक यौगिक है।
संदर्भ
- ↑ Jump up to: 1.0 1.1 1.2 1.3 1.4 "Potassium acetate".
- ↑ Jump up to: 2.0 2.1 Seidell, Atherton; Linke, William F. (1952). Solubilities of Inorganic and Organic Compounds. Van Nostrand.
- ↑ Jump up to: 3.0 3.1 Acetic acid, potassium salt in Linstrom, Peter J.; Mallard, William G. (eds.); NIST Chemistry WebBook, NIST Standard Reference Database Number 69, National Institute of Standards and Technology, Gaithersburg (MD) (retrieved 2014-05-18)
- ↑ http://chem.sis.nlm.nih.gov/chemidplus/rn/127-08-2[dead link]
- ↑ UK Food Standards Agency: "Current EU approved additives and their E Numbers". Retrieved 2011-10-27.
- ↑ US Food and Drug Administration: "Listing of Food Additives Status Part II". Food and Drug Administration. Retrieved 2011-10-27.
- ↑ Australia New Zealand Food Standards Code"Standard 1.2.4 - Labelling of ingredients". Retrieved 2011-10-27.
- ↑ Dale Ulmer (1994). "निर्धारण। अच्छे ऊतक संरक्षण की कुंजी" (PDF). Journal of the International Society for Plastination. 8 (1): 7–10. Archived from the original (PDF) on 2011-05-16. Retrieved 2017-09-08.
- ↑ Andrew Nagorski (2007). सबसे बड़ी लड़ाई. Simon and Schuster. p. 53.
- ↑ Eyder Peralta. "ओक्लाहोमा ने चार्ल्स वार्नर को मारने के लिए गलत दवा का इस्तेमाल किया". NPR.
- ↑ Jason Dearon. "फ्लोरिडा ने सजायाफ्ता हत्यारे मार्क एसे को नई दवा का इस्तेमाल कर फांसी दी". Sun Sentinel.
- ↑ Kathryn Varn. "सजायाफ्ता हत्यारे डोनाल्ड डिलबेक को मार दिया गया है। यहाँ नवीनतम है।". Tallahassee Democrat.
- ↑ Hosea Cheung, Robin S. Tanke, G. Paul Torrence "Acetic Acid" in Ullmann's Encyclopedia of Industrial Chemistry, 2005 Wiley-VCH, Weinheim. doi:10.1002/14356007.a01_045.