बायोहाइड्रोजन
बायोहाइड्रोजन H2 है जो जैविक रूप से उत्पन्न होता है।[1] इस विधि में रुचि अधिक है क्योंकि H2 स्वच्छ ईंधन है और इसे कुछ प्रकार के बायोमास से सरलता से उत्पादित किया जा सकता है।[2]
कई चुनौतियाँ इस विधि की विशेषताएँ हैं, जिनमें H2 के लिए आंतरिक सम्मिलित हैं, जैसे गैर-संघनित गैस का भंडारण और परिवहन। हाइड्रोजन उत्पादक जीवों को O2 द्वारा जहर दिया जाता है। H2 की उपज प्राय: कम होते हैं।
जैव रासायनिक सिद्धांत
मुख्य प्रतिक्रियाओं में शर्करा का किण्वन सम्मिलित है। महत्वपूर्ण प्रतिक्रियाएं ग्लूकोज से प्रारंभ होती हैं, जिसे सिरका अम्ल में बदल दिया जाता है:[3]
एक संबंधित प्रतिक्रिया कार्बन डाइऑक्साइड के अतिरिक्त फ़ॉर्मेट देती है:
ये प्रतिक्रियाएँ क्रमशः 216 और 209 किलो कैलोरी / मोल द्वारा एक्सर्जोनिक हैं।
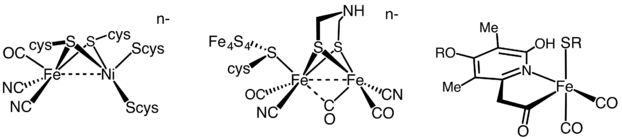
H2 उत्पादन दो हाइड्रोजन गैसों द्वारा उत्प्रेरित होता है। को [FeFe]-हाइड्रोजनेस कहा जाता है; दूसरे को [NiFe]-हाइड्रोजनेज कहा जाता है। कई जीव इन एंजाइमों को व्यक्त करते हैं। उल्लेखनीय उदाहरण जेनेरा क्लोस्ट्रीडियम, डेसल्फोविब्रियो, रालस्टोनिया और रोगज़नक़ हेलिकोबैक्टर के सदस्य हैं। ई. कोलाई हाइड्रोजन गैसों की जेनेटिक इंजीनियरिंग के लिए वर्कहॉर्स है।[4]
यह अनुमान लगाया गया है कि सभी जीवों का 99% डाइहाइड्रोजन (H2). इन प्रजातियों में से अधिकांश सूक्ष्म जीव हैं और H2 का उपयोग करने की उनकी क्षमता है मेटाबोलाइट के रूप में H2 की अभिव्यक्ति से उत्पन्न होता है मेटलोएंजाइम को हाइड्रोजन गैस के रूप में जाना जाता है।[5] सक्रिय साइट धातु सामग्री के आधार पर हाइड्रोजनीज़ को तीन अलग-अलग प्रकारों में उप-वर्गीकृत किया जाता है: आयरन-आयरन हाइड्रोजनेज़, निकल-आयरन हाइड्रोजनेज़ और आयरन हाइड्रोजनेज़।
शैवाल द्वारा उत्पादन
शैवाल के साथ जैविक हाइड्रोजन उत्पादन फोटोबायोलॉजिकल जल विभाजन की विधि है जो शैवाल द्वारा सौर ईंधन के रूप में हाइड्रोजन उत्पादन पर आधारित बंद प्रणाली बायोरिएक्टर या फोटोबायोरिएक्टर में किया जाता है।[6][7] शैवाल कुछ प्रतिबंध के अनुसार हाइड्रोजन का उत्पादन करते हैं। 2000 में यह पता चला कि यदि सी. रीन्हार्डेटी शैवाल गंधक से वंचित हैं, वे ऑक्सीजन के उत्पादन से, सामान्य प्रकाश संश्लेषण के रूप में, हाइड्रोजन के उत्पादन के लिए स्विच करेंगे।[8][9][10]
प्रकाश संश्लेषण
साइनोबैक्टीरीया और हरी शैवाल में प्रकाश संश्लेषण पानी को हाइड्रोजन आयनों और इलेक्ट्रॉनों में विभाजित करता है। इलेक्ट्रॉनों को फेरेडॉक्सिन पर ले जाया जाता है।[12] Fe-Fe-हाइड्रोजनेज (एंजाइम) उन्हें हाइड्रोजन गैस में मिलाते हैं। क्लैमाइडोमोनस रीन्हार्डेटी फोटोसिस्टम II में सूर्य के प्रकाश के सीधे रूपांतरण में 80% इलेक्ट्रॉन उत्पन्न होते हैं जो हाइड्रोजन गैस में समाप्त हो जाते हैं।[13] प्रकाश संचयन परिसर फोटोसिस्टम II प्रकाश संचयन प्रोटीन एलएचसीबीएम्9 कुशल प्रकाश ऊर्जा अपव्यय को बढ़ावा देता है।[14] Fe-Fe-हाइड्रोजनेज को अवायवीय जीव पर्यावरण की आवश्यकता होती है क्योंकि वे ऑक्सीजन द्वारा निष्क्रिय होते हैं। फूरियर रूपांतरण अवरक्त स्पेक्ट्रोस्कोपी का उपयोग चयापचय मार्गों की जांच के लिए किया जाता है।[15] 2020 में वैज्ञानिकों ने हवा के नीचे दिन के उजाले में प्रकाश संश्लेषण के माध्यम से ऑक्सीजन या CO2 के साथ-साथ हाइड्रोजन का उत्पादन करने में सक्षम बहुकोशिकीय गोलाकार माइक्रोरिएक्टर रिएक्टरों के लिए शैवाल-कोशिका आधारित सूक्ष्म बूंदों के विकास की सूचना दी। हाइड्रोजन उत्पादन के स्तर को बढ़ाने के लिए सिनर्जिस्टिक बैक्टीरिया के साथ माइक्रोरिएक्टरों को संलग्न करना दिखाया गया था।[16]
विशिष्ट क्लोरोफिल
फोटोबायोलॉजिकल सौर रूपांतरण दक्षता और H2 को अधिकतम करने के लिए हरे शैवाल में क्लोरोफिल (सीएचएल) एंटीना आकार को कम किया जाता है, या छोटा किया जाता है। छोटा सीएचएल ऐन्टेना आकार अलग-अलग कोशिकाओं द्वारा सूर्य के प्रकाश के अवशोषण और व्यर्थ अपव्यय को कम करता है, जिसके परिणामस्वरूप श्रेष्ठ प्रकाश उपयोग दक्षता और हरे शैवाल द्रव्यमान संस्कृति द्वारा अधिक प्रकाश संश्लेषक उत्पादकता होती है।[17]
अर्थशास्त्र
अकेले अमेरिका में गैसोलीन द्वारा प्रदान की जाने वाली ऊर्जा के समान बायोहाइड्रोजन का उत्पादन करने के लिए लगभग 25,000 वर्ग किलोमीटर शैवाल की खेती करनी होगी। यह क्षेत्र अमेरिका में सोया उगाने के लिए समर्पित क्षेत्र का लगभग 10% प्रतिनिधित्व करता है।[18]
बायोरिएक्टर डिजाइन उद्देश्य
- एक प्रोटॉन प्रवणता के संचय द्वारा प्रकाश संश्लेषक हाइड्रोजन उत्पादन का प्रतिबंध।
- कार्बन डाइऑक्साइड द्वारा प्रकाश संश्लेषक हाइड्रोजन उत्पादन का प्रतिस्पर्धी निषेध।
- फोटोसिंथेटिक दक्षता के लिए फोटोसिस्टम II (PSII) पर बाइकार्बोनेट बाइंडिंग की आवश्यकता।
- एल्गल हाइड्रोजन उत्पादन में ऑक्सीजन द्वारा इलेक्ट्रॉनों की प्रतिस्पर्धात्मक जल निकासी।
- अर्थशास्त्र को ऊर्जा के अन्य स्रोतों के लिए प्रतिस्पर्धी मूल्य तक पहुंचना चाहिए और अर्थशास्त्र कई मापदंडों पर निर्भर है।
- एक प्रमुख प्रविधि बाधा सौर ऊर्जा को आणविक हाइड्रोजन में संग्रहीत रासायनिक ऊर्जा में परिवर्तित करने की दक्षता है।
बायोइन्जिनियरिंग के माध्यम से इन समस्याओं का समाधान करने का प्रयास जारी है।
इतिहास
1933 में, मारजोरी स्टीफेंसन और उनके छात्र स्टिकलैंड ने बताया कि सेल निलंबन ने H2 के साथ मेथिलीन ब्लू की कमी को उत्प्रेरित किया। छह साल बाद, हंस गैफ्रॉन ने देखा कि हरे प्रकाश संश्लेषक शैवाल क्लैमाइडोमोनस रेन्हार्डेटी, कभी-कभी हाइड्रोजन का उत्पादन करते हैं।[19] 1990 के दशक के अंत में अनास्तासियस मेलिस ने पाया कि सल्फर का अभाव शैवाल को ऑक्सीजन के उत्पादन (सामान्य प्रकाश संश्लेषण) से हाइड्रोजन के उत्पादन में बदलने के लिए प्रेरित करता है। उन्होंने पाया कि इस प्रतिक्रिया के लिए उत्तरदायी एंजाइम हाइड्रोजनेज़ है, किन्तु ऑक्सीजन की उपस्थिति में हाइड्रोजनेज़ ने इस कार्य को खो दिया। मेलिस ने यह भी पता लगाया कि शैवाल के लिए उपलब्ध सल्फर की मात्रा में कमी ने उनके आंतरिक ऑक्सीजन प्रवाह को बाधित कर दिया, जिससे हाइड्रोजनेज़ को ऐसा वातावरण मिल गया जिसमें यह प्रतिक्रिया कर सके, जिससे शैवाल हाइड्रोजन का उत्पादन कर सके।[20] क्लैमाइडोमोनस मोएवुसी भी हाइड्रोजन के उत्पादन के लिए आशाजनक अस्तित्व है।[21][22]
औद्योगिक हाइड्रोजन
बायोहाइड्रोजन के लिए प्रतिस्पर्धा, कम से कम व्यावसायिक अनुप्रयोगों के लिए, कई परिपक्व औद्योगिक प्रक्रियाएँ हैं। प्राकृतिक गैस का भाप सुधार - जिसे कभी-कभी स्टीम मीथेन रिफॉर्मिंग (एसएम्आर) कहा जाता है - विश्व उत्पादन के लगभग 95% पर बल्क हाइड्रोजन के उत्पादन की सबसे आसन विधि है।[23][24][25]
यह भी देखें
- शैवाल पालन
- हाइड्रोजन उत्पादन
- हाइड्रोजनेज
- फोटोहाइड्रोजन
- हाइड्रोजन प्रौद्योगिकियों की समयरेखा
संदर्भ
- ↑ M. Rögner, ed. (2015). बायोहाइड्रोजन. De Gruyter. ISBN 978-3-11-033673-3.
- ↑ Y.-H. Percival Zhang "Hydrogen Production from Carbohydrates: A Mini-Review" in "Sustainable Production of Fuels, Chemicals, and Fibers from Forest Biomass" ACS Symposium Series, 2011, Volume 1067, pages=203-216.
- ↑ Thauer, R. K. (1998). "Biochemistry of Methanogenesis: a Tribute to Marjory Stephenson". Microbiology. 144: 2377–2406. doi:10.1099/00221287-144-9-2377. PMID 9782487.
- ↑ Cammack, R.; Frey, M.; Robson, R. (2001). Hydrogen as a Fuel: Learning from Nature. London: Taylor & Francis.
{{cite book}}: CS1 maint: uses authors parameter (link) - ↑ Lubitz, Wolfgang; Ogata, Hideaki; Rüdiger, Olaf; Reijerse, Edward (2014). "Hydrogenases". Chemical Reviews. 114 (8): 4081–148. doi:10.1021/cr4005814. PMID 24655035.
- ↑ 2013 - Gimpel JA, et al Advances in microalgae engineering and synthetic biology applications for biofuel production
- ↑ Hemschemeier, Anja; Melis, Anastasios; Happe, Thomas (2009). "Analytical approaches to photobiological hydrogen production in unicellular green algae". Photosynthesis Research. 102 (2–3): 523–540. doi:10.1007/s11120-009-9415-5. ISSN 0166-8595. PMC 2777220. PMID 19291418.
- ↑ Wired-Mutant Algae Is Hydrogen Factory Archived August 27, 2006, at the Wayback Machine
- ↑ "Further reading - New Scientist". Archived from the original on 2008-10-31. Retrieved 2009-03-11.
- ↑ Melis, Anastasios; Zhang, Liping; Forestier, Marc; Ghirardi, Maria L.; Seibert, Michael (2000-01-01). "Sustained Photobiological Hydrogen Gas Production upon Reversible Inactivation of Oxygen Evolution in the Green AlgaChlamydomonas reinhardtii". Plant Physiology (in English). 122 (1): 127–136. doi:10.1104/pp.122.1.127. ISSN 1532-2548. PMC 58851. PMID 10631256.
- ↑ Cite error: Invalid
<ref>tag; no text was provided for refs named10.1038/s41467-020-19823-5 - ↑ Peden, E. A.; Boehm, M.; Mulder, D. W.; Davis, R.; Old, W. M.; King, P. W.; Ghirardi, M. L.; Dubini, A. (2013). "Identification of Global Ferredoxin Interaction Networks in Chlamydomonas reinhardtii". Journal of Biological Chemistry. 288 (49): 35192–35209. doi:10.1074/jbc.M113.483727. ISSN 0021-9258. PMC 3853270. PMID 24100040.
- ↑ Volgusheva, A.; Styring, S.; Mamedov, F. (2013). "Increased photosystem II stability promotes H2 production in sulfur-deprived Chlamydomonas reinhardtii". Proceedings of the National Academy of Sciences. 110 (18): 7223–7228. Bibcode:2013PNAS..110.7223V. doi:10.1073/pnas.1220645110. ISSN 0027-8424. PMC 3645517. PMID 23589846.
- ↑ Grewe, S.; Ballottari, M.; Alcocer, M.; D'Andrea, C.; Blifernez-Klassen, O.; Hankamer, B.; Mussgnug, J. H.; Bassi, R.; Kruse, O. (2014). "Light-Harvesting Complex Protein LHCBM9 Is Critical for Photosystem II Activity and Hydrogen Production in Chlamydomonas reinhardtii". The Plant Cell. 26 (4): 1598–1611. doi:10.1105/tpc.114.124198. ISSN 1040-4651. PMC 4036574. PMID 24706511.
- ↑ Langner, U; Jakob, T; Stehfest, K; Wilhelm, C (2009). "An energy balance from absorbed photons to new biomass for Chlamydomonas reinhardtii and Chlamydomonas acidophila under neutral and extremely acidic growth conditions". Plant Cell Environ. 32 (3): 250–8. doi:10.1111/j.1365-3040.2008.01917.x. PMID 19054351.
- ↑ "Research creates hydrogen-producing living droplets, paving way for alternative future energy source". phys.org (in English). Retrieved 9 December 2020.
- ↑ Kirst, H.; Garcia-Cerdan, J. G.; Zurbriggen, A.; Ruehle, T.; Melis, A. (2012). "Truncated Photosystem Chlorophyll Antenna Size in the Green Microalga Chlamydomonas reinhardtii upon Deletion of the TLA3-CpSRP43 Gene". Plant Physiology. 160 (4): 2251–2260. doi:10.1104/pp.112.206672. ISSN 0032-0889. PMC 3510145. PMID 23043081.
- ↑ Growing hydrogen for the cars of tomorrow
- ↑ Algae: Power Plant of the Future?
- ↑ Reengineering Algae To Fuel The Hydrogen Economy
- ↑ Melis A, Happe T (2001). "Hydrogen Production. Green Algae as a Source of Energy". Plant Physiol. 127 (3): 740–748. doi:10.1104/pp.010498. PMC 1540156. PMID 11706159.
- ↑ Yang, Shihui; Guarnieri, Michael T; Smolinski, Sharon; Ghirardi, Maria; Pienkos, Philip T (2013). "De novo transcriptomic analysis of hydrogen production in the green alga Chlamydomonas moewusii through RNA-Seq". Biotechnology for Biofuels. 6 (1): 118. doi:10.1186/1754-6834-6-118. ISSN 1754-6834. PMC 3846465. PMID 23971877.
- ↑ P. Häussinger, R. Lohmüller, A. M. Watson, "Hydrogen, 2. Production" in Ullmann's Encyclopedia of Industrial Chemistry, 2012, Wiley-VCH, Weinheim. doi:10.1002/14356007.o13_o03
- ↑ Ogden, J.M. (1999). "Prospects for building a hydrogen energy infrastructure". Annual Review of Energy and the Environment. 24: 227–279. doi:10.1146/annurev.energy.24.1.227.
- ↑ "Hydrogen Production: Natural Gas Reforming". Department of Energy. Retrieved 6 April 2017.