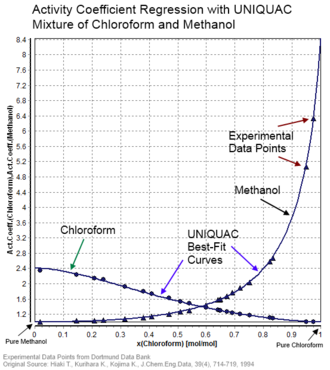
सक्रियता गुणांक
ऊष्मप्रवैगिकी में, गतिविधि गुणांक एक कारक है जिसका उपयोग आदर्श व्यवहार से रासायनिक पदार्थों के मिश्रण के विचलन के लिए किया जाता है।[1] एक आदर्श मिश्रण में, रासायनिक प्रजातियों के प्रत्येक जोड़े के बीच सूक्ष्म अंतःक्रिया समान होती है (या स्थूलदर्शी रूप से समतुल्य, विलयन में तापीय धारिता परिवर्तन और मिश्रण में मात्रा भिन्नता शून्य होती है) और, परिणामस्वरूप, मिश्रण के गुणों को सीधे मौजूद पदार्थों की साधारण सांद्रता या आंशिक दबाव के रूप में व्यक्त किया जा सकता है जैसे राउल्ट का नियम। एक गतिविधि गुणांक द्वारा सांद्रता को संशोधित करके आदर्शता से विचलन को समायोजित किया जाता है। अनुरूप रूप से, गैसों से जुड़े भावों को अस्पष्टता गुणांक द्वारा आंशिक दबावों को बढ़ाकर गैर-आदर्शता के लिए समायोजित किया जा सकता है।
गतिविधि गुणांक की अवधारणा रसायन विज्ञान में गतिविधि से निकटता से जुड़ी हुई है।
ऊष्मागतिकी परिभाषा
रासायनिक क्षमता, तरल पदार्थ के एक आदर्श मिश्रण या एक आदर्श विलयन में किसी पदार्थ B का मान दिया जाता है
- ,
जहाँ μo
B शुद्ध पदार्थ की रासायनिक क्षमता है , और मिश्रण में पदार्थ का मोल अंश है।
इसे लेखन द्वारा गैर-आदर्श व्यवहार को सम्मलित करने के लिए इसे सामान्यीकृत किया गया है
कब मिश्रण में पदार्थ की गतिविधि है,
- ,
जहाँ गतिविधि गुणांक है, जिस पर निर्भर हो सकता है, जैसा दृष्टिकोण 1, पदार्थ ऐसे व्यवहार करता है मानो वह आदर्श हो। उदाहरण के लिए, अगर ≈ 1, तो राउल्ट का नियम सटीक है। > 1 और < 1 के लिए, पदार्थ B क्रमशः राउल्ट के नियम से धनात्मक और ऋणात्मक विचलन दिखाता है। एक धनात्मक विचलन का तात्पर्य है कि पदार्थ B अधिक अस्थिर है।
कई कारको में, जैसे शून्य हो जाता है, पदार्थ B का गतिविधि गुणांक एक स्थिरांक के करीब पहुंच जाता है; यह संबंध विलायक के लिए हेनरी का नियम है। ये रिश्ते गिब्स-डुहेम समीकरण के माध्यम से एक दूसरे से संबंधित हैं।[2] ध्यान दें कि सामान्य गतिविधि में गुणांक आयाम रहित होते हैं।
विस्तार से: राउल्ट के नियम में कहा गया है कि घटक B का आंशिक दबाव उसके वाष्प दबाव (संतृप्ति दबाव) और उसके मोल अंश से संबंधित है तरल चरण में,
सम्मेलन के साथ दूसरे शब्दों में: शुद्ध तरल पदार्थ आदर्श स्थिति का प्रतिनिधित्व करते हैं।
अनंत तनुकरण पर, गतिविधि गुणांक अपने सीमित मूल्य तक पहुंचता है, ∞. हेनरी के नियम के साथ तुलना,
तुरंत देता है
दूसरे शब्दों में: यौगिक तनु कारक में गैर-आदर्श व्यवहार दिखाता है।
गतिविधि गुणांक की उपरोक्त परिभाषा अव्यावहारिक है यदि यौगिक शुद्ध तरल के रूप में मौजूद नहीं है। यह प्रायः विद्युत अपघट्य या जैव रासायनिक यौगिकों के कारक में होता है। ऐसे कारको में, एक अलग परिभाषा का उपयोग किया जाता है जो अनंत तनुकरण को आदर्श स्थिति मानती है:
के साथऔर
दो प्रकार के गतिविधि गुणांकों के बीच अंतर करने के लिए प्रतीक का उपयोग यहां किया गया है। समान्यता इसे छोड़ दिया जाता है, क्योंकि यह संदर्भ से स्पष्ट है कि किस प्रकार का आशय है। लेकिन ऐसे कारक हैं जहां दोनों प्रकार के गतिविधि गुणांक की आवश्यकता होती है और यहां तक कि एक ही समीकरण में भी दिखाई दे सकते हैं, उदाहरण के लिए, (जल + अल्कोहल) मिश्रण में लवण के विलयन के लिए। यह कभी-कभी त्रुटियों का स्रोत होता है।
गतिविधि गुणांकों द्वारा मोल अंशों या सांद्रता को संशोधित करने से घटकों की प्रभावी गतिविधियां मिलती हैं, और इसलिए राउल्ट के नियम और संतुलन स्थिरांक जैसे अभिव्यक्तियों को आदर्श और गैर-आदर्श मिश्रण दोनों पर लागू करने की अनुमति मिलती है।
विद्युतरसायन के संदर्भ में गतिविधि गुणांक का ज्ञान विशेष रूप से महत्वपूर्ण है क्योंकि आयनिक वायुमंडल के प्रभाव के कारण विद्युत अपघट्य विलयन का व्यवहार प्रायः आदर्श से बहुत दूर होता है। इसके अतिरिक्त, वे विलायक की कम मात्रा और परिणामस्वरूप, विद्युत अपघट्य की उच्च सांद्रता के कारण वे मृदा रसायन विज्ञान के संदर्भ में विशेष रूप से महत्वपूर्ण हैं।[3]
आयनिक विलयन
उन पदार्थों के विलयन के लिए जो विलयन में आयनित होते हैं, धनायन और आयन के गतिविधि गुणांक को प्रयोगात्मक रूप से एक दूसरे से स्वतंत्र रूप से निर्धारित नहीं किया जा सकता है क्योंकि विलयन गुण दोनों आयनों पर निर्भर करते हैं। एकल आयन गतिविधि गुणांक को विघटित विद्युत अपघट्य के गतिविधि गुणांक से जोड़ा जाना चाहिए जैसे कि अविभाजित। इस कारक में विघटित विद्युत अपघट्य, γ± का माध्य स्टोइकोमेट्रिक गतिविधि गुणांक का उपयोग किया जाता है। इसे रससमीकरणमितीय कहा जाता है क्योंकि यह विलयन की आदर्शता से विचलन और आयनिक यौगिक के अपूर्ण आयनिक पृथक्करण दोनों को व्यक्त करता है जो विशेष रूप से इसकी सांद्रता में वृद्धि के साथ होता है।
1:1 विद्युत अपघट्य, जैसे सोडियम क्लोराइड के लिए यह निम्नलिखित द्वारा दिया जाता है:
जहाँ और क्रमशः धनायन और ऋणायन के गतिविधि गुणांक हैं।
अधिक सामान्यतः, सूत्र के एक यौगिक का औसत गतिविधि गुणांक द्वारा दिया गया है[4]
एकल-आयन गतिविधि गुणांकों की सैद्धांतिक रूप से गणना की जा सकती है, उदाहरण के लिए डेबी-हुकेल समीकरण का उपयोग करके। सैद्धांतिक समीकरण का परीक्षण परिकलित एकल-आयन गतिविधि गुणांकों को मिलाकर औसत मान देने के लिए किया जा सकता है, जिसकी तुलना प्रयोगात्मक मानों से की जा सकती है।
प्रचलित दृष्टिकोण कि एकल आयन गतिविधि गुणांक स्वतंत्र रूप से अमापीय हैं, या शायद भौतिक रूप से अर्थहीन भी हैं, इसकी जड़ें 1920 के दशक के अंत में गुगेनहाइम के काम में हैं।[5] यद्यपि, रसायनज्ञ कभी भी एकल आयन गतिविधियों और निहितार्थ एकल आयन गतिविधि गुणांक के विचार को छोड़ने में सक्षम नहीं हुए हैं। उदाहरण के लिए, PH को हाइड्रोजन आयन गतिविधि के ऋणात्मक लघुगणक के रूप में परिभाषित किया गया है। यदि एकल आयन गतिविधियों के भौतिक अर्थ और मापनीयता पर प्रचलित दृष्टिकोण सही है तो PH को हाइड्रोजन आयन गतिविधि के ऋणात्मक लघुगणक के रूप में परिभाषित करना मात्रा को अचूक श्रेणी में वर्गाकार रूप से रखता है। इस तार्किक कठिनाई को स्वीकार करते हुए, शुद्ध और व्यावहारिक रसायन के अंतर्राष्ट्रीय संघ (IUPAC) का कहना है कि pH की गतिविधि-आधारित परिभाषा केवल एक काल्पनिक परिभाषा है।[6] एकल आयन गुणांकों की मापनीयता पर प्रचलित ऋणात्मक दृष्टिकोण के बावजूद, एकल आयन गतिविधियों की अवधारणा पर साहित्य में चर्चा जारी है, और कम से कम एक लेखक शुद्ध ऊष्मागतिकी मात्रा के संदर्भ में एकल आयन गतिविधि की परिभाषा प्रस्तुत करता है और एक विधि का प्रस्ताव करता है और विशुद्ध रूप से ऊष्मागतिकी प्रक्रियाओं के आधार पर एकल आयन गतिविधि गुणांक को मापने की एक विधि का प्रस्ताव करता है।[7]
केंद्रित आयनिक विलयन
केंद्रित आयनिक विलयनो के लिए आयनों के जलयोजन को ध्यान में रखा जाना चाहिए, जैसा कि 1948 से स्टोक्स और रॉबिन्सन ने अपने जलयोजन मॉडल में किया था।[8] विद्युत अपघट्य का गतिविधि गुणांक E. ग्लूकॉफ़ द्वारा विद्युत और सांख्यिकीय घटकों में विभाजित किया गया है जो रॉबिन्सन-स्टोक्स मॉडल को संशोधित करता है।
सांख्यिकीय भाग में जलयोजन सूचकांक संख्या h, पृथक्करण से आयनों की संख्या और विद्युत अपघट्य की स्पष्ट दाढ़ संपत्ति और जल और मोलिटी b की दाढ़ मात्रा के बीच अनुपात r सम्मलित है।
गतिविधि गुणांक का केंद्रित विलयन सांख्यिकीय भाग है:
स्टोक्स-रॉबिन्सन मॉडल का विश्लेषण और सुधार अन्य जांचकर्ताओं द्वारा भी किया गया है।
गतिविधि गुणांकों का प्रायोगिक निर्धारण
गैर-आदर्श मिश्रणों पर माप करके गतिविधि गुणांक प्रयोगात्मक रूप से निर्धारित किया जा सकता है। एक आदर्श मिश्रण के लिए एक मूल्य प्रदान करने के लिए राउल्ट के नियम या हेनरी के नियम का उपयोग किया जा सकता है जिसके विरुद्ध गतिविधि गुणांक प्राप्त करने के लिए प्रयोगात्मक मूल्य की तुलना की जा सकती है। आसमाटिक दबाव जैसे अन्य संपार्श्विक गुणों का भी उपयोग किया जा सकता है।
रेडियोरासायनिक विधियाँ
गतिविधि गुणांक रेडियो रसायन विधियों द्वारा निर्धारित किए जा सकते हैं।[12]
अनन्त तनुकरण पर
बाइनरी मिश्रण के लिए गतिविधि गुणांक प्रायः प्रत्येक घटक के अनंत कमजोर पड़ने पर रिपोर्ट किए जाते हैं। क्योंकि गतिविधि गुणांक मॉडल अनंत कमजोर पड़ने पर सरल होते हैं, ऐसे अनुभवजन्य मूल्यों का उपयोग अंतःक्रियात्मक ऊर्जाओं का अनुमान लगाने के लिए किया जा सकता है। जल के उदाहरण दिए गए हैं:
| X | γx∞ (K) | γW∞ (K) |
|---|---|---|
| एथेनॉल | 4.3800 (283.15) | 3.2800 (298.15) |
| एसीटोन | 6.0200 (307.85) |
गतिविधि गुणांक की सैद्धांतिक गणना
विद्युत अपघट्य विलयनो के गतिविधि गुणांकों की गणना सैद्धांतिक रूप से डेबी-हुकेल समीकरण या डेविस समीकरण,[14] पित्जर समीकरण[15] या TCPC मॉडल जैसे एक्सटेंशन(विस्तार) का उपयोग करके की जा सकती है।[16][17][18][19] विशिष्ट आयन अन्योन्यक्रिया सिद्धांत (SIT)[20] का भी उपयोग किया जा सकता है।
गैर-विद्युत अपघट्य विलयनो के लिए सहसंबंधी तरीके जैसे कि UNIQUAC, NRTL, MOSCED या UNIFAC जैसी सहसंबंधी विधियों को नियोजित किया जा सकता है, बशर्ते फिट किए गए घटक-विशिष्ट या मॉडल पैरामीटर उपलब्ध हों। COSMO-RS एक सैद्धांतिक पद्धति है जो मॉडल मापदंडों पर कम निर्भर है क्योंकि आवश्यक जानकारी सतह खंडों के सांख्यिकीय ऊष्मप्रवैगिकी उपचार के साथ संयुक्त प्रत्येक अणु (सिग्मा प्रोफाइल) के लिए विशिष्ट क्वांटम यांत्रिकी गणना से प्राप्त की जाती है।[21]
अनावेशित प्रजातियों के लिए, गतिविधि गुणांक γ0 अधिकतर सॉल्टिंग-आउट मॉडल का अनुसरण करता है:[22]
यह सरल मॉडल कई प्रजातियों (विघटित अविघटित गैसें जैसे CO2, H2S, NH3, अविघटित अम्ल और क्षार) की उच्च आयनिक शक्ति (5 mol/kg तक) की गतिविधियों की भविष्यवाणी करता है। CO2 के लिए स्थिरांक b का मान 10 डिग्री सेल्सियस पर 0.11 और 330 डिग्री सेल्सियस पर 0.20 है।[23]
विलायक के रूप में जल के लिए , गतिविधि की गणना निम्न का उपयोग करके की जा सकती है:[22]
जहां ν घुले हुए नमक के एक अणु के पृथक्करण से उत्पन्न आयनों की संख्या है, b जल में घुले नमक की मोललता है, φ जल का आसमाटिक गुणांक है, और निरंतर 55.51 जल की मोललता का प्रतिनिधित्व करता है। उपरोक्त समीकरण में, एक विलायक (यहाँ जल) की गतिविधि को नमक के कणों की संख्या बनाम विलायक की संख्या के व्युत्क्रमानुपाती के रूप में दर्शाया गया है।
आयनिक व्यास से लिंक करें
आयनिक गतिविधि गुणांक विद्युत अपघट्य के डेबी-हुकेल सिद्धांत से प्राप्त सूत्र द्वारा आयनिक त्रिज्या से जुड़ा हुआ है:
जहाँ A और B स्थिरांक हैं, ziआयन की संयोजकता संख्या है, और I आयनिक शक्ति है।
राज्य के मापदंडों पर निर्भरता
तापमान के संबंध में एक गतिविधि गुणांक का व्युत्पन्न अतिरिक्त दाढ़ तापीय धारिता से संबंधित है
इसी तरह, दबाव के संबंध में एक गतिविधि गुणांक का व्युत्पन्न अतिरिक्त दाढ़ मात्रा से संबंधित हो सकता है।
रासायनिक संतुलन के लिए अनुप्रयोग
संतुलन पर, अभिकारकों की रासायनिक क्षमता का योग उत्पादों की रासायनिक क्षमता के योग के बराबर होता है। गिब्स मुक्त ऊर्जा अभिक्रियाओं के लिए परिवर्तन, ΔrG, इन योगों के अंतर के बराबर है और इसलिए, संतुलन पर, शून्य के बराबर है। इस प्रकार, एक संतुलन के लिए जैसे
प्रत्येक अभिकारक की रासायनिक क्षमता के लिए व्यंजकों में स्थानापन्न:
पुनर्व्यवस्थित करने पर यह अभिव्यक्ति बन जाती है
योग
σμo
S + τμo
T − αμo
A − βμo
B प्रतिक्रिया के लिए मानक मुक्त ऊर्जा परिवर्तन है, .
इसलिए,
जहाँ K संतुलन स्थिरांक है। ध्यान दें कि गतिविधियाँ और संतुलन स्थिरांक आयाम रहित संख्याएँ हैं।
यह व्युत्पत्ति दो उद्देश्यों की पूर्ति करती है। यह मानक मुक्त ऊर्जा परिवर्तन और संतुलन स्थिरांक के बीच संबंध को दर्शाता है। यह यह भी दर्शाता है कि एक संतुलन स्थिरांक को गतिविधियों के भागफल के रूप में परिभाषित किया जाता है। व्यावहारिक दृष्टि से यह असुविधाजनक है। जब प्रत्येक गतिविधि को एक सांद्रता और एक गतिविधि गुणांक के उत्पाद द्वारा प्रतिस्थापित किया जाता है, तो संतुलन स्थिरांक को इस रूप में परिभाषित किया जाता है
जहाँ [S], S आदि की सांद्रता को दर्शाता है। व्यवहार में संतुलन स्थिरांक एक माध्यम में संतुलन स्थिरांक का निर्धारण होता है जैसे कि गतिविधि गुणांक का भागफल स्थिर होता है और इसे नजरअंदाज किया जा सकता है, जिससे सामान्य अभिव्यक्ति होती है
जो उन शर्तों के तहत लागू होता है कि गतिविधि भागफल का एक विशेष (स्थिर) मान होता है।
संदर्भ
- ↑ IUPAC, Compendium of Chemical Terminology, 2nd ed. (the "Gold Book") (1997). Online corrected version: (2006–) "Activity coefficient". doi:10.1351/goldbook.A00116
- ↑ DeHoff, Robert (2018). "सामग्री विज्ञान में ऊष्मप्रवैगिकी". Entropy (2nd ed.). 20 (7): 230–231. Bibcode:2018Entrp..20..532G. doi:10.3390/e20070532. ISBN 9780849340659. PMC 7513056. PMID 33265621.
- ↑ Ibáñez, Jorge G.; Hernández Esparza, Margarita; Doría Serrano, Carmen; Singh, Mono Mohan (2007). Environmental Chemistry: Fundamentals. Springer. ISBN 978-0-387-26061-7.
- ↑ Atkins, Peter; dePaula, Julio (2006). "Section 5.9, The activities of ions in solution". भौतिक रसायन (8th ed.). OUP. ISBN 9780198700722.
- ↑ Guggenheim, E. A. (1928). "दो चरणों और आयनों की व्यक्तिगत गतिविधियों के बीच विद्युत संभावित अंतर की अवधारणा". The Journal of Physical Chemistry. 33 (6): 842–849. doi:10.1021/j150300a003. ISSN 0092-7325.
- ↑ IUPAC, Compendium of Chemical Terminology, 2nd ed. (the "Gold Book") (1997). Online corrected version: (2006–) "pH". doi:10.1351/goldbook.P04524
- ↑ Rockwood, Alan L. (2015). "एकल-आयन गतिविधियों का अर्थ और मापनीयता, पीएच की थर्मोडायनामिक नींव, और असमान सामग्री के बीच आयनों के हस्तांतरण के लिए गिब्स मुक्त ऊर्जा". ChemPhysChem. 16 (9): 1978–1991. doi:10.1002/cphc.201500044. ISSN 1439-4235. PMC 4501315. PMID 25919971.
- ↑ Stokes, R. H; Robinson, R. A (1948). "आयनिक जलयोजन और इलेक्ट्रोलाइट समाधानों में गतिविधि". Journal of the American Chemical Society. 70 (5): 1870–1878. doi:10.1021/ja01185a065. PMID 18861802.
- ↑ Glueckauf, E. (1955). "केंद्रित इलेक्ट्रोलाइट समाधानों में गतिविधि गुणांक पर आयनिक जलयोजन का प्रभाव". Transactions of the Faraday Society. 51: 1235. doi:10.1039/TF9555101235.
- ↑ Glueckauf, E. (1957). "केंद्रित इलेक्ट्रोलाइट समाधानों में गतिविधि गुणांक पर आयनिक जलयोजन का प्रभाव". Transactions of the Faraday Society. 53: 305. doi:10.1039/TF9575300305.
- ↑ Kortüm, G. (1959). "इलेक्ट्रोलाइटिक समाधानों की संरचना". Angewandte Chemie. London: Herausgeg. von W. J. Hamer; John Wiley & Sons, Inc., New York; Chapman & Hall, Ltd. 72 (24): 97. doi:10.1002/ange.19600722427. ISSN 0044-8249.
- ↑ Betts, R. H.; MacKenzie, Agnes N. (1952). "मिश्रित इलेक्ट्रोलाइट्स में गतिविधि गुणांक के रेडियोरासायनिक माप". Canadian Journal of Chemistry. 30 (2): 146–162. doi:10.1139/v52-020.
- ↑ "Activity Coefficients at Infinite Dilution of 30 Important Components from Dortmund Data Bank". Dortmund Data Bank. DDBST GmbH. Retrieved 13 December 2018.
- ↑ King, E. L. (1964). "Book Review: Ion Association, C. W. Davies, Butterworth, Washington, D.C., 1962". Science. 143 (3601): 37. Bibcode:1964Sci...143...37D. doi:10.1126/science.143.3601.37. ISSN 0036-8075.
- ↑ Grenthe, I.; Wanner, H. "एक्सट्रपलेशन के लिए शून्य आयनिक शक्ति के लिए दिशानिर्देश" (PDF). Archived from the original (PDF) on 2008-12-17. Retrieved 2007-07-23.
- ↑ Ge, Xinlei; Wang, Xidong; Zhang, Mei; Seetharaman, Seshadri (2007). "Correlation and Prediction of Activity and Osmotic Coefficients of Aqueous Electrolytes at 298.15 K by the Modified TCPC Model". Journal of Chemical & Engineering Data. 52 (2): 538–547. doi:10.1021/je060451k. ISSN 0021-9568.
- ↑ Ge, Xinlei; Zhang, Mei; Guo, Min; Wang, Xidong (2008). "संशोधित टीसीपीसी मॉडल द्वारा गैर-जलीय इलेक्ट्रोलाइट्स के थर्मोडायनामिक गुणों का सहसंबंध और भविष्यवाणी". Journal of Chemical & Engineering Data. 53 (1): 149–159. doi:10.1021/je700446q. ISSN 0021-9568.
- ↑ Ge, Xinlei; Zhang, Mei; Guo, Min; Wang, Xidong (2008). "संशोधित तीन-विशेषता-पैरामीटर सहसंबंध मॉडल द्वारा कुछ जटिल जलीय इलेक्ट्रोलाइट्स के थर्मोडायनामिक गुणों का सहसंबंध और भविष्यवाणी". Journal of Chemical & Engineering Data. 53 (4): 950–958. doi:10.1021/je7006499. ISSN 0021-9568.
- ↑ Ge, Xinlei; Wang, Xidong (2009). "तापमान की एक विस्तृत श्रृंखला में जलीय इलेक्ट्रोलाइट समाधानों के लिए एक सरल दो-पैरामीटर सहसंबंध मॉडल". Journal of Chemical & Engineering Data. 54 (2): 179–186. doi:10.1021/je800483q. ISSN 0021-9568.
- ↑ "Project: Ionic Strength Corrections for Stability Constants". IUPAC. Archived from the original on 29 October 2008. Retrieved 2008-11-15.
- ↑ Klamt, Andreas (2005). COSMO-RS क्वांटम रसायन विज्ञान से द्रव चरण थर्मोडायनामिक्स और ड्रग डिज़ाइन तक (1st ed.). Amsterdam: Elsevier. ISBN 978-0-444-51994-8.
- ↑ 22.0 22.1 N. Butler, James (1998). Ionic equilibrium: solubility and pH calculations. New York, NY [u.a.]: Wiley. ISBN 9780471585268.
- ↑ Ellis, A. J.; Golding, R. M. (1963). "पानी में और सोडियम क्लोराइड समाधान में 100 डिग्री सेल्सियस से ऊपर कार्बन डाइऑक्साइड की घुलनशीलता". American Journal of Science. 261 (1): 47–60. Bibcode:1963AmJS..261...47E. doi:10.2475/ajs.261.1.47. ISSN 0002-9599.
बाहरी संबंध
- AIOMFAC online-model An interactive group-contribution model for the calculation of activity coefficients in organic–inorganic mixtures.
- Electrochimica Acta Single-ion activity coefficients