अम्ल शक्ति: Difference between revisions
mNo edit summary |
mNo edit summary |
||
| Line 23: | Line 23: | ||
== प्रबल अम्ल == | == प्रबल अम्ल == | ||
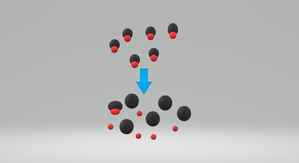
[[File:Strong_acid.png|thumb|एक प्रबल अम्ल की छवि ज्यादातर अलग कर रही है। छोटे लाल वृत्त H | [[File:Strong_acid.png|thumb|एक प्रबल अम्ल की छवि ज्यादातर अलग कर रही है। छोटे लाल वृत्त H <sup>+</sup> आयनों का प्रतिनिधित्व करते हैं।]]एक प्रबल अम्ल एक अम्ल होता है जो अभिक्रिया के अनुसार अलग हो जाता है | ||
:<chem>HA + S <=> SH+ + A-</chem> | :<chem>HA + S <=> SH+ + A-</chem> | ||
जहाँ S एक विलायक अणु का प्रतिनिधित्व करता है, जैसे कि जल का एक अणु या [[डाइमिथाइल सल्फ़ोक्साइड]] (DMSO), इस हद तक कि असंगठित प्रजातियों की सघनता <chem>HA</chem> मापने के लिए बहुत कम है। व्यावहारिक उद्देश्यों के लिए एक प्रबल अम्ल को पूरी तरह से वियोजित कहा जा सकता है। प्रबल अम्ल का उदाहरण हाइड्रोक्लोरिक अम्ल है। | जहाँ S एक विलायक अणु का प्रतिनिधित्व करता है, जैसे कि जल का एक अणु या [[डाइमिथाइल सल्फ़ोक्साइड]] (DMSO), इस हद तक कि असंगठित प्रजातियों की सघनता <chem>HA</chem> मापने के लिए बहुत कम है। व्यावहारिक उद्देश्यों के लिए एक प्रबल अम्ल को पूरी तरह से वियोजित कहा जा सकता है। प्रबल अम्ल का उदाहरण हाइड्रोक्लोरिक अम्ल है। | ||
:<chem>HCl -> H+ + Cl- </chem>(जलीय घोल में) | :<chem>HCl -> H+ + Cl- </chem>(जलीय घोल में) | ||
A के साथ कोई भी अम्ल <math chem="">\mathrm{p}K_\ce{a} </math> मान जो लगभग -2 से कम है, उसे प्रबल अम्ल के रूप में वर्गीकृत किया जाता है। यह 1 या उससे कम ph मान वाले विलयनो की बहुत अधिक बफर क्षमता के परिणामस्वरूप होता है और इसे समतल प्रभाव के रूप में जाना जाता है।<ref>Porterfield, William W. ''Inorganic Chemistry'' (Addison-Wesley 1984) p.260 {{ISBN|0-201-05660-7}}</ref> निम्नलिखित जलीय और डाइमिथाइल सल्फॉक्साइड घोल में प्रबल अम्ल हैं। के मान <math chem="">\mathrm{p}K_\ce{a} </math>, प्रयोगात्मक रूप से मापा नहीं जा सकता। निम्नलिखित तालिका में मान 8 विभिन्न सैद्धांतिक गणनाओं के औसत मान हैं। | |||
निम्नलिखित जलीय और डाइमिथाइल सल्फॉक्साइड घोल में प्रबल अम्ल हैं। के मान <math chem="">\mathrm{p}K_\ce{a} </math>, प्रयोगात्मक रूप से मापा नहीं जा सकता। निम्नलिखित तालिका में मान 8 विभिन्न सैद्धांतिक गणनाओं के औसत मान हैं। | |||
:{| class="wikitable" | :{| class="wikitable" | ||
|+Estimated [[acid dissociation constant|p''K''<sub>a</sub>]] values<ref name=Leito>{{cite journal |last1=Trummal |first1=Aleksander |last2=Lipping |first2=Lauri |last3=Kaljurand |first3=Ivari |last4=Koppel |first4=Ilmar A. |last5=Leito |first5=Ivo |title=Acidity of strong acids in water and dimethyl sulfoxide |journal=J. Phys. Chem. A |date=2016 |volume=120 |issue=20 |pages=3663–3669 |doi=10.1021/acs.jpca.6b02253 |pmid=27115918|bibcode=2016JPCA..120.3663T |s2cid=29697201 }}</ref> | |+Estimated [[acid dissociation constant|p''K''<sub>a</sub>]] values<ref name=Leito>{{cite journal |last1=Trummal |first1=Aleksander |last2=Lipping |first2=Lauri |last3=Kaljurand |first3=Ivari |last4=Koppel |first4=Ilmar A. |last5=Leito |first5=Ivo |title=Acidity of strong acids in water and dimethyl sulfoxide |journal=J. Phys. Chem. A |date=2016 |volume=120 |issue=20 |pages=3663–3669 |doi=10.1021/acs.jpca.6b02253 |pmid=27115918|bibcode=2016JPCA..120.3663T |s2cid=29697201 }}</ref> | ||
|- | |- | ||
! | !अम्ल!!सूत्र!! जल में||DMSO में | ||
|- | |- | ||
|[[Hydrochloric acid]] ||HCl||−5.9 ± 0.4 ||−2.0 ± 0.6 | |[[Hydrochloric acid|हाइड्रोक्लोरिक अम्ल]] ||HCl||−5.9 ± 0.4 ||−2.0 ± 0.6 | ||
|- | |- | ||
|[[Hydrobromic acid]] ||HBr ||−8.8 ± 0.8||−6.8 ± 0.8 | |[[Hydrobromic acid|हाइड्रोब्रोमिक अम्ल]] ||HBr ||−8.8 ± 0.8||−6.8 ± 0.8 | ||
|- | |- | ||
|[[Hydroiodic acid]]|| HI ||−9.5 ± 1||−10.9 ± 1 | |[[Hydroiodic acid|हाइड्रोआयोडिक अम्ल]]|| HI ||−9.5 ± 1||−10.9 ± 1 | ||
|- | |- | ||
|[[Triflic acid]]|| H[CF<sub>3</sub>SO<sub>3</sub>] ||−14 ± 2||−14 ± 2 | |[[Triflic acid|ट्राइफ्लिक अम्ल]]|| H[CF<sub>3</sub>SO<sub>3</sub>] ||−14 ± 2||−14 ± 2 | ||
|- | |- | ||
|[[Perchloric acid]]|| H[ClO<sub>4</sub>] ||−15 ± 2||−15 ± 2 | |[[Perchloric acid|परक्लोरिक अम्ल]]|| H[ClO<sub>4</sub>] ||−15 ± 2||−15 ± 2 | ||
|} | |} | ||
साथ ही, जल में | साथ ही, जल में | ||
* नाइट्रिक अम्ल <chem>HNO3</chem> <math chem="">\mathrm{p}K_\ce{a} </math> = −1.6 <ref>{{Citation |last=Bell |first=R. P. |title=The Proton in Chemistry |edition=2nd |publisher=Cornell University Press |location=Ithaca, NY |year=1973 }}</ref> | * नाइट्रिक अम्ल <chem>HNO3</chem> <math chem="">\mathrm{p}K_\ce{a} </math> = −1.6 <ref>{{Citation |last=Bell |first=R. P. |title=The Proton in Chemistry |edition=2nd |publisher=Cornell University Press |location=Ithaca, NY |year=1973 }}</ref> | ||
* सल्फ्यूरिक अम्ल <chem>H2SO4</chem> ( | * सल्फ्यूरिक अम्ल <chem>H2SO4</chem> (केवल पहला पृथक्करण, <math chem="">\mathrm{p}K_\ce{a1} </math>≈ −3)<ref name="Housecroft">{{Housecroft2nd}}</ref>{{rp|(p. 171)}} | ||
कार्बनिक रसायन विज्ञान में प्रोटोनेटर के रूप में निम्नलिखित का उपयोग किया जा सकता है | कार्बनिक रसायन विज्ञान में प्रोटोनेटर के रूप में निम्नलिखित का उपयोग किया जा सकता है | ||
* [[फ्लोरोएंटिमोनिक एसिड|फ्लोरोएंटिमोनिक अम्ल]] <chem>H[SbF6]</chem> | * [[फ्लोरोएंटिमोनिक एसिड|फ्लोरोएंटिमोनिक अम्ल]] <chem>H[SbF6]</chem> | ||
* [[मैजिक एसिड|मैजिक अम्ल]] <chem>H[FSO3SbF5]</chem> | * [[मैजिक एसिड|मैजिक(जादू का) अम्ल]] <chem>H[FSO3SbF5]</chem> | ||
* [[कार्बोरेन सुपरएसिड]] <chem>H[CHB11Cl11]</chem> | * [[कार्बोरेन सुपरएसिड|कार्बोरेन अति अम्ल]] <chem>H[CHB11Cl11]</chem> | ||
* [[फ्लोरोसल्फ्यूरिक एसिड|फ्लोरोसल्फ्यूरिक अम्ल]] <chem>H[FSO3]</chem>(<math chem="">\mathrm{p}K_\ce{a} </math> = −6.4)<ref name=Guthrie/> | * [[फ्लोरोसल्फ्यूरिक एसिड|फ्लोरोसल्फ्यूरिक अम्ल]] <chem>H[FSO3]</chem>(<math chem="">\mathrm{p}K_\ce{a} </math> = −6.4)<ref name=Guthrie/> | ||
[[सल्फोनिक एसिड|सल्फोनिक अम्ल]], जैसे कि [[पी-टोलुइनसल्फोनिक एसिड| | [[सल्फोनिक एसिड|सल्फोनिक अम्ल]], जैसे कि [[पी-टोलुइनसल्फोनिक एसिड|P-टोलुइनसल्फोनिक अम्ल]] (टॉसिलिक अम्ल) प्रबल कार्बनिक ऑक्सीकाइड्स का एक वर्ग है।<ref name="Guthrie">{{cite journal |last1=Guthrie |first1=J.P. |title=Hydrolysis of esters of oxy acids: p''K''<sub>a</sub> values for strong acids. |journal=Can. J. Chem. |date=1978 |volume=56 |issue=17 |pages=2342–2354 |doi=10.1139/v78-385}}</ref> कुछ सल्फोनिक अम्ल को ठोस के रूप में अलग किया जा सकता है। [[polystyrene|पॉलीस्टायरीन]] सल्फोनेट में क्रियाशील पॉलीस्टीरिन एक पदार्थ का एक उदाहरण है जो एक ठोस प्रबल अम्ल है। | ||
== दुर्बल अम्ल == | == दुर्बल अम्ल == | ||
{{main| | {{main|अम्ल पृथक्करण स्थिरांक}} | ||
[[File:Weak_acid.png|thumb|आंशिक रूप से अलग करने वाले एक दुर्बल अम्ल की छवि]]एक दुर्बल अम्ल एक पदार्थ है जो एक विलायक में घुलने पर आंशिक रूप से अलग हो जाता है। घोल में अम्ल के बीच एक संतुलन होता है, <chem>HA</chem>, और पृथक्करण के उत्पाद। | [[File:Weak_acid.png|thumb|आंशिक रूप से अलग करने वाले एक दुर्बल अम्ल की छवि]]एक दुर्बल अम्ल एक पदार्थ है जो एक विलायक में घुलने पर आंशिक रूप से अलग हो जाता है। घोल में अम्ल के बीच एक संतुलन होता है, <chem>HA</chem>, और पृथक्करण के उत्पाद। | ||
:<Math>\mathrm {HA} \rightleftharpoons \mathrm { H^+ + A^-}</math> | :<Math>\mathrm {HA} \rightleftharpoons \mathrm { H^+ + A^-}</math> | ||
| Line 69: | Line 68: | ||
&=[H]+[H]^2/K_a \end{align}</math> कहाँ<math>T_H</math>अम्ल की [[विश्लेषणात्मक एकाग्रता]] का मूल्य है। जब इस समीकरण में सभी मात्राओं को संख्याओं के रूप में माना जाता है, तो आयनिक आवेश नहीं दिखाए जाते हैं और यह हाइड्रोजन आयन सांद्रता मान के मान में एक [[द्विघात समीकरण]] बन जाता है, <chem>[H]</chem>. | &=[H]+[H]^2/K_a \end{align}</math> कहाँ<math>T_H</math>अम्ल की [[विश्लेषणात्मक एकाग्रता]] का मूल्य है। जब इस समीकरण में सभी मात्राओं को संख्याओं के रूप में माना जाता है, तो आयनिक आवेश नहीं दिखाए जाते हैं और यह हाइड्रोजन आयन सांद्रता मान के मान में एक [[द्विघात समीकरण]] बन जाता है, <chem>[H]</chem>. | ||
:<math>\frac{[H]^2}{K_a} + [H] - T_H = 0</math> | :<math>\frac{[H]^2}{K_a} + [H] - T_H = 0</math> | ||
यह समीकरण दर्शाता है कि किसी दुर्बल अम्ल के विलयन का pH उसके दोनों पर निर्भर करता है <math chem="">K_\ce{a} </math> मूल्य और इसकी एकाग्रता। दुर्बल अम्लों के विशिष्ट उदाहरणों में एसिटिक अम्ल और फॉस्फोरस अम्ल शामिल हैं। एक अम्ल जैसे [[ओकसेलिक अम्ल]] (<chem>HOOC-COOH</chem>) को द्विक्षारकीय अम्ल कहा जाता है क्योंकि यह दो प्रोटॉन खो सकता है और एक साधारण आधार के दो अणुओं के साथ | यह समीकरण दर्शाता है कि किसी दुर्बल अम्ल के विलयन का pH उसके दोनों पर निर्भर करता है <math chem="">K_\ce{a} </math> मूल्य और इसकी एकाग्रता। दुर्बल अम्लों के विशिष्ट उदाहरणों में एसिटिक अम्ल और फॉस्फोरस अम्ल शामिल हैं। एक अम्ल जैसे [[ओकसेलिक अम्ल]] (<chem>HOOC-COOH</chem>) को द्विक्षारकीय अम्ल कहा जाता है क्योंकि यह दो प्रोटॉन खो सकता है और एक साधारण आधार के दो अणुओं के साथ अभिक्रिया कर सकता है। [[फॉस्फोरिक एसिड|फॉस्फोरिक अम्ल]] (<chem>H3PO4</chem>) आदिवासी है। | ||
अम्ल शक्ति के अधिक कठोर उपचार के लिए अम्ल पृथक्करण स्थिरांक देखें। इसमें डिबासिक अम्ल [[ स्यूसेनिक तेजाब | स्यूसेनिक अम्ल]] जैसे अम्ल शामिल हैं, जिसके लिए ऊपर दिखाए गए घोल के ph की गणना करने की सरल विधि का उपयोग नहीं किया जा सकता है। | अम्ल शक्ति के अधिक कठोर उपचार के लिए अम्ल पृथक्करण स्थिरांक देखें। इसमें डिबासिक अम्ल [[ स्यूसेनिक तेजाब | स्यूसेनिक अम्ल]] जैसे अम्ल शामिल हैं, जिसके लिए ऊपर दिखाए गए घोल के ph की गणना करने की सरल विधि का उपयोग नहीं किया जा सकता है। | ||
| Line 91: | Line 90: | ||
एक विलायक का एक महत्वपूर्ण उदाहरण जो जल से अधिक क्षारीय है, डाइमिथाइल सल्फ़ोक्साइड, DMSO है। <chem>(CH3)2SO</chem>. एक यौगिक जो जल में एक दुर्बल अम्ल है, DMSO में एक प्रबल अम्ल बन सकता है। एसिटिक अम्ल ऐसे पदार्थ का एक उदाहरण है। की एक व्यापक ग्रंथ सूची <math chem="">\mathrm{p}K_\ce{a} </math> DMSO और अन्य विलायक में घोल में मूल्य [http://tera.chem.ut.ee/~ivo/HA_UT/ गैर-जलीय विलायक में एसिडिटी-बेसिसिटी डेटा] पर पाया जा सकता है। | एक विलायक का एक महत्वपूर्ण उदाहरण जो जल से अधिक क्षारीय है, डाइमिथाइल सल्फ़ोक्साइड, DMSO है। <chem>(CH3)2SO</chem>. एक यौगिक जो जल में एक दुर्बल अम्ल है, DMSO में एक प्रबल अम्ल बन सकता है। एसिटिक अम्ल ऐसे पदार्थ का एक उदाहरण है। की एक व्यापक ग्रंथ सूची <math chem="">\mathrm{p}K_\ce{a} </math> DMSO और अन्य विलायक में घोल में मूल्य [http://tera.chem.ut.ee/~ivo/HA_UT/ गैर-जलीय विलायक में एसिडिटी-बेसिसिटी डेटा] पर पाया जा सकता है। | ||
कम ढांकता हुआ स्थिरांक के विलायक में भी | कम ढांकता हुआ स्थिरांक के विलायक में भी अति अम्ल प्रबल अम्ल होते हैं। सुपरएसिड्स के उदाहरण हैं फ्लोरोएंटिमोनिक अम्ल और मैजिक अम्ल। कुछ सुपरसिड्स को क्रिस्टलीकृत किया जा सकता है।<ref>{{cite journal |last1=Zhang |first1=Dingliang |last2=Rettig |first2=Stephen J. |last3=Trotter |first3=James |last4=Aubke |first4=Friedhelm |title=Superacid Anions: Crystal and Molecular Structures of Oxonium Undecafluorodiantimonate(V), [H<sub>3</sub>O][Sb<sub>2</sub>F<sub>11</sub>], Cesium Fluorosulfate, CsSO<sub>3</sub>F, Cesium Hydrogen Bis(fluorosulfate), Cs[H(SO<sub>3</sub>F)<sub>2</sub>], Cesium Tetrakis(fluorosulfato)aurate(III), Cs[Au(SO<sub>3</sub>F)<sub>4</sub>], Cesium Hexakis(fluorosulfato)platinate(IV), Cs<sub>2</sub>[Pt(SO<sub>3</sub>F)<sub>6</sub>], and Cesium Hexakis(fluorosulfato)antimonate(V), Cs[Sb(SO<sub>3</sub>F)<sub>6</sub>] | ||
|journal=Inorg. Chem. |date=1996 |volume=35 |issue=21 |pages=6113–6130 |doi=10.1021/ic960525l}}</ref> वे [[कार्बोकेशन]] को मात्रात्मक रूप से स्थिर भी कर सकते हैं।<ref name=Olah1968>{{cite journal | author = [[George A. Olah]], Schlosberg RH | title = Chemistry in Super Acids. I. Hydrogen Exchange and Polycondensation of Methane and Alkanes in FSO<sub>3</sub>H–SbF<sub>5</sub> ("Magic Acid") Solution. Protonation of Alkanes and the Intermediacy of CH<sub>5</sub><sup>+</sup> and Related Hydrocarbon Ions. The High Chemical Reactivity of "Paraffins" in Ionic Solution Reactions | journal = Journal of the American Chemical Society | year = 1968 | volume = 90 | pages = 2726–7 | doi = 10.1021/ja01012a066 | issue = 10 }}</ref> | |journal=Inorg. Chem. |date=1996 |volume=35 |issue=21 |pages=6113–6130 |doi=10.1021/ic960525l}}</ref> वे [[कार्बोकेशन]] को मात्रात्मक रूप से स्थिर भी कर सकते हैं।<ref name=Olah1968>{{cite journal | author = [[George A. Olah]], Schlosberg RH | title = Chemistry in Super Acids. I. Hydrogen Exchange and Polycondensation of Methane and Alkanes in FSO<sub>3</sub>H–SbF<sub>5</sub> ("Magic Acid") Solution. Protonation of Alkanes and the Intermediacy of CH<sub>5</sub><sup>+</sup> and Related Hydrocarbon Ions. The High Chemical Reactivity of "Paraffins" in Ionic Solution Reactions | journal = Journal of the American Chemical Society | year = 1968 | volume = 90 | pages = 2726–7 | doi = 10.1021/ja01012a066 | issue = 10 }}</ref> | ||
गैस चरण और गैर-जलीय विलायक में लुईस क्षार के साथ | गैस चरण और गैर-जलीय विलायक में लुईस क्षार के साथ अभिक्रिया करने वाले [[लुईस एसिड|लुईस अम्ल]] को ECW मॉडल में वर्गीकृत किया गया है, और यह दिखाया गया है कि अम्ल की ताकत का कोई एक क्रम नहीं है।<ref>{{cite journal|author1=Vogel G. C. |author2=Drago, R. S. |year=1996|journal=Journal of Chemical Education|volume=73|pages=701–707|title=ईसीडब्ल्यू मॉडल|issue=8 |bibcode=1996JChEd..73..701V|doi=10.1021/ed073p701}}</ref> लुईस अम्ल की सापेक्ष स्वीकर्ता शक्ति, अन्य लुईस अम्ल बनाम आधारों की एक श्रृंखला की ओर, ईसीडब्ल्यू मॉडल | सीबी भूखंडों द्वारा सचित्र किया जा सकता है।<ref>Laurence, C. and Gal, J-F. Lewis Basicity and Affinity Scales, Data and Measurement, (Wiley 2010) pp 50-51 ISBN 978-0-470-74957-9</ref><ref>{{cite journal|author1=Cramer, R. E. |author2=Bopp, T. T. |year=1977|title= लुईस अम्ल और क्षार के लिए व्यसन निर्माण की एन्थैल्पी का चित्रमय प्रदर्शन|journal= Journal of Chemical Education |volume=54|pages=612–613|doi= 10.1021/ed054p612}} The plots shown in this paper used older parameters. Improved E&C parameters are listed in [[ECW model]]. </ref> यह दिखाया गया है कि लुईस अम्ल शक्ति के क्रम को परिभाषित करने के लिए कम से कम दो गुणों पर विचार किया जाना चाहिए। गुणात्मक एचएसएबी सिद्धांत के लिए दो गुण कठोरता और शक्ति हैं जबकि मात्रात्मक ईसीडब्ल्यू मॉडल के लिए दो गुण इलेक्ट्रोस्टैटिक और सहसंयोजक हैं। | ||
== अम्ल शक्ति का निर्धारण करने वाले कारक == | == अम्ल शक्ति का निर्धारण करने वाले कारक == | ||
| Line 105: | Line 104: | ||
!p''K''<sub>a</sub><!-- Dead reference <ref name="Evanspka">[https://www.scribd.com/doc/6792576/638478 Section 8: Electrolytes, Electromotive forces and Chemical Equilibrium]</ref> --> | !p''K''<sub>a</sub><!-- Dead reference <ref name="Evanspka">[https://www.scribd.com/doc/6792576/638478 Section 8: Electrolytes, Electromotive forces and Chemical Equilibrium]</ref> --> | ||
|- | |- | ||
|[[File:2chlorobutanoic.png]]||2-chlorobutanoic | |[[File:2chlorobutanoic.png]]||2-chlorobutanoic अम्ल||2.86 | ||
|- | |- | ||
|[[File:3chlorobutanoic.png]]||3-chlorobutanoic | |[[File:3chlorobutanoic.png]]||3-chlorobutanoic अम्ल||4.0 | ||
|- | |- | ||
|[[File:4chlorobutanoic.png]]||4-chlorobutanoic | |[[File:4chlorobutanoic.png]]||4-chlorobutanoic अम्ल||4.5 | ||
|- | |- | ||
|[[File:butanoic.png]]||[[Butyric acid|butanoic | |[[File:butanoic.png]]||[[Butyric acid|butanoic अम्ल]]||4.5 | ||
|} | |} | ||
| Line 123: | Line 122: | ||
!p''K''<sub>a</sub><!-- Dead reference <ref name="Evanspka">[https://www.scribd.com/doc/6792576/638478 Section 8: Electrolytes, Electromotive forces and Chemical Equilibrium]</ref> --> | !p''K''<sub>a</sub><!-- Dead reference <ref name="Evanspka">[https://www.scribd.com/doc/6792576/638478 Section 8: Electrolytes, Electromotive forces and Chemical Equilibrium]</ref> --> | ||
|-align="center" | |-align="center" | ||
|[[file:Perchloric-acid-2D-dimensions.png|100px]]||[[perchloric acid]]|| 7||style="width: 30pt;"| -8<sup>†</sup> | |[[file:Perchloric-acid-2D-dimensions.png|100px]]||[[perchloric acid|perchloric अम्ल]]|| 7||style="width: 30pt;"| -8<sup>†</sup> | ||
|-align="center" | |-align="center" | ||
|[[file:Chloric-acid-2D.png|100px]] ||[[chloric acid]]||5||-1 | |[[file:Chloric-acid-2D.png|100px]] ||[[chloric acid|chloric अम्ल]]||5||-1 | ||
|-align="center" | |-align="center" | ||
||[[file: Chlorous-acid-2D.png|100px]]||[[chlorous acid]]||3||2.0 | ||[[file: Chlorous-acid-2D.png|100px]]||[[chlorous acid|chlorous अम्ल]]||3||2.0 | ||
|-align="center" | |-align="center" | ||
|[[file:Hypochlorous-acid-2D-dimensions.svg|100px]] ||[[hypochlorous acid]]||1||7.53 | |[[file:Hypochlorous-acid-2D-dimensions.svg|100px]] ||[[hypochlorous acid|hypochlorous अम्ल]]||1||7.53 | ||
|} | |} | ||
† सैद्धांतिक | † सैद्धांतिक | ||
Revision as of 19:13, 4 June 2023
अम्ल शक्ति एक अम्ल की प्रवृत्ति है, जिसे रासायनिक सूत्र द्वारा दर्शाया जाता है , एक प्रोटॉन (रसायन विज्ञान) में अलग होने के लिए, , और एक ऋणायन, . घोल में एक प्रबल अम्ल का पृथक्करण (रसायन) प्रभावी रूप से पूरा हो गया है, इसके सबसे अधिक केंद्रित विलयनो को छोड़कर।
प्रबल अम्लों के उदाहरण हाइड्रोक्लोरिक अम्ल हैं , परक्लोरिक अम्ल , नाइट्रिक अम्ल और सल्फ्यूरिक अम्ल .
एक दुर्बल अम्ल केवल आंशिक रूप से अलग हो जाता है, दोनों असंगठित अम्ल और इसके पृथक्करण उत्पाद एक दूसरे के साथ संतुलन रसायन विज्ञान में घोल में मौजूद होते हैं।
एसीटिक अम्ल () दुर्बल अम्ल का उदाहरण है। एक दुर्बल अम्ल की ताकत उसके अम्ल पृथक्करण स्थिरांक द्वारा निर्धारित की जाती है, मान।
एक दुर्बल कार्बनिक रसायन अम्ल की ताकत स्थानापन्न प्रभावों पर निर्भर हो सकती है। एक अकार्बनिक रसायन विज्ञान अम्ल की ताकत उस परमाणु के लिए ऑक्सीकरण अवस्था पर निर्भर करती है जिससे प्रोटॉन जुड़ा हो सकता है। अम्ल शक्ति विलायक पर निर्भर है। उदाहरण के लिए, हाइड्रोजन क्लोराइड जलीय घोल में एक प्रबल अम्ल है, लेकिन ग्लेशियल एसिटिक(हिमनद अम्लीय) अम्ल में घुलने पर एक दुर्बल अम्ल है।
अम्ल शक्ति के उपाय
किसी अम्ल की सामर्थ्य का सामान्य माप उसका अम्ल पृथक्करण स्थिरांक होता है (), जिसे अनुमापन विधियों द्वारा प्रयोगात्मक रूप से निर्धारित किया जा सकता है। प्रबल अम्ल का एक बड़ा होता है और एक छोटा लघुगणकीय स्थिरांक () दुर्बल अम्लों की तुलना में। एक अम्ल जितना प्रबल होता है, उतनी ही आसानी से एक प्रोटॉन खो देता है, अवक्षेपण की आसानी में योगदान करने वाले दो प्रमुख कारक रासायनिक ध्रुवीयता बंधन और परमाणु A का आकार, जो की ताकत निर्धारित करते हैं गहरा संबंध। अम्ल की ताकत संयुग्म आधार की स्थिरता पर भी निर्भर करती है।
जब मूल्य एक अम्लीय विलेय की एक प्रोटॉन को एक मानक विलायक (समान्यता जल या DMSO) में स्थानांतरित करने की प्रवृत्ति को मापता है, एक अम्लीय विलायक की एक प्रोटॉन को एक संदर्भ विलेय (समान्यता एक दुर्बल एनिलिन क्षार) में स्थानांतरित करने की प्रवृत्ति को इसके हैमेट अम्लता समारोह द्वारा मापा जाता है । यद्यपि अम्ल शक्ति की ये दो अवधारणाएं प्रायः एक प्रोटॉन दान करने के लिए पदार्थ की समान सामान्य प्रवृत्ति की मात्रा होती हैं और मान विशिष्ट गुणों के माप हैं और कभी-कभी अलग हो सकते हैं। उदाहरण के लिए, हाइड्रोजन फ्लोराइड, चाहे जल में घुल जाए ( = 3.2) या DMSO ( = 15), है मान दर्शाता है कि यह इन विलायक में अधूरा पृथक्करण से गुजरता है, जिससे यह एक दुर्बल अम्ल बन जाता है। यद्यपि, कठोर सूखे, स्वच्छ अम्लीय माध्यम के रूप में, हाइड्रोजन फ्लोराइड में एक है -15 का मान,[1] यह 100% सल्फ्यूरिक अम्ल की तुलना में अधिक प्रबल प्रोटोनिंग माध्यम बनाता है और इस प्रकार, परिभाषा के अनुसार, एक अतिअम्ल [2] (अस्पष्टता को रोकने के लिए, इस लेख के बाकी हिस्सों में, प्रबल अम्ल, जब तक कि अन्यथा न कहा जाए, एक ऐसे अम्ल को संदर्भित करेगा जो इसके द्वारा मापा गया है मान ( <-1.74)। यह उपयोग अधिकांश अभ्यास करने वाले रसायनज्ञ के सामान्य बोलचाल के अनुरूप है।)
जब प्रश्न में अम्लीय माध्यम एक तनु जलीय घोल है, तो लगभग ph मान के बराबर है, जो जलीय की सांद्रता का ऋणात्मक लघुगणक है मिश्रण में। जल में एक अम्ल के सरल घोल का ph दोनों द्वारा निर्धारित किया जाता है और अम्ल की सघनता। दुर्बल अम्ल घोल के लिए, यह वियोजन (रसायन विज्ञान) पर निर्भर करता है, जो एक संतुलन गणना द्वारा निर्धारित किया जा सकता है। अम्ल के केंद्रित घोल के लिए, विशेष रूप से प्रबल अम्ल जिसके लिए ph <0, ph मान की तुलना में अम्लता का एक बेहतर उपाय है।
प्रबल अम्ल
एक प्रबल अम्ल एक अम्ल होता है जो अभिक्रिया के अनुसार अलग हो जाता है
जहाँ S एक विलायक अणु का प्रतिनिधित्व करता है, जैसे कि जल का एक अणु या डाइमिथाइल सल्फ़ोक्साइड (DMSO), इस हद तक कि असंगठित प्रजातियों की सघनता मापने के लिए बहुत कम है। व्यावहारिक उद्देश्यों के लिए एक प्रबल अम्ल को पूरी तरह से वियोजित कहा जा सकता है। प्रबल अम्ल का उदाहरण हाइड्रोक्लोरिक अम्ल है।
- (जलीय घोल में)
A के साथ कोई भी अम्ल मान जो लगभग -2 से कम है, उसे प्रबल अम्ल के रूप में वर्गीकृत किया जाता है। यह 1 या उससे कम ph मान वाले विलयनो की बहुत अधिक बफर क्षमता के परिणामस्वरूप होता है और इसे समतल प्रभाव के रूप में जाना जाता है।[3] निम्नलिखित जलीय और डाइमिथाइल सल्फॉक्साइड घोल में प्रबल अम्ल हैं। के मान , प्रयोगात्मक रूप से मापा नहीं जा सकता। निम्नलिखित तालिका में मान 8 विभिन्न सैद्धांतिक गणनाओं के औसत मान हैं।
Estimated pKa values[4] अम्ल सूत्र जल में DMSO में हाइड्रोक्लोरिक अम्ल HCl −5.9 ± 0.4 −2.0 ± 0.6 हाइड्रोब्रोमिक अम्ल HBr −8.8 ± 0.8 −6.8 ± 0.8 हाइड्रोआयोडिक अम्ल HI −9.5 ± 1 −10.9 ± 1 ट्राइफ्लिक अम्ल H[CF3SO3] −14 ± 2 −14 ± 2 परक्लोरिक अम्ल H[ClO4] −15 ± 2 −15 ± 2
साथ ही, जल में
कार्बनिक रसायन विज्ञान में प्रोटोनेटर के रूप में निम्नलिखित का उपयोग किया जा सकता है
सल्फोनिक अम्ल, जैसे कि P-टोलुइनसल्फोनिक अम्ल (टॉसिलिक अम्ल) प्रबल कार्बनिक ऑक्सीकाइड्स का एक वर्ग है।[7] कुछ सल्फोनिक अम्ल को ठोस के रूप में अलग किया जा सकता है। पॉलीस्टायरीन सल्फोनेट में क्रियाशील पॉलीस्टीरिन एक पदार्थ का एक उदाहरण है जो एक ठोस प्रबल अम्ल है।
दुर्बल अम्ल
एक दुर्बल अम्ल एक पदार्थ है जो एक विलायक में घुलने पर आंशिक रूप से अलग हो जाता है। घोल में अम्ल के बीच एक संतुलन होता है, , और पृथक्करण के उत्पाद।
विलायक (जैसे जल) इस अभिव्यक्ति से छोड़ा जाता है जब इसकी एकाग्रता अम्ल पृथक्करण की प्रक्रिया से प्रभावी रूप से अपरिवर्तित होती है। एक दुर्बल अम्ल की ताकत को संतुलन स्थिरांक के रूप में मापा जा सकता है, गणित रसायन => का </ गणित>, इस प्रकार परिभाषित किया गया है, जहांएक रासायनिक अंश, X की सांद्रता को दर्शाता है।
जब का एक संख्यात्मक मान यह ज्ञात है कि इसका उपयोग अम्ल की दी गई सांद्रता के साथ विलयन में पृथक्करण की सीमा निर्धारित करने के लिए किया जा सकता है, , द्रव्यमान के संरक्षण के नियम को लागू करके।
- कहाँअम्ल की विश्लेषणात्मक एकाग्रता का मूल्य है। जब इस समीकरण में सभी मात्राओं को संख्याओं के रूप में माना जाता है, तो आयनिक आवेश नहीं दिखाए जाते हैं और यह हाइड्रोजन आयन सांद्रता मान के मान में एक द्विघात समीकरण बन जाता है, .
यह समीकरण दर्शाता है कि किसी दुर्बल अम्ल के विलयन का pH उसके दोनों पर निर्भर करता है मूल्य और इसकी एकाग्रता। दुर्बल अम्लों के विशिष्ट उदाहरणों में एसिटिक अम्ल और फॉस्फोरस अम्ल शामिल हैं। एक अम्ल जैसे ओकसेलिक अम्ल () को द्विक्षारकीय अम्ल कहा जाता है क्योंकि यह दो प्रोटॉन खो सकता है और एक साधारण आधार के दो अणुओं के साथ अभिक्रिया कर सकता है। फॉस्फोरिक अम्ल () आदिवासी है।
अम्ल शक्ति के अधिक कठोर उपचार के लिए अम्ल पृथक्करण स्थिरांक देखें। इसमें डिबासिक अम्ल स्यूसेनिक अम्ल जैसे अम्ल शामिल हैं, जिसके लिए ऊपर दिखाए गए घोल के ph की गणना करने की सरल विधि का उपयोग नहीं किया जा सकता है।
प्रायोगिक निर्धारण
ए का प्रायोगिक निर्धारण मूल्य समान्यता अनुमापन के माध्यम से किया जाता है।[8] एक विशिष्ट प्रक्रिया इस प्रकार होगी। अम्ल या अम्ल के नमक युक्त घोल में प्रबल अम्ल की मात्रा को उस बिंदु तक जोड़ा जाता है जहां यौगिक पूरी तरह से प्रोटोनेटेड होता है। फिर घोल को एक प्रबल आधार के साथ अनुमापित किया जाता है
केवल अवक्षेपित प्रजातियों तक, , घोल में रहता है। अनुमापन में प्रत्येक बिंदु पर एक ग्लास इलेक्ट्रोड और एक ph मीटर का उपयोग करके ph को मापा जाता है। कम से कम वर्गों की विधि का उपयोग करते हुए, परिकलित ph मानों को प्रेक्षित मानों में फ़िट करके संतुलन स्थिरांक पाया जाता है।
संयुग्म अम्ल/क्षार जोड़ी
कभी-कभी यह कहा जाता है कि दुर्बल अम्ल का संयुग्मी प्रबल क्षार होता है। ऐसा बयान गलत है। उदाहरण के लिए, एसिटिक अम्ल एक दुर्बल अम्ल है जिसमें a = 1.75 x 10−5</सुप>. इसका संयुग्मी आधार K के साथ एसीटेट आयन हैb = 10-14/केa = 5.7 x 10-10 (संबंध से केa × केb = 10-14), जो निश्चित रूप से एक प्रबल आधार के अनुरूप नहीं है। एक दुर्बल अम्ल का संयुग्म प्रायः एक दुर्बल आधार होता है और इसके विपरीत।
गैर-जलीय विलायक में अम्ल
एक अम्ल की ताकत विलायक से विलायक में भिन्न होती है। एक अम्ल जो जल में प्रबल होता है वह कम बुनियादी विलायक में दुर्बल हो सकता है, और एक अम्ल जो जल में दुर्बल होता है वह अधिक बुनियादी विलायक में प्रबल हो सकता है। ब्रोंस्टेड-लोरी अम्ल-क्षार सिद्धांत के अनुसार, विलायक S एक प्रोटॉन ग्रहण कर सकता है।
उदाहरण के लिए, हाइड्रोक्लोरिक अम्ल शुद्ध एसिटिक अम्ल के घोल में एक दुर्बल अम्ल है, जो जल से अधिक अम्लीय है।
हाइड्रोजन हलाइड के आयनीकरण की सीमा क्रम में घट जाती है . एसिटिक अम्ल को लेवलिंग इफेक्ट # लेवलिंग और तीन अम्ल के लिए अलग-अलग विलायक कहा जाता है, जबकि जल नहीं है।[6]: (p. 217)
एक विलायक का एक महत्वपूर्ण उदाहरण जो जल से अधिक क्षारीय है, डाइमिथाइल सल्फ़ोक्साइड, DMSO है। . एक यौगिक जो जल में एक दुर्बल अम्ल है, DMSO में एक प्रबल अम्ल बन सकता है। एसिटिक अम्ल ऐसे पदार्थ का एक उदाहरण है। की एक व्यापक ग्रंथ सूची DMSO और अन्य विलायक में घोल में मूल्य गैर-जलीय विलायक में एसिडिटी-बेसिसिटी डेटा पर पाया जा सकता है।
कम ढांकता हुआ स्थिरांक के विलायक में भी अति अम्ल प्रबल अम्ल होते हैं। सुपरएसिड्स के उदाहरण हैं फ्लोरोएंटिमोनिक अम्ल और मैजिक अम्ल। कुछ सुपरसिड्स को क्रिस्टलीकृत किया जा सकता है।[9] वे कार्बोकेशन को मात्रात्मक रूप से स्थिर भी कर सकते हैं।[10] गैस चरण और गैर-जलीय विलायक में लुईस क्षार के साथ अभिक्रिया करने वाले लुईस अम्ल को ECW मॉडल में वर्गीकृत किया गया है, और यह दिखाया गया है कि अम्ल की ताकत का कोई एक क्रम नहीं है।[11] लुईस अम्ल की सापेक्ष स्वीकर्ता शक्ति, अन्य लुईस अम्ल बनाम आधारों की एक श्रृंखला की ओर, ईसीडब्ल्यू मॉडल | सीबी भूखंडों द्वारा सचित्र किया जा सकता है।[12][13] यह दिखाया गया है कि लुईस अम्ल शक्ति के क्रम को परिभाषित करने के लिए कम से कम दो गुणों पर विचार किया जाना चाहिए। गुणात्मक एचएसएबी सिद्धांत के लिए दो गुण कठोरता और शक्ति हैं जबकि मात्रात्मक ईसीडब्ल्यू मॉडल के लिए दो गुण इलेक्ट्रोस्टैटिक और सहसंयोजक हैं।
अम्ल शक्ति का निर्धारण करने वाले कारक
आगमनात्मक प्रभाव
कार्बनिक कार्बोक्जिलिक अम्ल में, एक इलेक्ट्रोनगेटिव प्रतिस्थापन एक अम्लीय बंधन से आगमनात्मक प्रभाव के माध्यम से इलेक्ट्रॉन घनत्व को खींच सकता है, जिसके परिणामस्वरूप एक छोटा होता है मान। प्रभाव कम हो जाता है, आगे इलेक्ट्रोनगेटिव तत्व कार्बोक्सिलेट समूह से होता है, जैसा कि हलोजनयुक्त ब्यूटेनिक अम्ल की निम्नलिखित श्रृंखला द्वारा दिखाया गया है।
| Structure | Name | pKa |
|---|---|---|
 |
2-chlorobutanoic अम्ल | 2.86 |
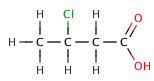 |
3-chlorobutanoic अम्ल | 4.0 |
 |
4-chlorobutanoic अम्ल | 4.5 |
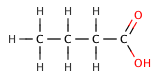 |
butanoic अम्ल | 4.5 |
ऑक्सीकरण अवस्था का प्रभाव
किसी तत्व के ऑक्सोअम्लों के समुच्चय में, तत्व की ऑक्सीकरण अवस्था के साथ मान घटता है। क्लोरीन के ऑक्सोएसिड इस प्रवृत्ति को दर्शाते हैं।[6]: (p. 171)
| Structure | Name | Oxidation state |
pKa |
|---|---|---|---|
 |
perchloric अम्ल | 7 | -8† |
 |
chloric अम्ल | 5 | -1 |
| chlorous अम्ल | 3 | 2.0 | |
 |
hypochlorous अम्ल | 1 | 7.53 |
† सैद्धांतिक
संदर्भ
- ↑ Liang, Joan-Nan Jack (1976). हाइड्रोफ्लोरिक एसिड और कुछ संबंधित सुपरसिड सिस्टम्स (पीएचडी थीसिस) के लिए हैमेट एसिडिटी फ़ंक्शन (PDF). Hamilton, Ontario: McMaster University. p. 94.
- ↑ Miessler G.L. and Tarr D.A. Inorganic Chemistry (2nd ed., Prentice-Hall 1998, p.170) ISBN 0-13-841891-8
- ↑ Porterfield, William W. Inorganic Chemistry (Addison-Wesley 1984) p.260 ISBN 0-201-05660-7
- ↑ Trummal, Aleksander; Lipping, Lauri; Kaljurand, Ivari; Koppel, Ilmar A.; Leito, Ivo (2016). "Acidity of strong acids in water and dimethyl sulfoxide". J. Phys. Chem. A. 120 (20): 3663–3669. Bibcode:2016JPCA..120.3663T. doi:10.1021/acs.jpca.6b02253. PMID 27115918. S2CID 29697201.
- ↑ Bell, R. P. (1973), The Proton in Chemistry (2nd ed.), Ithaca, NY: Cornell University Press
- ↑ 6.0 6.1 6.2 Housecroft, C. E.; Sharpe, A. G. (2004). Inorganic Chemistry (2nd ed.). Prentice Hall. ISBN 978-0-13-039913-7.
- ↑ 7.0 7.1 Guthrie, J.P. (1978). "Hydrolysis of esters of oxy acids: pKa values for strong acids". Can. J. Chem. 56 (17): 2342–2354. doi:10.1139/v78-385.
- ↑ Martell, A.E.; Motekaitis, R.J. (1992). स्थिरता स्थिरांक का निर्धारण और उपयोग. Wiley. ISBN 0-471-18817-4. Chapter 4: Experimental Procedure for Potentiometric pH Measurement of Metal Complex Equilibria
- ↑ Zhang, Dingliang; Rettig, Stephen J.; Trotter, James; Aubke, Friedhelm (1996). "Superacid Anions: Crystal and Molecular Structures of Oxonium Undecafluorodiantimonate(V), [H3O][Sb2F11], Cesium Fluorosulfate, CsSO3F, Cesium Hydrogen Bis(fluorosulfate), Cs[H(SO3F)2], Cesium Tetrakis(fluorosulfato)aurate(III), Cs[Au(SO3F)4], Cesium Hexakis(fluorosulfato)platinate(IV), Cs2[Pt(SO3F)6], and Cesium Hexakis(fluorosulfato)antimonate(V), Cs[Sb(SO3F)6]". Inorg. Chem. 35 (21): 6113–6130. doi:10.1021/ic960525l.
- ↑ George A. Olah, Schlosberg RH (1968). "Chemistry in Super Acids. I. Hydrogen Exchange and Polycondensation of Methane and Alkanes in FSO3H–SbF5 ("Magic Acid") Solution. Protonation of Alkanes and the Intermediacy of CH5+ and Related Hydrocarbon Ions. The High Chemical Reactivity of "Paraffins" in Ionic Solution Reactions". Journal of the American Chemical Society. 90 (10): 2726–7. doi:10.1021/ja01012a066.
- ↑ Vogel G. C.; Drago, R. S. (1996). "ईसीडब्ल्यू मॉडल". Journal of Chemical Education. 73 (8): 701–707. Bibcode:1996JChEd..73..701V. doi:10.1021/ed073p701.
- ↑ Laurence, C. and Gal, J-F. Lewis Basicity and Affinity Scales, Data and Measurement, (Wiley 2010) pp 50-51 ISBN 978-0-470-74957-9
- ↑ Cramer, R. E.; Bopp, T. T. (1977). "लुईस अम्ल और क्षार के लिए व्यसन निर्माण की एन्थैल्पी का चित्रमय प्रदर्शन". Journal of Chemical Education. 54: 612–613. doi:10.1021/ed054p612. The plots shown in this paper used older parameters. Improved E&C parameters are listed in ECW model.
बाहरी संबंध
- Titration of acids - freeware for data analysis and simulation of potentiometric titration curves