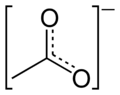
एसीटेट

| |
| Names | |
|---|---|
| IUPAC name
Acetate
| |
| Systematic IUPAC name
Ethanoate | |
| Identifiers | |
3D model (JSmol)
|
|
| ChemSpider | |
PubChem CID
|
|
| UNII | |
| |
| |
| Properties | |
| C 2H 3O− 2 | |
| Molar mass | |
| Conjugate acid | Acetic acid |
Except where otherwise noted, data are given for materials in their standard state (at 25 °C [77 °F], 100 kPa).
| |
एसीटेट /ˈæsɪteɪt/ एक क्षार (जैसे क्षार धातु, क्षारीय पृथ्वी धातु, संक्रमण धातु, अधातु या मूल रेडिकल (रसायन विज्ञान)) के साथ एसीटिक अम्ल के संयोजन द्वारा गठित नमक (रसायन विज्ञान) है। एसीटेट संयुग्म एसिड या आयन का भी वर्णन करता है (विशेष रूप से, नकारात्मक रूप से आवेशित आयन जिसे आयन कहा जाता है) सामान्यतः जलीय घोल में पाया जाता है और रासायनिक सूत्र के साथ लिखा जाता है। C
2H
3O−
2. एसीटेट आयन और धनात्मक आयन (जिसे धनायन कहा जाता है) के संयोजन से बनने वाले तटस्थ अणुओं को भी सामान्यतः एसीटेट कहा जाता है (इसलिए, सीसा का एसीटेट, एल्यूमीनियम का एसीटेट, आदि)। इनमें से सबसे सरल हाइड्रोजन एसीटेट है (जिसे एसिटिक एसिड कहा जाता है) जिसमें संबंधित लवण, एस्टर और पॉलीऐटोमिक आयन CH
3CO−
2, या CH
3COO−
होते हैं।
उद्योग में सालाना लगभग 5 बिलियन किलोग्राम एसिटिक एसिड का उत्पादन एसीटेट के उत्पादन में किया जाता है, जो सामान्यतः पॉलिमर का रूप ले लेता है। प्रकृति में, जैव संश्लेषण के लिए एसीटेट सबसे साधारण बिल्डिंग ब्लॉक है।
नामकरण और सामान्य सूत्र
जब किसी लवण (रसायन) का भाग एसीटेट आयन के सूत्र के रूप में लिखा जाता है CH
3CO−
2, C
2H
3O−
2, या CH
3COO−
रसायनज्ञ अधिकांशतः एसीटेट को OAc− के रूप में प्रस्तुत करते हैं या, सामान्यतः कम, AcO− इस प्रकार, HOAc एसिटिक एसिड के लिए, NaOAc एथिल एसीटेट के लिए, और EtOAc एथिल एसीटेट के लिए प्रतीक है।[1] (चूंकि AC एसिटल समूह CH3CO के लिए सामान्य प्रतीक है[2][3] छद्म तत्व प्रतीक "Ac" भी कभी-कभी पूरे एसीटेट आयन का संकेत के रूप में रासायनिक सूत्रों में सामना करना पड़ा है (CH
3CO−
2) इसे एक्टिनाइड श्रृंखला के पहले तत्व, जंगी के प्रतीक के साथ भ्रमित नहीं होना है प्रसंग विसंबद्धता का मार्गदर्शन करता है। उदाहरण के लिए, सोडियम एसीटेट के सूत्र को "NaC2H3O2" के अतिरिक्त NaOAc के रूप में संक्षिप्त किया जा सकता है OAc संक्षिप्त नाम का उपयोग करते समय पेरासटिक एसिड के साथ भ्रम से बचने के लिए भी सावधानी बरतनी चाहिए; स्पष्टता के लिए और अनुवाद करते समय त्रुटियों से बचने के लिए, दोनों यौगिकों का उल्लेख करते हुए साहित्य में HOAc से बचना चाहिए।
चूंकि इसका व्यवस्थित नाम इथेनोएट है (/ɪˈθænoʊ.eɪt/), सामान्य एसीटेट पसंदीदा IUPAC नाम बना हुआ है।[4]
लवण
एसीटेट [CH3COO]−,(या [C2H3O2]−) कार्बोक्सिलेट परिवार में से एक है। यह एसिटिक अम्ल का संयुग्मी अम्ल है। 5.5 के पीएच से ऊपर, एसिटिक एसिड एसीटेट में परिवर्तित हो जाता है[1]
CH3COOH ⇌ CH3COO− + H+
कई एसीटेट लवण आयनिक होते हैं, जो पानी में अच्छी तरह से घुलने की उनकी प्रवृत्ति से संकेत मिलता है। घर में सामान्यतः पाया जाने वाला एसीटेट सोडियम एसीटेट है, सफेद ठोस जिसे सिरका और सोडियम बाईकारबोनेट (सोडा का बाइकार्बोनेट) के संयोजन से तैयार किया जा सकता है:
- CH3COOH + NaHCO3 → CH3COO−Na+ + H2O + CO2
संक्रमण धातुओं को एसीटेट द्वारा जटिल किया जा सकता है। एसीटेट कॉम्प्लेक्स के उदाहरणों में क्रोमियम (II) एसीटेट और बेसिक जिंक एसीटेट सम्मिलित हैं।
वाणिज्यिक रूप से महत्वपूर्ण एसीटेट लवण एल्यूमीनियम एसीटेट हैं, जो रंगाई, अम्मोणिउम असेटट, एसिटामाइड के अग्रदूत और पोटेशियम एसीटेट में उपयोग किया जाता है, जो मूत्रवर्धक के रूप में उपयोग किया जाता है। तीनों लवण रंगहीन और पानी में अत्यधिक घुलनशील होते हैं।[5]
एस्टर
एसीटेट एस्टर का सामान्य सूत्र CH3CO2 जहां R स्थानापन्न है। एस्टर बाजार में एसीटेट के प्रमुख रूप हैं। एसीटेट लवण के विपरीत, एसीटेट एस्टर अधिकांशतः तरल, लिपोफिलिक और कभी-कभी अस्थिर होते हैं। वे लोकप्रिय हैं क्योंकि उनके पास निरापद, अधिकांशतः मीठी गंध होती है, वे सस्ती होती हैं, और वे सामान्यतः कम विषाक्तता वाली होती हैं।
विनयल असेटेट के उत्पादन में लगभग आधे एसिटिक एसिड उत्पादन की खपत होती है, जो पॉलीविनायल अल्कोहल का अग्रदूत है जो कई पेंट्स का घटक है। सेलूलोज़ एसीटेट के उत्पादन में एसिटिक एसिड का दूसरा सबसे बड़ा उपयोग होता है। वास्तव में, एसीटेट सेलूलोज एसीटेट के लिए शब्दजाल है, जिसका उपयोग फाइबर या विविध उत्पादों के उत्पादन में किया जाता है, उदा। ऑडियो रिकॉर्ड उत्पादन में उपयोग की जाने वाली एसीटेट डिस्क सेल्युलोज एसीटेट कई घरेलू उत्पादों में पाया जा सकता है। कई औद्योगिक विलायक एसीटेट हैं, जिनमें मिथाइल एसीटेट, एथिल एसीटेट, आइसोप्रोपिल एसीटेट, एथिलहेक्सिल एसीटेट सम्मिलित हैं। ब्यूटाइल एसीटेट सुगंध है जिसका उपयोग खाद्य उत्पादों में किया जाता है।[5]
जीव विज्ञान में एसीटेट
जीव विज्ञान में एसीटेट सामान्य आयन है। यह मुख्य रूप से एसिटाइल कोएंजाइम A के रूप में जीवों द्वारा उपयोग किया जाता है।[6]
सोडियम एसीटेट का इंट्रापेरिटोनियल इंजेक्शन (20 या 60 मिलीग्राम प्रति किलो शरीर द्रव्यमान) संवेदनशील चूहों में सिरदर्द पैदा करने के लिए पाया गया था, और यह प्रस्तावित किया गया है कि इथेनॉल के ऑक्सीकरण से उत्पन्न एसीटेट अत्यधिक नशा उत्पन करने का प्रमुख कारक है। सीरम एसीटेट के स्तर में वृद्धि से मस्तिष्क सहित कई ऊतकों में एडेनोसिन का संचय होता है, और एडेनोसाइन रिसेप्टर प्रतिपक्षी कैफीन को चूहों के लिए प्रशासित के बाद इथेनॉल को नोसिसेप्टिव व्यवहार को कम करने के लिए पाया गया था।[7][8]
एसीटेट ने इम्यूनोमॉड्यूलेटरी गुणों को जाना जाता है और रोगजनक जीवाणु बैक्टीरिया जैसे श्वसन रोगज़नक़ हीमोफिलस इन्फ्लुएंजा के जन्मजात प्रतिरक्षा प्रणाली की प्रतिक्रिया को प्रभावित कर सकता है।[9]
किण्वन एसिटाइल CoA से एसीटेट
पाइरूवेट को एंजाइम पाइरूवेट डिहाइड्रोजनेज द्वारा एसिटाइल-कोएंजाइम A (एसिटाइल-CoA) में परिवर्तित किया जाता है। यह एसिटाइल-CoA तब ई. कोलाई में एसीटेट में परिवर्तित हो जाता है, जबकि सब्सट्रेट-स्तर फास्फारिलीकरण द्वारा एटीपी का उत्पादन होता है। एसीटेट के निर्माण के लिए दो एंजाइमों की आवश्यकता होती है फॉस्फेट एसिटाइलट्रांसफेरेज़ और एसीटेट किनेज।[10]

acetyl-CoA + phosphate → acetyl-phosphate + CoA
acetyl-phosphate + ADP → acetate + ATP
एसीटेट का किण्वन
मीथेन और कार्बन डाईऑक्साइड का उत्पादन करने के लिए एसिटिक एसिड भी विघटन प्रतिक्रिया से गुजर सकता है:[11][12]
- CH3COO− + H+ → CH4 + CO2 ΔG° = −36 किलोग्राम/मोल
यह असमानुपातन प्रतिक्रिया उनके किण्वक चयापचय में मेथनोजेन आर्किया द्वारा उत्प्रेरित होती है। इलेक्ट्रॉन को कार्बोनिल फ़ंक्शन (इलेक्ट्रॉन दाता (e− दाता) कार्बोक्जिलिक समूह से मिथाइल समूह (ई-स्वीकर्ता) में क्रमशः CO2 और मीथेन गैस का उत्पादन करने के लिए स्थानांतरित किया जाता है।
संरचनाएं
- Space-filling model of the acetate anion
- resonance hybrid of the acetate anion
- canonical forms of the acetate anion
यह भी देखें
- एसिटिलीकरण
- सेलूलोज एसीटेट
- कॉपर (द्वितीय) एसीटेट
- किण्वन (जैव रसायन)
- नाजिया
- मिश्रित एसिड किण्वन
- एसीटिक अम्ल
- एसिटाइल क्लोराइड
- जिंक एसीटेट
संदर्भ
- ↑ 1.0 1.1 Zumdahl, S. S. “Chemistry” Heath, 1986: Lexington, MA. ISBN 0-669-04529-2.
- ↑ International Union of Pure and Applied Chemistry (2005). Nomenclature of Inorganic Chemistry (IUPAC Recommendations 2005). Cambridge (UK): RSC–IUPAC. ISBN 0-85404-438-8. p. 63. Electronic version.
- ↑ Brimble, Margaret A.; Black, David StC.; Hartshorn, Richard; Rauter, Amélia P.; Sha, Chin-Kang; Sydnes, Leiv K. (10 November 2012). "सुरक्षा समूहों (आईयूपीएसी तकनीकी रिपोर्ट) के संक्षेप के नियम". Pure and Applied Chemistry. 85 (1): 310. doi:10.1351/PAC-REP-12-07-12. S2CID 55102299.
- ↑ R-9.1 Trivial and semisystematic names retained for naming organic compounds Archived 2014-02-08 at the Wayback Machine, A Guide to IUPAC Nomenclature of Organic Compounds, IUPAC Commission on Nomenclature of Organic Chemistry
- ↑ 5.0 5.1 Hosea Cheung, Robin S. Tanke, G. Paul Torrence "Acetic acid" in Ullmann's Encyclopedia of Industrial Chemistry Weinheim, Germany: Wiley-VCH, 2005. doi:10.1002/14356007.a01_045
- ↑ Nelson, D. L.; Cox, M. M. "Lehninger, Principles of Biochemistry" 3rd Ed. Worth Publishing: New York, 2000. ISBN 1-57259-153-6.
- ↑ Maxwell, Christina; et al. (2010). "चूहों में एसीटेट अल्कोहल हैंगओवर सिरदर्द का कारण बनता है". PLOS ONE. 5 (12): e15963. Bibcode:2010PLoSO...515963M. doi:10.1371/journal.pone.0015963. PMC 3013144. PMID 21209842.
- ↑ 'Is coffee the real cure for a hangover?' by Bob Holmes, New Scientist, Jan. 15 2011, p. 17.
- ↑ Hosmer, Jennifer; Nasreen, Marufa; Dhouib, Rabeb; Essilfie, Ama-Tawiah; Schirra, Horst Joachim; Henningham, Anna; Fantino, Emmanuelle; Sly, Peter; McEwan, Alastair G.; Kappler, Ulrike (2022-01-27). "अत्यधिक विशिष्ट विकास सबस्ट्रेट्स तक पहुंच और उपकला इम्यूनोमॉड्यूलेटरी मेटाबोलाइट्स का उत्पादन मानव वायुमार्ग उपकला कोशिकाओं में हीमोफिलस इन्फ्लुएंजा के अस्तित्व को निर्धारित करता है". PLOS Pathogens (in English). 18 (1): e1010209. doi:10.1371/journal.ppat.1010209. ISSN 1553-7374. PMC 8794153. PMID 35085362.
- ↑ Keseler, Ingrid M.; et al. (2011). "EcoCyc: a comprehensive database of Escherichia coli biology". Nucleic Acids Research. 39 (Database issue): D583–D590. doi:10.1093/nar/gkq1143. PMC 3013716. PMID 21097882.
- ↑ Ferry, J.G. (1992). "एसीटेट से मीथेन". Journal of Bacteriology. 174 (17): 5489–5495. doi:10.1128/jb.174.17.5489-5495.1992. PMC 206491. PMID 1512186.
- ↑ Vogels, G. D.; Keltjens, J. T.; Van Der Drift, C. (1988). "Biochemistry of methane production". In Zehnder A.J.B. (ed.). अवायवीय सूक्ष्मजीवों की जीवविज्ञान. New York: Wiley. pp. 707–770.