रासायनिक यौगिक: Difference between revisions
m (→परिभाषाएं) |
No edit summary |
||
| Line 11: | Line 11: | ||
चार प्रमुख प्रकार के यौगिक हैं, जो इस बात से पहचाने जाते हैं कि घटक परमाणु एक साथ कैसे बंधे हैं। [[ आणविक यौगिक |आणविक यौगिक]] एक साथ सहसंयोजक बंधों द्वारा जुड़े होते हैं; [[ आयनिक यौगिक |आयनिक]] [[ आणविक यौगिक |यौगिक]] [[ आयनिक यौगिक |आयनिक]] बंध द्वारा एक साथ जुड़े होते है; धातु बंधन द्वारा [[ इंटरमेटेलिक यौगिक |अंतरधात्विक यौगिकों]] को एक साथ रखा जाता है;[[ समन्वय परिसर | उपसहसंयोजक संकुल]] को उपसहसंयोजक सहसंयोजक बंधों द्वारा एक साथ रखा जाता है। [[ गैर-स्टोइकोमेट्रिक यौगिक |गैर-स्टोइकोमेट्रिक यौगिक]] एक विवादित सीमांत मामला बनाते हैं। | चार प्रमुख प्रकार के यौगिक हैं, जो इस बात से पहचाने जाते हैं कि घटक परमाणु एक साथ कैसे बंधे हैं। [[ आणविक यौगिक |आणविक यौगिक]] एक साथ सहसंयोजक बंधों द्वारा जुड़े होते हैं; [[ आयनिक यौगिक |आयनिक]] [[ आणविक यौगिक |यौगिक]] [[ आयनिक यौगिक |आयनिक]] बंध द्वारा एक साथ जुड़े होते है; धातु बंधन द्वारा [[ इंटरमेटेलिक यौगिक |अंतरधात्विक यौगिकों]] को एक साथ रखा जाता है;[[ समन्वय परिसर | उपसहसंयोजक संकुल]] को उपसहसंयोजक सहसंयोजक बंधों द्वारा एक साथ रखा जाता है। [[ गैर-स्टोइकोमेट्रिक यौगिक |गैर-स्टोइकोमेट्रिक यौगिक]] एक विवादित सीमांत मामला बनाते हैं। | ||
एक [[ रासायनिक सूत्र |रासायनिक सूत्र]] संख्यात्मक[[ सबस्क्रिप्ट ]]के साथ मानक [[ रासायनिक प्रतीक |रासायनिक प्रतीक]] का उपयोग करते हुए, एक यौगिक अणु में प्रत्येक तत्व के परमाणुओं की संख्या निर्दिष्ट करता है। कई रासायनिक यौगिकों में रासायनिक सार सेवा द्वारा निर्दिष्ट एक विशिष्ट [[ सीएएस संख्या |सीएएस संख्या(CAS)]] होता है। विश्व स्तर पर, 350,000 से अधिक रासायनिक यौगिकों (रसायनों के मिश्रण सहित) को उत्पादन और उपयोग के लिए पंजीकृत किया गया है।<ref>{{Cite journal|last1=Wang|first1=Zhanyun|last2=Walker|first2=Glen W.|last3=Muir|first3=Derek C. G.|last4=Nagatani-Yoshida|first4=Kakuko|date=2020-01-22|title=रासायनिक प्रदूषण की वैश्विक समझ की ओर: राष्ट्रीय और क्षेत्रीय रासायनिक सूची का पहला व्यापक विश्लेषण|journal=[[Environmental Science & Technology]]|volume=54|issue=5|pages=2575–2584|doi=10.1021/acs.est.9b06379|pmid=31968937|bibcode=2020EnST...54.2575W|doi-access=free}}</ref> | एक [[ रासायनिक सूत्र |रासायनिक सूत्र]] संख्यात्मक[[ सबस्क्रिप्ट ]]के साथ मानक [[ रासायनिक प्रतीक |रासायनिक प्रतीक]] का उपयोग करते हुए, एक यौगिक अणु में प्रत्येक तत्व के परमाणुओं की संख्या निर्दिष्ट करता है। कई रासायनिक यौगिकों में रासायनिक सार सेवा द्वारा निर्दिष्ट एक विशिष्ट [[ सीएएस संख्या |सीएएस संख्या(CAS)]] होता है। विश्व स्तर पर, 350,000 से अधिक रासायनिक यौगिकों(रसायनों के मिश्रण सहित) को उत्पादन और उपयोग के लिए पंजीकृत किया गया है।<ref>{{Cite journal|last1=Wang|first1=Zhanyun|last2=Walker|first2=Glen W.|last3=Muir|first3=Derek C. G.|last4=Nagatani-Yoshida|first4=Kakuko|date=2020-01-22|title=रासायनिक प्रदूषण की वैश्विक समझ की ओर: राष्ट्रीय और क्षेत्रीय रासायनिक सूची का पहला व्यापक विश्लेषण|journal=[[Environmental Science & Technology]]|volume=54|issue=5|pages=2575–2584|doi=10.1021/acs.est.9b06379|pmid=31968937|bibcode=2020EnST...54.2575W|doi-access=free}}</ref> | ||
Revision as of 15:06, 22 November 2022
रासायनिक यौगिक एक रासायनिक पदार्थ है जो कई समान अणुओं (या आणविक इकाई) से बना होता है जिसमें रासायनिक बंधों द्वारा एक से अधिक रासायनिक तत्वों के परमाणु होते हैं। इसलिए होमोन्यूक्लियर अणु एक यौगिक नहीं है। एक रासायनिक अभिक्रिया द्वारा एक यौगिक को अलग पदार्थ में परिवर्तित किया जा सकता है, जिसमें अन्य पदार्थों के साथ परस्पर अभिक्रिया शामिल हो सकती है। इस प्रक्रिया में, परमाणुओं के बीच के बंध टूटते हैं और नए बंध बनते हैं।
चार प्रमुख प्रकार के यौगिक हैं, जो इस बात से पहचाने जाते हैं कि घटक परमाणु एक साथ कैसे बंधे हैं। आणविक यौगिक एक साथ सहसंयोजक बंधों द्वारा जुड़े होते हैं; आयनिक यौगिक आयनिक बंध द्वारा एक साथ जुड़े होते है; धातु बंधन द्वारा अंतरधात्विक यौगिकों को एक साथ रखा जाता है; उपसहसंयोजक संकुल को उपसहसंयोजक सहसंयोजक बंधों द्वारा एक साथ रखा जाता है। गैर-स्टोइकोमेट्रिक यौगिक एक विवादित सीमांत मामला बनाते हैं।
एक रासायनिक सूत्र संख्यात्मकसबस्क्रिप्ट के साथ मानक रासायनिक प्रतीक का उपयोग करते हुए, एक यौगिक अणु में प्रत्येक तत्व के परमाणुओं की संख्या निर्दिष्ट करता है। कई रासायनिक यौगिकों में रासायनिक सार सेवा द्वारा निर्दिष्ट एक विशिष्ट सीएएस संख्या(CAS) होता है। विश्व स्तर पर, 350,000 से अधिक रासायनिक यौगिकों(रसायनों के मिश्रण सहित) को उत्पादन और उपयोग के लिए पंजीकृत किया गया है।[1]
परिभाषाएं
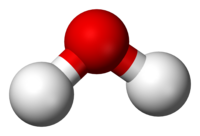
एक निश्चित स्टोइकोमेट्रिक अनुपात में दो या दो से अधिक विभिन्न प्रकार के परमाणुओं (रासायनिक तत्वों) से युक्त किसी भी पदार्थ को रासायनिक यौगिक कहा जा सकता है; शुद्ध रासायनिक पदार्थों पर विचार करते समय इस अवधारणा को सबसे आसानी से समझा जाता है।[2]: 15 [3][4] यह उनके दो या दो से अधिक प्रकार के परमाणुओं के निश्चित अनुपात से बना होने के कारण होता है, रासायनिक यौगिकों को रासायनिक अभिक्रिया के माध्यम से यौगिकों या पदार्थों में परिवर्तित किया जा सकता है जिनमें से प्रत्येक में कम परमाणु होते हैं।[5] एक रासायनिक सूत्र, परमाणुओं के बारे में जानकारी व्यक्त करने का एक तरीका है जो एक विशेष रासायनिक यौगिक का गठन करता है, रासायनिक सूत्र रासायनिक तत्वों के लिए रासायनिक प्रतीकों का उपयोग करता है, और शामिल परमाणुओं की संख्या को इंगित करने के लिए सबस्क्रिप्ट करता है। उदाहरण के लिए, जल एक ऑक्सीजन परमाणु से बंधे दो हाइड्रोजन परमाणुओं से बना होता है: रासायनिक सूत्र H2O है। गैर-स्टोइकोमेट्रिक यौगिकों के मामले में, यह अनुपात उनकी तैयारी के संबंध में पुनरुत्पादित हो सकते हैं, और उनके घटक तत्वों को निश्चित अनुपात दे सकते हैं, लेकिन यह अनुपात अभिन्न नहीं हैं [उदाहरण के लिए, पैलेडियम हाइड्राइड, PdHx (0.02 < x < 0.58)]।[6]
रासायनिक यौगिकों में एक विशिष्ट और स्पष्ट रासायनिक संरचना होती है जो त्रिविम व्यवस्था में रासायनिक बंधों द्वारा एक साथ जुडी होती है। रासायनिक यौगिक सहसंयोजक बंधों द्वारा एक साथ रखे गए आण्विक यौगिक हो सकते हैं, लवण के अणुओं में आयनिक बंध होता है, अंतरधात्विक यौगिक धात्विक बंधों द्वारा आपस में जुड़े रहते हैं, या उपसहसंयोजक संकुल बनाने वाले अणुओं में उपसहसंयोजक बंध होता हैं।[7] शुद्ध रासायनिक तत्वों को आम तौर पर रासायनिक यौगिक नहीं माना जाता है, दो या दो से अधिक परमाणु से मिलकर अणु बनते हैं जैसे द्विपरमाणुक अणु H2 में या बहुपरमाणुक अणु S8, आदि।) से बने अणुओं से मिलकर बने होते हैं।[7] कई रासायनिक यौगिकों में रासायनिक सार सेवा (CAS) द्वारा निर्दिष्ट एक विशिष्ट संख्यात्मक पहचानकर्ता होता है: वह इसकी CAS संख्या कहलाती है।
अलग-अलग और कभी-कभी असंगत नामकरण वाले विभेदक पदार्थ होते हैं, जिनमें वास्तव में गैर-स्टोइकोमेट्रिक उदाहरण शामिल होते हैं, जिन्हें निश्चित अनुपात की आवश्यकता होती है। कई ठोस रासायनिक पदार्थ आते हैं -उदाहरण के लिए कई सिलिकेट खनिज -रासायनिक पदार्थ हैं, लेकिन उनके पास निश्चित अनुपात में तत्वों के रासायनिक रूप से एक दूसरे से के साथ बने बंध को दर्शाने वाले सरल सूत्र नहीं होते हैं; फिर भी, इन क्रिस्टल संरचना वाले पदार्थों को अक्सर गैर-स्टोइकोमेट्रिक यौगिक कहा जाता है। यह तर्क दिया जा सकता है कि, उनकी रचनाओं में परिवर्तनशीलता अक्सर या तो किसी अन्य ज्ञात वास्तविक रासायनिक यौगिक की क्रिस्टल संरचना के भीतर फंसे विदेशी तत्वों की उपस्थिति के कारण होती है, या इसकी संरचना में स्थानों पर घटक तत्वों की कमी के कारण उत्पन्न होने वाले ज्ञात यौगिक के सापेक्ष संरचना में गड़बड़ी के कारण इसलिए वे रासायनिक यौगिक होने के बजाय एक दूसरे से सम्बन्धित हैं। इस तरह के गैर-स्टोइकोमेट्रिक पदार्थ पृथ्वी के अधिकांश क्रस्ट (भूविज्ञान) और मेंटल (भूविज्ञान) का निर्माण करते हैं। रासायनिक रूप से समान माने जाने वाले अन्य यौगिकों में घटक तत्वों के भारी या हल्के समस्थानिकों की मात्रा भिन्न हो सकती है, जो तत्वों के द्रव्यमान के अनुपात को थोड़ा बदल देता है।
प्रकार
अणु
एक अणु दो या दो से अधिक विधुत उदासीन परमाणुओं का एक समूह है जो रासायनिक बंधों द्वारा एक साथ जुड़ा होता है।[8][9][10] एक अणु होमोन्यूक्लियर हो सकता है, अर्थात इसमें एक रासायनिक तत्व के परमाणु होते हैं, जैसे ऑक्सीजन अणु में दो परमाणु होते हैं (O2); या हेटेरोन्यूक्लियर हो सकता है, जिसमें एक रासायनिक यौगिक जो एक से अधिक तत्वों से बना होता है, जैसे कि जल (अणु) (दो हाइड्रोजन परमाणु और एक ऑक्सीजन परमाणु; H2O)। अणु किसी पदार्थ की सबसे छोटी इकाई है जिसमे उस पदार्थ के सभी भौतिक और रासायनिक गुण होते हैं।[11]
आयनिक यौगिक
एक आयनिक यौगिक एक रासायनिक यौगिक है जिसमें आयन आपस में विद्युत आकर्षण बल द्वारा आपस में जुड़े होते हैं इसे आयनिक बंध कहा जाता है। यौगिक समग्र रूप से विद्युत उदासीन होता है, लेकिन इसमें आयन धनावेशित होते हैं जिन्हें धनायन कहा जाता है और ऋणात्मक रूप से आवेशित आयन को ऋणायन कहा जाता है। ये साधारण आयन हो सकते हैं जैसे सोडियम क्लोराइड मेंसोडियम (Na+) और क्लोराइड (Cl−), या पॉलीऐटोमिक आयन प्रजातियों जैसे अमोनियम कार्बोनेट में अमोनियम आयन (NH+
4) और कार्बोनेट (CO2−
3) आयन। आमतौर पर एक क्रिस्टलीय संरचना के एक आयनिक यौगिक में व्यक्तिगत आयनों के साथ-साथ आमतौर पर कई निकटतम पड़ोसी आयन भी होते हैं, इसलिए उन्हें अणुओं का हिस्सा नहीं माना जाता है, बल्कि एक निरंतर त्रि-आयामी नेटवर्क का हिस्सा माना जाता है।
आयनिक यौगिक युक्त क्षारीय आयन हाइड्रॉक्साइड (OH−) या ऑक्साइड (O2−) को क्षारों के रूप में वर्गीकृत किया गया है। इन आयनों के बिना आयनिक यौगिकों को लवण (रसायन विज्ञान) के रूप में भी जाना जाता है और ये लवण अम्ल और क्षार की आपस में अभिक्रिया करके प्राप्त होते हैं। आयनिक यौगिकों को उनकेविलायक के वाष्पीकरण, अवक्षेपण, हिमीकरण, एक ठोस अवस्था अभिक्रिया, या अभिक्रिया शील अधातुओं के साथ अभिक्रिया शील धातुओं की इलेक्ट्रॉन स्थानांतरण अभिक्रिया केवाष्पीकरण द्वारा उनके घटक आयनों से भी उत्पादित किया जा सकता है। जैसे हैलोजन गैसें।
आयनिक यौगिकों में आमतौर पर उच्च गलनांक और क्वथनांक होते हैं, और इनमें कठोरता और भंगुरता होती हैं। ठोस के रूप में वे लगभग हमेशा इन्सुलेटर होते हैं, लेकिन पिघलने या विघटन (रसायन विज्ञान) में वे अत्यधिक विद्युत प्रतिरोधकता और चालकता प्रदर्शित करते हैं, क्योंकि आयन गतिशील हो जाते हैं।
अंतरधात्विक यौगिक
एक अंतरधात्विक यौगिक एक प्रकार कामिश्र धातु है जो दो या दो से अधिक धातु तत्वों के बीच एक ठोस-अवस्था वाला यौगिक बनाता है। अंतरधात्विक आमतौर पर दृढ़ और भंगुर होते हैं, जिनमें अच्छे उच्च तापमान वाले यांत्रिक गुण होते हैं।[12][13][14] उन्हें स्टोइकोमेट्रिक या नॉनस्टोइकोमेट्रिक अंतरधात्विक यौगिकों के रूप में वर्गीकृत किया जा सकता है।[12]
संकुल
एक उपसहसंयोजक संकुल में एक केंद्रीय परमाणु या आयन होता है, जो आमतौर पर धात्विक होता है और इसे उपसहसंयोजक केंद्र कहा जाता है, और वह अपने आस पास अणुओं या आयनों से बंध बनाता है, जिसेलिगैंड या कॉम्प्लेक्सिंग एजेंट के रूप में जाना जाता है।[15][16][17] कई धातु युक्त यौगिक, विशेष रूप से संक्रमण धातुओं से बने हुए यौगिक, उपसहसंयोजक संकुल हैं।[18] एक उपसहसंयोजक संकुल जिसका केंद्र एक धातु परमाणु होता है उसे d ब्लॉक तत्व का धातु संकुल कहा जाता है।
बंध और बल
विभिन्न प्रकार के बंध और बलों के आधार पर यौगिकों को एक साथ रखा जाता है। यौगिकों को दो प्रकार में बांटा गया है एक यौगिकों में उपस्थित बंध के प्रकार के आधार पर और दूसरा अंतर यौगिक में मौजूद तत्वों के प्रकार के आधार पर।
लंदन परिक्षेपण बल सभी अंतर-आणविक बलों में से सबसे कमजोर बल है। वे अस्थायी आकर्षक बल हैं जो तब बनते हैं जब दो आसन्न परमाणुओं को इस प्रकार तैनात किया जाता है की वे एक अस्थायी द्विध्रुव बना सकें। इसके अतिरिक्त, लंदन परिक्षेपण बल रासायनिक ध्रुवता वाले पदार्थों को तरल पदार्थ में संघनित करने के लिए और पर्यावरण के तापमान के कम होने पर एक ठोस अवस्था में जमने के लिए जिम्मेदार हैं।[19] एक सहसंयोजक बंध, जिसे आणविक बंध के रूप में भी जाना जाता है, ये दो परमाणुओं के बीच इलेक्ट्रॉनों की साझेदारी द्वारा बनते हैं। मुख्य रूप से, इस प्रकार का बंध उन तत्वों के बीच होता है जो तत्व आवर्त सारणी में एक दूसरे के करीब होते हैं, यह कुछ धातुओं और अधातुओं के बीच में होते हैं। यह इस प्रकार के बंध की क्रियाविधि के कारण होता है। आवर्त सारणी पर एक दूसरे के करीब मौजूद तत्वों की वैद्युतीयऋणात्मकता समान होती है, जिसका अर्थ है कि उनमें इलेक्ट्रॉन बंधुता भी समान है। चूंकि किसी भी तत्व में इलेक्ट्रॉनों को दान करने या प्राप्त करने के लिए एक प्रबल इलेक्ट्रॉन बंधुता नहीं है, यह तत्वों में इलेक्ट्रॉनों के साझा करने से बनता है, इसलिए दोनों तत्वों में अधिक स्थायी अष्टक नियम होता है।
आयनिक बंध तब होता है जब संयोजी इलेक्ट्रॉनों को तत्वों के बीच पूरी तरह से स्थानांतरित कर दिया जाता है। सहसंयोजक बंध के विपरीत, यह रासायनिक बंध दो विपरीत आवेशित आयन बनाता है। आयनिक बंध में धातुएं आमतौर पर अपने संयोजी इलेक्ट्रॉनों को खो देती हैं, एक धनात्मक आवेशित आयन से धनायन बन जाता है। अधातु धातु से इलेक्ट्रॉनों को प्राप्त करेगा, जिससे अधातु ऋणात्मक आवेशित आयन बन जाएगा। जैसा कि उल्लिखित है, आमतौर परआयनिक बंध एक इलेक्ट्रॉन दाता एक धातु और एक इलेक्ट्रॉन स्वीकर्ता के बीच होते हैं, जो एक अधातु होता है।[20] यह तब होता है जब एक विद्युत ऋणात्मक परमाणु से जुड़ा हाइड्रोजन परमाणु दूसरे विद्युत ऋणात्मक परमाणु के साथ अंतःक्रियात्मक द्विध्रुव या आवेश के माध्यम से इलेक्ट्रोस्टैटिक कनेक्शन बनाता है तब इस प्रकार बने बंध को हाइड्रोजन बंध कहते हैं।[21][22][23]
अभिक्रियाएँ
रासायनिक अभिक्रिया के माध्यम से एक रासायनिक यौगिक को दूसरे रासायनिक यौगिक के साथ परस्पर क्रिया करके एक अलग रासायनिक संघटन में परिवर्तित किया जा सकता है। इस प्रक्रिया में, दोनों परस्पर क्रिया करने वाले यौगिकों में परमाणुओं के बीच के बंध टूट जाते हैं, और फिर दूसरे बंध बनते हैं ताकि परमाणुओं के बीच नए बंध बन सकें और नया यौगिक प्राप्त हो सके, इस अभिक्रिया को इस प्रकार वर्णित किया जा सकता है AB + CD → AD + CB, जहां A, B, C और D प्रत्येक विशिष्टपरमाणु हैं; और AB, AD, CD और CB प्रत्येक विशिष्ट यौगिक हैं।
यह भी देखें
- रासायनिक संरचना
- IUPAC नामकरण
- रासायनिक सूत्रों का शब्दकोश
- यौगिकों की सूची
संदर्भ
- ↑ Wang, Zhanyun; Walker, Glen W.; Muir, Derek C. G.; Nagatani-Yoshida, Kakuko (2020-01-22). "रासायनिक प्रदूषण की वैश्विक समझ की ओर: राष्ट्रीय और क्षेत्रीय रासायनिक सूची का पहला व्यापक विश्लेषण". Environmental Science & Technology. 54 (5): 2575–2584. Bibcode:2020EnST...54.2575W. doi:10.1021/acs.est.9b06379. PMID 31968937.
- ↑ Whitten, Kenneth W.; Davis, Raymond E.; Peck, M. Larry (2000), General Chemistry (6th ed.), Fort Worth, TX: Saunders College Publishing/Harcourt College Publishers, ISBN 978-0-03-072373-5
- ↑ Brown, Theodore L.; LeMay, H. Eugene; Bursten, Bruce E.; Murphy, Catherine J.; Woodward, Patrick (2013), Chemistry: The Central Science (3rd ed.), Frenchs Forest, NSW: Pearson/Prentice Hall, pp. 5–6, ISBN 9781442559462, archived from the original on 2021-05-31, retrieved 2020-12-08
- ↑ Hill, John W.; Petrucci, Ralph H.; McCreary, Terry W.; Perry, Scott S. (2005), General Chemistry (4th ed.), Upper Saddle River, NJ: Pearson/Prentice Hall, p. 6, ISBN 978-0-13-140283-6, archived from the original on 2009-03-22
- ↑ Wilbraham, Antony; Matta, Michael; Staley, Dennis; Waterman, Edward (2002), Chemistry (1st ed.), Upper Saddle River, NJ: Pearson/Prentice Hall, p. 36, ISBN 978-0-13-251210-7
- ↑ Manchester, F. D.; San-Martin, A.; Pitre, J. M. (1994). "एच-पीडी (हाइड्रोजन-पैलेडियम) प्रणाली". Journal of Phase Equilibria. 15: 62–83. doi:10.1007/BF02667685. S2CID 95343702. Phase diagram for Palladium-Hydrogen System
- ↑ 7.0 7.1 Atkins, Peter; Jones, Loretta (2004). रासायनिक सिद्धांत: अंतर्दृष्टि की खोज. W.H. Freeman. ISBN 978-0-7167-5701-6.
- ↑ IUPAC, Compendium of Chemical Terminology, 2nd ed. (the "Gold Book") (1997). Online corrected version: (2006–) "Molecule". doi:10.1351/goldbook.M04002
- ↑ Ebbin, Darrell D. (1990). सामान्य रसायन शास्त्र (3rd ed.). Boston: Houghton Mifflin Co. ISBN 978-0-395-43302-7.
- ↑ Brown, T.L.; Kenneth C. Kemp; Theodore L. Brown; Harold Eugene LeMay; Bruce Edward Bursten (2003). रसायन विज्ञान - केंद्रीय विज्ञान (9th ed.). New Jersey: Prentice Hall. ISBN 978-0-13-066997-1.
- ↑ "अणु की परिभाषा - NCI कैंसर शब्दों का शब्दकोश - NCI". www.cancer.gov (in English). 2011-02-02. Retrieved 2022-08-26.
- ↑ 12.0 12.1 Askeland, Donald R.; Wright, Wendelin J. (January 2015). "11-2 Intermetallic Compounds". सामग्री का विज्ञान और इंजीनियरिंग (Seventh ed.). Boston, MA. pp. 387–389. ISBN 978-1-305-07676-1. OCLC 903959750. Archived from the original on 2021-05-31. Retrieved 2020-11-10.
{{cite book}}: CS1 maint: location missing publisher (link) - ↑ Panel On Intermetallic Alloy Development, Commission On Engineering And Technical Systems (1997). इंटरमेटेलिक मिश्र धातु विकास: एक कार्यक्रम मूल्यांकन. National Academies Press. p. 10. ISBN 0-309-52438-5. OCLC 906692179. Archived from the original on 2021-05-31. Retrieved 2020-11-10.
- ↑ Soboyejo, W. O. (2003). "1.4.3 Intermetallics". इंजीनियर सामग्री के यांत्रिक गुण. Marcel Dekker. ISBN 0-8247-8900-8. OCLC 300921090. Archived from the original on 2021-05-31. Retrieved 2020-11-10.
- ↑ Lawrance, Geoffrey A. (2010). समन्वय रसायन विज्ञान का परिचय. Wiley. doi:10.1002/9780470687123. ISBN 9780470687123.
- ↑ IUPAC, Compendium of Chemical Terminology, 2nd ed. (the "Gold Book") (1997). Online corrected version: (2006–) "complex". doi:10.1351/goldbook.C01203
- ↑ IUPAC, Compendium of Chemical Terminology, 2nd ed. (the "Gold Book") (1997). Online corrected version: (2006–) "coordination entity". doi:10.1351/goldbook.C01330
- ↑ Greenwood, Norman N.; Earnshaw, Alan (1997). Chemistry of the Elements (2nd ed.). Butterworth-Heinemann. ISBN 978-0-08-037941-8.
- ↑ "लंदन फैलाव बल". www.chem.purdue.edu. Archived from the original on 2017-01-13. Retrieved 2017-09-13.
- ↑ "आयनिक और सहसंयोजक बंधन". Chemistry LibreTexts (in English). 2013-10-02. Archived from the original on 2017-09-13. Retrieved 2017-09-13.
- ↑ IUPAC, Compendium of Chemical Terminology, 2nd ed. (the "Gold Book") (1997). Online corrected version: (2006–) "hydrogen bond". doi:10.1351/goldbook.H02899
- ↑ "हाइड्रोजन बंध". www.chem.purdue.edu. Archived from the original on 2011-08-08. Retrieved 2017-10-28.
- ↑ "इंटरमॉलिक्युलर बॉन्डिंग - हाइड्रोजन बॉन्ड". www.chemguide.co.uk. Archived from the original on 2016-12-19. Retrieved 2017-10-28.
अग्रिम पठन
- Robert Siegfried (2002), From elements to atoms: a history of chemical composition, American Philosophical Society, ISBN 978-0-87169-924-4