वृत्तीय द्विवर्णता
वृत्ताकार द्वैतवाद (CD) द्वैतवाद है जिसमें वृत्ताकार ध्रुवीकरण प्रकाश, यानी बाएँ और दाएँ हाथ के प्रकाश का विभेदक अवशोषण (विद्युत चुम्बकीय विकिरण) शामिल है।[1][2] बाएँ हाथ का वृत्ताकार (LHC) और दाएँ हाथ का वृत्ताकार (RHC) ध्रुवीकृत प्रकाश एक फोटॉन के लिए प्रकाश अवस्थाओं के दो संभावित स्पिन कोणीय गति का प्रतिनिधित्व करता है, और इसलिए वृत्ताकार द्वैतवाद को स्पिन कोणीय गति के लिए द्वैतवाद भी कहा जाता है।[3] इस घटना की खोज 19वीं सदी के पहले भाग में जीन-बैप्टिस्ट बायोट, ऑगस्टिन फ्रेस्नेल और ऐमे कॉटन ने की थी।[4] वृत्ताकार द्वैतवाद और ऑप्टिकल रोटेशन ऑप्टिकल गतिविधि की अभिव्यक्तियाँ हैं। यह ऑप्टिकल गतिविधि चिरलिटी (रसायन विज्ञान) अणुओं के अवशोषण (विद्युत चुम्बकीय विकिरण) में प्रदर्शित होता है। सीडी स्पेक्ट्रोस्कोपी में कई अलग-अलग क्षेत्रों में अनुप्रयोगों की एक विस्तृत श्रृंखला है। विशेष रूप से, पराबैंगनी सीडी का उपयोग प्रोटीन की द्वितीयक संरचना की जांच के लिए किया जाता है।[5] यूवी/विज़ सीडी का उपयोग चार्ज-ट्रांसफर कॉम्प्लेक्स | चार्ज-ट्रांसफर ट्रांजिशन की जांच के लिए किया जाता है।[6] निकट-अवरक्त सीडी का उपयोग संक्रमण धातु डी ऑर्बिटल → डी कक्षीय संक्रमणों की जांच करके आणविक संरचना और इलेक्ट्रॉनिक संरचना की जांच के लिए किया जाता है।[2]कंपन संबंधी वृत्ताकार द्वैतवाद, जो अवरक्त ऊर्जा क्षेत्र से प्रकाश का उपयोग करता है, का उपयोग छोटे कार्बनिक अणुओं और हाल ही में प्रोटीन और डीएनए के संरचनात्मक अध्ययन के लिए किया जाता है।[5]
भौतिक सिद्धांत
प्रकाश का वृत्ताकार ध्रुवीकरण
विद्युत चुम्बकीय विकिरण में एक विद्युत होता है और चुंबकीय क्षेत्र जो एक दूसरे से लम्बवत् और प्रसार दिशा में दोलन करता है,[7] एक अनुप्रस्थ तरंग। जबकि ध्रुवीकरण (तरंगें) प्रकाश तब होता है जब विद्युत क्षेत्र वेक्टर केवल एक विमान में दोलन करता है, गोलाकार ध्रुवीकृत प्रकाश तब होता है जब विद्युत क्षेत्र वेक्टर की दिशा इसके प्रसार की दिशा में घूमती है जबकि वेक्टर निरंतर परिमाण बनाए रखता है। अंतरिक्ष में एक बिंदु पर, गोलाकार ध्रुवीकृत-वेक्टर तरंग आवृत्ति की एक अवधि में एक चक्र का पता लगाएगा, इसलिए नाम। नीचे दिए गए दो चित्र एक समय में, कई स्थितियों के लिए रैखिक और गोलाकार ध्रुवीकृत प्रकाश के विद्युत क्षेत्र वैक्टर दिखाते हैं; गोलाकार ध्रुवीकृत इलेक्ट्रिक वेक्टर का प्लॉट प्रसार की दिशा में एक हेलिक्स बनाता है . प्रेक्षक की ओर प्रसार के साथ बाएं गोलाकार ध्रुवीकृत प्रकाश (LCP) के लिए, विद्युत वेक्टर दक्षिणावर्त घूमता है।[2]दाएं गोलाकार ध्रुवीकृत प्रकाश (RCP) के लिए, विद्युत वेक्टर दक्षिणावर्त घूमता है।
File:Linearly pol.png File:Circularly pol.png
पदार्थ के साथ गोलाकार ध्रुवीकृत प्रकाश की परस्पर क्रिया
जब गोलाकार रूप से ध्रुवीकृत प्रकाश एक अवशोषित वैकल्पिक रूप से सक्रिय माध्यम से गुजरता है, तो दाएं और बाएं ध्रुवीकरणों के बीच की गति भिन्न होती है () साथ ही साथ उनकी तरंग दैर्ध्य () और जिस सीमा तक वे अवशोषित होते हैं (). वृत्ताकार द्वैतवाद अंतर है .[5]एक प्रकाश किरण का विद्युत क्षेत्र अणु (विद्युत द्विध्रुव) के साथ परस्पर क्रिया करते समय आवेश के रैखिक विस्थापन का कारण बनता है, जबकि इसका चुंबकीय क्षेत्र आवेश के संचलन (चुंबकीय द्विध्रुव) का कारण बनता है। ये दो गति संयुक्त रूप से एक पेचदार गति में एक इलेक्ट्रॉन के उत्तेजना का कारण बनती हैं, जिसमें अनुवाद (भौतिकी) और ROTATION और उनके संबंधित ऑपरेटर (गणित) शामिल हैं। घूर्णी शक्ति के बीच प्रयोगात्मक रूप से निर्धारित संबंध एक नमूने की और द्वारा दिया गया है
घूर्णी शक्ति भी सैद्धांतिक रूप से निर्धारित की गई है,
हम इन दो समीकरणों से देखते हैं कि गैर-शून्य होने के लिए विद्युत और चुंबकीय द्विध्रुव आघूर्ण संचालक ( और ) समान समूह सिद्धांत के रूप में परिवर्तित होना चाहिए। और केवल बिंदु समूह हैं जहां यह हो सकता है, जिससे केवल चिरल अणु सीडी सक्रिय हो जाते हैं।
सीधे शब्दों में कहें, चूंकि गोलाकार रूप से ध्रुवीकृत प्रकाश स्वयं चिराल है, यह चिरायता (रसायन विज्ञान) के साथ अलग तरह से संपर्क करता है। अर्थात्, दो प्रकार के गोलाकार ध्रुवीकृत प्रकाश अलग-अलग सीमा तक अवशोषित होते हैं। एक सीडी प्रयोग में, एक चयनित तरंग दैर्ध्य के बाएँ और दाएँ गोलाकार ध्रुवीकृत प्रकाश की समान मात्रा को वैकल्पिक रूप से एक (चिरल) नमूने में विकीर्ण किया जाता है। दो ध्रुवीकरणों में से एक दूसरे की तुलना में अधिक अवशोषित होता है, और अवशोषण के इस तरंग दैर्ध्य-निर्भर अंतर को मापा जाता है, जिससे नमूने के सीडी स्पेक्ट्रम का उत्पादन होता है। अणु के साथ परस्पर क्रिया के कारण, प्रकाश का विद्युत क्षेत्र सदिश नमूने से गुजरने के बाद एक अण्डाकार पथ का पता लगाता है।
यह महत्वपूर्ण है कि अणु की चिरायता संरचनात्मक के बजाय गठनात्मक हो सकती है। उदाहरण के लिए, एक पेचदार प्रोटीन माध्यमिक संरचना वाले प्रोटीन अणु में एक सीडी हो सकती है जो रचना में परिवर्तन के साथ बदलती है।
डेल्टा अवशोषक
परिभाषा से,
कहाँ (डेल्टा अवशोषक) बाएं गोलाकार ध्रुवीकृत (LCP) और दाएं गोलाकार ध्रुवीकृत (RCP) प्रकाश के अवशोषण के बीच का अंतर है (यह आमतौर पर मापा जाता है)। तरंग दैर्ध्य का एक कार्य है, इसलिए माप के अर्थपूर्ण होने के लिए जिस तरंग दैर्ध्य पर यह किया गया था उसे ज्ञात होना चाहिए।
मोलर सर्कुलर डाइक्रोइज्म
इसे बीयर-लैंबर्ट कानून लागू करके भी व्यक्त किया जा सकता है। बीयर का कानून, इस प्रकार है:
कहाँ
- और LCP और RCP प्रकाश के लिए दाढ़ विलोपन गुणांक हैं,
- दाढ़ एकाग्रता है,
- सेंटीमीटर (सेमी) में पथ की लंबाई है।
तब
दाढ़ वृत्ताकार द्वैतवाद है। यह आंतरिक संपत्ति वह है जो आमतौर पर पदार्थ के वृत्ताकार द्वैतवाद से होती है। तब से तरंग दैर्ध्य का एक कार्य है, एक दाढ़ वृत्ताकार द्वैतवाद मान () तरंग दैर्ध्य निर्दिष्ट करना चाहिए जिस पर यह मान्य है।
परिपत्र द्वैतवाद पर बाहरी प्रभाव
वृत्ताकार द्वैतवाद (सीडी) के कई व्यावहारिक अनुप्रयोगों में, जैसा कि नीचे चर्चा की गई है, मापी गई सीडी केवल अणु की आंतरिक संपत्ति नहीं है, बल्कि आणविक रचना पर निर्भर करती है। ऐसे मामले में सीडी तापमान, एकाग्रता और सॉल्वैंट्स सहित रासायनिक वातावरण का एक कार्य भी हो सकता है। इस मामले में रिपोर्ट किए गए सीडी मूल्य को अर्थपूर्ण होने के लिए इन अन्य प्रासंगिक कारकों को भी निर्दिष्ट करना चाहिए।
दो गुना घूर्णी समरूपता, ऑप्टिकल गतिविधि की कमी वाली क्रमबद्ध संरचनाओं में,[8][9] अंतर संचरण सहित[10] (और प्रतिबिंब[11]) गोलाकार ध्रुवीकृत तरंगें सामग्री के माध्यम से प्रसार दिशा पर भी निर्भर करती हैं। इस मामले में, तथाकथित चिरलिटी (विद्युत चुंबकत्व) # एक्सट्रिंसिक 3 डी चिरायता प्रकाश किरण और संरचना के पारस्परिक अभिविन्यास से जुड़ी है।
मोलर अण्डाकारता
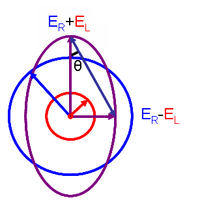
यद्यपि आमतौर पर मापा जाता है, ऐतिहासिक कारणों से अधिकांश माप अण्डाकारता की डिग्री में रिपोर्ट किए जाते हैं। दाढ़ अण्डाकारता एकाग्रता के लिए सही किया गया वृत्ताकार द्वैतवाद है। दाढ़ वृत्ताकार द्वैतवाद और दाढ़ अण्डाकारता, , समीकरण द्वारा आसानी से परस्पर परिवर्तित हो जाते हैं:
:
यह संबंध ध्रुवीकरण (तरंगों) को परिभाषित करके प्राप्त किया गया है:
कहाँ
- और क्रमशः दाएं-गोलाकार और बाएं-वृत्ताकार ध्रुवीकृत प्रकाश के विद्युत क्षेत्र वेक्टर (ज्यामिति) के परिमाण हैं।
कब के बराबर होती है (जब दाएं और बाएं गोलाकार ध्रुवीकृत प्रकाश के अवशोषण में कोई अंतर नहीं होता है), 0° है और प्रकाश रैखिक ध्रुवीकरण है। जब भी या शून्य के बराबर है (जब एक दिशा में गोलाकार ध्रुवीकृत प्रकाश का पूर्ण अवशोषण होता है), 45° है और प्रकाश वृत्ताकार ध्रुवीकरण है।
आम तौर पर, परिपत्र द्वैतवाद प्रभाव छोटा होता है, इसलिए छोटा है और अनुमानित किया जा सकता है कांति में। दीप्तिमान तीव्रता या विकिरण के बाद से, , प्रकाश का विद्युत-क्षेत्र वेक्टर के वर्ग के समानुपाती होता है, दीर्घवृत्त बन जाता है:
फिर बीयर-लैंबर्ट कानून का उपयोग करके I के लिए प्रतिस्थापन करके | प्राकृतिक लघुगणक रूप में बीयर का नियम:
दीर्घवृत्त को अब इस प्रकार लिखा जा सकता है:
तब से , टेलर श्रृंखला में घातीयों को पहले-क्रम में विस्तारित करके और फिर की शर्तों को छोड़कर इस अभिव्यक्ति का अनुमान लगाया जा सकता है एकता की तुलना में और रेडियन से डिग्री में बदलना:
दाढ़ अण्डाकारता को परिभाषित करके विलेय सांद्रता और पथ की लंबाई की रैखिक निर्भरता को हटा दिया जाता है,
फिर बीयर-लैंबर्ट कानून के साथ अंतिम दो अभिव्यक्ति का संयोजन | बीयर का नियम, दाढ़ दीर्घवृत्त बन जाता है:
मोलर अण्डाकारता की इकाइयाँ ऐतिहासिक रूप से (deg·cm2/dmol). दाढ़ अण्डाकारता की गणना करने के लिए, नमूना एकाग्रता (g/L), कोशिका पथ-लम्बाई (cm), और आणविक भार (g/mol) ज्ञात होना चाहिए।
यदि नमूना एक प्रोटीन है, तो औसत अवशेष भार (अमीनो एसिड अवशेषों का औसत आणविक भार) अक्सर आणविक भार के स्थान पर उपयोग किया जाता है, अनिवार्य रूप से प्रोटीन को अमीनो एसिड के समाधान के रूप में माना जाता है। औसत अवशेष अण्डाकारता का उपयोग विभिन्न आणविक भार के प्रोटीन की सीडी की तुलना करने की सुविधा प्रदान करता है; प्रोटीन संरचना के अध्ययन में इस सामान्यीकृत सीडी का उपयोग महत्वपूर्ण है।
औसत अवशेष अण्डाकारता
विशेष रूप से पॉलिमर, प्रोटीन और पॉलीपेप्टाइड्स में द्वितीयक संरचना का अनुमान लगाने के तरीकों के लिए अक्सर आवश्यकता होती है कि मापी गई दाढ़ दीर्घवृत्तीयता स्पेक्ट्रम को सामान्यीकृत मान में परिवर्तित किया जाए, विशेष रूप से बहुलक लंबाई से स्वतंत्र मूल्य। इस प्रयोजन के लिए औसत अवशेष अण्डाकारता का उपयोग किया जाता है; यह केवल अणु में मोनोमर इकाइयों (अवशेषों) की संख्या से विभाजित अणु की मोलर अण्डाकारता है।
जैविक अणुओं के लिए आवेदन

निचला पैनल: CDSSTR एल्गोरिथम का उपयोग करके CD स्पेक्ट्रा से अनुमानित माध्यमिक संरचनाओं की सामग्री। एसडीएस समाधान में प्रोटीन अनियंत्रित संरचनाओं की बढ़ी हुई सामग्री और हेलिस सामग्री में कमी दिखाता है।[12]
सामान्य तौर पर, इस घटना को किसी ऑप्टिकल गतिविधि अणु के अवशोषण बैंड में प्रदर्शित किया जाएगा। एक परिणाम के रूप में, उनके dextrorotary और levorotary घटकों के कारण, जैविक अणुओं द्वारा वृत्ताकार द्वैतवाद का प्रदर्शन किया जाता है। इससे भी अधिक महत्वपूर्ण यह है कि एक द्वितीयक संरचना अपने संबंधित अणुओं को एक अलग सीडी भी प्रदान करेगी। इसलिए, प्रोटीन के [[अल्फा हेलिक्स]] और न्यूक्लिक एसिड के दोहरी कुंडली में सीडी वर्णक्रमीय हस्ताक्षर उनकी संरचनाओं के प्रतिनिधि हैं। एक प्रतिनिधि संरचनात्मक हस्ताक्षर देने के लिए सीडी की क्षमता इसे आधुनिक जैव रसायन में एक शक्तिशाली उपकरण बनाती है, जो कि अध्ययन के लगभग हर क्षेत्र में पाया जा सकता है।
सीडी ऑप्टिकल रोटेटरी फैलाव (ओआरडी) तकनीक से निकटता से संबंधित है, और इसे आमतौर पर अधिक उन्नत माना जाता है। सीडी को ब्याज के अणु के अवशोषण बैंड में या उसके पास मापा जाता है, जबकि ओआरडी को इन बैंडों से दूर मापा जा सकता है। डेटा विश्लेषण में सीडी का लाभ स्पष्ट है। संरचनात्मक तत्व अधिक स्पष्ट रूप से प्रतिष्ठित हैं क्योंकि उनके रिकॉर्ड किए गए बैंड विशेष तरंग दैर्ध्य पर व्यापक रूप से ओवरलैप नहीं होते हैं जैसा कि वे ओआरडी में करते हैं। सिद्धांत रूप में, इन दो वर्णक्रमीय मापों को एक अभिन्न परिवर्तन (क्रामर्स-क्रोनिग संबंध) के माध्यम से एक दूसरे में परिवर्तित किया जा सकता है, यदि माप में सभी अवशोषण शामिल हैं।
प्रोटीन के दूर-यूवी (पराबैंगनी) सीडी स्पेक्ट्रम उनकी माध्यमिक संरचना की महत्वपूर्ण विशेषताओं को प्रकट कर सकते हैं। सीडी स्पेक्ट्रा का आसानी से एक अणु के अंश का अनुमान लगाने के लिए उपयोग किया जा सकता है जो अल्फा-हेलिक्स संरचना, बीटा पत्रक संरचना, बीटा बारी संरचना, या कुछ अन्य (जैसे यादृच्छिक कॉइल) संरचना में है।[13][14][15][16] ये भिन्नात्मक असाइनमेंट प्रोटीन में हो सकने वाले संभावित द्वितीयक अनुरूपताओं पर महत्वपूर्ण बाधाएँ डालते हैं। सामान्य तौर पर, सीडी यह नहीं कह सकती है कि अणु के भीतर पाए जाने वाले अल्फा हेलिकॉप्टर कहाँ स्थित हैं या यहां तक कि पूरी तरह से भविष्यवाणी करते हैं कि कितने हैं। इसके बावजूद, सीडी एक मूल्यवान उपकरण है, विशेष रूप से रचना में परिवर्तन दिखाने के लिए। उदाहरण के लिए, यह अध्ययन करने के लिए इस्तेमाल किया जा सकता है कि अणु की द्वितीयक संरचना तापमान के कार्य के रूप में या विकृतीकरण एजेंटों की एकाग्रता के रूप में कैसे बदलती है, उदा। गुआनिडीन या यूरिया। इस तरह यह अणु के बारे में महत्वपूर्ण थर्मोडायनामिक जानकारी प्रकट कर सकता है (जैसे तापीय धारिता और विकृतीकरण की गिब्स मुक्त ऊर्जा) जिसे अन्यथा आसानी से प्राप्त नहीं किया जा सकता है। प्रोटीन का अध्ययन करने का प्रयास करने वाले किसी भी व्यक्ति को व्यापक और/या महंगे प्रयोग करने से पहले यह सत्यापित करने के लिए सीडी एक मूल्यवान उपकरण मिलेगा कि प्रोटीन अपनी मूल संरचना में है। इसके अलावा, प्रोटीन रसायन विज्ञान में सीडी स्पेक्ट्रोस्कोपी के कई अन्य उपयोग हैं जो अल्फा-हेलिक्स अंश अनुमान से संबंधित नहीं हैं। इसके अलावा, जैव अकार्बनिक इंटरफ़ेस अध्ययनों में सीडी स्पेक्ट्रोस्कोपी का उपयोग किया गया है। विशेष रूप से इसका उपयोग अभिकर्मक के साथ अनुमापन से पहले और बाद में एक इंजीनियर प्रोटीन की माध्यमिक संरचना में अंतर का विश्लेषण करने के लिए किया गया है।[17] निकट-यूवी सीडी स्पेक्ट्रम (>250 एनएम) प्रोटीन तृतीयक संरचना के बारे में जानकारी प्रदान करता है। 250–300 एनएम क्षेत्र में प्राप्त संकेत फेनिलएलनिन, टाइरोसिन, सिस्टीन (या एस-एस डाइसल्फ़ाइड बंधन) और ट्रिप्टोफैन एमिनो एसिड के अवशोषण, द्विध्रुवीय अभिविन्यास और आसपास के वातावरण की प्रकृति के कारण होते हैं। दूर-यूवी सीडी के विपरीत, निकट-यूवी सीडी स्पेक्ट्रम को किसी विशेष 3डी संरचना को नहीं सौंपा जा सकता है। बल्कि, निकट-यूवी सीडी स्पेक्ट्रा प्रोटीन में प्रोस्थेटिक समूहों की प्रकृति पर संरचनात्मक जानकारी प्रदान करते हैं, उदाहरण के लिए, हीमोग्लोबिन और साइटोक्रोम सी में हीम समूह।
दर्शनीय सीडी स्पेक्ट्रोस्कोपी धातु-प्रोटीन इंटरैक्शन का अध्ययन करने के लिए एक बहुत ही शक्तिशाली तकनीक है और अलग-अलग बैंड के रूप में व्यक्तिगत डी-डी इलेक्ट्रॉनिक संक्रमणों को हल कर सकती है। दृश्य प्रकाश क्षेत्र में सीडी स्पेक्ट्रा केवल तब उत्पन्न होता है जब एक धातु आयन चिरल वातावरण में होता है, इस प्रकार, समाधान में मुक्त धातु आयनों का पता नहीं चलता है। यह केवल प्रोटीन-बाध्य धातु को देखने का लाभ है, इसलिए पीएच निर्भरता और स्टोइकियोमेट्रीज आसानी से प्राप्त होते हैं। संक्रमण धातु आयन परिसरों में ऑप्टिकल गतिविधि को विन्यास, गठनात्मक और vicinal प्रभाव के लिए जिम्मेदार ठहराया गया है। क्लेवपटीनोंड और विल्स (2007) ने Cu के लिए दृश्यमान सीडी स्पेक्ट्रा की उपस्थिति की भविष्यवाणी करने के लिए अनुभवजन्य नियमों का एक सेट तैयार किया है।2+ और नि2+ हिस्टडीन और मेन-चेन समन्वय से जुड़े स्क्वायर-प्लानर कॉम्प्लेक्स।
सीडी एक्स - रे क्रिस्टलोग्राफी और प्रोटीन एनएमआर स्पेक्ट्रोस्कोपी की तुलना में कम विशिष्ट संरचनात्मक जानकारी देता है, उदाहरण के लिए, जो दोनों परमाणु संकल्प डेटा देते हैं। हालांकि, सीडी स्पेक्ट्रोस्कोपी एक त्वरित तरीका है जिसके लिए बड़ी मात्रा में प्रोटीन या व्यापक डेटा प्रोसेसिंग की आवश्यकता नहीं होती है। इस प्रकार सीडी का उपयोग बड़ी संख्या में विलायक स्थितियों, अलग-अलग तापमान, पीएच, लवणता और विभिन्न सहकारकों की उपस्थिति का सर्वेक्षण करने के लिए किया जा सकता है।
सीडी स्पेक्ट्रोस्कोपी आमतौर पर समाधान में प्रोटीन का अध्ययन करने के लिए प्रयोग किया जाता है, और इस प्रकार यह ठोस अवस्था का अध्ययन करने वाले तरीकों का पूरक होता है। यह भी एक सीमा है, जिसमें कई प्रोटीन अपने मूल राज्य में जैविक झिल्ली में एम्बेडेड होते हैं, और झिल्ली संरचनाओं वाले समाधान अक्सर जोरदार बिखरने वाले होते हैं। सीडी को कभी-कभी पतली फिल्मों में मापा जाता है।
टीआईओ जैसे अर्धचालक पदार्थों का उपयोग करके सीडी स्पेक्ट्रोस्कोपी भी की गई है2 तरंग दैर्ध्य की यूवी रेंज में बड़े संकेत प्राप्त करने के लिए, जहां जैव-अणुओं के लिए इलेक्ट्रॉनिक संक्रमण अक्सर होता है।[18]
प्रायोगिक सीमाएँ
This article needs additional citations for verification. (March 2010) (Learn how and when to remove this template message) |
सीडी का कार्बोहाइड्रेट में भी अध्ययन किया गया है, लेकिन स्पेक्ट्रम के वैक्यूम पराबैंगनी (वीयूवी) क्षेत्र (100-200 एनएम) में सीडी स्पेक्ट्रा के मापन से जुड़ी प्रयोगात्मक कठिनाइयों के कारण सीमित सफलता के साथ, जहां असंबद्ध कार्बोहाइड्रेट के संबंधित सीडी बैंड स्थित हैं। . वीयूवी क्षेत्र के ऊपर बैंड वाले प्रतिस्थापित कार्बोहाइड्रेट को सफलतापूर्वक मापा गया है।
सीडी का मापन इस तथ्य से भी जटिल है कि विशिष्ट जलीय बफर सिस्टम अक्सर उस सीमा में अवशोषित होते हैं जहां संरचनात्मक विशेषताएं गोलाकार ध्रुवीकृत प्रकाश अंतर अवशोषण प्रदर्शित करती हैं। फास्फेट , सल्फेट, कार्बोनेट और एसीटेट बफ़र आमतौर पर सीडी के साथ असंगत होते हैं जब तक कि अत्यधिक पतला नहीं किया जाता है उदा। 10-50 एमएम रेंज में। दूर-यूवी सीडी का प्रदर्शन करते समय टीआरआईएस बफर सिस्टम से पूरी तरह बचा जाना चाहिए। सीडी प्रयोगों के लिए उचित पीएच रेंज स्थापित करने के लिए अक्सर बोरेट और ओनियम यौगिकों का उपयोग किया जाता है। कुछ प्रयोगकर्ताओं ने क्लोराइड आयन के लिए फ्लोराइड को प्रतिस्थापित किया है क्योंकि फ्लोराइड सुदूर यूवी में कम अवशोषित करता है, और कुछ ने शुद्ध पानी में काम किया है। एक और, लगभग सार्वभौमिक, तकनीक है, सुदूर यूवी में काम करते समय छोटी पथ लंबाई कोशिकाओं का उपयोग करके विलायक अवशोषण को कम करना, इस काम में 0.1 मिमी पथ लंबाई असामान्य नहीं है।
जलीय प्रणालियों में मापने के अलावा, सीडी, विशेष रूप से दूर-यूवी सीडी, कार्बनिक सॉल्वैंट्स में मापा जा सकता है उदा। इथेनॉल, मेथनॉल, ट्राइफ्लोरोएथेनॉल (TFE)। उत्तरार्द्ध में प्रोटीन के संरचना निर्माण को प्रेरित करने का लाभ होता है, कुछ में बीटा-शीट्स को प्रेरित करता है और अन्य में अल्फा हेलिक्स, जो वे सामान्य जलीय परिस्थितियों में नहीं दिखाएंगे। अधिकांश सामान्य कार्बनिक सॉल्वैंट्स जैसे एसीटोनिट्रिल, टीएचएफ, क्लोरोफार्म , डाइक्लोरोमेथेन, हालांकि, दूर-यूवी सीडी के साथ असंगत हैं।
यह ध्यान देने योग्य हो सकता है कि द्वितीयक संरचना आकलन में प्रयुक्त प्रोटीन सीडी स्पेक्ट्रा अमीनो एसिड को जोड़ने वाले बंधन के बीच के π से π* कक्षीय अवशोषण से संबंधित हैं। ये अवशोषण बैंड आंशिक रूप से तथाकथित वैक्यूम पराबैंगनी # वैक्यूम यूवी (तरंग दैर्ध्य लगभग 200 एनएम से कम) में स्थित हैं। इन तरंग दैर्ध्य पर ऑक्सीजन द्वारा प्रकाश के मजबूत अवशोषण के कारण रुचि का तरंग दैर्ध्य क्षेत्र वास्तव में हवा में दुर्गम है। व्यवहार में इन स्पेक्ट्रा को निर्वात में नहीं बल्कि ऑक्सीजन रहित उपकरण (शुद्ध नाइट्रोजन गैस से भरे) में मापा जाता है।
एक बार ऑक्सीजन समाप्त हो जाने के बाद, शायद 200 एनएम से नीचे काम करने में दूसरा सबसे महत्वपूर्ण तकनीकी कारक बाकी ऑप्टिकल सिस्टम को इस क्षेत्र में कम नुकसान के लिए डिज़ाइन करना है। इस संबंध में महत्वपूर्ण मिरर # उपकरणों का उपयोग है जिनके कोटिंग्स को स्पेक्ट्रम के इस क्षेत्र में कम नुकसान के लिए अनुकूलित किया गया है।
इन उपकरणों में सामान्य प्रकाश स्रोत एक उच्च दबाव, शॉर्ट-आर्क क्सीनन आर्क लैंप है। साधारण क्सीनन चाप लैंप कम यूवी में उपयोग के लिए अनुपयुक्त हैं। इसके बजाय, उच्च शुद्धता वाले सिंथेटिक फ्युज़्ड सिलिका से बने लिफाफे के साथ विशेष रूप से निर्मित लैंप का उपयोग किया जाना चाहिए।
सिंक्रोटॉन स्रोतों से प्रकाश का प्रवाह कम तरंग दैर्ध्य पर बहुत अधिक होता है, और इसका उपयोग सीडी को 160 एनएम तक रिकॉर्ड करने के लिए किया जाता है। 2010 में डेनमार्क में आरहूस विश्वविद्यालय में इलेक्ट्रॉन स्टोरेज रिंग सुविधा आईएसए में सीडी स्पेक्ट्रोफोटोमीटर का उपयोग ठोस अवस्था सीडी स्पेक्ट्रा को 120 एनएम तक रिकॉर्ड करने के लिए किया गया था।[19] क्वांटम यांत्रिकी स्तर पर, वृत्ताकार द्वैतवाद और ऑप्टिकल रोटेशन की विशेषता घनत्व समान हैं। ऑप्टिकल रोटरी फैलाव और वृत्ताकार द्वैतवाद समान क्वांटम सूचना सामग्री साझा करते हैं।
यह भी देखें
- रेखीय द्वैतवाद
- चुंबकीय वृत्ताकार द्वैतवाद
- ऑप्टिकल गतिविधि
- ऑप्टिकल समावयवता
- ऑप्टिकल रोटेशन
- ऑप्टिकल रोटेटरी फैलाव
- प्रोटीन वृत्ताकार द्वैतवाद डेटा बैंक
- दो फोटॉन वृत्ताकार द्वैतवाद
- कंपन परिपत्र द्वैतवाद
- हाइपर रेले स्कैटरिंग ऑप्टिकल गतिविधि
संदर्भ
- ↑ P. Atkins; J. de Paula (2005). भौतिक रसायन विज्ञान के तत्व (4th ed.). Oxford University Press. ISBN 978-0-7167-7329-0.
- ↑ 2.0 2.1 2.2 Edward I. Solomon; A. B. P. Lever (3 February 2006). अकार्बनिक इलेक्ट्रॉनिक संरचना और स्पेक्ट्रोस्कोपी. Wiley-Interscience. p. 78. ISBN 978-0-471-97124-5. Retrieved 29 April 2011.
- ↑ Introduction to Quantum Theory 2ED David Park Sec 2.2 Pg32 "...the polarization of a beam of light is exactly the same kind of thing as the spin of a beam of electrons, the differences of terminology reflecting only the accidents of the historical order of discovery."
- ↑ Gerald D. Fasman (1996). वृत्ताकार द्वैतवाद और बायोमोलेक्यूल्स का गठनात्मक विश्लेषण. Springer. pp. 3–. ISBN 978-0-306-45142-3. Retrieved 29 April 2011.
- ↑ 5.0 5.1 5.2 Kōji Nakanishi; Nina Berova; Robert Woody (1994). Circular dichroism: principles and applications. VCH. p. 473. ISBN 978-1-56081-618-8. Retrieved 29 April 2011.
- ↑ Solomon, Neidig; A. T. Wecksler; G. Schenk; T. R. Holman (2007). "Kinetic and Spectroscopic Studies of N694C Lipoxygenase: A Probe of the Substrate Activation Mechanism of a Non-Heme Ferric Enzyme". J. Am. Chem. Soc. 129 (24): 7531–7537. doi:10.1021/ja068503d. PMC 2896304. PMID 17523638.
- ↑ Alison Rodger; Bengt Nordén (1997). वृत्ताकार द्वैतवाद और रेखीय द्वैतवाद. Oxford University Press. ISBN 978-0-19-855897-2. Retrieved 29 April 2011.
- ↑ R. Williams (1968). "p-Azoxyanisole के निमेटिक तरल चरण में ऑप्टिकल रोटेटरी प्रभाव". Physical Review Letters. 21 (6): 342. Bibcode:1968PhRvL..21..342W. doi:10.1103/PhysRevLett.21.342.
- ↑ R. Williams (1969). "p-azoxyanisole के नेमैटिक लिक्विड क्रिस्टल में ऑप्टिकल-रोटरी पावर और लीनियर इलेक्ट्रो-ऑप्टिक प्रभाव". Journal of Chemical Physics. 50 (3): 1324. Bibcode:1969JChPh..50.1324W. doi:10.1063/1.1671194.
- ↑ Plum, E.; Fedotov, V. A.; Zheludev, N. I. (2008). "बाहरी रूप से चिराल मेटामेट्री में ऑप्टिकल गतिविधि" (PDF). Applied Physics Letters. 93 (19): 191911. arXiv:0807.0523. Bibcode:2008ApPhL..93s1911P. doi:10.1063/1.3021082. S2CID 117891131.
- ↑ Plum, E.; Fedotov, V. A.; Zheludev, N. I. (2016). "अचिरल मेटासर्फ्स की स्पेक्युलर ऑप्टिकल गतिविधि" (PDF). Applied Physics Letters. 108 (14): 141905. Bibcode:2016ApPhL.108n1905P. doi:10.1063/1.4944775. hdl:10220/40854.
- ↑ Surma M.A.; Szczepaniak A.; Króliczewski J. (2014). "Comparative Studies on Detergent-Assisted Apocytochrome b6 Reconstitution into Liposomal Bilayers Monitored by Zetasizer Instruments". PLOS ONE. 9 (11): e111341. Bibcode:2014PLoSO...9k1341S. doi:10.1371/journal.pone.0111341. ISSN 1932-6203. PMC 4244035. PMID 25423011.
- ↑ Hall V, Nash A, Rodger A (2014). "SSNN, तंत्रिका नेटवर्क प्रोटीन माध्यमिक संरचना फिटिंग के लिए एक विधि है जो सर्कुलर डाइक्रोइज्म डेटा का उपयोग करती है" (PDF). Analytical Methods. 6 (17): 6721–26. doi:10.1039/C3AY41831F. Archived (PDF) from the original on 2022-10-09.
- ↑ Hall V, Nash A, Hines E, Rodger A (2013). "वृत्ताकार द्वैतवाद और एक तंत्रिका नेटवर्क के साथ प्रोटीन माध्यमिक संरचना को स्पष्ट करना". Journal of Computational Chemistry. 34 (32): 2774–86. doi:10.1002/jcc.23456. PMID 24122928. S2CID 19685126.
- ↑ Whitmore L, Wallace BA (2008). "Protein secondary structure analyses from circular dichroism spectroscopy: methods and reference databases". Biopolymers. 89 (5): 392–400. doi:10.1002/bip.20853. PMID 17896349.
- ↑ Greenfield NJ (2006). "प्रोटीन द्वितीयक संरचना का अनुमान लगाने के लिए वृत्ताकार द्वैतवाद स्पेक्ट्रा का उपयोग करना". Nature Protocols. 1 (6): 2876–90. doi:10.1038/nprot.2006.202. PMC 2728378. PMID 17406547.
- ↑ Bioinorganic Interface: Mechanistic Studies of Protein-Directed Nanomaterial Synthesis. (2016, May 5). Retrieved March 1, 2019, from https://pubs.acs.org/doi/pdf/10.1021/acs.jpcc.6b02569
- ↑ Sarkar, Sumant, Ryan Behunin, and John G. Gibbs. "Shape-Dependent, Chiro-Optical Response of UV-Active, Nanohelix Metamaterials." Nano letters (2019). https://pubs.acs.org/doi/10.1021/acs.nanolett.9b03274
- ↑ U. Meierhenrich; J.J. Filippi; C. Meinert; J. H. Bredehöft; J. Takahashi; L. Nahon; N. C. Jones; S. V. Hoffmann (2010). "वैक्यूम-पराबैंगनी क्षेत्र में अमीनो एसिड का वृत्ताकार द्वैतवाद". Angew. Chem. Int. Ed. 49 (42): 7799–7802. doi:10.1002/anie.201003877. PMID 20845349.
बाहरी संबंध
- Circular Dichroism spectroscopy by Alliance Protein Laboratories, a commercial service provider
- An Introduction to Circular Dichroism Spectroscopy by Applied Photophysics, an equipment supplier
- An animated, step-by-step tutorial on Circular Dichroism and Optical Rotation by Prof Valev.